Ванкозамин - Vancosamine
 Циклогексан и изображения ванкозамина (вверху) и эпиванкозамина (внизу) на стуле. Обратите внимание на другой стереоцентр у углерода 4. | |
| Имена | |
|---|---|
| Название ИЮПАК (3S,4S,5S) -3-амино-4,5-дигидрокси-3-метилгексаналь | |
| Другие имена 3-амино-2,3,6-тридеокси-3-метил-L-Lyxo-гексопираноза | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| C7ЧАС15NО3 | |
| Молярная масса | 161.201 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ванкозамины находятся аминосахара которые являются частью ванкомицин и другие молекулы в семействе антибиотиков ванкомицина. Синтез ванкозамина кодируется ванкомицином (vps) биосинтетический кластер. Эпиванкозамин, близкородственный аминосахар, кодируется хлорэремомицином (белый гриб) биосинтетический кластер.[1]
История
Ванкозамин был впервые выделен Ломакиной. и другие в 1968 г.[2] В 1972 году Джонсон и другие были первыми, кто идентифицировал и полностью охарактеризовал ванкозамин.[3] Эпиванкозамин был впоследствии выделен в 1988 году Хантом. и другие в Эли Лилли[4]
Биосинтез
Биосинтез ванкозамина и эпиванкозамина идентичен, за исключением последней стадии.[5] Ферменты, катализирующие реакции, получили обозначение EvaA-E. Молекула TDP-D-глюкозы входит в этот путь через превращение в молекулу 1 ферментом оксидоредуктазой, а затем ферментом дегидратазой. На следующем этапе EvaA дегидратирует молекулу 1 путем депротонирования при 3-C с образованием и еноляцией, которая затем удаляет 2-OH с образованием молекулы 2. Молекула 2 превращается в молекулу 3 посредством таутомеризация к его кето-форме, а затем трансаминированный от EvaB с использованием L-Glu в качестве источника аммиака и PLP в качестве кофактора.
 Биосинт ванкозамина часть 1
Биосинт ванкозамина часть 1
Затем EvaC метилирует молекулу 3 по 3-C с образованием молекулы 4 путем депротонирования с образованием промежуточного енолята, который затем атакует СЭМ метильная группа в активном центре EvaC. Затем EvaD эпимеризует молекулу 4 при 5-C с образованием молекулы 5. Наконец, EvaE может образовывать эпи / ванкозамин путем восстановления с использованием либо НАДН или же НАДФН для восстановления карбонила при 4 ° C. Стереохимический результат зависит от EvaE, который кодируется в биосинтетическом кластере. Ванкомицин vps EvaE приводит к образованию ванкозамина, тогда как хлороремомицин белый гриб EvaE приводит к образованию эпиванкозамина.
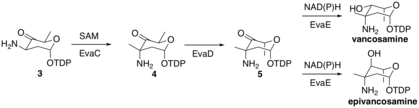 Биосинтез ванкозамина, часть 2
Биосинтез ванкозамина, часть 2
Затем ванкозамины используются клеткой для синтеза ванкомицина и родственных молекул. Гликозилтрансфераза присоединяет аминосахар через α-1 эфирные связи.
Возможны дополнительные модификации в аминогруппе 3-C для создания N-алкил или N-ацильные производные этого сахара.
Всего синтезов
Было опубликовано несколько синтезов ванкозамина.[6][7][8]
Смотрите также
Рекомендации
- ^ Йим, Г., Такер, М. Н., Котева, К., Райт, Г. "Биосинтез гликопептидных антибиотиков". Журнал антибиотиков, 2017, 67, 31-41.
- ^ Ломакина Н.Н., Спиридонова И.А., Богнар Р., Пукшас М., Старицкая Ф. Антибиотики. 1968, 13, 975.
- ^ Джонсон, А. В., Смит, Р. М., Гатри, Р. Д. «Ванкозамин: структура и конфигурация нового аминосахара из ванкомицина». Дж. С. С. Перкин I, 1972, 2153-2159.
- ^ Хант, А. Х., Моллой, Р. М., Дебоно, М., Окколовиц, Дж. Л. «Выделение и характеристика 4-эпи-ванкозамина». Tetrahedron Lett, 1988, 29, 1223-1226.
- ^ Чен, Х., Томас, М. Г., Хаббард, Б. К., Лоузи, Х. С., Уолш, К. Т., Буркарт, М. Д. «Дезоксисахары в гликопептидных антибиотиках: ферментативный синтез TDP-L-эпиванкозамина в биосинтезе хлорэремомицина». PNAS, 2000, 97 (22), 11942-11947
- ^ Хаузер, Ф. М., Элленбергер, С. Р., Глускер, Дж. П., Смарт, Ф. Дж., Каррелл, Х. Л. «Стереоселективный синтез или +/- даунозамин, +/- ванкозамин и +/- ристозамин из ациклических предшественников». J. Org. Chem. 1986, 51, 50-57.
- ^ Николау, К. К., Митчелл, Х. Дж., Ван Делфт, Ф. Л., Рюбсам, Ф., Родригруес, Р. М. «Быстрые пути к производным и синтезу эвернитрозы и ванкозамина или модельного ванкомицин-арилгликозида». Энгью. Chem. Int. Эд. 1998, 37, № 13/14, 1871–1874.
- ^ Паркер, К. А., Чанг, В. «Синтез производных L-ванкозамина из неуглеводных предшественников с помощью короткой последовательности на основе реакций Маршалла, Макдональда и Дюбуа». Орг. Lett. 2003, 5 (21), 3891-3893.


