Перестановка Кэрролла - Carroll rearrangement
В Перестановка Кэрролла это реакция перегруппировки в органическая химия и включает в себя преобразование β-кето аллил сложный эфир в α-аллил-β-кетокарбоновую кислоту.[1] Этот органическая реакция сопровождается декарбоксилирование и конечный продукт представляет собой γ, δ-аллилкетон. Перестановка Кэрролла - это адаптация Перестановка Клейзена и эффективно декарбоксилированное аллилирование.
Механизм реакции
Перестановка Кэрролла (1940) в присутствии основание и с высокой температурой реакции (путь А) происходит через промежуточный энол который затем перестраивается в электроциклической перегруппировке Клейзена. Следующим шагом является декарбоксилирование. С палладий (0) как катализатор, реакция (Tsuji, 1980) гораздо мягче (путь B) с промежуточным катионом аллил / анион карбоновой кислоты металлоорганический сложный.[2]
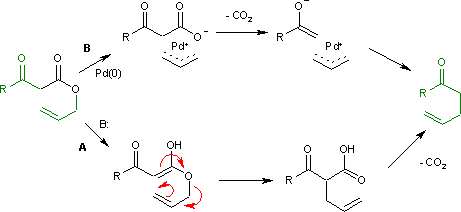
Декарбоксилирование предшествует аллилированию, о чем свидетельствует эта реакция, катализируемая тетракис (трифенилфосфин) палладий (0):[3]
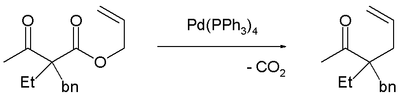
Асимметричное декарбоксилированное аллилирование
При введении подходящих хиральных лигандов реакция становится энантиоселективный.[4]
Первый сообщил асимметричный перегруппировка катализируется трис (дибензилиденацетон) дипалладий (0) и Лиганд Троста:[3]
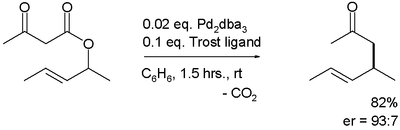
Подобная реакция[5] использует дополнительные нафтол.

Эта реакция дает основную энантиомер с 88% энантиомерный избыток. Еще неизвестно, будет ли эта реакция иметь широкий размах, потому что ацетамидо группа кажется предпосылкой.
В этом случае используется тот же катализатор, но другой лиганд. энантиосонвергентный реакция:[6]
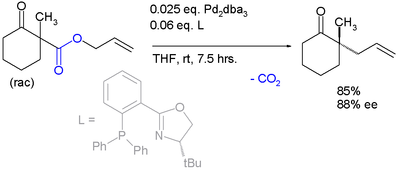
Сфера применения расширена до асимметричного α-алкилирования кетоны замаскированные под их енол карбонатные эфиры:[7]

Рекомендации
- ^ Кэрролл, М. Ф. «131. Добавление α, β-ненасыщенных спиртов к активной метиленовой группе. Часть I. Действие этилацетоацетата на линалоол и гераниол». Журнал химического общества 1940, 704–706. Дои:10.1039 / JR9400000704
- ^ Катализируемая палладием перегруппировка аллиловых эфиров ацетоуксусной кислоты с образованием γ, δ-ненасыщенных метилкетонов Буквы Тетраэдра, Том 21, Выпуск 33, 1980, Страницы 3199-3202 Исао Симидзу, Тоширо Ямада и Дзиро Цудзи Дои:10.1016 / S0040-4039 (00) 77444-2
- ^ а б Асимметричное аллильное алкилирование енолатов кетонов: асимметричный суррогат Клейзена Эрин С. Бургер и Джон А. Тандж Орг. Lett.; 2004; 6 (22), стр. 4113–4115; (Письмо) Дои:10.1021 / ol048149t
- ^ Энантиоселективное декарбоксилирующее аллильное алкилирование, катализируемое палладием Шу-Ли Ю и Ли-Синь Дай Энгью. Chem. Int. Эд. 2006, 45, 5246 – 5248 Дои:10.1002 / anie.200601889
- ^ Kuwano, R .; Ishida N .; Мураками, М. «Асимметричная перегруппировка Кэрролла аллил α-ацетамидо-β-кетокарбоксилатов, катализируемая хиральным комплексом палладия». Химические коммуникации 2005, (31), 3951–3952. Дои:10.1039 / b505105c
- ^ Дерацемизация четвертичных стереоцентров путем энантиоконвергентного декарбоксилированного аллилирования рацемических b-кетоэфиров, катализируемых Pd Джастин Т. Мор, Дуглас К. Бехенна, Эндрю М. Харнед и Брайан М. Штольц Энджью. Chem. Int. Эд. 2005, 44, 6924 –6927 Дои:10.1002 / anie.200502018
- ^ Катализируемое палладием асимметричное аллильное α-алкилирование ациклических кетонов Барри М. Трост и Цзяи СюйВаренье. Chem. Soc.; 2005; 127 (49) стр. 17180–17181; (Коммуникация) Дои:10.1021 / ja055968f
