Пиннер реакция - Pinner reaction
| Пиннер реакция | |
|---|---|
| Названный в честь | Адольф Пиннер |
| Тип реакции | Реакция сцепления |
| Идентификаторы | |
| Портал органической химии | пиннер-реакция |
| RSC ID онтологии | RXNO: 0000361 |
В Пиннер реакция относится к катализируемой кислотой реакции нитрил с алкоголь с образованием соли сложного эфира имино (алкил imidate соль); это иногда называют Пиннерская соль.[1]Реакция названа в честь Адольф Пиннер, который впервые описал его в 1877 году.[2][3][4]Пиннер-соли сами по себе реакционноспособны и подвергаются дополнительному нуклеофильные добавки дарить различные полезные продукты:[5][6]
- При избытке алкоголя с образованием ортоэфир
- С участием аммиак или амин сформировать амидин
- С водой, чтобы сформировать сложный эфир
- С сероводородом с образованием тионоэфира
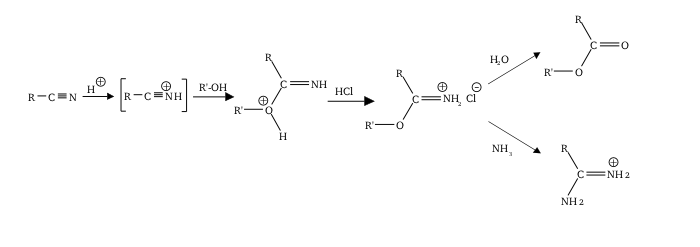
Обычно соль Пиннера не выделяют, и реакцию продолжают с получением желаемой функциональной группы (ортоэфир и т.д.) за один раз. Следует понимать, что реакция Пиннера относится конкретно к процессу, катализируемому кислотой, но аналогичные результаты часто могут быть достигнуты с использованием основного катализа. Эти два подхода могут дополнять друг друга, когда нитрилы, которые не реагируют в кислотных условиях, часто дают лучшие результаты в присутствии основания, и наоборот.[7] Определяющим фактором обычно является то, насколько нитрил богат электронами или беден. Например: бедный электронами нитрил - хороший электрофил (легко поддается атаке со стороны алкоксиды и др.), но слабый нуклеофил будет трудно протонировать, и, следовательно, можно ожидать, что он будет реагировать более легко в основных, а не в кислых условиях.
Смотрите также
- Реакция Хёша
- Перестройка сверхчеловека
- Синтез альдегида Стивена - по сути такая же реакция, но с сокращение и с водой в качестве нуклеофила; образует альдегид.
Рекомендации
- ^ «Реакция Пиннера». Комплексные органические названия реакций и реагенты (504): 2237–2240. 2010. Дои:10.1002 / 9780470638859.conrr504. ISBN 9780470638859.
- ^ А. Пиннер, Ф. Кляйн; Кляйн (1877). "Umwandlung der Nitrile in Imide". Berichte der deutschen chemischen Gesellschaft. 10 (2): 1889–1897. Дои:10.1002 / cber.187701002154.
- ^ А. Пиннер, о. Кляйн; Клейн (1878 г.). "Umwandlung der Nitrile in Imide". Berichte der deutschen chemischen Gesellschaft. 11 (2): 1475–1487. Дои:10.1002 / cber.18780110258.
- ^ А. Пиннер (1883). "Ueber die Umwandlung der Nitrile in Imide". Berichte der deutschen chemischen Gesellschaft. 16 (2): 1643–1655. Дои:10.1002 / cber.18830160235.
- ^ Roger, R .; Нилсон, Д. Г. (1961). «Химия имидатов». Chem. Ред. 61 (2): 179–211. Дои:10.1021 / cr60210a003.
- ^ Адамс, Роджер; Тал, А. Ф. (1922). «Этилфенилацетат». Органический синтез. 2: 27. Дои:10.15227 / orgsyn.002.0027.
- ^ Schaefer, F.C .; Петерс, Г. А. (1961). «Катализируемая основанием реакция нитрилов со спиртами. Удобный путь к имидатам и солям амидина». Журнал органической химии. 26 (2): 412. Дои:10.1021 / jo01061a034.
