Белок SCIMP - SCIMP protein
SLP65 / SLP76, Csk -взаимодействующий мембранный белок, называемый SCIMP, принадлежит к семейству трансмембранных адаптерных белков (TRAP), которые не связаны напрямую с рецептором, таким как LAT, NTAL, ЛАЙМ или же LAX.[1][2][3][4] SCIMP выражается в антигенпрезентирующие клетки (APC), а именно В-клетки, дендритные клетки костного мозга и макрофаги.
Структура и взаимодействия
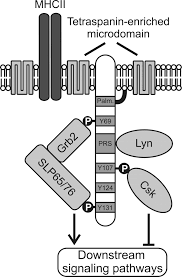
Как и другие TRAP, SCIMP имеет незначительный внеклеточный домен и трансмембранный домен, за которым следует внутриклеточный домен, содержащий несколько тирозинов и один богатая пролином область (PRR). При фосфорилировании эти тирозины служат стыковочными доменами для SH2 домены содержащие белки. В отличие от фосфотирозинов, богатые пролином области, как правило, менее восприимчивы к посттрансляционным модификациям и являются скорее мишенями конститутивных взаимодействий с SH3 домены содержащие белки.[5] Было показано, что SCIMP взаимодействует через SH2-домены с Csk-киназой, негативным регулятором Киназы семейства SRC, но также с Slp65 / 76 и Grb2 адаптеры, которые являются ключевыми про-сигнализирующими растворимыми адапторными белками в сигнальной сети лимфоцитов. SCIMP конститутивно связан с Линкиназа через домен SH3.
Мембранная локализация
Некоторые из TRAP пальмитоилированы в пограничной области между трансмембранным и внутриклеточным доменом. Алифатическая цепочка Пальмитиновая кислота прикрепляется к двойному слою мембраны и, таким образом, влияет на нацеливание белка на мембранные микродомены. SCIMP также пальмитоилирован и связан с микродомены, обогащенные тетраспанином (ТЕА). ТЕА, в отличие от липидные рафты, основаны больше на взаимодействиях белок-белок, чем на взаимодействиях липид-липид / липид-белок.[6] Один из резидентных белков ТЕА - это Молекула MHC класса II. SCIMP присутствует в иммунологический синапс во время презентации антигена между Т-клетка и антигенпрезентирующая клетка (БТР).
Исследования in vitro и предполагаемая функция
SCIMP становится сильно фосфорилированным после стимуляции MHC II. Исследования, проведенные с гибридным белком CD25 -SCIMP показал свою способность вызывать высвобождение кальция и Эрк фосфорилирование при лечении антителом к CD25. Высвобождение кальция было даже сильнее у мутантного белка CD25-SCIMP на стороне связывания Csk. Указывая петля отрицательной обратной связи в исполнении Csk kinase. Слитые белки обычно используются для изучения сигнальной способности белков с небольшим внеклеточным доменом, скрытым для антител в мембране. гликокаликс. тем не мение сбить SCIMP не влиял на высвобождение кальция после обработки антителом против MHC II, а только снижал уровень фосфорилирования Erk в более длительный промежуток времени (10 мин).[7]
Рекомендации
- ^ Brdicka, T .; Imrich, M .; Ангелисова, П .; Brdickova, N .; Хорват, О .; Spicka, J .; Hilgert, I .; Лускова, П .; Draber, P .; Новак, П .; Энгельс, Н .; Wienands, J .; Симеони, Л .; Osterreicher, J .; Aguado, E .; Malissen, M .; Schraven, B .; Хорейси, В. (9 декабря 2002 г.). «Линкер активации не Т-клеток (NTAL): белок трансмембранного адаптера, участвующий в передаче сигналов иммунорецептора». Журнал экспериментальной медицины. 196 (12): 1617–1626. Дои:10.1084 / jem.20021405. ЧВК 2196071. PMID 12486104.
- ^ Hur, E.M .; Сын, М .; Lee, O.-H .; Choi, Y.B .; Парк, Ц .; Lee, H .; Юнь, Ю. (10 ноября 2003 г.). «LIME, новый трансмембранный адаптерный белок, ассоциирует с p56lck и опосредует активацию Т-клеток». Журнал экспериментальной медицины. 198 (10): 1463–1473. Дои:10.1084 / jem.20030232. ЧВК 2194117. PMID 14610044.
- ^ Вебер, младший (6 апреля 1998 г.). «Молекулярное клонирование кДНК, кодирующей pp36, тирозин-фосфорилированный адаптерный белок, селективно экспрессируемый Т-клетками и естественными клетками-киллерами». J Exp Med. 187 (7): 1157–1161. Дои:10.1084 / jem.187.7.1157. ЧВК 2212210. PMID 9529333.
- ^ Чжу, М. (30 сентября 2002 г.). «Молекулярное клонирование нового гена, кодирующего мембранно-связанный адаптерный белок (LAX) в передаче сигналов лимфоцитов». Журнал биологической химии. 277 (48): 46151–46158. Дои:10.1074 / jbc.M208946200. PMID 12359715.
- ^ Уильямсон, член парламента (15 января 1994 г.). «Структура и функция богатых пролином областей в белках». Biochem. J. 297 (Pt 2) (2): 249–60. Дои:10.1042 / bj2970249. ЧВК 1137821. PMID 8297327.
- ^ Степанек, Ондрей; Драбер, Питер; Хорейси, Вацлав (май 2014 г.). «Пальмитоилированные трансмембранные адаптерные белки в передаче сигналов лейкоцитов». Сотовая связь. 26 (5): 895–902. Дои:10.1016 / j.cellsig.2014.01.007. PMID 24440308.
- ^ Draber, P .; Вонькова, И .; Степанек, О .; Хрдинка, М .; Куцова, М .; Скопцова, Т .; Otahal, P .; Ангелисова, П .; Хорейси, В .; Yeung, M .; Weiss, A .; Brdicka, T. (19 сентября 2011 г.). «SCIMP, трансмембранный адаптерный белок, участвующий в передаче сигналов класса II главного комплекса гистосовместимости». Молекулярная и клеточная биология. 31 (22): 4550–4562. Дои:10.1128 / MCB.05817-11. ЧВК 3209250. PMID 21930792.
