Побочная реакция - Side reaction
А побочная реакция это химическая реакция это происходит одновременно с основной реакцией, но в меньшей степени. Это приводит к образованию побочный продукт, таким образом урожай основного продукта сокращается:[1]
п1 является основным продуктом, если k1> k2. Побочный продукт P2 обычно нежелательно и должно быть отделенный от фактического основного продукта (обычно в дорогостоящий процесс ).
В органическом синтезе
B и C из приведенных выше уравнений обычно представляют разные соединения. Однако они также могут находиться в разных положениях в одной и той же молекуле.
Побочная реакция также называется конкурирующей реакцией.[2][3] когда разные соединения (B, C) конкурируют за другой реагент (A). Если побочная реакция возникает примерно так же часто, как и основная реакция, говорят о параллельных реакциях.[4] (особенно в кинетике, см. ниже).
Также могут быть более сложные отношения: соединение A может обратимо, но быстро реагировать на вещество B (со скоростью k1) или необратимым, но медленным (k1> k−1 >> k2) к веществу C:
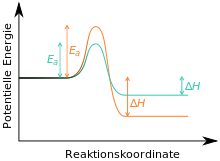
Предполагая, что реакция на вещество C необратимо, поскольку оно термодинамически очень стабильно. В этом случае B - кинетический, а C - термодинамический продукт реакции (см. Также здесь ).[5][6][7] Если реакцию проводят при низких температурах и останавливают через короткое время, то говорят о кинетическом контроле, в первую очередь, образуется кинетический продукт B. Когда реакция проводится при высоких температурах и в течение длительного времени (в этом случае доступна необходимая энергия активации для реакции на C, которая постепенно образуется с течением времени), говорят о термодинамическом контроле; в первую очередь образуется термодинамический продукт C.
Условия побочных реакций
В органическом синтезе повышенный температуры обычно приводят к большему количеству побочных продуктов. Побочные продукты обычно нежелательны, поэтому предпочтительны низкие температуры («мягкие условия»). На соотношение конкурирующих реакций может влиять изменение температуры, поскольку их энергии активации в большинстве случаев разные. Реакции с высокой энергией активации могут быть сильнее ускорены повышением температуры, чем реакции с низкой энергией активации. Также состояние равновесие зависит от температуры.[8]
Обнаружение реакции могут искажаться побочными реакциями.
Кинетика
Побочные реакции также описаны в кинетика реакции, а ответвляться из физическая химия. Под побочными реакциями понимаются сложная реакция, поскольку общая реакция (основная реакция + побочная реакция) состоит из нескольких (минимум двух) элементарные реакции.[9] Другие сложные реакции - это конкурирующие реакции, параллельные реакции, последовательные реакции, цепные реакции, обратимые реакции и т. Д. [10][10]:280–291
Если одна реакция происходит намного быстрее, чем другая (k1 > k2), это (k1) будем называть основной реакцией, другую (k2) побочная реакция. Если обе реакции примерно одинаковой скорости (k1 ≅ к2) говорится о параллельных реакциях.[4]
Если реакции и необратимо (без обратной реакции), то отношение P1 и P2 соответствует относительной реактивности B и C по сравнению с A:
Смотрите также
Рекомендации
- ^ "побочная реакция на merriam-webster.com". Получено 2015-08-30.
- ^ "Konkurrenzreaktion auf chemgapedia.de". Получено 2015-08-30.
- ^ "Konkurrenzreaktion auf universal_lexikon.deacademic.com". Получено 2015-08-30.
- ^ а б «4. Kinetik und Katalyse» (PDF). Получено 2015-08-30.
- ^ "Kinetische und thermodynamische Kontrolle von chemischen Reaktionen auf Chemgapedia.de". Получено 2015-12-06.
- ^ Джон Гилберт; Стивен Мартин, Экспериментальная органическая химия: миниатюрный и микромасштабный подход (на немецком)
- ^ Роберт Дж. Мортимер (2008), Физическая химия (на немецком языке), Academic Press
- ^ Клаус Шветлик (2009). Organikum: Organisch-Chemisches Grundpraktikum (на немецком языке) (23-е изд.). Вайнхайм: Wiley-VCH. п. 156. ISBN 978-3-527-32292-3.
- ^ "Komplexe Reaktionen auf spektrum.de". Получено 2015-08-30.
- ^ Зима, фон Клаус Чеслик, Хайко Зееманн, Роланд (2010). Basiswissen Physikalische Chemie (4., aktualisierte Aufl. Ed.). Висбаден: Vieweg + Teubner Verlag / GWV Fachverlage, Висбаден. ISBN 9783834893598.

![{displaystyle {ce {{A} + B -> [{k_ {1}}] P1}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3168fbf52fc171ac42d721d1eccf57ba532c8419)
![{displaystyle {ce {{A} + C -> [{k_ {2}}] P2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2d16a27a665d4cc910e04f9e3f9481f216cf0e43)
![{displaystyle {ce {B <=> A -> [{k_ {2}}] C}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9eb19cb35defcfd33bd5bbdbaf15c92c90c55320)
![{displaystyle {frac {ce {[P1]}} {ce {[P2]}}}} = {frac {k_ {1} [{ce {B}}]} {k_ {2} [{ce {C}} » ]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d6a40a7ee5d985fab93032d041123b6459e562fb)