Тефлиевая кислота - Википедия - Teflic acid
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Пентафторортотеллуровая кислота | |||
| Другие имена Тефлиевая кислота | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.161.534 | ||
| |||
| |||
| Характеристики | |||
| HF5OTe | |||
| Молярная масса | 239.6 | ||
| Внешность | бесцветное твердое вещество | ||
| Температура плавления | 39,1 ° С (102,4 ° F, 312,2 К) | ||
| Точка кипения | 59,7 ° С (139,5 ° F, 332,8 К) | ||
| Опасности | |||
| Главный опасности | коррозионный, токсичный | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
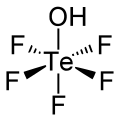
Тефлиевая кислота это химическое соединение с формула HOTeF5. Этот сильный кислота относится к ортотеллуровой кислоте, Те (ОН)6. Тефлиевая кислота имеет слегка искаженную октаэдрическую форму.
Подготовка
Тефлиевая кислота была случайно открыта Энгельбрехтом и Сладким. Их синтез не дал ожидаемого теллурилфторида TeO2F2, но смесь летучих теллурических соединений, я. HOTeF5:[1]
- BaTeO4 + 10HOSO2F → HOTeF5 (25 %)
Тефлиновую кислоту также можно получить из фторсульфоновая кислота и теллурат бария:[2]
- 5HOSO2F + BaO2Те (ОН)4 → HOTeF5 + 4 часа2ТАК4 + BaSO4
Это также первый продукт гидролиза гексафторид теллура:
- TeF6 + H2O → HOTeF5 + ВЧ
Тефлаты

В сопряженное основание тефлиевой кислоты называют анионом тефлата, F5TeO− (не путать с тройной ). Известно много тефлатов, например, B (OTeF5)3 и ангидрид кислоты O (TeF5)2. Пиролиз соединения бора дает димер (TeF4O)2[2]
- 2 Б (OTeF5)3 → 2 Б (OTeF5)2F + (OTeF4)2
Известно, что тефлат-анион сопротивляется окислению. Это свойство позволило приготовить несколько очень необычных видов, таких как гексатфлаты M (OTeF5)6− (M = As, Sb, Bi). Ксенон формирует катион Xe (OTeF5)+.[3]
Рекомендации
- ^ Engelbrecht, A .; Сладкий, Ф. "Пентафтор-ортотеллурсаура, ХОТеФ"5" Энгью. Chem. 1964. 76(9), 379-380, Дои:10.1002 / ange.19640760912.
- ^ а б Холлеман, А. Ф .; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5.
- ^ Mercier, H.PA .; Sanders, J. C. P .; Schrobilgen, G.J. "Анионы Hexakis (пентафтороксотеллюрато) пниктата (V), M (OTeF5)6− (M = As, Sb, Bi): серия очень слабо координирующих анионов » Журнал Американского химического общества, том 116, 2921, (1994). Дои:10.1021 / ja00086a025.
дальнейшее чтение
- Р. Б. Кинг; Неорганическая химия элементов основных групп, VCH Publishers, Нью-Йорк, 1994.