Asx поворот - Asx turn
В Asx поворот[1][2][3][4][5][6][7]структурная особенность в белки и полипептиды. Он состоит из трех аминокислота остатки (обозначенные i, i + 1 и i + 2), в которых остаток i является аспартат (Asp) или аспарагин (Asn), который образует водородная связь от CO-группы боковой цепи к NH-группе основной цепи остатка i + 2. Около 14% остатков Asx, присутствующих в белках, принадлежат виткам Asx.
Название «Asx» используется здесь для обозначения одной из аминокислот аспартат (Asp) или аспарагин (Asn).
Типы
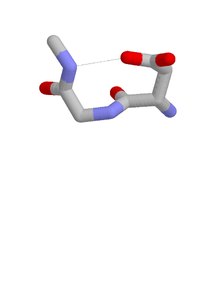
Можно выделить четыре типа разворота Asx:[8] типы I, I ’, II и II’. Эти категории соответствуют более известным категориям водородных связей. бета-ходы, которые имеют четыре остатка и водородную связь между CO остатка i и NH остатка i + 3. Asx поворачивается и бета-ходы имеют структурно похожие петли с водородными связями и демонстрируют мимикрию боковой цепи-основной цепи в том смысле, что боковая цепь остатка i в витке Asx имитирует основную цепь остатка i из бета-ход. Что касается их присутствия в белках, они отличаются тем, что тип I является наиболее распространенным из четырех. бета-ходы в то время как тип II ’- самый распространенный из поворотов Asx.
Вхождение
Asx и ST повороты оба часто встречаются в N-конец из α-спирали.[9][10][11][12] как часть Мотивы Asx или же Мотивы ST таким образом, что Asx, серин или треонин являются N крышка остаток. Таким образом, они часто рассматриваются как элементы, закрывающие спираль.
Связанные мотивы
Подобные мотивы встречаются с серин или же треонин как остаток i, которые называются ST повороты.[13] Несмотря на то, что серин и треонин имеют на один атом боковой цепи меньше, так что мимикрия β-витков боковой и основной цепи является несовершенной, эти особенности проявляются в белках как четыре типа по количеству, приближающимся к числам витков Asx. Они также демонстрируют тенденцию замещать друг друга в течение эволюционного времени.[14]
Часть витков Asx сопровождается водородной связью между основной цепью и основной цепью, которая квалифицирует их как Мотивы Asx.
Рекомендации
- ^ Ричардсон, Дж. С. (1981). «Анатомия и таксономия структуры белка». Достижения в химии белков Том 34. Успехи в химии белков. 34. С. 167–339. Дои:10.1016 / S0065-3233 (08) 60520-3. ISBN 9780120342341. PMID 7020376.
- ^ Тайнер, JA; Getzoff ED (1982). «Определение и анализ 2 A-структуры меди, супероксиддисмутазы цинка». Журнал молекулярной биологии. 160 (2): 181–217. Дои:10.1016/0022-2836(82)90174-7. PMID 7175933.
- ^ Рис, округ Колумбия; Льюис М (1983). «Уточненная кристаллическая структура карбоксипептидазы а при разрешении 1,54 Å». Журнал молекулярной биологии. 168 (2): 367–387. Дои:10.1016 / S0022-2836 (83) 80024-2. PMID 6887246.
- ^ Eswar, N; Рамачандран C (1999). «Вторичные структуры без остова: анализ мимикрии остова полярными боковыми цепями в белках». Белковая инженерия. 12 (6): 447–455. Дои:10.1093 / белок / 12.6.447. PMID 10388841.
- ^ Чакрабарти, П; Приятель Д. (2001). «Взаимосвязь конформаций боковой и основной цепи в белках». Прогресс в биофизике и молекулярной биологии. 76 (1–2): 1–102. Дои:10.1016 / с0079-6107 (01) 00005-0. PMID 11389934.
- ^ Дадди, WJ; Nissink WMJ; Аллен, Фрэнк Х .; Милнер-Уайт, Э. Джеймс (2004). «Мимикрия asx- и ST-поворотов четырех основных типов β-поворотов в белках». Белковая наука. 13 (11): 3051–3055. Дои:10.1110 / пс 04920904. ЧВК 2286581. PMID 15459339.
- ^ Такур, AK; Кишор Р. (2006). «Характеристика мимикрии β-поворотов и asx-поворотов в модельном пептиде: стабилизация посредством взаимодействия C-H ••• O». Биополимеры. 81 (6): 440–449. Дои:10.1002 / bip.20441. PMID 16411188.
- ^ Дадди, WJ; Nissink WMJ; Аллен, Фрэнк Х .; Милнер-Уайт, Э. Джеймс (2004). «Мимикрия asx- и ST-поворотов четырех основных типов бета-поворотов в белках». Белковая наука. 13 (11): 3051–3055. Дои:10.1110 / пс 04920904. ЧВК 2286581. PMID 15459339.
- ^ Дойг, AJ; Macarthur MW; MacArthur, Malcolm W .; Торнтон, Джанет М. (1997). «Структуры N-концов спиралей в белках». Белковая наука. 6 (1): 147–155. Дои:10.1002 / pro.5560060117. ЧВК 2143508. PMID 9007987.
- ^ Presta, LG; Роза Г.Д. (1988). «Крышки Helix». Наука. 240 (4859): 1632–1641. Bibcode:1988Научный ... 240.1632П. Дои:10.1126 / science.2837824. PMID 2837824.
- ^ Аврора, Р. Роза Г.Д. (1998). «Укупорка спирали». Белковая наука. 7 (1): 21–38. Дои:10.1002 / pro.5560070103. ЧВК 2143812. PMID 9514257.
- ^ Gunasekaran, K; Нагараджам HA; Рамакришнан, К; Баларам, П. (1998). «Стерохимические знаки препинания в структуре белка». Журнал молекулярной биологии. 275 (5): 917–932. Дои:10.1006 / jmbi.1997.1505. PMID 9480777. S2CID 35919397.
- ^ Дадди, WJ; Nissink WMJ; Аллен, Фрэнк Х .; Милнер-Уайт, Э. Джеймс (2004). «Мимикрия asx- и ST-поворотов четырех основных типов β-поворотов в белках». Белковая наука. 13 (11): 3051–3055. Дои:10.1110 / пс 04920904. ЧВК 2286581. PMID 15459339.
- ^ Ван, Висконсин; Милнер-Уайт EJ (2009). «Повторяющийся мотив с двумя водородными связями, включающий в себя остаток серина или треонина, обнаруживается как на α-спиральном N-конце, так и в других ситуациях». Журнал молекулярной биологии. 286 (5): 1651–1662. Дои:10.1006 / jmbi.1999.2551. PMID 10064721.
внешняя ссылка
- ^ Лидер, ДП; Милнер-Уайт EJ (2009). «Мотивированные белки: веб-приложение для изучения небольших трехмерных белковых мотивов». BMC Bioinformatics. 10: 60. Дои:10.1186/1471-2105-10-60. ЧВК 2651126. PMID 19210785.
- ^ Головин А; Хенрик К. (2008). «MSDmotif: изучение сайтов и мотивов белков». BMC Bioinformatics. 9: 312. Дои:10.1186/1471-2105-9-312. ЧВК 2491636. PMID 18637174.
