Треонин - Threonine
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Треонин | |
| Другие имена 2-амино-3-гидроксибутановая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.704 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C4ЧАС9NО3 | |
| Молярная масса | 119.120 г · моль−1 |
| (H2O, г / дл) 10,6 (30 °), 14,1 (52 °), 19,0 (61 °) | |
| Кислотность (пKа) | 2,63 (карбоксил), 10,43 (амино)[1] |
| Страница дополнительных данных | |
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ |
| УФ, ИК, ЯМР, РС | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Треонин (символ Thr или Т)[2] является аминокислота что используется в биосинтез из белки. Он содержит α-аминогруппа (который находится в протонированном −NH+
3 форма в биологических условиях), карбоксильная группа (который находится в депротонированном -COO− образуются в биологических условиях), и боковая цепь, содержащая гидроксильная группа, что делает его полярной незаряженной аминокислотой. это существенный у людей это означает, что организм не может его синтезировать: он должен быть получен с пищей. Треонин синтезируется из аспартат у бактерий, таких как Кишечная палочка.[3] это закодированный всеми кодоны пусковой AC (ACU, ACC, ACA и ACG).
Боковые цепи треонина часто связаны водородными связями; наиболее распространенные небольшие мотивы основаны на взаимодействии с серин: ST повороты, Мотивы ST (часто в начале альфа-спиралей) и Скобы ST (обычно в середине альфа-спиралей).
Модификации
Остаток треонина подвержен многочисленным посттрансляционные модификации. В гидроксил боковая цепь может пройти О-связанное гликозилирование. Кроме того, остатки треонина подвергаются фосфорилирование через действие треонина киназа. В фосфорилированной форме его можно обозначить как фосфотреонин. Фосфотреонин имеет три потенциальных координационных сайта (карбоксильная, аминная и фосфатная группа), и определение способа координации между фосфорилированными лигандами и ионами металлов, происходящими в организме, важно для объяснения функции фосфотреонина в биологических процессах.[4]
Это предшественник из глицин, и может использоваться как пролекарство для надежного повышения уровня глицина в мозге.
История
Треонин был последним из 20 распространенных протеиногенный аминокислоты, которые предстоит открыть. Он был открыт в 1936 г. Уильям Камминг Роуз[5], сотрудничая с Кертисом Мейером. Аминокислота была названа треонином, потому что она была похожа по структуре на треоновая кислота, четырехуглеродный моносахарид с участием молекулярная формула C4ЧАС8О5[6]
  |
| L-Треонин (2S,3р) и D-Треонин (2р,3S) |
 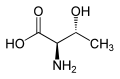 |
| L-Аллотреонин (2S,3S) и D-Аллотреонин (2р,3р) |
Треонин - одна из двух протеиногенных аминокислот с двумя хиральный центры, другое существо изолейцин. Треонин может существовать в четырех возможных стереоизомеры со следующими конфигурациями: (2S,3р), (2р,3S), (2S,3S) и (2р,3р). Однако имя L-реонин используется для одного сингла диастереомер, (2S,3р) -2-амино-3-гидроксибутановая кислота. Второй стереоизомер (2S,3S), редко встречающийся в природе, называется L-аллотреонин.[7] Два стереоизомера (2р,3S) - и (2р,3р) -2-амино-3-гидроксибутановая кислота имеют второстепенное значение.[нужна цитата ]
Биосинтез
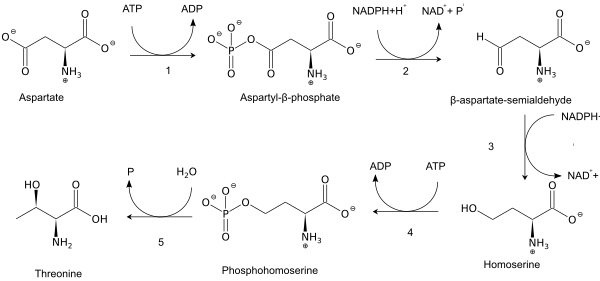
Как незаменимая аминокислота, треонин не синтезируется в организме человека и должен присутствовать в белках с пищей. Взрослым людям требуется около 20 мг / кг массы тела в день.[8] У растений и микроорганизмов треонин синтезируется из аспарагиновая кислота через α-аспартил-полуальдегид и гомосерин. Гомосерин подвергается О-фосфорилирование; этот фосфат сложный эфир подвергается гидролизу одновременно с перемещением группы ОН.[9] Ферменты, участвующие в типичном биосинтезе треонина, включают:
- аспартокиназа
- β-аспартат-полуальдегиддегидрогеназа
- гомосериндегидрогеназа
- гомосеринкиназа
- треонинсинтаза.
Метаболизм
Треонин метаболизируется по крайней мере тремя способами:
- У многих животных он превращается в пируват через треониндегидрогеназа. Промежуточное звено на этом пути может пройти тиолиз с CoA для производства ацетил-КоА и глицин.
- У человека ген треониндегидрогеназы неактивен. псевдоген[10], поэтому треонин превращается в α-кетобутират. Механизм первой стадии аналогичен катализируемому сериндегидратаза, и реакции серина и треониндегидратазы, вероятно, катализируются одним и тем же ферментом.[11]
- У многих организмов это О-фосфорилированный от киназа подготовительный к дальнейшему метаболизму. Это особенно важно в бактерии как часть биосинтез кобаламина (Витамин B12 ), поскольку продукт преобразуется в (R) -1-аминопропан-2-ол для включения в боковую цепь витамина.[12]
Источники
Продукты с высоким содержанием треонина включают: творог, домашняя птица, рыбы, мясо, чечевица, черная черепаха[13] и кунжут семена.[14]
Рацемический треонин можно получить из кротоновая кислота путем альфа-функционализации с использованием ацетат ртути (II).[15]
использованная литература
- ^ Доусон, R.M.C. и др., Данные для биохимических исследований, Oxford, Clarendon Press, 1959.
- ^ «Номенклатура и символика аминокислот и пептидов». Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983 г. В архиве из оригинала от 9 октября 2008 г.. Получено 5 марта 2018.
- ^ Раис, Бадр; Шассаньоль, Кристоф; Леттелье, Тьерри; Упал, Дэвид; Мазат, Жан-Пьер (2001). «Синтез треонина из аспартата в бесклеточных экстрактах Escherichia coli: динамика пути». J Biochem. 356 (Pt 2): 425–32. Дои:10.1042 / bj3560425. ЧВК 1221853. PMID 11368769.
- ^ Ястрзаб, Рената (2013). «Исследования новых комплексов фосфотреонина, образующихся в бинарных и тройных системах, включая биогенные амины и медь (II)». Журнал координационной химии. 66 (1): 98-113. DOI: 10.1080 / 00958972.2012.746678
- ^ Словарь ученых. Дейнтит, Джон., Гьертсен, Дерек. Оксфорд: Издательство Оксфордского университета. 1999. с. 459. ISBN 9780192800862. OCLC 44963215.CS1 maint: другие (ссылка на сайт)
- ^ Мейер, Кертис (20 июля 1936 г.). «Пространственная конфигурация альфа-амино-бета-гидрокси-н-масляной кислоты» (PDF). Журнал биологической химии. 115 (3).
- ^ «Номенклатура и символика аминокислот и пептидов (Рекомендации 1983 г.)». Чистая и прикладная химия. 56 (5): 601, 603, 608. 1 января 1984 г. Дои:10.1351 / pac198456050595.
- ^ Институт медицины (2002). «Белок и аминокислоты». Нормы потребления энергии, углеводов, клетчатки, жиров, жирных кислот, холестерина, белков и аминокислот с пищей. Вашингтон, округ Колумбия: The National Academies Press. С. 589–768.
- ^ Lehninger, Albert L .; Нельсон, Дэвид Л .; Кокс, Майкл М. (2000). Принципы биохимии (3-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 1-57259-153-6..
- ^ Стипанук, Марта Х .; Кодилл, Мари А. (13 августа 2013 г.). Биохимические, физиологические и молекулярные аспекты питания человека - электронная книга. Elsevier Health Sciences. ISBN 9780323266956.
- ^ Бхардвадж, Ума; Бхардвадж, Равиндра. Биохимия для медсестер. Pearson Education India. ISBN 9788131795286.
- ^ Фанг, H; Канг, Дж; Чжан, Д. (30 января 2017 г.). «Микробное производство витамина B12: обзор и перспективы ». Фабрики микробных клеток. 16 (1): 15. Дои:10.1186 / s12934-017-0631-у. ЧВК 5282855. PMID 28137297.
- ^ "Ошибка". ndb.nal.usda.gov.
- ^ «Данные о питании SELF - факты, информация о продуктах питания и калькулятор калорий». Nutritiondata.self.com. Получено 27 марта 2018.
- ^ Картер, Герберт Э.; Уэст, Гарольд Д. (1940). "dl-треонин". Органический синтез. 20: 101.; Коллективный объем, 3, п. 813.

