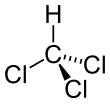
Хлороформ - Chloroform
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Трихлорметан | |||
| Другие имена Хлороформ[1] Трихлорид метана Метилтрихлорид Метенилтрихлорид Метенилхлорид TCM Фреон 20 Хладагент-20 R-20 ООН 1888 | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.603 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Свойства | |||
| CЧАСCl3 | |||
| Молярная масса | 119.37 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Обманчиво приятный эфирный запах, приводящий к обонятельной усталости | ||
| Плотность | 1,564 г / см3 (-20 ° С) 1,489 г / см3 (25 ° С) 1,394 г / см3 (60 ° С) | ||
| Температура плавления | -63,5 ° С (-82,3 ° F, 209,7 К) | ||
| Точка кипения | 61,15 ° С (142,07 ° F, 334,30 К) разлагается при 450 ° C | ||
| 10,62 г / л (0 ° С) 8,09 г / л (20 ° С) 7,32 г / л (60 ° С) | |||
| Растворимость | Растворим в бензол Смешивается в диэтиловый эфир, масла, лигроин, алкоголь, CCl4, CS2 | ||
| Растворимость в ацетон | ≥ 100 г / л (19 ° C) | ||
| Растворимость в диметилсульфоксид | ≥ 100 г / л (19 ° C) | ||
| Давление газа | 0,62 кПа (-40 ° C) 7,89 кПа (0 ° C) 25,9 кПа (25 ° C) 313 кПа (100 ° C) 2,26 МПа (200 ° C) | ||
Закон Генри постоянный (kЧАС) | 3,67 л · атм / моль (24 ° C) | ||
| Кислотность (пKа) | 15,7 (20 ° С) | ||
| УФ-видимый (λМаксимум) | 250 нм, 260 нм, 280 нм | ||
| −59.30·10−6 см3/ моль | |||
| Теплопроводность | 0,13 Вт / м · К (20 ° C) | ||
| 1,4459 (20 ° С) | |||
| Вязкость | 0,563 сП (20 ° C) | ||
| Структура | |||
| Тетраэдр | |||
| 1,15 D | |||
| Термохимия | |||
Теплоемкость (C) | 114,25 Дж / моль · К | ||
Стандартный моляр энтропия (S | 202,9 Дж / моль · К | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -134,3 кДж / моль | ||
Свободная энергия Гиббса (Δжг˚) | −71,1 кДж / моль | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | 473,21 кДж / моль | ||
| Фармакология | |||
| N01AB02 (КТО) | |||
| Опасности[7] | |||
| Основной опасности | Канцероген – Репродуктивная токсичность – Специфическая избирательная токсичность, поражающая отдельные органы-мишени (STOT )[2][3][4] | ||
| Паспорт безопасности | Увидеть: страница данных [1] | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H302, H315, H319, H331, H336, H351, H361d, H372 | |||
| P201, P202, P260, P264, P270, P271, P280, P281, P301 + 330 + 331, P310, P302 + 352, P304 + 340, P311, P305 + 351 + 338, P308 + 313, P314, P332 + 313, P337 + 313, P362, P403 + 233, P235, P405, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Не воспламеняется | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 704 мг / кг (мышь, кожный)[5] | ||
LC50 (средняя концентрация ) | 9617 частей на миллион (крыса, 4 часа)[6] | ||
LCLo (самый низкий опубликованный ) | 20000 частей на миллион (морская свинка, 2 часа) 7,056 частей на миллион (кошка, 4 часа) 25000 частей на миллион (человек, 5 мин)[6] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | 50 частей на миллион (240 мг / м3)[3] | ||
REL (Рекомендуемые) | Ca ST 2 частей на миллион (9,78 мг / м3) [60 минут][3] | ||
IDLH (Непосредственная опасность) | 500 частей на миллион[3] | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Хлороформ, или трихлорметан, является органическое соединение с участием формула CЧАСCl3. Это бесцветная, плотная жидкость с сильным запахом, которая производится в больших количествах как предшественник PTFE. Это также предшественник различных хладагенты.[8] Это один из четырех хлорметанов и тригалометан. Это мощный анестетик, эйфорический, анксиолитик и успокаивающее при вдыхании или проглатывании.[9][10]
Структура
Молекула принимает тетраэдрическая молекулярная геометрия с C3в симметрия.[нужна цитата ]
Естественное явление
Общий глобальный поток хлороформа через окружающую среду составляет приблизительно 660000 тонн в год,[11] и около 90% выбросов имеют естественное происхождение. Многие виды водоросли производить хлороформ, и грибы считается, что они производят хлороформ в почве.[12] Также считается, что абиотический процесс способствует естественному производству хлороформа в почвах, хотя механизм до сих пор неясен.[13]
Хлороформ легко улетучивается из почвы и поверхностных вод и подвергается разложению в воздухе с образованием фосген, дихлорметан, формилхлорид, монооксид углерода, углекислый газ, и хлористый водород. это период полураспада в воздухе колеблется от 55 до 620 суток. Биоразложение в воде и почве происходит медленно. Хлороформ практически не накапливается в водных организмах.[14]
История
Хлороформ был синтезирован независимо несколькими исследователями примерно в 1831 году:
- Молденхауэр, немецкий фармацевт из Франкфурт-на-Одере, похоже, произвел хлороформ в 1830 году путем смешивания хлорированная известь с участием этиловый спирт; однако он принял это за Chloräther (хлорноватый эфир, 1,2-дихлорэтан ).[15][16]
- Сэмюэл Гатри, американский врач из Сакетс-Харбор, Нью-Йорк, также, по-видимому, произвел хлороформ в 1831 году путем реакции хлорированной извести с этанолом, а также с учетом его анестезирующих свойств; однако он также считал, что приготовил хлорноватый эфир.[17][18][19]
- Юстус фон Либих выполнил щелочное расщепление из хлорал.[20][21]
- Эжен Субейран получил соединение под действием хлорный отбеливатель на обоих этиловый спирт и ацетон.[22]
- В 1834 г. французский химик Жан-Батист Дюма определил эмпирическую формулу хлороформа и назвал ее.[23] В 1835 году Дюма получил вещество щелочным расщеплением трихлоруксусная кислота. Regnault подготовил хлороформ хлорирование из хлорметан.[нужна цитата ]
- В 1842 г. Роберт Мортимер Гловер в Лондоне открыл анестезирующие свойства хлороформа на лабораторных животных.[24]
- В 1847 году шотландский акушер Джеймс Ю. Симпсон был первым, кто продемонстрировал анестезирующие свойства хлороформа на людях и помог популяризировать препарат для использования в медицине.[25] К 1850-м годам хлороформ производился на коммерческой основе с использованием процедуры Либиха, которая сохраняла свое значение до 1960-х годов. Сегодня хлороформ - вместе с дихлорметан - производится исключительно и в массовом порядке путем хлорирования метана и хлорметана.[8]
Производство
В промышленном производстве хлороформ получают путем нагревания смеси хлор и либо хлорметан (CH3Cl) или метан (CH4).[8] При 400–500 ° С свободнорадикальное галогенирование происходит, превращая эти прекурсоры во все более хлорированные соединения:
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
Хлороформ подвергается дальнейшему хлорированию с получением четыреххлористый углерод (CCl4):
- CHCl3 + Cl2 → CCl4 + HCl
Результатом этого процесса является смесь четырех хлорметанов (хлорметан, дихлорметан, хлороформ и четыреххлористый углерод), которые затем могут быть разделены дистилляция.[8]
Хлороформ также может производиться в небольших количествах через галоформная реакция между ацетон и гипохлорит натрия:[нужна цитата ]
- 3 NaClO + (CH3)2CO → CHCl3 + 2 NaOH + CH3COONa
Дейтерохлороформ
Дейтерированный хлороформ является изотополог хлороформа с одним дейтерий атом. CDCl3 является обычным растворителем, используемым в ЯМР-спектроскопия. Дейтерохлороформ производится галоформная реакция,[нужна цитата ] реакция ацетона (или этанола) с гипохлорит натрия или гипохлорит кальция.[8] Галоформный процесс в настоящее время является устаревшим для производства обычного хлороформа. Дейтерохлороформ можно получить реакцией дейтероксида натрия с хлоралгидрат.[26][27]
Непреднамеренное образование хлороформа
Галоформная реакция также может произойти непреднамеренно в домашних условиях. Отбеливание с участием гипохлорит образует галогенированные соединения в побочных реакциях; хлороформ является основным побочным продуктом.[28] Раствор гипохлорита натрия (хлорный отбеливатель ) смешанный с обычными бытовыми жидкостями, такими как ацетон, метилэтилкетон, этиловый спирт, или изопропиловый спирт может производить некоторое количество хлороформа в дополнение к другим соединениям, таким как хлорацетон или дихлорацетон.[нужна цитата ]
Использует
С точки зрения масштаба, наиболее важная реакция хлороформа с фтороводород давать монохлордифторметан (CFC-22), прекурсор при производстве политетрафторэтилена (Тефлон ):[8]
- CHCl3 + 2 HF → CHClF2 + 2 HCl
Реакция проводится в присутствии каталитического количества смешанные галогениды сурьмы. Затем хлордифторметан превращается в тетрафторэтилен, основной предшественник Тефлон. Перед Монреальский протокол, хлордифторметан (обозначенный как R-22) также был популярным хладагентом.[нужна цитата ]
Растворитель
В водород прикреплен к углерод в хлороформе участвует в образовании водородных связей.[29][30] Во всем мире хлороформ также используется в составах пестицидов в качестве растворитель для жиры, масла, резина, алкалоиды, воск, гуттаперча, и смолы, как очищающее средство, зерно фумигант, в огнетушители, и в резиновой промышленности.[14][31] CDCl3 является обычным растворителем, используемым в ЯМР-спектроскопия.[нужна цитата ]
Кислота Льюиса
В растворителях, таких как CCl4 и алканы, водородные связи хлороформа с множеством оснований Льюиса. HCCl3 классифицируется как твердая кислота и Модель ECW перечисляет свои кислотные параметры как EА = 1,56 и CА = 0.44.
Реагент
Как реагент, хлороформ служит источником дихлоркарбен : CCl2 группа.[32] Реагирует с водным гидроксид натрия обычно в присутствии катализатор межфазного переноса производить дихлоркарбен,: CCl2.[33][34] Этот реагент вызывает орто-формилирование активированных ароматические кольца такие как фенолы, производящий арил альдегиды в реакции, известной как Реакция Реймера – Тимана.. В качестве альтернативы карбен может быть пойман алкен сформировать циклопропан производная. в Дополнение Хараша, хлороформ образует CHCl2 свободный радикал в дополнение к алкенам.[нужна цитата ]
Анестетик

В анестетик свойства хлороформа были впервые описаны в 1842 г. в диссертации Роберт Мортимер Гловер, завоевавшего Золотую медаль Харвейское общество на тот год. Гловер также проводил практические эксперименты на собаках, чтобы доказать свою теорию. Гловер усовершенствовал свои теории и представил их в диссертации на соискание докторской степени в Эдинбургский университет летом 1847 года. Шотландская акушер Джеймс Янг Симпсон был одним из лиц, которым требовалось прочитать диссертацию, но позже заявил, что никогда не читал диссертацию и пришел к своим выводам независимо.[нужна цитата ]
4 ноября 1847 года Симпсон впервые обнаружил анестезирующие свойства хлороформа на людях. Он и двое его коллег развлекались, пробуя действие различных веществ, и таким образом раскрыли потенциал хлороформа в медицинских процедурах.[35]
Через несколько дней во время стоматологической процедуры в Эдинбург, Фрэнсис Броди Имлах стал первым человеком, который применил хлороформ к пациенту в клинических условиях.[36]
В мае 1848 г. Роберт Халлидей Ганнинг выступил с презентацией для Медико-хирургического общества Эдинбурга после серии лабораторных эксперименты на кроликах это подтвердило выводы Гловера, а также опровергло утверждения Симпсона об оригинальности. Однако рыцарство для Симпсона, а широкое освещение в СМИ чудес хлороформа обеспечило сохранение репутации Симпсона на высоком уровне, в то время как лабораторные эксперименты, доказывающие опасность хлороформа, в значительной степени игнорировались. Ганнинг, который стал одним из самых богатых людей Британии, предоставил около 13 университетских стипендий от имени других ученых, а не от своего имени. Он считал Симпсона шарлатаном, но одна из этих премий называется «Приз Симпсона в области акушерства». Однако это, вероятно, странный обратный комплимент, поскольку, возможно, любая премия Симпсона в глазах широкой общественности должна быть призом за анестезию. Не называя это так, он фактически пренебрегал Симпсоном, в то же время, казалось, оказывая ему честь.[37]
Применение хлороформа во время хирургия после этого быстро расширилась в Европе. В 1850-х годах хлороформ использовался при рождении Королева Виктория двое последних детей.[38] В США хлороформ начали заменять эфир как обезболивающее в начале 20 века; однако от него быстро отказались в пользу эфира после обнаружения его токсичности, особенно его склонности вызывать смертельный исход. аритмия сердца аналогично тому, что сейчас называется "внезапная смерть сниффера ". Некоторые люди использовали хлороформ как рекреационный наркотик или пытались покончить жизнь самоубийством.[39] Один из возможных механизмов действия хлороформа заключается в том, что он увеличивает движение калий ионов через определенные типы калиевые каналы в нервные клетки.[40] Хлороформ также можно смешивать с другими анестетиками, такими как эфир, чтобы получить смесь C.E., или эфир и алкоголь делать A.C.E. смесь.[нужна цитата ]
В 1848 году Ханна Гринер, 15-летняя девочка, которой удалили инфицированный ноготь на ноге, умерла после введения анестетика.[41] Ее вскрытие, установившее причину смерти, было проведено Джон Файф при поддержке Роберт Мортимер Гловер.[24] Несколько физически здоровых пациентов умерли после его вдыхания. Однако в 1848 г. Джон Сноу разработали ингалятор, который регулировал дозировку и таким образом успешно снижал количество смертей.[42]
Противники и сторонники хлороформа в основном расходились с вопросом о том, были ли осложнения исключительно из-за нарушения дыхания или хлороформ оказывает специфическое воздействие на сердце. Между 1864 и 1910 годами многочисленные комиссии в Великобритании изучали хлороформ, но не смогли прийти к каким-либо четким выводам. Только в 1911 году Леви в экспериментах на животных доказал, что хлороформ может вызывать фибрилляцию сердца. Оговорки по поводу хлороформа не могли остановить его стремительный рост. Примерно между 1865 и 1920 годами хлороформ использовался в 80-95% всех наркозов, проводившихся в Великобритании и немецкоязычных странах. В Америке, однако, хлороформный наркоз проявлял меньше энтузиазма. В Германии первые всесторонние исследования уровня смертности во время наркоза были проведены Гурлтом между 1890 и 1897 годами. В 1934 году Киллиан собрал всю статистику, собранную к тому времени, и обнаружил, что шансы получить летальные осложнения под действием эфира составляли от 1:14 000 до 1: 28 000, тогда как под хлороформом шансы были от 1: 3 000 до 1: 6 000. Рост газовой анестезии с использованием оксид азота, улучшенное оборудование для введения анестетиков и открытие гексобарбитал в 1932 г. привел к постепенному упадку хлороформного наркоза.[43]
Преступное использование
Хлороформ, по общему мнению, использовался преступниками для нокаутации, ошеломления или даже убийства жертв. В 1894 году Джозефу Харрису было предъявлено обвинение в использовании хлороформа для ограбления людей.[44] Серийный убийца Х. Х. Холмс использовал передозировку хлороформа, чтобы убить своих жертв женского пола. В сентябре 1900 года хлороформ был причастен к убийству американского бизнесмена. Уильям Марш Райс, тезка учреждения, ныне известного как Университет Райса. Хлороформ был признан фактором предполагаемого убийства женщины в 1991 году, когда она задохнулась во время сна.[45] В сделке о признании вины в 2007 году мужчина признался в использовании электрошокеры и хлороформ для сексуальных посягательств несовершеннолетних.[46]
Использование хлороформа в качестве выводящий из строя агент получила широкое признание, граничащая с клише, из-за популярности криминальная фантастика Авторы, имеющие преступников, используют пропитанные хлороформом тряпки, чтобы потерять сознание. Однако таким способом вывести из строя кого-либо, используя хлороформ, практически невозможно.[47] Чтобы потерять сознание, нужно как минимум пять минут вдохнуть предмет, пропитанный хлороформом. Большинство уголовных дел, связанных с хлороформом, также связаны с совместным применением другого наркотика, такого как алкоголь или диазепам, или потерпевший был признан соучастником в его применении. После того, как человек потерял сознание из-за вдыхания хлороформа, необходимо ввести постоянный объем и поддержать подбородок, чтобы язык не препятствовал прохождению дыхательных путей, - сложная процедура, обычно требующая навыков специалиста. анестезиолог. В 1865 г., как прямое следствие криминальной репутации хлороформа, медицинский журнал Ланцет предлагал «постоянную научную репутацию» любому, кто мог продемонстрировать «мгновенную нечувствительность», то есть мгновенно терять сознание, используя хлороформ.[48]
Безопасность
Воздействие
Известно, что хлороформ образуется как побочный продукт хлорирование воды наряду с рядом других побочные продукты дезинфекции и как таковой обычно присутствует в муниципальной водопроводной воде и плавательных бассейнах. Сообщаемые диапазоны значительно различаются, но в целом они ниже текущего стандарта здоровья. тригалометаны 100 мкг / л.[49] Тем не менее, некоторые считают наличие хлороформа в питьевой воде в любой концентрации спорным.[нужна цитата ]
Исторически воздействие хлороформа могло быть выше из-за его обычного использования в качестве анестетика, в качестве ингредиента сиропов от кашля и в качестве компонента табачный дым где п, п'-ДДТ ранее использовался как фумигант.[50]
Фармакология
Он хорошо всасывается, метаболизируется и быстро выводится млекопитающими после перорального, ингаляционного или кожного воздействия. Случайное попадание брызг в глаза вызвало раздражение.[14] Длительное воздействие на кожу может привести к развитию язв в результате обезжиривание. Выведение происходит в основном из легких в виде хлороформа и диоксида углерода; менее 1% выводится с мочой.[31]
Хлороформ метаболизируется в печени цитохром Р-450 ферменты путем окисления до хлорметанол и восстановлением до дихлорметила свободный радикал. Другие метаболиты хлороформа включают: соляная кислота и диглуатионил дитиокарбонат, с участием углекислый газ как преобладающий конечный продукт метаболизма.[51]
Как и большинство других общих анестетиков и седативно-снотворных средств, хлороформ положительный аллостерический модулятор для ГАМКА рецептор.[52] Хлороформ вызывает угнетение Центральная нервная система (ЦНС), в конечном итоге производя глубокое кома угнетение дыхательного центра.[51] При проглатывании хлороформ вызывал симптомы, подобные тем, которые наблюдаются при вдыхании. После приема 7,5 г (0,26 унции) наступило серьезное заболевание. Средняя летальная пероральная доза для взрослого оценивается примерно в 45 г (1,6 унции).[14]
Анестезирующее использование хлороформа было прекращено, поскольку оно приводило к смерти из-за дыхательной недостаточности и сердечной аритмии. После анестезии хлороформом некоторые пациенты пострадали тошнота, рвота, гипертермия, желтуха, и кома из-за печеночная дисфункция. При вскрытии печень некроз и дегенерация наблюдались.[14]
Хлороформ вызвал опухоли печени у мышей и опухоли почек у мышей и крыс.[14] Считается, что гепатотоксичность и нефротоксичность хлороформа в основном связаны с фосген.[51]
Превращение в фосген
В воздухе хлороформ медленно превращается в чрезвычайно ядовитый фосген (COCl2), выпуская HCl в процессе.[53]
- 2 CHCl3 + O2 → 2 COCl2 + 2 HCl
Чтобы предотвратить несчастные случаи, коммерческий хлороформ стабилизирован этиловый спирт или амилен, но образцы, которые были восстановлены или высушены, больше не содержат стабилизатора. Амилен оказался неэффективным, а фосген может влиять на анализируемые вещества в образцах, липиды и нуклеиновые кислоты, растворенные в хлороформе или экстрагированные им.[54] Фосген и HCl можно удалить из хлороформа промыванием насыщенным водным раствором. карбонат решения, такие как бикарбонат натрия. Эта процедура проста и дает безвредные продукты. Фосген реагирует с водой с образованием углекислый газ и HCl,[55] и карбонатная соль нейтрализует полученная кислота.[нужна цитата ]
Подозрительные образцы могут быть проверены на фосген с использованием фильтровальной бумаги (обработанной 5% дифениламин, 5% диметиламинобензальдегид в этиловый спирт, а затем сушат), который желтеет в парах фосгена. Есть несколько колориметрический и флуорометрический реагенты на фосген, а также его можно количественно определить с помощью масс-спектрометрии.[нужна цитата ]
Регулирование
Предполагается, что хлороформ вызывает рак (т.е. возможно канцерогенный, IARC Group 2B ) в соответствии с Международное агентство по изучению рака (МАИР) Монографии. [PDF]
Классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как определено в Разделе 302 США Закон о чрезвычайном планировании и праве общества на информацию (42 U.S.C. 11002) и подлежат строгим требованиям отчетности предприятий, которые производят, хранят или используют его в значительных количествах.[56]
Биоремедиация хлороформа
Некоторые анаэробные бактерии используют хлороформ для дыхания, называемого органогалогенидное дыхание, превращая его в дихлорметан.[57][58]
использованная литература
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 661. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
Сохраненные названия «бромоформ» для HCBr3, «хлороформ» для HCCl3, и «йодоформ» для HCI3 приемлемы в общей номенклатуре. Предпочтительные названия IUPAC - замещающие названия.
- ^ «Часть 3: опасность для здоровья» (PDF). Согласованная на глобальном уровне система классификации и маркировки химических веществ (СГС). Издание второе исправленное. Организация Объединенных Наций. Получено 30 сентября 2017.
- ^ а б c d Карманный справочник NIOSH по химической опасности. "#0127". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Токсичность на PubChem
- ^ Льюис, Ричард Дж. (2012). Опасные свойства промышленных материалов Sax (12-е изд.). ISBN 978-0-470-62325-1.
- ^ а б "Хлороформ". Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ «PubChem: Безопасность и опасности - Классификация GHS». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d е ж Россберг, М .; и другие. «Хлорированные углеводороды». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a06_233.pub2.
- ^ «Эфир и хлороформ». В архиве из оригинала 24 марта 2018 г.. Получено 24 апреля 2018.
- ^ Ac08468611], [Анонимус (2012). «Хлороформ [MAK Value Documentation, 2000]». МАК-Сборник по охране труда. С. 20–58. Дои:10.1002 / 3527600418.mb6766e0014. ISBN 978-3527600410.CS1 maint: лишняя пунктуация (ссылка на сайт) CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ Гриббл, Гордон В. (2004). «Природные органогалогены: новый рубеж для лекарственных средств?». Журнал химического образования. 81 (10): 1441. Bibcode:2004JChEd..81.1441G. Дои:10.1021 / ed081p1441.
- ^ Каппеллетти, М. (2012). «Микробное разложение хлороформа». Прикладная микробиология и биотехнология. 96 (6): 1395–409. Дои:10.1007 / s00253-012-4494-1. PMID 23093177. S2CID 12429523.
- ^ Цзяо, И; и другие. (2018). «Выбросы галоуглерода из деградированных лесных водно-болотных угодий в прибрежной части Южной Каролины, подвергшейся воздействию повышения уровня моря». ACS Earth and Space Chemistry. 2 (10): 955–967. Bibcode:2018ECS ..... 2..955J. Дои:10.1021 / acsearthspacechem.8b00044.
- ^ а б c d е ж Хлороформ (PDF), CICAD, 58, Всемирная организация здоровья, 2004, в архиве (PDF) из оригинала 31 июля 2020 г.
- ^ Молденхауэра (1830 г.). "Verfahren den Spiritus von dem Fuselöl auf leichte Weise zu befreien" [Процедура легкого удаления этанола из сивушного масла]. Magazin für Pharmacie. 8 (31): 222–227.
- ^ Дефалк, Рэй Дж .; Райт, А. Дж. (2000). «Производился ли хлороформ до 1831 года?». Анестезиология. 92 (1): 290–291. Дои:10.1097/00000542-200001000-00060. PMID 10638939.
- ^ Гатри, Сэмюэл (1832). «Новый режим приготовления спиртового раствора хлорнового эфира». Американский журнал науки и искусства. 21: 64–65 и 405–408.
- ^ Гатри, Оссиан (1887). Мемуары доктора Сэмюэля Гатри и история открытия хлороформа. Чикаго: Джордж К. Хэзлитт и Ко, стр.1.
- ^ Стратманн, Линда (2003). "Глава 2". Хлороформ: поиски забвения. Страуд: Саттон Паблишинг. ISBN 9780752499314.
- ^ Либих, Юстус фон (1831). "Ueber die Zersetzung des Alkohols durch Chlor" [О разложении спирта хлором]. Annalen der Physik und Chemie. 99 (11): 444. Bibcode:1831АнП .... 99..444Л. Дои:10.1002 / andp.18310991111.
- ^ Либих, Юстус фон (1832). "Ueber die Verbindungen, welche durch die Einwirkung des Chlors auf Alkohol, Aether, ölbildendes Gas und Essiggeist entstehen" [О соединениях, которые возникают при реакции хлора со спиртом [этанолом], эфиром [диэтиловым эфиром], маслообразующим газом [этиленом] и спиртом уксуса [ацетоном]]. Annalen der Physik und Chemie. 100 (2): 243–295. Bibcode:1832АнП ... 100..243л. Дои:10.1002 / andp.18321000206.
На страницах 259–265 Либих описывает Chlorkohlenstoff («хлористый углерод», хлороформ), но на стр. 264, Либих неправильно утверждает, что эмпирическая формула хлороформа - C2Cl5. - ^ Субейран, Эжен (1831). "Recherches sur quelques combinaisons du chlore" [Исследования некоторых соединений хлора]. Annales de Chimie et de Physique. Серия 2. 48: 113–157.
- Перепечатано в Субейран, Эжен (1831). "Recherches sur quelques combinaisons du chlore" [Исследования некоторых соединений хлора]. Journal de Pharmacie et des Sciences Accessoires. 17: 657–672.
- Перепечатано в Субейран, Эжен (1832). «Suite des recherches sur quelques combinaisons du chlore» [Продолжение исследований некоторых соединений хлора]. Journal de Pharmacie et des Sciences Accessoires. 18: 1–24.
- ^ Дюма, Ж.-Б. (1834 г.). «Récherches rélative à l'action du chlore sur l'alcool» [Эксперименты, касающиеся действия хлора на спирт]. L'Institut, Journal Général des Sociétés et Travaux Scientifiques de la France et de l'Etranger. 2: 106–108 и 112–115.
- Перепечатано в Дюма, Ж.-Б. (1834 г.). "Untersuchung über die Wirkung des Chlors auf den Alkohol" [Исследование действия хлора на спирт]. Annalen der Physik und Chemie. 107 (42): 657–673. Bibcode:1834AnP ... 107..657D. Дои:10.1002 / andp.18341074202.
На стр. 653, Дюма приводит эмпирическую формулу хлороформа:
- "Es scheint mir also erweisen, dass die von mir analysirte Substance,… zur Formel hat: C2ЧАС2Cl6." (Таким образом, мне кажется, что это вещество, [которое] проанализировано мной… имеет в качестве [своей эмпирической] формулы: C2ЧАС2Cl6.) [Примечание: коэффициенты его эмпирической формулы должны быть уменьшены вдвое.]
- Затем Дюма отмечает, что хлороформ прост. эмпирическая формула похож на Муравьиная кислота. Кроме того, если хлороформ кипятить с гидроксид калия, один из продуктов формиат калия. На стр. 654, Дюма называет хлороформ:
- "Diess hat mich veranlasst diese Substanz mit dem Namen 'Chloroform' zu belegen". (Это заставило меня присвоить этому веществу название «хлороформ» [т.е. формилхлорид или хлорид муравьиной кислоты].)
- Перепечатано в Дюма, Ж.-Б. (1835 г.). "Ueber die Wirkung des Chlors auf den Alkohol" [О действии хлора на спирт]. Annalen der Pharmacie. 16 (2): 164–171. Дои:10.1002 / jlac.18350160213.
- Перепечатано в Дюма, Ж.-Б. (1834 г.). "Untersuchung über die Wirkung des Chlors auf den Alkohol" [Исследование действия хлора на спирт]. Annalen der Physik und Chemie. 107 (42): 657–673. Bibcode:1834AnP ... 107..657D. Дои:10.1002 / andp.18341074202.
- ^ а б Defalque, R.J .; Райт, А. Дж. (2004). «Короткая трагическая жизнь Роберта М. Гловера» (PDF). Анестезия. 59 (4): 394–400. Дои:10.1111 / j.1365-2044.2004.03671.x. PMID 15023112. S2CID 46428403. В архиве (PDF) из оригинала от 9 марта 2016 г.
- ^ "Сэр Джеймс Янг Симпсон". Британская энциклопедия. В архиве из оригинала 27 июля 2013 г.. Получено 23 августа 2013.
- ^ Брейер, Ф. В. (1935). «Хлороформ-д (дейтериохлороформ) 1». Журнал Американского химического общества. 57 (11): 2236–2237. Дои:10.1021 / ja01314a058.
- ^ Клугер, Рональд (1964). «Удобный препарат хлороформа-d1». Журнал органической химии. 29 (7): 2045–2046. Дои:10.1021 / jo01030a526.
- ^ Зюсс, Ганс Ульрих. «Отбеливание». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH.
- ^ Wiley, G.R .; Миллер, С. И. (1972). «Термодинамические параметры водородной связи хлороформа с основаниями Льюиса в циклогексане. Исследование протонного магнитного резонанса». Журнал Американского химического общества. 94 (10): 3287–3293. Дои:10.1021 / ja00765a001.
- ^ Kwak, K .; Розенфельд, Д. Э .; Chung, J. K .; Файер, М. Д. (2008). «Динамика переключения комплекса растворенное вещество-растворитель хлороформа между ацетоном и диметилсульфоксидом - двумерная ИК-спектроскопия химического обмена». Журнал физической химии B. 112 (44): 13906–13915. Дои:10.1021 / jp806035w. ЧВК 2646412. PMID 18855462.
- ^ а б Leikin, Jerrold B .; Палоучек, Фрэнк П., ред. (2008). "Хлороформ". Справочник по отравлению и токсикологии (4-е изд.). Informa. п. 774.
- ^ Сребник, М .; Лалоэ, Э. (2001). "Хлороформ". Энциклопедия реагентов для органического синтеза. Вайли. Дои:10.1002 / 047084289X.rc105. ISBN 978-0471936237.
- ^ Vogel, E .; Klug, W .; Брейер, А. (1988). «1,6-Метано [10] аннулен». Органический синтез.; Коллективный объем, 6, п. 731
- ^ Gokel, G.W .; Widera, R.P .; Вебер, В. П. (1988). "Фазовая реакция карбиламина Гофмана: терт-Бутил изоцианид ». Органический синтез.; Коллективный объем, 6, п. 232
- ^ Гордон, Х. Лэйнг (ноябрь 2002 г.). Сэр Джеймс Янг Симпсон и хлороформ (1811–1870). Минерва Групп. С. 106–109. ISBN 978-1-4102-0291-8.
- ^ Дингуолл (апрель 2004 г.). «Новаторская история: стоматология и Королевский колледж хирургов Эдинбурга» (PDF). historyofdentistry.co.uk. Архивировано из оригинал (PDF) 1 февраля 2013 г.
- ^ Бэйли, Т. В. (2003). "Роберт Халлидей Ганнинг и награды юбилея Виктории" (PDF). Шотландский медицинский журнал. 48 (2): 54–57. Дои:10.1177/003693300304800209. PMID 12774598. S2CID 10998512. Архивировано из оригинал (PDF) 22 августа 2016 г.. Получено 18 августа 2016.
- ^ «Анестезия и королева Виктория». ph.ucla.edu. В архиве из оригинала 16 июля 2012 г.. Получено 13 августа 2012.
- ^ Мартин, Уильям (3 июля 1886 г.). «Случай отравления хлороформом; выздоровление». Британский медицинский журнал. 2 (1331): 16–17. Дои:10.1136 / bmj.2.1331.16-а. ЧВК 2257365. PMID 20751619.
- ^ Патель, Аманда Дж .; Оноре, Эрик; Лесаж, Флориан; Финк, Мишель; Роми, Жорж; Лаздунски, Мишель (май 1999). «Ингаляционные анестетики активируют двухпоровый фон K+ каналы". Природа Неврология. 2 (5): 422–426. Дои:10.1038/8084. PMID 10321245. S2CID 23092576.
- ^ Найт, Пол Р., III; Бэкон, Дуглас Р. (2002). «Необъяснимая смерть: Ханна Гринер и хлороформ». Анестезиология. 96 (5): 1250–1253. Дои:10.1097/00000542-200205000-00030. PMID 11981167. S2CID 12865865.
- ^ Сноу, Джон (1858). О хлороформе и других анестетиках, их действии и применении. Лондон: Джон Черчилль. С. 82–85. В архиве из оригинала от 23 ноября 2015 г.
- ^ Ваверсик Дж. (1997). «История хлороформной анестезии». Анестезиология и реанимация. 22 (6): 144–152. PMID 9487785.
- ^ «Нокаут и хлороформ». The Philadelphia Record. 9 февраля 1894 г.. Получено 31 марта 2011.
- ^ «Продолжается повторное рассмотрение дела о хлороформе». Запись-Журнал. 7 июля 1993 г.. Получено 31 марта 2011.
- ^ «Мужчина признался в изнасиловании дочерей друзей». USA Today. 6 ноября 2007 г. В архиве из оригинала 29 апреля 2011 г.. Получено 31 марта 2011.
- ^ Пейн, Дж. П. (июль 1998 г.). «Преступное использование хлороформа». Анестезия. 53 (7): 685–690. Дои:10.1046 / j.1365-2044.1998.528-az0572.x. PMID 9771177. S2CID 1718276.
- ^ «Медицинская аннотация: Хлороформ среди воров». Ланцет. 2 (2200): 490–491. 1865. Дои:10.1016 / с0140-6736 (02) 58434-8.
- ^ Nieuwenhuijsen, MJ; Толедано, МБ; Эллиотт, П. (8 августа 2000 г.). «Использование побочных продуктов дезинфекции хлорированием; обзор и обсуждение их значения для оценки воздействия в эпидемиологических исследованиях». Журнал анализа воздействия и экологической эпидемиологии. 10 (6 Pt 1): 586–99. Дои:10.1038 / sj.jea.7500139. PMID 11140442.
- ^ Инь-Так Ву, Дэвид Ю. Лай, Джозеф С. Аркос Алифатические и полигалогенированные канцерогены: структурные основы и биологические В архиве 5 июня 2018 г. Wayback Machine
- ^ а б c Вентилятор, Анна М. (2005). "Хлороформ". Энциклопедия токсикологии. 1 (2-е изд.). Эльзевир. С. 561–565.
- ^ Дженкинс, Эндрю; Гринблатт, Эрик П .; Фолкнер, Ховард Дж .; Бертаччини, Эдвард; Свет, Адам; Лин, Одри; Андреасен, Элисон; Винер, Анна; Trudell, James R .; Харрисон, Нил Л. (15 марта 2001 г.). «Доказательства наличия общей связывающей полости для трех общих анестетиков в рецепторе ГАМК». Журнал неврологии. 21 (6): RC136. Дои:10.1523 / JNEUROSCI.21-06-j0002.2001. ISSN 0270-6474. ЧВК 6762625. PMID 11245705.
- ^ «Хлороформ и фосген, химическая гигиена и безопасность». Earlham College. В архиве с оригинала 19 августа 2017 г.. Получено 17 августа 2017.
- ^ Терк, Эрик (2 марта 1998 г.). «Фосген из хлороформа». Новости химии и машиностроения. 76 (9): 6. Дои:10.1021 / cen-v076n009.p006.
- ^ «фосген (химическое соединение)». Британская энциклопедия. В архиве из оригинала 5 июня 2013 г.. Получено 16 августа 2013.
- ^ «40 C.F.R .: Приложение A к Части 355 - Список особо опасных веществ и их планируемые пороговые количества» (PDF) (1 июля 2008 г. ред.). Государственная типография. Архивировано из оригинал (PDF) 25 февраля 2012 г.. Получено 29 октября 2011. Цитировать журнал требует
| журнал =(Помогите) - ^ Шуйцюань Тан; Элизабет А. Эдвардс (2013). «Идентификация дегалогеназ, восстанавливающих Dehalobacter, которые катализируют дехлорирование хлороформа, 1,1,1-трихлорэтана и 1,1-дихлорэтана». Philos Trans R Soc Lond B Biol Sci. 368 (1616): 20120318. Дои:10.1098 / rstb.2012.0318. ЧВК 3638459. PMID 23479748.
- ^ Югдер, Бат-Эрдене; Эртан, Халук; Вонг, Йе Куан; Брейди, Нади; Мэнфилд, Майкл; Маркиз, Кристофер П .; Ли, Мэтью (10 августа 2016 г.). «Геномный, транскриптомный и протеомный анализ Dehalobacter UNSWDHB в ответ на хлороформ». Отчеты по микробиологии окружающей среды. 8 (5): 814–824. Дои:10.1111/1758-2229.12444. ISSN 1758-2229. PMID 27452500.
внешние ссылки
- Хлороформ «Молекулярный спасатель» Статья в Оксфордском университете, содержащая факты о хлороформе.
- Краткий международный документ по химической оценке 58
- Обобщения и оценки МАИР: Vol. 1 (1972), Vol. 20 (1979), Дополнение 7 (1987), Vol. 73 (1999)
- Международная карта химической безопасности 0027
- Карманный справочник NIOSH по химической опасности. "#0127". Национальный институт охраны труда и здоровья (NIOSH).
- Стандартная справочная база данных NIST