Водород - Hydrogen
 Пурпурное свечение в плазменном состоянии | |||||||||||||||||||||
| Водород | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Внешность | бесцветный газ | ||||||||||||||||||||
| Стандартный атомный вес Аr, std(ЧАС) | [1.00784, 1.00811] общепринятый:1.008 | ||||||||||||||||||||
| Водород в периодическая таблица | |||||||||||||||||||||
| |||||||||||||||||||||
| Атомный номер (Z) | 1 | ||||||||||||||||||||
| Группа | 1: H и щелочные металлы | ||||||||||||||||||||
| Период | период 1 | ||||||||||||||||||||
| Блокировать | s-блок | ||||||||||||||||||||
| Категория элемента | Реактивный неметалл | ||||||||||||||||||||
| Электронная конфигурация | 1 с1 | ||||||||||||||||||||
| Электронов на оболочку | 1 | ||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||
| Фаза вSTP | газ | ||||||||||||||||||||
| Температура плавления | (ЧАС2) 13.99 K (-259,16 ° С, -434,49 ° F) | ||||||||||||||||||||
| Точка кипения | (ЧАС2) 20,271 К (-252,879 ° С, -423,182 ° F) | ||||||||||||||||||||
| Плотность (на СТП) | 0,08988 г / л | ||||||||||||||||||||
| в жидком состоянии (приm.p.) | 0,07 г / см3 (твердое вещество: 0,0763 г / см3)[1] | ||||||||||||||||||||
| в жидком состоянии (приб.п.) | 0,07099 г / см3 | ||||||||||||||||||||
| Тройная точка | 13,8033 К, 7,041 кПа | ||||||||||||||||||||
| Критическая точка | 32,938 К, 1,2858 МПа | ||||||||||||||||||||
| Теплота плавления | (ЧАС2) 0.117 кДж / моль | ||||||||||||||||||||
| Теплота испарения | (ЧАС2) 0,904 кДж / моль | ||||||||||||||||||||
| Молярная теплоемкость | (ЧАС2) 28,836 Дж / (моль · К) | ||||||||||||||||||||
Давление газа
| |||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||
| Состояния окисления | −1, +1 (анамфотерный окись) | ||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,20 | ||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||
| Ковалентный радиус | 31±5 вечера | ||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 120 вечера | ||||||||||||||||||||
| Другие свойства | |||||||||||||||||||||
| Естественное явление | изначальный | ||||||||||||||||||||
| Кристальная структура | шестиугольник | ||||||||||||||||||||
| Скорость звука | 1310 РС (газ, 27 ° C) | ||||||||||||||||||||
| Теплопроводность | 0,1805 Вт / (м · К) | ||||||||||||||||||||
| Магнитный заказ | диамагнитный[2] | ||||||||||||||||||||
| Магнитная восприимчивость | −3.98·10−6 см3/ моль (298 К)[3] | ||||||||||||||||||||
| Количество CAS | 12385-13-6 1333-74-0 (Н2) | ||||||||||||||||||||
| История | |||||||||||||||||||||
| Открытие | Генри Кавендиш[4][5] (1766) | ||||||||||||||||||||
| Названный | Антуан Лавуазье[6] (1783) | ||||||||||||||||||||
| Главный изотопы водорода | |||||||||||||||||||||
| |||||||||||||||||||||
Водород это химический элемент с символ ЧАС и атомный номер 1. С стандартный атомный вес из 1.008, водород - самый легкий элемент в периодическая таблица. Водород - это Наиболее обильные химическое вещество в вселенная, что составляет примерно 75% всех барионный масса.[7][примечание 1] Не-остаток звезды в основном состоят из водорода в состояние плазмы. Самый распространенный изотоп водорода, называемого протий (название используется редко, символ 1H), имеет один протон и нет нейтроны.
Повсеместное появление атомарного водорода впервые произошло во время эпоха рекомбинации (Большой взрыв ). В стандартная температура и давление, водород - это бесцветный, без запаха, безвкусный, нетоксичный, неметаллических, высоко горючий двухатомный газ с молекулярная формула ЧАС2. Поскольку водород легко образует ковалентный соединения с большинством неметаллических элементов, большая часть водорода на Земле существует в молекулярные формы Такие как воды или же органические соединения. Водород играет особенно важную роль в кислотно-основные реакции потому что большинство кислотно-основных реакций включают обмен протонами между растворимыми молекулами. В ионные соединения, водород может иметь форму отрицательного заряда (т. е. анион ) когда он известен как гидрид, или как положительно заряженный (т.е. катион ) разновидность обозначается символом H+. Катион водорода записывается, как если бы он состоял из чистого протона, но на самом деле катионы водорода в ионных соединениях всегда более сложные. Как единственный нейтральный атом, для которого Уравнение Шредингера можно решить аналитически,[8] изучение энергетики и связи атома водорода сыграло ключевую роль в развитии квантовая механика.
Впервые газообразный водород был искусственно получен в начале 16 века путем реакции кислот на металлы. В 1766–81 гг. Генри Кавендиш был первым, кто осознал, что газообразный водород представляет собой дискретное вещество,[9] и что он производит воду при сгорании, свойство, в честь которого он был позже назван: по-гречески водород означает «водообразователь».
Промышленное производство в основном происходит от парового риформинга природного газа и реже от более энергоемких методов, таких как электролиз воды.[10] Большая часть водорода используется рядом с местом его производства, причем двумя наиболее крупными видами использования являются: ископаемое топливо обработка (например, гидрокрекинг ) и аммиак производство, в основном для рынка удобрений. Водород проблематичен металлургия потому что это может хрупкий много металлов,[11] усложнение конструкции трубопроводов и резервуаров для хранения.[12]
Характеристики
Горение

Водородный газ (дигидроген или молекулярный водород)[13] легко воспламеняется:
- 2 ч2(г) + O2(г) → 2 H2O (l) + 572 кДж (286 кДж / моль)[заметка 2]
В энтальпия горения составляет -286 кДж / моль:[14]
Газообразный водород образует с воздухом взрывоопасные смеси в концентрациях от 4 до 74%.[15] и с хлором 5–95%. Взрывные реакции могут быть вызваны искрой, теплом или солнечным светом. Водород температура самовоспламенения, температура самовозгорания на воздухе составляет 500 ° C (932 ° F).[16]
Пламя
Чистый водород-кислород испускать пламя ультрафиолетовый свет и смесь с высоким содержанием кислорода почти невидимы невооруженным глазом, о чем свидетельствует слабый шлейф Главный двигатель космического челнока, по сравнению с хорошо заметным шлейфом Ракетный ускоритель космического челнока, который использует композит перхлората аммония. Обнаружение утечки горящего водорода может потребовать детектор пламени; такие утечки могут быть очень опасными. Пламя водорода в других условиях имеет синий цвет, напоминающий голубое пламя природного газа.[17] В уничтожение дирижабля Гинденбург был печально известным примером горения водорода, и причина этого до сих пор обсуждается. Видимое оранжевое пламя в этом инциденте было результатом богатой смеси водорода и кислорода в сочетании с углеродными соединениями обшивки дирижабля.
Реагенты
ЧАС2 относительно инертен. Термодинамической основой этой низкой реакционной способности является очень прочная связь H-H с энергия диссоциации связи 435,7 кДж / моль.[18] Кинетическая основа низкой реакционной способности - неполярная природа H2 и его слабая поляризуемость. Самопроизвольно реагирует с хлор и фтор формировать хлористый водород и фтороводород, соответственно.[19] Реакционная способность H2 сильно зависит от наличия металлических катализаторов. Таким образом, пока H2 легко горит, смеси H2 и O2 не реагируют в отсутствие катализатора.
Уровни энергии электронов

В основное состояние уровень энергии электрона в атоме водорода составляет -13,6эВ,[20] что эквивалентно ультрафиолету фотон из примерно 91нм длина волны.[21]
Уровни энергии водорода можно довольно точно рассчитать с помощью Модель Бора атома, который концептуализирует электрон как "вращающийся вокруг" протона по аналогии с орбитой Земли вокруг Солнца. Однако атомный электрон и протон удерживаются вместе за счет электромагнитная сила, а планеты и небесные объекты удерживаются сила тяжести. Из-за дискретности угловой момент постулированный в начале квантовая механика Согласно Бору, электрон в модели Бора может занимать только определенные разрешенные расстояния от протона и, следовательно, только определенные разрешенные энергии.[22]
Более точное описание атома водорода можно получить с помощью чисто квантово-механической обработки, в которой используется Уравнение Шредингера, Уравнение Дирака или даже Фейнман формулировка интеграла по путям рассчитать плотность вероятности электрона вокруг протона.[23] Самые сложные методы лечения позволяют получить небольшие эффекты специальная теория относительности и поляризация вакуума. С точки зрения квантовой механики, электрон в основном состоянии атома водорода вообще не имеет углового момента, что показывает, чем «планетарная орбита» отличается от движения электрона.
Элементарные молекулярные формы

Молекулярный H2 существует как два спиновые изомеры, т.е. соединения с двумя ядерное вращение состояния.[24] в ортоводород формы спины двух ядер параллельны и образуют триплетное состояние с квантовым числом спина молекулы, равным 1 (1⁄2+1⁄2); в параводород спины антипараллельны и образуют синглет с квантовым числом спина молекулы 0 (1⁄2–1⁄2). При стандартной температуре и давлении газообразный водород содержит около 25% пара-формы и 75% орто-формы, также известной как «нормальная форма».[25] Равновесное отношение ортоводорода к параводороду зависит от температуры, но поскольку орто-форма является возбужденное состояние и имеет более высокую энергию, чем пара-форма, она нестабильна и не может быть очищена. При очень низких температурах состояние равновесия состоит почти исключительно из пара-формы. Тепловые свойства чистого параводорода в жидкой и газовой фазах значительно отличаются от свойств нормальной формы из-за различий во вращательной теплоемкости, что более подробно обсуждается в спиновые изомеры водорода.[26] Орто / пара-различие также встречается в других водородсодержащих молекулах или функциональных группах, таких как вода и метилен, но не имеет большого значения для их тепловых свойств.[27]
Ортоформа, которая медленно превращается в пара-форму при низких температурах.[28] Отношение орто / пара в конденсированном H2 является важным фактором при приготовлении и хранении жидкий водород: преобразование орто в пара экзотермический и выделяет достаточно тепла, чтобы испарить часть жидкого водорода, что приводит к потере сжиженного материала. Катализаторы для орто-пара взаимного преобразования, например оксид железа, Активированный уголь, платинированный асбест, редкоземельные металлы, соединения урана, оксид хрома, или немного никеля[29] соединения, используются при водородном охлаждении.[30]
Фазы
Соединения
Ковалентные и органические соединения
Хотя H2 не очень реакционноспособен в стандартных условиях, он действительно образует соединения с большинством элементов. Водород может образовывать соединения с элементами, которые более электроотрицательный, Такие как галогены (F, Cl, Br, I), или кислород; в этих соединениях водород принимает частичный положительный заряд.[31] При соединении с более электроотрицательным элементом, особенно фтор, кислород, или же азот, водород может участвовать в форме нековалентной связи средней силы с другим электроотрицательным элементом с неподеленной парой, явление, называемое водородная связь это критически важно для стабильности многих биологических молекул.[32][33] Водород также образует соединения с менее электроотрицательными элементами, такими как металлы и металлоиды, где он принимает частичный отрицательный заряд. Эти соединения часто называют гидриды.[34]
Водород образует широкий спектр соединений с углерод называется углеводороды, и даже более обширный массив с гетероатомы которые из-за их общей связи с живыми существами называются органические соединения.[35] Изучение их свойств известно как органическая химия[36] и их изучение в контексте проживания организмы известен как биохимия.[37] Согласно некоторым определениям, «органические» соединения должны содержать только углерод. Однако большинство из них также содержат водород, и поскольку именно углерод-водородная связь придает этому классу соединений большинство его конкретных химических характеристик, углерод-водородные связи требуются в некоторых определениях слова «органический» в химии.[35] Миллионы углеводороды известны, и они обычно образуются сложными путями, которые редко включают элементарный водород.
Водород хорошо растворяется во многих редкоземельный и переходные металлы[38] и растворим как в нанокристаллических, так и в аморфные металлы.[39] Водород растворимость в металлах под влиянием локальных искажений или примесей в кристаллическая решетка.[40] Эти свойства могут быть полезны, когда водород очищается путем пропускания через горячую палладий дисков, но высокая растворимость газа является металлургической проблемой, что способствует охрупчивание из многих металлов,[11] усложнение конструкции трубопроводов и резервуаров для хранения.[12]
Гидриды
Соединения водорода часто называют гидриды, термин, который используется довольно свободно. Термин «гидрид» предполагает, что атом H приобрел отрицательный или анионный характер, обозначается H−, и используется, когда водород образует соединение с более электроположительный элемент. Существование гидрид-анион, предложено Гилберт Н. Льюис в 1916 г. для солеподобных гидридов 1 и 2 групп был продемонстрирован Моерсом в 1920 г. электролизом расплавленных гидрид лития (LiH), производя стехиометрический количество водорода на аноде.[41] Для гидридов, отличных от металлов 1 и 2 групп, этот термин вводит в заблуждение, учитывая низкую электроотрицательность водорода. Исключением в группе 2 гидридов являются BeH
2, который является полимерным. В литийалюминийгидрид, то AlH−
4 анион несет гидридные центры, прочно прикрепленные к Al (III).
Хотя гидриды могут быть образованы почти со всеми элементами основной группы, количество и комбинация возможных соединений широко варьируется; например, известно более 100 бинарных гидридов борана, но только один бинарный гидрид алюминия.[42] Двоичный индий гидрид еще не идентифицирован, хотя существуют более крупные комплексы.[43]
В неорганическая химия, гидриды также могут служить мостиковые лиганды которые соединяют два металлических центра в координационный комплекс. Эта функция особенно часто встречается в группа 13 элементов, особенно в бораны (бор гидриды) и алюминий комплексов, а также в кластерных карбораны.[44]
Протоны и кислоты
Окисление водорода удаляет его электрон и дает ЧАС+, в котором нет электронов и ядро который обычно состоит из одного протона. Поэтому ЧАС+
часто называют протоном. Этот вид занимает центральное место в обсуждении кислоты. Под Кислотно-основная теория Бренстеда – Лоури, кислоты являются донорами протонов, а основания - акцепторами протонов.
Голый протон, ЧАС+
, не может существовать в растворе или в ионных кристаллах из-за его неудержимого притяжения к другим атомам или молекулам с электронами. За исключением высоких температур, связанных с плазмой, такие протоны невозможно удалить из электронные облака атомов и молекул, и останется прикрепленным к ним. Однако термин «протон» иногда используется свободно и метафорически для обозначения положительно заряженных или катионный водород присоединен к другим видам таким образом, и как таковой обозначается "ЧАС+
"без всякого указания на то, что отдельные протоны существуют свободно как вид.
Чтобы избежать воздействия голого «сольватированного протона» в растворе, иногда считается, что кислые водные растворы содержат менее маловероятные фиктивные частицы, называемые «гидроксоний ион "(ЧАС
3О+
). Однако даже в этом случае такие сольватированные катионы водорода более реалистично рассматриваются как организованные в кластеры, которые образуют частицы, близкие к H
9О+
4.[45] Другой ионы оксония обнаруживаются, когда вода находится в кислом растворе с другими растворителями.[46]
Хотя это и экзотично для Земли, одним из самых распространенных ионов во Вселенной является ЧАС+
3 ион, известный как протонированный молекулярный водород или трехводородный катион.[47]
Атомарный водород
НАСА исследовал использование атомарного водорода в качестве ракетное топливо. Его можно хранить в жидком гелии, чтобы предотвратить его рекомбинацию в молекулярный водород. Когда гелий испаряется, атомарный водород высвобождается и снова соединяется с молекулярным водородом. В результате получился бы очень горячий поток водорода и газообразного гелия. Таким способом можно уменьшить взлетную массу ракет на 50%.[48]
Наиболее межзвездный водород находится в форме атомарного водорода, потому что атомы редко сталкиваются и объединяются. Они являются источником важных 21 см. водородная линия в астрономия на 1420 МГц.[49]
Изотопы


Водород имеет три встречающихся в природе изотопа, обозначенных 1
ЧАС, 2
ЧАС и 3
ЧАС. Другие, крайне нестабильные ядра (4
ЧАС к 7
ЧАС) были синтезированы в лаборатории, но не наблюдались в природе.[50][51]
- 1
ЧАС является наиболее распространенным изотопом водорода с содержанием более 99,98%. Поскольку ядро этого изотопа состоит только из одного протона, ему дано описательное, но редко используемое формальное название протий.[52] - 2
ЧАС, другой стабильный изотоп водорода, известен как дейтерий и содержит один протон и один нейтрон в ядре. Считается, что весь дейтерий во Вселенной был произведен во время Большой взрыв, и с тех пор терпит. Дейтерий не радиоактивен и не представляет значительной опасности токсичности. Вода, обогащенная молекулами, которые содержат дейтерий вместо обычного водорода, называется тяжелая вода. Дейтерий и его соединения используются в качестве нерадиоактивной метки в химических экспериментах и в растворителях для 1
ЧАС-ЯМР-спектроскопия.[53] Тяжелая вода используется как замедлитель нейтронов и теплоноситель для ядерных реакторов. Дейтерий также является потенциальным топливом для коммерческих термоядерная реакция.[54] - 3
ЧАС известен как тритий и содержит в своем ядре один протон и два нейтрона. Он радиоактивен, распадается на гелий-3 через бета-распад с период полураспада 12,32 года.[44] Он настолько радиоактивен, что его можно использовать в светящаяся краска, что делает его полезным в таких вещах, как часы. Стекло предотвращает выход небольшого количества излучения.[55] Небольшие количества трития образуются естественным путем при взаимодействии космических лучей с атмосферными газами; тритий также был выделен во время испытания ядерного оружия.[56] Он используется в реакциях ядерного синтеза,[57] как трассировщик в изотопная геохимия,[58] и в специализированных автономное освещение устройств.[59] Тритий также использовался в экспериментах по химической и биологической маркировке в качестве радиоактивная метка.[60]
Уникальный среди элементов, его изотопам, широко используемым сегодня, присвоены различные имена. Во время ранних исследований радиоактивности различным тяжелым радиоактивным изотопам были даны собственные названия, но такие названия больше не используются, за исключением дейтерия и трития. Символы D и T (вместо 2
ЧАС и 3
ЧАС) иногда используются для дейтерия и трития, но соответствующий символ для протия, P, уже используется для фосфор и поэтому недоступен для протия.[61] В своем номенклатурный руководящие принципы, Международный союз теоретической и прикладной химии (IUPAC) допускает любой из D, T, 2
ЧАС, и 3
ЧАС будет использоваться, хотя 2
ЧАС и 3
ЧАС являются предпочтительными.[62]
В экзотический атом мюоний (символ Му), состоящий из антимюон и электрон, также иногда считается легким радиоизотопом водорода из-за разницы в массах антимюона и электрона.[63] Мюоний был открыт в 1960 году.[64] Во время мюона 2.2 мкс время жизни, мюоний может входить в состав таких соединений, как хлорид мюония (MuCl) или мюонид натрия (NaMu), аналогично хлористый водород и гидрид натрия соответственно.[65]
История
Открытие и использование
В 1671 г. Роберт Бойл открыл и описал реакцию между утюг опилки и разбавить кислоты, что приводит к образованию газообразного водорода.[66][67] В 1766 г. Генри Кавендиш был первым, кто распознал водородный газ как дискретное вещество, назвав газ из металл-кислотная реакция «легковоспламеняющийся воздух». Он предположил, что «воспламеняющийся воздух» на самом деле идентичен гипотетическому веществу под названием «флогистон "[68][69] и дальнейшее открытие в 1781 году, что газ производит воду при сгорании. Ему обычно приписывают открытие водорода как элемента.[4][5] В 1783 г. Антуан Лавуазье дал элементу название водород (от греч. ὑδρο- гидро означает "вода" и -γενής гены что означает "создатель")[70] когда он и Лаплас воспроизвел открытие Кавендиша о том, что при сжигании водорода образуется вода.[5]

Лавуазье произвел водород для своих экспериментов по сохранению массы, реагируя поток пара с металлическими утюг через раскаленную железную трубку, нагретую в огне. Анаэробное окисление железа протонами воды при высокой температуре схематично можно представить совокупностью следующих реакций:
- Fe + H2О → FeO + H2
- 2 Fe + 3 H2O → Fe2О3 + 3 часа2
- 3 Fe + 4 H2O → Fe3О4 + 4 часа2
Многие металлы, такие как цирконий проходят аналогичную реакцию с водой, приводящую к образованию водорода.
Водород был сжиженный впервые Джеймс Дьюар в 1898 г. с помощью регенеративное охлаждение и его изобретение, термос.[5] Он произвел твердый водород в следующем году.[5] Дейтерий был открыт в декабре 1931 г. Гарольд Юри, и тритий был подготовлен в 1934 г. Эрнест Резерфорд, Марк Олифант, и Пол Хартек.[4] Тяжелая вода, который состоит из дейтерия вместо обычного водорода, был открыт группой Юри в 1932 году.[5] Франсуа Исаак де Риваз построил первый двигатель де Риваз, двигатель внутреннего сгорания, работающий на смеси водорода и кислорода в 1806 году. Эдвард Дэниел Кларк изобрел водородный газовый паял в 1819 году. Лампа доберейнера и внимание были изобретены в 1823 году.[5]
Первый наполненный водородом воздушный шар был изобретен Жак Шарль в 1783 г.[5] Водород обеспечил подъемную силу для первой надежной формы полета по воздуху после изобретения в 1852 году первого дирижабля на водороде. Анри Жиффар.[5] Немецкий граф Фердинанд фон Цеппелин продвигал идею жестких дирижаблей, поднимаемых водородом, которые позже были названы Цеппелины; Первый из них совершил первый полет в 1900 году.[5] Регулярные рейсы по расписанию начались в 1910 году, а к началу Первой мировой войны в августе 1914 года они перевезли 35 000 пассажиров без серьезных инцидентов. Водородные дирижабли использовались в качестве смотровых площадок и бомбардировщиков во время войны.
Первый беспосадочный трансатлантический переход совершил британский дирижабль. R34 в 1919 году. Регулярные пассажирские перевозки возобновились в 1920-х годах, и открытие гелий Запасы в США обещали повышенную безопасность, но правительство США отказалось продавать газ для этой цели. Следовательно, H2 использовался в Гинденбург дирижабль, который был уничтожен пожаром в воздухе над Нью-Джерси 6 мая 1937 г.[5] Инцидент транслировали в прямом эфире по радио и снимали на видео. Широко предполагается, что причиной является воспламенение протекающего водорода, но более поздние исследования указали на воспламенение алюминизированный покрытие ткани статичное электричество. Но ущерб репутации водорода как подъемный газ уже было сделано и коммерческое путешествие на водородном дирижабле прекратился. Водород по-прежнему используется, а не негорючий, но более дорогой гелий, в качестве подъемного газа для метеорологические шары.
В том же году первый турбогенератор с водородным охлаждением поступил на вооружение с газообразным водородом в качестве охлаждающая жидкость в роторе и статоре в 1937 г. Дейтон, Огайо, компанией Dayton Power & Light Co .;[71] из-за теплопроводности и очень низкой вязкости газообразного водорода, следовательно, более низкого сопротивления, чем у воздуха, на сегодняшний день это наиболее распространенный тип в своей области для больших генераторов (обычно 60 МВт и больше; генераторы меньшего размера обычно с воздушным охлаждением ).
В никель-водородный аккумулятор впервые был использован в 1977 году на борту спутника навигационных технологий ВМС США-2 (NTS-2).[72] Например, МКС,[73] Марс Одиссея[74] и Mars Global Surveyor[75] оснащены никель-водородными батареями. В темной части своей орбиты Космический телескоп Хаббла также работает от никель-водородных батарей, которые были окончательно заменены в мае 2009 года,[76] более 19 лет после запуска и 13 лет после истечения срока их службы.[77]
Роль в квантовой теории

Благодаря простой атомной структуре, состоящей только из протона и электрона, атом водорода вместе со спектром света, производимого им или поглощаемого им, занимали центральное место в развитии теории атомный структура.[78] Кроме того, изучение соответствующей простоты молекулы водорода и соответствующего катиона ЧАС+
2 принес понимание природы химическая связь, который последовал вскоре после того, как в середине 1920-х годов была разработана квантово-механическая трактовка атома водорода.
Одним из первых квантовых эффектов, которые были явно замечены (но не поняты в то время), было наблюдение Максвелла с участием водорода за полвека до полной квантово-механическая теория прибывший. Максвелл заметил, что удельная теплоемкость из H2 необъяснимым образом отличается от двухатомный температура газа ниже комнатной и начинает все больше напоминать одноатомный газ при криогенных температурах. Согласно квантовой теории, такое поведение возникает из-за расстояния между (квантованными) вращательными энергетическими уровнями, которые особенно широко разнесены в H2 из-за малой массы. Эти широко расположенные уровни препятствуют равному разделению тепловой энергии на вращательное движение в водороде при низких температурах. Двухатомные газы, состоящие из более тяжелых атомов, не имеют столь широко разнесенных уровней и не проявляют такого же эффекта.[79]
Антиводород (
ЧАС
) это антивещество аналог водорода. Он состоит из антипротон с позитрон. Антиводород - единственный тип атома антивещества, произведенный по состоянию на 2015 год.[Обновить].[80][81]
Космическое преобладание и распространение
Водород, как атомарный H, является наиболее обильный химический элемент во Вселенной, составляя 75 процентов нормальное дело к масса и более 90 процентов по количеству атомов. (Однако большая часть массы Вселенной находится не в форме материи типа химического элемента, а скорее постулируется, что она существует как еще необнаруженные формы массы, такие как темная материя и темная энергия.[82]) Этот элемент в большом количестве содержится в звездах и газовый гигант планеты. Молекулярные облака из H2 связаны с звездообразование. Водород играет жизненно важную роль в обеспечении звезды сквозь протон-протонная реакция в случае звезд с массой Солнца от очень низкой до примерно 1 и Цикл CNO из термоядерная реакция в случае звезд более массивных, чем наша солнце.[83]
состояния
Во Вселенной водород в основном находится в атомный и плазма состояния со свойствами, совершенно отличными от свойств молекулярного водорода. В качестве плазмы электрон и протон водорода не связаны друг с другом, что приводит к очень высокой электропроводности и высокой излучательной способности (излучению Солнца и других звезд). На заряженные частицы сильно влияют магнитные и электрические поля. Например, в Солнечный ветер они взаимодействуют с земными магнитосфера давая начало Биркеланд течения и Аврора. Водород находится в нейтральном атомарном состоянии в межзвездная среда. Считается, что большое количество нейтрального водорода, обнаруженного в затухающих системах Лайман-альфа, доминирует над космологической барионной плотностью Вселенной вплоть до красное смещение z=4.[84]
В обычных условиях на Земле элементарный водород существует в виде двухатомного газа H2. Однако газообразный водород очень редко встречается в атмосфере Земли (1 промилле по объему) из-за его небольшого веса, что позволяет сбежать из земного притяжения легче, чем более тяжелые газы. Однако водород является третьим по распространенности элементом на поверхности Земли.[85] в основном в виде химические соединения Такие как углеводороды и вода.[44] Газообразный водород вырабатывается некоторыми бактериями и водоросли и является естественным компонентом газы, как есть метан, сам по себе источник водорода, значение которого возрастает.[86]
Молекулярная форма, называемая протонированный молекулярный водород (ЧАС+
3) находится в межзвездной среде, где он генерируется ионизацией молекулярного водорода из космические лучи. Этот ион также наблюдался в верхних слоях атмосферы планеты. Юпитер. Ион относительно стабилен в окружающей среде космического пространства из-за низкой температуры и плотности. ЧАС+
3 является одним из самых распространенных ионов во Вселенной, и он играет заметную роль в химии межзвездной среды.[87] Нейтральный трехатомный водород ЧАС3 может существовать только в возбужденном виде и нестабильно.[88] Напротив, положительные молекулярный ион водорода (ЧАС+
2) - редкая молекула во Вселенной.
Производство
ЧАС
2 производится в химических и биологических лабораториях, часто как побочный продукт других реакций; в промышленности для гидрирование из ненасыщенный субстраты; и в природе как средство изгнания сокращение эквиваленты в биохимических реакциях.
Электролиз воды

В электролиз воды это простой метод производства водорода. Через воду проходит ток низкого напряжения, и газообразный кислород образуется в анод а газообразный водород образуется на катод. Обычно катод изготавливают из платины или другого инертного металла при производстве водорода для хранения. Однако, если газ должен сжигаться на месте, желателен кислород для содействия горению, и поэтому оба электрода должны быть сделаны из инертных металлов. (Железо, например, окислится и, таким образом, уменьшит количество выделяемого кислорода.) Теоретический максимальный КПД (затраченное электричество по сравнению с энергетической ценностью производимого водорода) находится в диапазоне 88–94%.[89][90]
- 2 ЧАС
2О(l) → 2 ЧАС
2(г) + О
2(грамм)
При определении электрического КПД электролиза PEM (протонообменной мембраны) используется более высокая теплотворная способность (HHV).[91] Это потому, что слой катализатора взаимодействует с водой как пар. Поскольку для электролизеров PEM процесс протекает при 80 ° C, отходящее тепло может быть перенаправлено через систему для создания пара, что приведет к повышению общего электрического КПД. Для щелочных электролизеров необходимо использовать более низкую теплотворную способность (LHV), поскольку процесс в этих электролизерах требует воды в жидкой форме и использует щелочность для облегчения разрыва связи, удерживающей атомы водорода и кислорода вместе. Для топливных элементов также необходимо использовать более низкую теплотворную способность, поскольку пар является выходом, а не входом.
Паровой риформинг (промышленный метод)
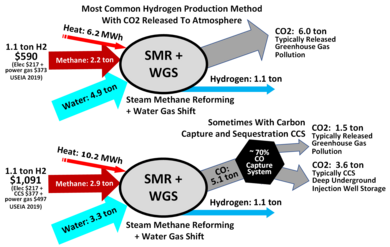
Водород часто производится с использованием природного газа, который включает удаление водорода из углеводородов при очень высоких температурах, при этом 48% производства водорода приходится на паровой риформинг.[92][93] Промышленный водород в больших объемах обычно производится паровой риформинг из натуральный газ.[94] Этот метод также известен как Процесс Bosch и широко используется для промышленного получения водорода.
При высоких температурах (1000–1400 K, 700–1100 ° C или 1300–2000 ° F) пар (водяной пар) реагирует с метан уступить монооксид углерода и ЧАС
2.
- CH
4 + ЧАС
2О → СО + 3 ЧАС
2
Эта реакция предпочтительна при низких давлениях, но, тем не менее, проводится при высоких давлениях (2,0 МПа, 20 атм или 600 бар).дюйм рт. ст. ). Это потому, что высокое давление ЧАС
2 самый продаваемый продукт, и адсорбция при переменном давлении Системы очистки (PSA) лучше работают при более высоких давлениях. Смесь продуктов известна как "синтез-газ "потому что он часто используется непосредственно для производства метанол и родственные соединения. Углеводороды кроме метана, можно использовать для производства синтез-газа с различным соотношением продуктов. Одной из многих сложностей этой оптимизированной технологии является образование кокса или углерода:
- CH
4 → С + 2 ЧАС
2
Следовательно, при паровом риформинге обычно используется избыток ЧАС
2О. Дополнительный водород может быть извлечен из пара с помощью моноксида углерода через реакция конверсии водяного газа, особенно с оксид железа катализатор. Эта реакция также является обычным промышленным источником углекислый газ:[94]
- CO + ЧАС
2О → CO
2 + ЧАС
2
Другие важные методы для CO и ЧАС
2 производство включает частичное окисление углеводородов:[95]
- 2 CH
4 + О
2 → 2 СО + 4 ЧАС
2
и угольная реакция, которая может служить прелюдией к указанной выше реакции сдвига:[94]
- C + ЧАС
2О → СО + ЧАС
2
Иногда водород производится и потребляется в одном промышленном процессе без разделения. в Процесс Габера для производство аммиака, водород образуется из природного газа.[96] Электролиз из рассол уступить хлор также производит водород в качестве побочного продукта.[97]
Пиролиз метана (промышленный метод)

Производство водорода с использованием природного газа метана пиролиз это недавний процесс «без парниковых газов».[98][99] Развитие массового производства с использованием этого метода является ключом к ускорению сокращения выбросов углерода за счет использования водорода в топливная ячейка электрические перевозки тяжелых грузовиков,[100][101][102][103] в газотурбинной выработке электроэнергии,[104][105] и в производственных процессах.[106] Использование пиролиза метана метан CH
4 пузырился через расплавленный металлический катализатор при высоких температурах (1340 K, 1065 ° C или 1950 ° F) для производства экологически чистого водорода ЧАС
2 газ в больших объемах по низкой цене и производит экологически чистое твердое вещество углерод C [107][108] без выбросов парниковых газов.[109][110]
- CH
4(ж) → С (т) + 2 ЧАС
2(г) ΔH ° = 74 кДж / моль
Углерод промышленного качества может быть продан как производственное сырье или навсегда захоронен. Пиролиз метана находится в стадии разработки и считается подходящим для промышленного производства водорода. Объем производства оценивается в BASF Опытная установка "пиролиз метана в масштабе".[111] Дальнейшие исследования продолжаются в нескольких лабораториях, в том числе в Лаборатории жидких металлов Карлсруэ (KALLA).[112] и лаборатория химической инженерии Калифорнийского университета - Санта-Барбара[113]
Металл-кислота
Многие металлы реагируют с водой с образованием ЧАС
2, но скорость выделения водорода зависит от металла, pH и присутствия легирующих добавок. Чаще всего выделение водорода вызывается кислотами. Щелочные и щелочноземельные металлы, алюминий, цинк, марганец и железо легко реагируют с водными кислотами. Эта реакция лежит в основе Аппарат Киппа, который когда-то использовался как лабораторный источник газа:
- Zn + 2 ЧАС+
→ Zn2+
+ ЧАС
2
В отсутствие кислоты эволюция ЧАС
2 медленнее. Имея технологическое значение, поскольку железо является широко используемым конструкционным материалом, является его анаэробная коррозия:
- Fe + 2 ЧАС
2O → Fe (ОН)
2 + ЧАС
2
Многие металлы, например алюминий, медленно реагируют с водой, поскольку образуют пассивированные оксидные покрытия. Сплав алюминия и галлий однако реагирует с водой.[114] При высоком pH алюминий может производить ЧАС
2:
- 2 Al + 6 ЧАС
2О + 2 ОЙ−
→ 2 Al (ОН)−
4 + 3 ЧАС
2
Некоторые металлосодержащие соединения вступают в реакцию с кислотами с образованием ЧАС
2. В анаэробных условиях гидроксид железа (Fe (ОН)
2) окисляется протонами воды с образованием магнетит и ЧАС
2. Этот процесс описывается Реакция Шикорра:
- 3 Fe (ОН)
2 → Fe
3О
4 + 2 ЧАС
2O + ЧАС
2
Этот процесс происходит при анаэробной коррозии утюг и стали в бескислородный грунтовые воды и в сокращении почвы ниже уровень грунтовых вод.
Термохимический
Можно использовать более 200 термохимических циклов для расщепление воды. Многие из этих циклов, такие как цикл оксида железа, оксид церия (IV) – оксид церия (III) цикл, цинк цинк-оксидный цикл, серно-йодный цикл, цикл медь-хлор и гибридный цикл серы были оценены их коммерческий потенциал для производства водорода и кислорода из воды и тепла без использования электричества.[115] Ряд лабораторий (в том числе во Франции, Германии, Греции, Японии и США) разрабатывают термохимические методы получения водорода из солнечной энергии и воды.[116]
Реакция серпентинизации
В глубоких геологических условиях, преобладающих вдали от атмосферы Земли, водород (ЧАС
2) производится в процессе серпентинизация. В этом процессе протоны воды (H+) восстанавливаются железом (Fe2+) ионов, обеспечиваемых фаялит (Fe
2SiO
4). Формы реакции магнетит (Fe
3О
4), кварц (SiО
2) и водород (ЧАС
2):[117][118]
- 3Fe
2SiO
4 + 2 ЧАС
2O → 2 Fe
3О
4 + 3 SiО
2 + 3 ЧАС
2 - фаялит + вода → магнетит + кварц + водород
Эта реакция очень похожа на Реакция Шикорра наблюдается при анаэробном окислении гидроксид железа при контакте с водой.
Приложения
Нефтехимическая промышленность
Большое количество ЧАС
2 используются для «повышения качества» ископаемого топлива. Основные потребители ЧАС
2 включают гидродеалкилирование, гидрообессеривание, и гидрокрекинг. Многие из этих реакций можно классифицировать как гидрогенолиз, т.е. разрыв связей с углеродом. Показательным является отделение серы от жидкого ископаемого топлива:
- R-S-R + 2 H2 → H2S + 2 RH
Гидрирование
Гидрирование, Добавление ЧАС
2 к различным субстратам проводится в больших масштабах. Гидрирование N2 с получением аммиака путем Процесс Габера-Боша потребляет несколько процентов бюджета энергии во всей отрасли. Полученный аммиак используется для обеспечения большей части белка, потребляемого людьми.[119] Гидрирование используется для преобразования ненасыщенные жиры и масла к насыщенным жирам и маслам. Основное применение - производство маргарин. Метанол производится гидрированием диоксида углерода. Он также является источником водорода при производстве соляная кислота. ЧАС
2 также используется как Восстановитель для преобразования некоторых руды к металлам.[120]
Охлаждающая жидкость
Водород обычно используется на электростанциях в качестве хладагента в генераторах из-за ряда благоприятных свойств, которые являются прямым результатом его легких двухатомных молекул. К ним относятся низкие плотность, низкий вязкость, и самый высокий удельная теплоемкость и теплопроводность всех газов.
Энергоноситель
Водород не является энергетическим ресурсом в качестве топлива для сжигания, потому что в природе нет источника водорода в полезных количествах.[121] Энергия Солнца исходит от термоядерная реакция водорода, но этот процесс трудно контролировать на Земле.[122] Для получения элементарного водорода из солнечных, биологических или электрических источников требуется больше энергии, чем при его сжигании, поэтому в этих случаях водород действует как носитель энергии, как батарея. Водород можно получить из ископаемых источников (таких как метан), но эти источники неустойчивы.[121]
В плотность энергии на единицу объем обоих жидкий водород и сжатый водород газ при любом практически достижимом давлении значительно меньше, чем у традиционных источников топлива, хотя плотность энергии на единицу топлива масса выше.[121] Тем не менее, элементарный водород широко обсуждается в контексте энергетики как возможное будущее. перевозчик энергии в экономическом масштабе.[123] Например, CO
2 секвестрация с последующим улавливание и хранение углерода может проводиться в момент ЧАС
2 производство из ископаемого топлива.[124] Водород, используемый в транспорте, будет гореть относительно чисто, а некоторые НЕТИкс выбросы,[125] но без выбросов углерода.[124] Однако затраты на инфраструктуру, связанные с полным переходом на водородную экономию, будут значительными.[126] Топливные элементы может преобразовывать водород и кислород непосредственно в электричество более эффективно, чем двигатели внутреннего сгорания.[127]
Полупроводниковая промышленность
Водород используется для насыщения разорванных («оборванных») связей аморфный кремний и аморфный углерод что помогает стабилизировать свойства материала.[128] Это тоже потенциал донор электронов в различных оксидных материалах, в том числе ZnO,[129][130] SnO2, CdO, MgO,[131] ZrO2, HfO2, Ла2О3, Y2О3, TiO2, SrTiO3, LaAlO3, SiO2, Al2О3, ZrSiO4, HfSiO4, и SrZrO3.[132]
Ниша и развивающиеся виды использования
Помимо использования в качестве реагента, ЧАС
2 имеет множество небольших приложений. Он используется как защитный газ в сварка такие методы как атомно-водородная сварка.[133][134] ЧАС2 используется в качестве охлаждающей жидкости ротора в электрические генераторы в энергостанции, потому что у него самый высокий теплопроводность любого газа. Жидкий H2 используется в криогенный исследования, в том числе сверхпроводимость исследования.[135] Потому что ЧАС
2 легче воздуха, имея чуть больше1⁄14 плотности воздуха, он когда-то широко использовался как подъемный газ в воздушных шарах и дирижабли.[136]
Чистый или смешанный с азотом (иногда называемый формовочный газ ) водород является индикаторный газ для обнаружения мельчайших утечек. Применения можно найти в автомобильной, химической, энергетической, аэрокосмической и телекоммуникационной отраслях.[137] Водород - это разрешенная пищевая добавка (E 949), которая, помимо других антиоксидантных свойств, позволяет проводить испытания пищевых продуктов на герметичность.[138]
Каждый из более редких изотопов водорода также имеет свое применение. Дейтерий (водород-2) используется в применения ядерного деления как Модератор замедлить нейтроны, И в термоядерная реакция реакции.[5] Соединения дейтерия находят применение в химии и биологии при изучении реакций. изотопные эффекты.[139] Тритий (водород-3), произведенный в ядерные реакторы, используется в производстве водородные бомбы,[140] как изотопная метка в бионауках,[60] и как радиация источник в светящихся красках.[141]
В тройная точка температура равновесного водорода является определяющей фиксированной точкой на ИТС-90 температурная шкала 13,8033Кельвин.[142]
Биологические реакции
ЧАС2 является продуктом некоторых видов анаэробный метаболизм и производится несколькими микроорганизмы, обычно через реакции катализированный к утюг - или же никель -содержащий ферменты называется гидрогеназы. Эти ферменты катализируют обратимое редокс реакция между H2 и его составляющая два протона и два электрона. Создание газообразного водорода происходит при переносе восстановительных эквивалентов, полученных во время пируват ферментация к воде.[143] Естественный цикл производства и потребления водорода организмами называется водородный цикл.[144] Частей на миллион (частей на миллион) H2 возникает при дыхании здорового человека. Это результат метаболической активности содержащих гидрогеназу микроорганизмов в толстом кишечнике.[145]
Расщепление воды, в котором вода разлагается на составляющие протоны, электроны и кислород, происходит в легкие реакции в целом фотосинтетический организмы. Некоторые такие организмы, в том числе водоросли Хламидомонада Reinhardtii и цианобактерии, сделали второй шаг в темные реакции в котором протоны и электроны восстанавливаются до H2 газа специализированными гидрогеназами в хлоропласт.[146] Были предприняты усилия по генетической модификации гидрогеназ цианобактерий для эффективного синтеза H2 газ даже в присутствии кислорода.[147] Также были предприняты усилия с генетически модифицированными водоросли в биореакторе.[148]
Безопасность и меры предосторожности
| Опасности | |
|---|---|
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Опасность |
| H220 | |
| P202, P210, P271, P403, P377, P381[149] | |
| NFPA 704 (огненный алмаз) | |
Водород представляет ряд опасностей для безопасности человека из-за потенциальных взрывы и загорается при смешивании с воздухом, чтобы быть удушающий в чистом виде, кислород -свободная форма.[150] Кроме того, жидкий водород - это криоген и представляет опасность (например, обморожение ) связаны с очень холодными жидкостями.[151] Водород растворяется во многих металлах и, помимо утечки, может оказывать на них неблагоприятное воздействие, например хрупкость водорода,[152] приводящие к трещинам и взрывам.[153] Утечка газообразного водорода в наружный воздух может спонтанно воспламениться. Более того, водородное пламя, будучи очень горячим, почти незаметно и, следовательно, может привести к случайным ожогам.[154]
Даже интерпретация данных по водороду (включая данные по безопасности) затруднена рядом явлений. Многие физические и химические свойства водорода зависят от параводород / ортоводород соотношение (часто требуется несколько дней или недель при данной температуре для достижения равновесного отношения, для которого обычно приводятся данные). Параметры водородной детонации, такие как критическое давление детонации и температура, сильно зависят от геометрии контейнера.[150]
Примечания
- ^ Однако большая часть массы Вселенной находится не в форме барионов или химических элементов. Видеть темная материя и темная энергия.
- ^ 286 кДж / моль: энергия на моль горючего материала (молекулярного водорода).
Смотрите также
Рекомендации
- ^ Виберг, Эгон; Виберг, Нильс; Холлеман, Арнольд Фредерик (2001). Неорганическая химия. Академическая пресса. п. 240. ISBN 978-0123526519.
- ^ Лиде, Д. Р., изд. (2005). «Магнитная восприимчивость элементов и неорганических соединений». CRC Справочник по химии и физике (PDF) (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 978-0-8493-0486-6.
- ^ Weast, Роберт (1984). CRC, Справочник по химии и физике. Бока-Ратон, Флорида: Издательство Chemical Rubber Company. стр. E110. ISBN 978-0-8493-0464-4.
- ^ а б c «Водород». Энциклопедия химии Ван Ностранда. Wylie-Interscience. 2005. С. 797–799. ISBN 978-0-471-61525-5.
- ^ а б c d е ж грамм час я j k л Эмсли, Джон (2001). Строительные блоки природы. Оксфорд: Издательство Оксфордского университета. С. 183–191. ISBN 978-0-19-850341-5.
- ^ Ствертка, Альберт (1996). Путеводитель по элементам. Издательство Оксфордского университета. С. 16–21. ISBN 978-0-19-508083-4.
- ^ Бойд, Пади (19 июля 2014 г.). "Каков химический состав звезд?". НАСА. В архиве из оригинала 15 января 2015 г.. Получено 5 февраля 2008.
- ^ Laursen, S .; Chang, J .; Medlin, W .; Gürmen, N .; Фоглер, Х.С. (27 июля 2004 г.). «Чрезвычайно краткое введение в вычислительную квантовую химию». Молекулярное моделирование в химической инженерии. Университет Мичигана. В архиве из оригинала 20 мая 2015 г.. Получено 4 мая 2015.
- ^ Ведущий: профессор Джим Аль-Халили (21 января 2010 г.). «Открытие элементов». Химия: изменчивая история. 25:40 мин. BBC. BBC Четыре. В архиве из оригинала 25 января 2010 г.. Получено 9 февраля 2010.
- ^ «Основы водорода - Производство». Флоридский центр солнечной энергии. 2007. Архивировано с оригинал 18 февраля 2008 г.. Получено 5 февраля 2008.
- ^ а б Роджерс, Х.С. (1999). «Водородная хрупкость металлов». Наука. 159 (3819): 1057–1064. Bibcode:1968Научный ... 159.1057R. Дои:10.1126 / science.159.3819.1057. PMID 17775040. S2CID 19429952.
- ^ а б Christensen, C.H .; Nørskov, J. K .; Йоханнесен, Т. (9 июля 2005 г.). «Сделать общество независимым от ископаемого топлива - датские исследователи открывают новые технологии». Технический университет Дании. В архиве из оригинала 21 мая 2015 г.. Получено 19 мая 2015.
- ^ «Дигидроген». O = каталог CHem. Университет Южного Мэна. Архивировано из оригинал 13 февраля 2009 г.. Получено 6 апреля 2009.
- ^ Комитет по альтернативам и стратегиям будущего производства и использования водорода, Национальный исследовательский совет США, Национальная инженерная академия США (2004). Водородная экономика: возможности, затраты, препятствия и потребности в исследованиях и разработках. Национальная академия прессы. п. 240. ISBN 978-0-309-09163-3.CS1 maint: несколько имен: список авторов (связь)
- ^ Carcassi, M.N .; Финески, Ф. (2005). "Дефлаграции H2–Воздуш и CH4–Бедные воздушные смеси в вентилируемой многокамерной среде ». Энергия. 30 (8): 1439–1451. Дои:10.1016 / j.energy.2004.02.012.
- ^ Патнаик, П. (2007). Всеобъемлющее руководство по опасным свойствам химических веществ. Wiley-Interscience. п. 402. ISBN 978-0-471-71458-3.
- ^ Schefer, E.W .; Kulatilaka, W. D .; Patterson, B.D .; Сеттерстен, Т. Б. (июнь 2009 г.). «Видимое излучение водородного пламени». Горение и пламя. 156 (6): 1234–1241. Дои:10.1016 / j.combustflame.2009.01.011.
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 0-8493-0487-3.
- ^ Клейтон, Д. Д. (2003). Справочник изотопов в космосе: от водорода до галлия. Издательство Кембриджского университета. ISBN 978-0-521-82381-4.
- ^ Лаборатории NAAP (2009). «Уровни энергии». Университет Небраски Линкольн. В архиве из оригинала 11 мая 2015 г.. Получено 20 мая 2015.
- ^ "длина волны фотона 13,6 эВ". вольфрам Альфа. 20 мая 2015. В архиве из оригинала 12 мая 2016 г.. Получено 20 мая 2015.
- ^ Стерн, Д. П. (16 мая 2005 г.). «Атомное ядро и ранняя модель атома Бора». Центр космических полетов имени Годдарда НАСА (зеркало). Архивировано из оригинал 17 октября 2008 г.. Получено 20 декабря 2007.
- ^ Стерн, Д. П. (13 февраля 2005 г.). «Волновая механика». Центр космических полетов имени Годдарда НАСА. В архиве из оригинала 13 мая 2008 г.. Получено 16 апреля 2008.
- ^ Персонал (2003). «Водород (H2) Свойства, использование, применение: газообразный водород и жидкий водород ». Universal Industrial Gases, Inc. В архиве из оригинала 19 февраля 2008 г.. Получено 5 февраля 2008.
- ^ Тихонов, В. И .; Волков, А.А. (2002). «Разделение воды на орто- и пара-изомеры». Наука. 296 (5577): 2363. Дои:10.1126 / science.1069513. PMID 12089435. S2CID 26190863.
- ^ Гриц, Дж. (Март 2006 г.). «СН. 6 - Водород» (PDF). Руководство по безопасности Гленна Исследовательского центра НАСА Гленна, документ GRC-MQSA.001. НАСА. В архиве (PDF) из оригинала 16 февраля 2008 г.. Получено 5 февраля 2008.
- ^ Шиницкий, М .; Элицур, А. С. (2006). «Орто-пара-спиновые изомеры протонов метиленовой группы». Хиральность. 18 (9): 754–756. Дои:10.1002 / chir.20319. PMID 16856167.
- ^ Миленко, Ю. Я .; Сибилева, Р. М .; Стржемечный, М.А. (1997). «Скорость естественной орто-пара-конверсии в жидком и газообразном водороде». Журнал физики низких температур. 107 (1–2): 77–92. Bibcode:1997JLTP..107 ... 77M. Дои:10.1007 / BF02396837. S2CID 120832814.
- ^ Амос, Уэйд А. (1 ноября 1998 г.). «Затраты на хранение и транспортировку водорода» (PDF). Национальная лаборатория возобновляемых источников энергии. С. 6–9. В архиве (PDF) из оригинала 26 декабря 2014 г.. Получено 19 мая 2015.
- ^ Svadlenak, R.E .; Скотт, А. Б. (1957). "Превращение орто- в параводород на катализаторах оксид железа-оксид цинка". Журнал Американского химического общества. 79 (20): 5385–5388. Дои:10.1021 / ja01577a013.
- ^ Кларк, Дж. (2002). «Кислотность галогенидов водорода». Chemguide. Архивировано из оригинал 20 февраля 2008 г.. Получено 9 марта 2008.
- ^ Кимбалл, Дж. У. (7 августа 2003 г.). «Водород». Страницы биологии Кимбалла. В архиве из оригинала 4 марта 2008 г.. Получено 4 марта 2008.
- ^ Сборник химической терминологии ИЮПАК, электронная версия, Водородная связь В архиве 19 марта 2008 г. Wayback Machine
- ^ Сандрок, Г. (2 мая 2002 г.). «Металл-водородные системы». Сандийские национальные лаборатории. Архивировано из оригинал 24 февраля 2008 г.. Получено 23 марта 2008.
- ^ а б «Состав и номенклатура углеводородов». Университет Пердью. Архивировано из оригинал 31 июля 2012 г.. Получено 23 марта 2008.
- ^ "Органическая химия". Dictionary.com. Издательская группа «Лексико». 2008 г. В архиве из оригинала 18 апреля 2008 г.. Получено 23 марта 2008.
- ^ «Биохимия». Dictionary.com. Издательская группа «Лексико». 2008 г. В архиве из оригинала 29 марта 2008 г.. Получено 23 марта 2008.
- ^ Takeshita, T .; Wallace, W. E .; Крейг, Р. С. (1974). «Растворимость водорода в соединениях 1: 5 между иттрием или торием и никелем или кобальтом». Неорганическая химия. 13 (9): 2282–2283. Дои:10.1021 / ic50139a050.
- ^ Kirchheim, R .; Mutschele, T .; Кенингер, В .; Gleiter, H .; Birringer, R .; Кобле, Т. (1988). «Водород в аморфных и нанокристаллических металлах». Материаловедение и инженерия. 99 (1–2): 457–462. Дои:10.1016/0025-5416(88)90377-1.
- ^ Кирххейм, Р. (1988). «Растворимость и коэффициент диффузии водорода в дефектных и аморфных металлах». Прогресс в материаловедении. 32 (4): 262–325. Дои:10.1016/0079-6425(88)90010-2.
- ^ Моерс, К. (1920). «Исследования солевого характера гидрида лития». Zeitschrift für Anorganische und Allgemeine Chemie. 113 (191): 179–228. Дои:10.1002 / zaac.19201130116. В архиве (PDF) с оригинала 24 августа 2019 г.. Получено 24 августа 2019.
- ^ Даунс, А. Дж .; Пулхэм, К. Р. (1994). «Гидриды алюминия, галлия, индия и таллия: переоценка». Обзоры химического общества. 23 (3): 175–184. Дои:10.1039 / CS9942300175.
- ^ Hibbs, D. E .; Jones, C .; Smithies, N.A. (1999). «Замечательно стабильный комплекс тригидрида индия: синтез и характеристика [InH3ПК6ЧАС11)3]". Химические коммуникации (2): 185–186. Дои:10.1039 / a809279f.
- ^ а б c Miessler, G.L .; Тарр, Д. А. (2003). Неорганическая химия (3-е изд.). Прентис Холл. ISBN 978-0-13-035471-6.
- ^ Окумура, А. М .; Да, L. I .; Myers, J.D .; Ли, Ю. Т. (1990). «Инфракрасные спектры сольватированного иона гидроксония: спектроскопия колебательной предиссоциации масс-селективного H3O + • (H2О) п•(ЧАС2)м". Журнал физической химии. 94 (9): 3416–3427. Дои:10.1021 / j100372a014.
- ^ Perdoncin, G .; Скоррано, Г. (1977). «Равновесия протонирования в воде при нескольких температурах спиртов, простых эфиров, ацетона, диметилсульфида и диметилсульфоксида». Журнал Американского химического общества. 99 (21): 6983–6986. Дои:10.1021 / ja00463a035.
- ^ Carrington, A .; Макнаб И. Р. (1989). "Инфракрасный спектр предиссоциации трехатомного катиона водорода (H3+)". Отчеты о химических исследованиях. 22 (6): 218–222. Дои:10.1021 / ar00162a004.
- ^ "NASA / TM — 2002-211915: эксперименты с твердым водородом для получения атомного топлива" (PDF). Архивировано из оригинал (PDF) 27 сентября 2011 г.. Получено 27 сентября 2011.
- ^ «Водород». mysite.du.edu. В архиве из оригинала 18 апреля 2009 г.. Получено 20 апреля 2008.
- ^ Гуров Ю.Б .; Алешкин, Д. В .; Behr, M. N .; Лапушкин, С.В .; Морохов, П. В .; Печкуров, В. А .; Порошин, Н.О .; Сандуковский, В.Г .; Телькушев, М. В .; Чернышев, Б. А .; Чуренкова, Т. Д. (2004). «Спектроскопия сверхтяжелых изотопов водорода при поглощении остановившихся пионов ядрами». Физика атомных ядер. 68 (3): 491–97. Bibcode:2005ПАН .... 68..491Г. Дои:10.1134/1.1891200. S2CID 122902571.
- ^ Коршенинников, А .; Никольский, Э .; Кузьмин, Е .; Ozawa, A .; Morimoto, K .; Tokanai, F .; Kanungo, R .; Tanihata, I .; и другие. (2003). "Экспериментальные доказательства существования 7H и для конкретной структуры 8Он". Письма с физическими проверками. 90 (8): 082501. Bibcode:2003ПхРвЛ..90х2501К. Дои:10.1103 / PhysRevLett.90.082501. PMID 12633420.
- ^ Urey, H.C .; Brickwedde, F. G .; Мерфи, Г. М. (1933). «Названия изотопов водорода». Наука. 78 (2035): 602–603. Bibcode:1933Sci .... 78..602U. Дои:10.1126 / science.78.2035.602. PMID 17797765.
- ^ Oda, Y .; Nakamura, H .; Yamazaki, T .; Nagayama, K .; Yoshida, M .; Каная, С .; Икехара, М. (1992). «Исследования ЯМР 1H дейтерированной рибонуклеазы HI, селективно меченной протонированными аминокислотами». Журнал биомолекулярного ЯМР. 2 (2): 137–47. Дои:10.1007 / BF01875525. PMID 1330130. S2CID 28027551.
- ^ Броуд, В. Дж. (11 ноября 1991 г.). «Прорыв в области ядерного синтеза дает надежду на мощь будущего». Нью-Йорк Таймс. Получено 12 февраля 2008.
- ^ Трауб, Р. Дж .; Дженсен, Дж. А. (июнь 1995 г.). «Тритиевые радиолюминесцентные устройства. Руководство по охране труда» (PDF). Международное агентство по атомной энергии. п. 2.4. В архиве (PDF) из оригинала 6 сентября 2015 г.. Получено 20 мая 2015.
- ^ Персонал (15 ноября 2007 г.). «Тритий». Агентство по охране окружающей среды США. В архиве из оригинала от 2 января 2008 г.. Получено 12 февраля 2008.
- ^ Нейв, К. Р. (2006). "Дейтерий-тритиевый синтез". Гиперфизика. Государственный университет Джорджии. В архиве из оригинала 16 марта 2008 г.. Получено 8 марта 2008.
- ^ Kendall, C .; Колдуэлл, Э. (1998). К. Кендалл; Дж. Дж. Макдоннелл (ред.). «Глава 2: Основы геохимии изотопов». Изотопные индикаторы в гидрологии водосбора. Геологическая служба США. Дои:10.1016 / B978-0-444-81546-0.50009-4. Архивировано из оригинал 14 марта 2008 г.. Получено 8 марта 2008.
- ^ «Тритиевая лаборатория». Университет Майами. 2008. Архивировано с оригинал 28 февраля 2008 г.. Получено 8 марта 2008.
- ^ а б Holte, A.E .; Houck, M. A .; Колли, Н. Л. (2004). «Возможная роль паразитизма в эволюции мутуализма у астигматидных клещей». Экспериментальная и прикладная акарология. 25 (2): 97–107. Дои:10.1023 / А: 1010655610575. PMID 11513367. S2CID 13159020.
- ^ ван дер Крогт, П. (5 мая 2005 г.). «Водород». Элементимология и элементы Multidict. Архивировано из оригинал 23 января 2010 г.. Получено 20 декабря 2010.
- ^ § IR-3.3.2, Предварительные рекомендации В архиве 9 февраля 2016 г. Wayback Machine, Номенклатура неорганической химии, Химическая номенклатура и структурное представительство, IUPAC. Проверено в строке 3 октября 2007 г.
- ^ ИЮПАК (1997). «Мюоний». В A.D. McNaught, A. Wilkinson (ed.). Сборник химической терминологии (2-е изд.). Научные публикации Blackwell. Дои:10.1351 / goldbook.M04069. ISBN 978-0-86542-684-9.
- ^ В.В. Хьюз; и другие. (1960). «Образование мюония и наблюдение его ларморовой прецессии». Письма с физическими проверками. 5 (2): 63–65. Bibcode:1960PhRvL ... 5 ... 63H. Дои:10.1103 / PhysRevLett.5.63.
- ^ W.H. Коппенол; ИЮПАК (2001). «Названия атомов мюония и водорода и их ионов» (PDF). Чистая и прикладная химия. 73 (2): 377–380. Дои:10.1351 / pac200173020377. S2CID 97138983. В архиве (PDF) из оригинала 14 мая 2011 г.. Получено 15 ноября 2016.
- ^ Бойл, Р. (1672). «Трактаты, написанные достопочтенным Робертом Бойлем, содержащие новые эксперименты, затрагивающие отношения между пламенем и воздухом ...» Лондон.
- ^ Винтер, М. (2007). «Водород: историческая справка». WebElements Ltd. Архивировано с оригинал 10 апреля 2008 г.. Получено 5 февраля 2008.
- ^ Масгрейв, А. (1976). «Почему кислород вытеснил флогистон? Исследовательские программы в период химической революции». В Howson, C. (ред.). Метод и оценка в физических науках. Критический фон современной науки, 1800–1905 гг. Издательство Кембриджского университета. Дои:10.1017 / CBO9780511760013. ISBN 9780521211109. Получено 22 октября 2011.
- ^ Кавендиш, Генри (12 мая 1766 г.). "Три статьи достопочтенного Генри Кавендиша, содержащие эксперименты с надуманным воздухом, Ф. Р. С." Философские труды. 56: 141–184. Bibcode:1766РСПТ ... 56..141С. Дои:10.1098 / рстл.1766.0019. JSTOR 105491.
- ^ Ствертка, Альберт (1996). Путеводитель по элементам. Издательство Оксфордского университета. стр.16–21. ISBN 978-0-19-508083-4.
- ^ Национальная ассоциация производителей электрооборудования (1946 г.). Хронологическая история развития электричества с 600 г. до н. Э.. Нью-Йорк, штат Нью-Йорк, Национальная ассоциация производителей электрооборудования. п. 102. В архиве из оригинала 4 марта 2016 г.. Получено 9 февраля 2016.
- ^ Stockel, J.F; j.d. Данлоп; Бец, Ф (1980). «Никель-водородная аккумуляторная батарея НТС-2 Характеристики 31». Журнал космических аппаратов и ракет. 17: 31–34. Bibcode:1980JSpRo..17 ... 31S. Дои:10.2514/3.57704.
- ^ Jannette, A. G .; Hojnicki, J. S .; McKissock, D. B .; Fincannon, J .; Kerslake, T. W .; Родригес, К. Д. (июль 2002 г.). Валидация модели электрических характеристик международной космической станции с помощью орбитальной телеметрии (PDF). IECEC '02. 2002 37-я Межобщественная конференция по инженерии преобразования энергии, 2002 г.. С. 45–50. Дои:10.1109 / IECEC.2002.1391972. ISBN 0-7803-7296-4. В архиве (PDF) из оригинала 14 мая 2010 г.. Получено 11 ноября 2011.
- ^ Андерсон, П. М .; Койн, Дж. У. (2002). Легкая высоконадежная система питания на одной батарее для межпланетных космических кораблей. Материалы аэрокосмической конференции. 5. С. 5–2433. Дои:10.1109 / AERO.2002.1035418. ISBN 978-0-7803-7231-3. S2CID 108678345.
- ^ "Mars Global Surveyor". Astronautix.com. Архивировано из оригинал 10 августа 2009 г.. Получено 6 апреля 2009.
- ^ Лори Тяхла, изд. (7 мая 2009 г.). "Хаббл обслуживающий миссию 4: главное". НАСА. В архиве из оригинала 13 марта 2015 г.. Получено 19 мая 2015.
- ^ Хендрикс, Сьюзен (25 ноября 2008 г.). Лори Тяхла (ред.). «Продление срока службы Хаббла за счет новых батарей». НАСА. В архиве из оригинала 5 марта 2016 г.. Получено 19 мая 2015.
- ^ Крепо, Р. (1 января 2006 г.). Нильс Бор: модель атома. Великие научные умы. ISBN 978-1-4298-0723-4.
- ^ Берман, Р .; Cooke, A.H .; Хилл, Р. У. (1956). «Криогеника». Ежегодный обзор физической химии. 7: 1–20. Bibcode:1956ARPC .... 7 .... 1B. Дои:10.1146 / annurev.pc.07.100156.000245.
- ^ Чарльтон, Майк; Ван дер Верф, Дирк Питер (1 марта 2015 г.). «Успехи физики антиводорода». Научный прогресс. 98 (1): 34–62. Дои:10.3184 / 003685015X14234978376369. PMID 25942774. S2CID 23581065.
- ^ Келлербауэр, Албан (29 января 2015 г.). "Почему имеет значение антивещество". Европейский обзор. 23 (1): 45–56. Дои:10.1017 / S1062798714000532. S2CID 58906869.
- ^ Ганьон, С. «Водород». Jefferson Lab. Архивировано из оригинал 10 апреля 2008 г.. Получено 5 февраля 2008.
- ^ Haubold, H .; Матхай, А. М. (15 ноября 2007 г.). «Производство солнечной термоядерной энергии». Колумбийский университет. Архивировано из оригинал 11 декабря 2011 г.. Получено 12 февраля 2008.
- ^ Сторри-Ломбарди, Л. Дж .; Вулф, А. М. (2000). «Обзоры для z> 3 амортизированных систем поглощения Лайман-альфа: эволюция нейтрального газа». Астрофизический журнал. 543 (2): 552–576. arXiv:Astro-ph / 0006044. Bibcode:2000ApJ ... 543..552S. Дои:10.1086/317138.
- ^ Dresselhaus, M .; и другие. (15 мая 2003 г.). «Необходимые фундаментальные исследования для водородной экономики» (PDF). Тезисы мартовского собрания APS. Аргоннская национальная лаборатория, Департамент энергетики США, Научная лаборатория. 2004: m1.001. Bibcode:2004APS..MAR.m1001D. Архивировано из оригинал (PDF) 13 февраля 2008 г.. Получено 5 февраля 2008.
- ^ Бергер, В. Х. (15 ноября 2007 г.). «Будущее метана». Калифорнийский университет в Сан-Диего. Архивировано из оригинал 24 апреля 2008 г.. Получено 12 февраля 2008.
- ^ McCall Group; Ока Групп (22 апреля 2005 г.). «Ресурсный центр H3 +». Университеты Иллинойса и Чикаго. Архивировано из оригинал 11 октября 2007 г.. Получено 5 февраля 2008.
- ^ Helm, H .; и другие. (2003), «Связь связанных состояний с состояниями сплошной среды в нейтральном трехатомном водороде», Диссоциативная рекомбинация молекулярных ионов с электронами., Департамент молекулярной и оптической физики, Фрайбургский университет, Германия, стр. 275–288, Дои:10.1007/978-1-4615-0083-4_27, ISBN 978-1-4613-4915-0
- ^ Томассен, Магнус. «Снижение затрат и повышение производительности электролизеров из ПЭМ» (PDF). fch.europa.eu. FCH JU. В архиве (PDF) из оригинала 17 апреля 2018 г.. Получено 22 апреля 2018.
- ^ Kruse, B .; Grinna, S .; Буч, К. (2002). «Состояние водорода и мулигетер» (PDF). Беллона. Архивировано из оригинал (PDF) 16 февраля 2008 г.. Получено 12 февраля 2008.
- ^ Крузе, Бьёрнар. «Водородный статус и мультигетер» (PDF). bellona.org/. Беллона Норвегия. В архиве (PDF) из оригинала 22 апреля 2018 г.. Получено 22 апреля 2018.
- ^ Фрейермут, Джордж Х. Патент 1934 года: «Производство водорода из метановых углеводородов под действием пара при повышенной температуре."". Патентные полнотекстовые базы данных. Ведомство США по патентам и товарным знакам. Получено 30 октября 2020.
- ^ Press, Roman J .; Santhanam, K. S. V .; Мири, Масуд Дж .; Бейли, Алла В .; Такач, Джеральд А. (2008). Введение в водородную технологию. Джон Вили и сыновья. п. 249. ISBN 978-0-471-77985-8.
- ^ а б c Окстоби, Д. В. (2002). Принципы современной химии (5-е изд.). Томсон Брукс / Коул. ISBN 978-0-03-035373-4.
- ^ «Свойства водорода, использование, применение». Universal Industrial Gases, Inc. 2007. В архиве из оригинала 27 марта 2008 г.. Получено 11 марта 2008.
- ^ Фундербург, Э. (2008). «Почему цены на азот такие высокие?». Благородный фонд Сэмюэля Робертса. Архивировано из оригинал 9 мая 2001 г.. Получено 11 марта 2008.
- ^ Лис, А. (2007). «Химия из соли». BBC. Архивировано из оригинал 26 октября 2007 г.. Получено 11 марта 2008.
- ^ Фон Вальд, Грегори А. «Оптимизационный технико-экономический анализ пиролиза метана в расплавленных средах для снижения выбросов CO2 в промышленном секторе». Устойчивая энергетика и топливо. Королевское химическое общество. Получено 31 октября 2020.
- ^ Шнайдер, Стефан. «Современное состояние производства водорода пиролизом природного газа». ChemBioEng Обзоры. Интернет-библиотека Wiley. Получено 30 октября 2020.
- ^ Фиалка, Джон. «Министерство энергетики стремится увеличить количество водородного топлива для больших грузовиков». Новости E&E. Scientific American. Получено 7 ноября 2020.
- ^ CCJ News. «Как грузовики на топливных элементах производят электроэнергию и как они заправляются». Новости CCJ. Журнал коммерческого перевозчика. Получено 19 октября 2020.
- ^ Toyota. «Грузовик с водородными топливными элементами класса 8». Грузовик с водородным двигателем будет работать в тяжелых условиях и с чистыми выбросами. Toyota. Получено 19 октября 2020.
- ^ Колиас, Майк. «Автопроизводители переносят акцент на водород на большие буровые установки». Wall Street Journal. Получено 26 октября 2020.
- ^ GE Turbines. «Энергетические турбины, работающие на водороде». Газовые турбины, работающие на водороде. General Electric. Получено 19 октября 2020.
- ^ Солнечные турбины. «Энергетические турбины, работающие на водороде». Энергия из водородного газа для сокращения выбросов углерода. Солнечные турбины. Получено 19 октября 2020.
- ^ Кролиус, Стивен Х. «Метан в аммиак посредством пиролиза». Аммиачная энергетическая ассоциация. Аммиачная энергетическая ассоциация. Получено 19 октября 2020.
- ^ Упхэм, Д. Честер. «Каталитические расплавленные металлы для прямого превращения метана в водород и отделяемый углерод». ScienceMag.org. Американская ассоциация развития науки. Получено 31 октября 2020.
- ^ Кларк, Палмер. «Сухой риформинг метана, катализируемый расплавленными металлическими сплавами». nature.com. природный катализ. Получено 31 октября 2020.
- ^ Картрайт, Джон. «Реакция, которая навсегда даст нам чистое ископаемое топливо». Новый ученый. Получено 30 октября 2020.
- ^ Карлсруэский технологический институт. «Водород из метана без выбросов СО2». Phys.Org. Phys.Org. Получено 30 октября 2020.
- ^ BASF. «Исследователи BASF работают над принципиально новыми процессами производства с низким содержанием углерода - пиролизом метана». Устойчивое развитие США. BASF. Получено 19 октября 2020.
- ^ Гусев Александр. «KITT / IASS - Производство водорода без CO2 из природного газа для использования в энергии». Европейские энергетические инновации. Институт перспективных исследований в области устойчивого развития. Получено 30 октября 2020.
- ^ Фернандес, Соня. «Исследователи разрабатывают потенциально недорогую технологию с низким уровнем выбросов, которая может преобразовывать метан без образования CO2». Phys-Org. Американский институт физики. Получено 19 октября 2020.
- ^ Пармузина, А.В .; Кравченко, О. (2008). «Активация металлического алюминия для выделения водорода из воды». Международный журнал водородной энергетики. 33 (12): 3073–3076. Дои:10.1016 / j.ijhydene.2008.02.025.
- ^ Веймер, Эл (25 мая 2005 г.). «Развитие термохимического производства водорода из воды на солнечных батареях» (PDF). Проект солнечной термохимической генерации водорода. В архиве (PDF) из оригинала 17 апреля 2007 г.. Получено 21 декабря 2008.
- ^ Перре, Р. «Развитие термохимического производства водорода из воды на солнечных батареях, Водородная программа Министерства энергетики, 2007» (PDF). Архивировано из оригинал (PDF) 27 мая 2010 г.. Получено 17 мая 2008.
- ^ Рассел, М. Дж .; Холл, А. Дж .; Мартин, В. (2010). «Серпентинизация как источник энергии у истоков жизни». Геобиология. 8 (5): 355–371. Дои:10.1111 / j.1472-4669.2010.00249.x. PMID 20572872.
- ^ Schrenk, M. O .; Brazelton, W. J .; Ланг, С.К. (2013). «Серпентинизация, углерод и глубокая жизнь». Обзоры по минералогии и геохимии. 75 (1): 575–606. Bibcode:2013РвМГ ... 75..575С. Дои:10.2138 / RMG.2013.75.18.
- ^ Смил, Вацлав (2004). Обогащая Землю: Фриц Габер, Карл Бош и трансформация мирового производства продуктов питания (1-е изд.). Кембридж, Массачусетс: MIT. ISBN 9780262693134.
- ^ Chemistry Operations (15 декабря 2003 г.). «Водород». Лос-Аламосская национальная лаборатория. Архивировано из оригинал 4 марта 2011 г.. Получено 5 февраля 2008.
- ^ а б c Маккарти, Дж. (31 декабря 1995 г.). «Водород». Стэндфордский Университет. Архивировано из оригинал 14 марта 2008 г.. Получено 14 марта 2008.
- ^ «Глава 13: Ядерная энергия - деление и синтез». Энергетическая история. Энергетическая комиссия Калифорнии. 2006. Архивировано с оригинал 2 марта 2008 г.. Получено 14 марта 2008.
- ^ «Министерство энергетики ищет кандидатов на рассмотрение вопроса о последствиях перехода к водородной экономике для занятости». Водородная программа (Пресс-релиз). Министерство энергетики США. 22 марта 2006 г. Архивировано с оригинал 19 июля 2011 г.. Получено 16 марта 2008.
- ^ а б «Стратегия улавливания углерода может привести к созданию автомобилей без выбросов» (Пресс-релиз). Технологический институт Джорджии. 11 февраля 2008 г. В архиве из оригинала 28 сентября 2013 г.. Получено 16 марта 2008.
- ^ Хеффель, Дж. У. (2002). «Данные о выбросах NOx и характеристиках двигателя внутреннего сгорания, работающего на водороде, при 1500 об / мин с использованием рециркуляции выхлопных газов». Международный журнал водородной энергетики. 28 (8): 901–908. Дои:10.1016 / S0360-3199 (02) 00157-X.
- ^ Ромм, Дж. Дж. (2004). Шумиха вокруг водорода: факты и вымысел в борьбе за сохранение климата (1-е изд.). Island Press. ISBN 978-1-55963-703-9.
- ^ Гарбак, Джон (2011). «Обзор подпрограммы проверки технологий VIII.0» (PDF). Программа Министерства энергетики США по технологиям топливных элементов, Годовой отчет о проделанной работе за 2010 г.. Архивировано из оригинал (PDF) 24 сентября 2015 г.. Получено 20 мая 2015.
- ^ Ле Комбер, П. Г .; Джонс, Д. И .; Копье, У. Э. (1977). «Эффект Холла и примесная проводимость в аморфном кремнии, легированном замещением». Философский журнал. 35 (5): 1173–1187. Bibcode:1977PMag ... 35.1173C. Дои:10.1080/14786437708232943.
- ^ Ван де Валле, К. Г. (2000). «Водород как причина допинга в оксиде цинка» (PDF). Письма с физическими проверками. 85 (5): 1012–1015. Bibcode:2000ПхРвЛ..85.1012В. Дои:10.1103 / PhysRevLett.85.1012. HDL:11858 / 00-001M-0000-0026-D0E6-E. PMID 10991462. В архиве (PDF) с оригинала 15 августа 2017 г.. Получено 1 августа 2018.
- ^ Janotti, A .; Ван Де Валле, К. Г. (2007). «Водородные многоцентровые связи». Материалы Природы. 6 (1): 44–47. Bibcode:2007 НатМа ... 6 ... 44J. Дои:10.1038 / nmat1795. PMID 17143265.
- ^ Килич, К .; Зунгер, Алекс (2002). «легирование оксидов водородом n-типа». Письма по прикладной физике. 81 (1): 73–75. Bibcode:2002АпФЛ..81 ... 73К. Дои:10.1063/1.1482783. S2CID 96415065.
- ^ Peacock, P.W .; Робертсон, Дж. (2003). «Поведение водорода в оксидных изоляторах затворов с высокой диэлектрической проницаемостью». Письма по прикладной физике. 83 (10): 2025–2027. Bibcode:2003АпФЛ..83.2025П. Дои:10.1063/1.1609245.
- ^ Дургутлу, А. (2003). «Экспериментальное исследование влияния водорода в аргоне в качестве защитного газа на сварку TIG аустенитной нержавеющей стали». Материалы и дизайн. 25 (1): 19–23. Дои:10.1016 / j.matdes.2003.07.004.
- ^ «Сварка атомарным водородом». Специальные сварные швы. 2007. Архивировано с оригинал 16 июля 2011 г.
- ^ Харди, В. Н. (2003). «От H2 к криогенным H-мазерам и к сверхпроводникам HiTc: маловероятный, но полезный путь». Physica C: сверхпроводимость. 388–389: 1–6. Bibcode:2003PhyC..388 .... 1H. Дои:10.1016 / S0921-4534 (02) 02591-1.
- ^ Альмквист, Эббе (2003). История промышленных газов. Нью-Йорк, Нью-Йорк: Kluwer Academic / Plenum Publishers. С. 47–56. ISBN 978-0306472770. Получено 20 мая 2015.
- ^ Блок, М. (3 сентября 2004 г.). Водород как индикаторный газ для обнаружения утечек. 16-й WCNDT 2004 г.. Монреаль, Канада: Сенсисторные технологии. Архивировано из оригинал 8 января 2009 г.. Получено 25 марта 2008.
- ^ «Отчет Комиссии по потреблению диетических пищевых добавок» (PDF). Евросоюз. В архиве (PDF) из оригинала 16 февраля 2008 г.. Получено 5 февраля 2008.
- ^ Reinsch, J .; Кац, А .; Wean, J .; Aprahamian, G .; МакФарланд, Дж. Т. (1980). «Влияние изотопа дейтерия на реакцию жирной ацил-КоА дегидрогеназы и бутирил-КоА». J. Biol. Chem. 255 (19): 9093–97. PMID 7410413.
- ^ Бержерон, К. Д. (2004). «Смерть отсутствия двойного назначения». Бюллетень ученых-атомщиков. 60 (1): 15–17. Bibcode:2004BuAtS..60a..15B. Дои:10.2968/060001004. В архиве из оригинала 19 апреля 2008 г.. Получено 13 апреля 2008.
- ^ Куигг, К. Т. (март 1984 г.). «Предупреждение о тритии». Бюллетень ученых-атомщиков. 40 (3): 56–57. Дои:10.1080/00963402.1984.11459199.
- ^ Международная температурная шкала 1990 г. (PDF). Procès-Verbaux du Comité International des Poids et Mesures. 1989. С. T23 – T42. В архиве (PDF) из оригинала 13 апреля 2008 г.. Получено 25 марта 2008.
- ^ Cammack, R .; Робсон, Р. Л. (2001). Водород как топливо: уроки природы. Тейлор и Фрэнсис Лтд., Стр. 202–203. ISBN 978-0-415-24242-4.
- ^ Rhee, T. S .; Brenninkmeijer, C.A.M .; Рёкманн, Т. (19 мая 2006 г.). «Подавляющая роль почв в глобальном круговороте водорода в атмосфере» (PDF). Атмосферная химия и физика. 6 (6): 1611–1625. Дои:10.5194 / acp-6-1611-2006. В архиве (PDF) с оригинала 24 августа 2019 г.. Получено 24 августа 2019.
- ^ Эйзенманн, Александр; Аманн, Антон; Сказал, Майкл; Датта, Беттина; Ледоховски, Максимилиан (2008). «Выполнение и интерпретация водородных дыхательных тестов». Журнал исследования дыхания. 2 (4): 046002. Bibcode:2008JBR ..... 2d6002E. Дои:10.1088/1752-7155/2/4/046002. PMID 21386189.
- ^ Kruse, O .; Rupprecht, J .; Бадер, К .; Thomas-Hall, S .; Schenk, P.M .; Finazzi, G .; Ханкамер, Б. (2005). "Улучшенный фотобиологический H2 производство в искусственно созданных клетках зеленых водорослей » (PDF). Журнал биологической химии. 280 (40): 34170–7. Дои:10.1074 / jbc.M503840200. PMID 16100118. S2CID 5373909.
- ^ Smith, Hamilton O .; Сюй, Цин (2005). «IV.E.6 Водород из воды в новой рекомбинантной кислородно-толерантной системе цианобактерий» (PDF). Отчет о проделанной работе за 2005 финансовый год. Министерство энергетики США. В архиве (PDF) из оригинала 29 декабря 2016 г.. Получено 6 августа 2016.
- ^ Уильямс, К. (24 февраля 2006 г.). «Жизнь в пруду: будущее энергетики». Наука. Реестр. В архиве из оригинала 9 мая 2011 г.. Получено 24 марта 2008.
- ^ «MyChem: Химическая промышленность» (PDF). Архивировано из оригинал (PDF) 1 октября 2018 г.. Получено 1 октября 2018.
- ^ а б Brown, W. J .; и другие. (1997). «Стандарт безопасности для водорода и водородных систем» (PDF). НАСА. В архиве (PDF) с оригинала на 1 мая 2017 г.. Получено 12 июля 2017.
- ^ «Жидкий водород MSDS» (PDF). Praxair, Inc., сентябрь 2004 г. Архивировано с оригинал (PDF) 27 мая 2008 г.. Получено 16 апреля 2008.
- ^ "'Жуки и водородная хрупкость ». Новости науки. 128 (3): 41, 20 июля 1985 г. Дои:10.2307/3970088. JSTOR 3970088.
- ^ Хейс, Б. "Башня абсорбера аминов масла Union". TWI. Архивировано из оригинал 20 ноября 2008 г.. Получено 29 января 2010.
- ^ Уокер, Джеймс Л .; Уолтрип, Джон С .; Занкер, Адам (1988). «Отношения между спросом и предложением молочной кислоты и магния». У Джона Дж. МакКетты; Уильям Аарон Каннингем (ред.). Энциклопедия химической обработки и дизайна. 28. Нью-Йорк: Деккер. п. 186. ISBN 978-0824724788. Получено 20 мая 2015.
дальнейшее чтение
| Библиотечные ресурсы о Водород |
- Карта нуклидов (17-е изд.). Атомная энергетическая лаборатория Кноллса. 2010 г. ISBN 978-0-9843653-0-2.
- Ferreira-Aparicio, P .; Benito, M. J .; Санс, Дж. Л. (2005). «Новые тенденции в технологиях реформирования: от водородных промышленных установок до многотопливных микрореформаторов». Обзоры катализа. 47 (4): 491–588. Дои:10.1080/01614940500364958. S2CID 95966974.
- Ньютон, Дэвид Э. (1994). Химические элементы. Нью-Йорк: Франклин Уоттс. ISBN 978-0-531-12501-4.
- Ригден, Джон С. (2002). Водород: важнейший элемент. Кембридж, Массачусетс: Издательство Гарвардского университета. ISBN 978-0-531-12501-4.
- Ромм, Джозеф Дж. (2004). Шумиха вокруг водорода, фактов и вымысла в гонке за сохранение климата. Island Press. ISBN 978-1-55963-703-9.
- Шерри, Эрик (2007). Периодическая система, ее история и значение. Нью-Йорк: Издательство Оксфордского университета. ISBN 978-0-19-530573-9.
- Водородная безопасность охватывает безопасное производство, обращение и использование