Углеводород - Hydrocarbon
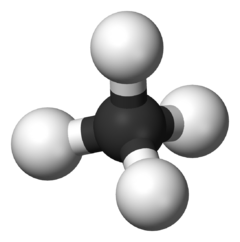
В органическая химия, а углеводород является органическое соединение состоящий полностью из водород и углерод.[1]:620 Углеводороды являются примерами группа 14 гидридов. Углеводороды, из которых один водород атом был удален функциональные группы называется гидрокарбилы.[2] Углеводороды обычно бесцветны и гидрофобны, со слабым запахом. Из-за их разнообразной молекулярной структуры трудно делать дальнейшие обобщения. Большинство антропогенных выбросов углеводородов происходит от сжигания ископаемых видов топлива, включая производство и сжигание топлива. Природные источники углеводородов, таких как этилен, изопрен и монотерпены, происходят из выбросов растительности.[3]
Типы
Как определено Номенклатура органической химии ИЮПАК, классификации углеводородов:
- Насыщенный углеводороды являются простейшими из углеводородных разновидностей. Они полностью состоят из одинарные облигации и насыщены водородом. Формула для ациклический насыщенные углеводороды (т.е. алканы ) является CпЧАС2п+2.[1]:623 Самая общая форма предельных углеводородов - CпЧАС2п+2(1-р), куда р количество колец. Те, у кого ровно одно кольцо, являются циклоалканы. Насыщенные углеводороды являются основой нефтяное топливо и встречаются как линейные, так и разветвленные. Реакция замещения является их характеристическим свойством (например, реакция хлорирования формировать хлороформ ). Углеводороды с таким же молекулярная формула но разные структурные формулы называются структурные изомеры.[1]:625 Как указано в примере 3-метилгексан и его выше гомологи, разветвленные углеводороды могут быть хиральный.[1]:627 Хиральные насыщенные углеводороды составляют боковые цепи биомолекулы Такие как хлорофилл и токоферол.[4]
- Ненасыщенные углеводороды имеют одну или несколько двойных или тройных связей между атомами углерода. Те, у кого есть двойная связь, называются алкены. Те, у кого есть один двойная связь имеют формулу CпЧАС2п (в предположении нециклических структур).[1]:628 Те, которые содержат тройные облигации называются алкин. Те, у кого одна тройная связь, имеют формулу CпЧАС2п−2.[1]:631
- Ароматические углеводороды, также известный как арены, представляют собой углеводороды, которые имеют хотя бы один ароматическое кольцо. 10% от общего объема выбросов неметанового органического углерода составляют ароматические углеводороды из выхлопных газов автомобилей с бензиновым двигателем.[5]
Углеводороды могут быть газы (например. метан и пропан ), жидкости (например. гексан и бензол ), воск или низкоплавкий твердые вещества (например. парафиновая свеча и нафталин ) или же полимеры (например. полиэтилен, полипропилен и полистирол ).
Термин «алифатический» относится к неароматическим углеводородам. Насыщенные алифатические углеводороды иногда называют «парафинами». Алифатические углеводороды, содержащие двойную связь между атомами углерода, иногда называют «олефинами».
Простые углеводороды и их разновидности
| Количество атомы углерода | Алкан (одинарная облигация) | Алкен (двойная связь) | Алкин (тройная связь) | Циклоалкан | Алькадиен |
|---|---|---|---|---|---|
| 1 | Метан | — | — | — | — |
| 2 | Этан | Этен (этилен) | Ethyne (ацетилен) | — | — |
| 3 | Пропан | Пропен (пропилен) | Пропин (метилацетилен) | Циклопропан | Пропадиене (аллен) |
| 4 | Бутан | Бутен (бутилен) | Бутыне | Циклобутан | Бутадиен |
| 5 | Пентан | Пентен | Pentyne | Циклопентан | Пентадиен (пиперилен) |
| 6 | Гексан | Гексен | Hexyne | Циклогексан | Гексадиен |
| 7 | Гептан | Гептен | Heptyne | Циклогептан | Гептадиен |
| 8 | Октан | Октен | Octyne | Циклооктан | Октадиен |
| 9 | Нонан | Нонен | Nonyne | Циклононан | Нонадиен |
| 10 | Decane | Decene | Децин | Циклодекан | Декадиен |
| 11 | Ундекан | Ундекбаллен | Ундецин | Циклоундекан | Ундекадиен |
| 12 | Додекан | Додецен | Додецин | Циклододекан | Додекадиен |
использование


Преимущественно углеводороды используются в качестве горючих веществ. топливо источник. Метан - преобладающий компонент природного газа. C6 через C10 алканы, алкены и изомерные циклоалканы являются главными компонентами бензин, нафта, реактивное топливо и специализированные промышленные смеси растворителей. С постепенным добавлением углеродных единиц простые углеводороды без кольца имеют более высокую вязкости, смазочные показатели, температуры кипения, затвердевание температуры и более глубокий цвет. На противоположной стороне от метана лежит тяжелый смолы которые остаются наименьшая фракция в сырой нефти очистка возразить. Их собирают и широко используют в качестве кровельных смесей, дорожных покрытий (битум ), консерванты для древесины ( креозот серии) и как жидкости с очень высокой вязкостью, устойчивые к сдвигу.
Некоторые крупномасштабные нетопливные применения углеводородов начинаются с этана и пропана, которые получают из нефти и природного газа. Эти два газа превращаются либо в синтез-газ.[6] или чтобы этилен и пропилен.[7][8] Эти два алкена являются предшественниками полимеров, в том числе полиэтилен, полистирол, акрилаты,[9][10][11] полипропилен и др. Еще один класс специальных углеводородов - BTX, смесь бензол, толуол, а три изомеры ксилола.[12] Мировое потребление бензола оценивается более чем в 40 000 000 тонн (2009 г.).[13]
Углеводороды также широко распространены в природе. Некоторые общественные членистоногие, такие как бразильская пчела без жала, Schwarziana quadripunctata используйте уникальные углеводородные «запахи», чтобы отличить родственников от других. Химический углеводородный состав варьируется в зависимости от возраста, пола, местоположения гнезда и иерархического положения.[14]
Также существует потенциал для сбора углеводородов с таких растений, как Молочай lathyri и Молочай тирукалли как альтернативный и возобновляемый источник энергии для автомобилей, использующих дизельное топливо.[15] Более того, эндофитный Бактерии из растений, которые естественным образом производят углеводороды, использовались для разложения углеводородов в попытках снизить концентрацию углеводородов в загрязненных почвах.[16]
Реакции
Примечательной особенностью углеводородов является их инертность, особенно для насыщенных членов. В противном случае можно выделить три основных типа реакций:
Свободнорадикальные реакции
Реакции замещения происходят только в насыщенных углеводородах (одинарные углерод-углеродные связи). Для таких реакций требуются высокореакционные реагенты, такие как хлор и фтор. В случае хлорирования один из атомов хлора замещает атом водорода. Реакции протекают через свободнорадикальные пути.
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
вплоть до CCl4 (четыреххлористый углерод )
- C2ЧАС6 + Cl2 → С2ЧАС5Cl + HCl
- C2ЧАС4Cl2 + Cl2 → С2ЧАС3Cl3 + HCl
полностью до C2Cl6 (гексахлорэтан )
Замена
Из классов углеводородов ароматические соединения однозначно (или почти так) подвергаются реакциям замещения. Примером может служить химический процесс, применяемый в самых крупных масштабах: реакция бензола и этилена с образованием этилбензол.
Реакции сложения
Реакции присоединения относятся к алкенам и алкинам. В этой реакции различные реагенты добавляют "поперек" пи-связи (ей). Хлор, хлористый водород, воды, и водород являются иллюстративными реагентами. Алкенес и некоторые алкины также подвергаются полимеризация, метатезис алкенов, и метатезис алкинов.
Окисление
Углеводороды в настоящее время являются основным источником мирового электроэнергия и источники тепла (например, домашнее отопление) из-за энергии, производимой при их сжигании.[17] Часто эта энергия используется непосредственно в качестве тепла, например, в домашних обогревателях, которые используют либо нефть или же натуральный газ. Углеводород сжигается, а тепло используется для нагрева воды, которая затем циркулирует. Аналогичный принцип используется для создания электроэнергия в электростанции.
Общие свойства углеводородов заключаются в том, что они производят пар, углекислый газ и тепло во время горение и это кислород требуется для сгорания. Самый простой углеводород, метан, горит следующим образом:
- CH4 + 2 O2 → 2 H2O + CO2 + энергия
При недостаточной подаче воздуха, монооксид углерода газ и водяной пар формируются:
- 2 канала4 + 3 O2 → 2 СО + 4 Н2О
Другой пример - возгорание пропан:
- C3ЧАС8 + 5 O2 → 4 H2O + 3 CO2 + энергия
И наконец, для любого линейный алкан из n атомов углерода,
- CпЧАС2п+2 + 3п + 1/2 О2 → (п + 1) H2O + п CO2 + энергия.
Частичное окисление характеризует реакции алкенов и кислорода. Этот процесс лежит в основе прогоркание и сушка краски.
Источник
Подавляющее большинство углеводородов, обнаруженных на земной шар происходить в нефть, каменный уголь, и природный газ. Нефть (буквально «каменная нефть» - сокращенно бензин) и уголь обычно считаются продуктами разложения органических веществ. В отличие от нефти, это уголь, который богаче углеродом и беднее водородом. Природный газ - это продукт метаногенез.[18][19]
Нефть состоит из безграничного разнообразия соединений, отсюда и необходимость нефтеперерабатывающих заводов. Эти углеводороды состоят из насыщенных углеводородов, ароматических углеводородов или их комбинации. В нефти отсутствуют алкены и алкины. Их производство требует нефтеперерабатывающих заводов. Углеводороды нефтяного происхождения в основном используются в качестве топлива, но они также являются источником практически всех синтетических органических соединений, включая пластмассы и фармацевтические препараты. Природный газ потребляется почти исключительно в качестве топлива. Уголь используется в качестве топлива и восстановителя в металлургия.
Абиологические углеводороды
Считается, что небольшая часть углеводородов, обнаруженных на Земле, абиологический.[20]
Некоторые углеводороды также широко распространены и широко представлены в Солнечная система. Озера жидкого метана и этана обнаружены на Титан, Сатурн самая большая луна, подтвержденная Миссия Кассини-Гюйгенса.[21] Углеводороды также широко распространены в туманностях, образующих полициклический ароматический углеводород (ПАУ) соединения.[22]
Биоремедиация
Биовосстановление углеводородов из загрязненной почвы или воды представляет собой серьезную проблему из-за химической инертности, которая характерна для углеводородов (следовательно, они выжили в материнской породе миллионы лет). Тем не менее, было разработано множество стратегий, в том числе биоремедиация. Основная проблема биоремедиации - нехватка действующих на них ферментов. Тем не менее, этот район регулярно привлекает внимание.[23]Бактерии в габбровый слой коры океана могут разлагать углеводороды; но экстремальные условия затрудняют исследования.[24] Другие бактерии, такие как Lutibacterium anuloederans может также разлагать углеводороды.[25]Mycoremediation или разрушение углеводорода мицелий и грибы возможно.[26][27]
Безопасность
Углеводороды, как правило, обладают низкой токсичностью, поэтому широко используется бензин и связанные с ним летучие продукты. Ароматические соединения, такие как бензол являются наркотическими и хроническими токсинами и являются канцерогенный. Некоторые редкие полициклические ароматические соединения обладают канцерогенными свойствами. легковоспламеняющийся.
Воздействие на окружающую среду
Сжигание углеводородов в качестве топлива, которое производит углекислый газ и воды, является основным источником антропогенного глобальное потепление. Углеводороды попадают в окружающую среду в результате их широкого использования в качестве топлива и химикатов, а также в результате утечек или случайных разливов во время разведки, добычи, переработки или транспортировки ископаемого топлива. Антропогенное загрязнение почвы углеводородами является серьезной глобальной проблемой из-за стойкости загрязнителей и их негативного воздействия на здоровье человека.[28]
Когда почва загрязнена углеводородами, это может оказать значительное влияние на ее микробиологические, химические и физические свойства. Это может служить для предотвращения, замедления или даже ускорения роста растительности в зависимости от конкретных происходящих изменений. Сырая нефть и природный газ - два основных источника загрязнения почвы углеводородами.[29]
Смотрите также
Рекомендации
- ^ а б c d е ж Зильберберг, Мартин (2004). Химия: молекулярная природа материи и изменений. Нью-Йорк: компании McGraw-Hill. ISBN 0-07-310169-9.
- ^ Золотая книга ИЮПАК гидрокарбильные группы В архиве 7 января 2010 г. Wayback Machine
- ^ Девульф, Джо. «Углеводороды в атмосфере» (PDF). Получено 26 октября 2020.
- ^ Мейерхенрих, Уве. Аминокислоты и асимметрия жизни В архиве 2 марта 2017 г. Wayback Machine. Спрингер, 2008. ISBN 978-3-540-76885-2
- ^ Барнс, И. «ТРОПОСФЕРНАЯ ХИМИЯ И СОСТАВ (Ароматические углеводороды)». Получено 26 октября 2020.
- ^ Лю, Шэнлинь; Сюн, Госин; Ян, Вэйшэн; Сюй, Лунья (1 июля 2000 г.). «Частичное окисление этана в синтез-газ на металлических катализаторах на носителе». Кинетика реакций и буквы катализа. 70 (2): 311–317. Дои:10.1023 / А: 1010397001697. ISSN 1588-2837. S2CID 91569579.
- ^ Ге, Мэн; Чен, Синъе; Ли, Яньонг; Ван, Цзямен; Сюй, Яньхун; Чжан, Лихонг (1 июня 2020 г.). «Катализатор на основе кобальта на основе перовскита для каталитического дегидрирования пропана». Кинетика, механизмы и катализ реакции.. 130 (1): 241–256. Дои:10.1007 / s11144-020-01779-8. ISSN 1878-5204. S2CID 218496057.
- ^ Ли, Цянь; Ян, Гонгбин; Ван, Канг; Ван, Ситао (2020). «Приготовление гранул оксида алюминия, легированного углеродом, и их применение в качестве носителей для Pt – Sn – K катализаторов дегидрирования пропана». Кинетика, механизмы и катализ реакции.. 129 (2): 805–817. Дои:10.1007 / s11144-020-01753-4. S2CID 212406355.
- ^ Науманн д'Алнонкур, Рауль; Чепеи, Ленард-Иштван; Хэвекер, Майкл; Girgsdies, Франк; Schuster, Manfred E .; Шлёгль, Роберт; Траншке, Аннетт (2014). «Реакционная сеть при окислении пропана на фазово-чистых оксидных катализаторах MoVTeNb M1». Дж. Катал. 311: 369–385. Дои:10.1016 / j.jcat.2013.12.008. HDL:11858 / 00-001M-0000-0014-F434-5.
- ^ Хэвекер, Майкл; Врабец, Сабина; Крёнерт, Ютта; Чепеи, Ленард-Иштван; Науманн д'Алнонкур, Рауль; Коленько, Юрий В .; Girgsdies, Франк; Шлёгль, Роберт; Траншке, Аннетт (2012). «Химия поверхности фазово-чистого оксида M1 MoVTeNb при работе с селективным окислением пропана до акриловой кислоты». Дж. Катал. 285: 48–60. Дои:10.1016 / j.jcat.2011.09.012. HDL:11858 / 00-001M-0000-0012-1BEB-F.
- ^ Кинетические исследования окисления пропана на смешанных оксидных катализаторах на основе Mo и V (PDF). ТУ Берлин. 2011 г.
- ^ Ли, Гуйсянь; Ву, Чао; Джи, Донг; Донг, Пэн; Чжан, Юнфу; Ян, Юн (1 апреля 2020 г.). «Кислотность и каталитические свойства двух форм-селективных катализаторов HZSM-5 для алкилирования толуола метанолом». Кинетика, механизмы и катализ реакции.. 129 (2): 963–974. Дои:10.1007 / s11144-020-01732-9. ISSN 1878-5204. S2CID 213601465.
- ^ Будущее бензола и пара-ксилола после беспрецедентного роста в 2010 году В архиве 2011-10-05 на Wayback Machine. Из отчета ChemSystems за 2011 год.
- ^ Nunes, T.M .; Turatti, I.C.C .; Mateus, S .; Nascimento, F.S .; Lopes, N.P .; Zucchi, R. (2009). «Кутикулярные углеводороды у безжальной пчелы Schwarziana quadripunctata (Hymenoptera, Apidae, Meliponini): различия между колониями, кастами и возрастом» (PDF). Генетика и молекулярные исследования. 8 (2): 589–595. Дои:10.4238 / vol8-2kerr012. PMID 19551647. В архиве (PDF) из оригинала 26 сентября 2015 г.
- ^ Кальвин, Мелвин. «Углеводороды растений: аналитические методы и наблюдения». Получено 26 октября 2020.
- ^ Павлик, Малгожата. «Потенциал разложения углеводородов и стимулирующая рост растений активность культивируемых эндофитных бактерий Lotus corniculatus и Oenothera biennis с длительно загрязненного участка». Получено 26 октября 2020.
- ^ Мировой уголь, уголь и электроэнергия В архиве 22 октября 2015 г. Wayback Machine. Всемирная угольная ассоциация
- ^ Clayden, J., Greeves, N., et al. (2001) Органическая химия Оксфорд ISBN 0-19-850346-6 п. 21 год
- ^ Макмерри, Дж. (2000). Органическая химия 5-е изд. Брукс / Коул: обучение Томсона. ISBN 0-495-11837-0 стр. 75–81
- ^ Sephton, M. A .; Хазен, Р. М. (2013). «О происхождении глубинных углеводородов». Обзоры по минералогии и геохимии. 75 (1): 449–465. Bibcode:2013РвМГ ... 75..449С. Дои:10.2138 / RMG.2013.75.14.
- ^ Космический корабль НАСА Кассини раскрывает подсказки о Луне Сатурна В архиве 2 сентября 2014 г. Wayback Machine. НАСА (12 декабря 2013 г.)
- ^ Guzman-Ramirez, L .; Lagadec, E .; Jones, D .; Zijlstra, A. A .; Гесицки, К. (2014). «Образование ПАУ в богатых кислородом планетарных туманностях». Ежемесячные уведомления Королевского астрономического общества. 441 (1): 364–377. arXiv:1403.1856. Bibcode:2014МНРАС.441..364Г. Дои:10.1093 / mnras / stu454. S2CID 118540862.
- ^ Лим, Ми Вэй; Lau, Ee Von; Пох, Пайк Еонг (2016). «Комплексное руководство по технологиям реабилитации нефтезагрязненных почв - настоящие работы и будущие направления». Бюллетень загрязнения морской среды. 109 (1): 14–45. Дои:10.1016 / j.marpolbul.2016.04.023. PMID 27267117.
- ^ Мейсон О.Ю., Накагава Т., Рознер М., Ван Ностранд Д.Д., Чжоу Дж., Маруяма А., Фиск М.Р., Джованнони С.Дж. (2010). «Первое исследование микробиологии самого глубокого слоя океанской коры». PLOS ONE. 5 (11): e15399. Bibcode:2010PLoSO ... 515399M. Дои:10.1371 / journal.pone.0015399. ЧВК 2974637. PMID 21079766.
- ^ Якимов, М. М .; Тиммис, К. Н .; Голышин П. Н. (2007). «Облигатные морские бактерии, разлагающие нефть». Curr. Мнение. Биотехнология. 18 (3): 257–266. CiteSeerX 10.1.1.475.3300. Дои:10.1016 / j.copbio.2007.04.006. PMID 17493798.
- ^ Стамец, Пол (2008). «6 способов, которыми грибы могут спасти мир» (видео). TED Talk. В архиве из оригинала 31 октября 2014 г.
- ^ Стамец, Пол (2005). "Mycoremediation". Бегущий мицелий: как грибы могут помочь спасти мир. Десятискоростной пресс. п.86. ISBN 9781580085793.
- ^ «Микробное разложение алканов (доступна загрузка PDF-файла)». ResearchGate. В архиве из оригинала 24 февраля 2017 г.. Получено 23 февраля 2017.
- ^ «Присадки, влияющие на микробную деградацию углеводородов нефти», Биоремедиация загрязненных почв, CRC Press, стр. 353–360, 9 июня 2000 г., Дои:10.1201/9781482270235-27, ISBN 978-0-429-07804-0

