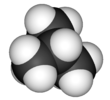
Изобутан - Isobutane
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 2-метилпропан[1] | |||
| Другие имена Изобутан | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 1730720 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.780 | ||
| Номер ЕС |
| ||
| Номер E | E943b (глазурь, ...) | ||
| 1301 | |||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1969 | ||
| |||
| |||
| Характеристики | |||
| C4ЧАС10 | |||
| Молярная масса | 58.124 г · моль−1 | ||
| Внешность | Бесцветный газ | ||
| Запах | Без запаха | ||
| Плотность |
| ||
| Температура плавления | -159,42 ° С (-254,96 ° F, 113,73 К)[4] | ||
| Точка кипения | -11,7 ° С (10,9 ° F, 261,4 К)[4] | ||
| 48.9 мг⋅л−1 (при 25 ° C (77 ° F))[2] | |||
| Давление газа | 3,1 атм (310 кПа) (при 21 ° C (294 K; 70 ° F))[3] | ||
Закон Генри постоянный (kЧАС) | 8.6 нмоль⋅Па−1⋅кг−1 | ||
| Конъюгированная кислота | Изобутан | ||
| −51.7·10−6 см3/ моль | |||
| Термохимия | |||
Теплоемкость (C) | 96.65 J⋅K−1⋅mol−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −134.8 – −133.6 кДж⋅моль−1 | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | −2.86959 – −2.86841 MJ⋅mol−1 | ||
| Опасности | |||
| Паспорт безопасности | Увидеть: страница данных praxair.com | ||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Опасность | ||
| H220 | |||
| P210 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -83 ° С (-117 ° F, 190 К) | ||
| 460 ° С (860 ° F, 733 К) | |||
| Пределы взрываемости | 1.4–8.3% | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | Никто[5] | ||
REL (Рекомендуемые) | TWA 800 частей на миллион (1900 мг / м3)[5] | ||
IDLH (Непосредственная опасность) | N.D.[5] | ||
| Родственные соединения | |||
Связанный алкан | Изопентан | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Изобутан, также известен как я-бутан, 2-метилпропан или метилпропан, это химическое соединение с молекулярная формула HC (CH3)3. Это изомер из бутан. Изобутан - это газ без цвета и запаха. алкан с третичный углерод. Изобутан используется в качестве молекулы-предшественника в нефтехимическая промышленность, например при синтезе изооктан.[6]
Производство
Изобутан получают изомеризация бутана.
Использует
Изобутан является основным сырьем в установки алкилирования нефтеперерабатывающих заводов. При использовании изобутана образуются бензиновые «смеси» с высокой степенью разветвления для хороших характеристик сгорания. Типичные продукты из изобутана: 2,4-диметилпентан и особенно 2,2,4-триметилпентан.[7]

Растворитель
В процессе суспензии Chevron Phillips для изготовления полиэтилен высокой плотности, изобутан используется в качестве разбавителя. При удалении суспендированного полиэтилена изобутан «испаряется», конденсируется и для этой цели возвращается обратно в петлевой реактор.[8]
Предшественник терт-Бутилгидропероксид
Изобутан окисляется до терт-Бутилгидропероксид, который впоследствии реагирует с пропилен уступить оксид пропилена. В трет-бутанол получаемый в качестве побочного продукта, обычно используется для изготовления присадок к бензину, таких как метил-трет-бутиловый эфир (МТБЭ).
Разное использование
Изобутан также используется в качестве пропеллента для аэрозольные баллончики.
Изобутан используется в составе топливных смесей, особенно в топливных канистрах, используемых для кемпинг.[9]
Хладагент
Изобутан используется как хладагент.[10] Их использование в холодильниках началось в 1993 году, когда Гринпис представила проект Greenfreeze с немецкой компанией Foron.[11] В этом отношении смеси чистого сухого «изобутана» (R-600a) (то есть смеси изобутана) имеют незначительное озоноразрушающая способность и очень низкий потенциал глобального потепления (имеющий значение ПГП углекислого газа в 3,3 раза) и может служить функциональной заменой R-12, R-22 (оба они широко известны под торговой маркой Фреон ), R-134a, и другие хлорфторуглерод или гидрофторуглерод хладагенты в обычных стационарных системах охлаждения и кондиционирования воздуха.
В качестве хладагента изобутан представляет опасность взрыва в дополнение к опасностям, связанным с негорючими хладагентами CFC. Замена этого хладагента в автомобильных системах кондиционирования воздуха, изначально не предназначенных для работы с изобутаном, широко запрещена или не рекомендуется.[12][13][14][15][16][17][18]
Продавцы и сторонники углеводородных хладагентов выступают против таких запретов на том основании, что таких инцидентов было очень мало по сравнению с количеством автомобильных систем кондиционирования воздуха, заполненных углеводородами.[19][20]
Номенклатура
Традиционное название изобутан сохранилось и в 1993 г. ИЮПАК рекомендации,[21] но больше не рекомендуется в соответствии с рекомендациями 2013 года.[1] Поскольку самая длинная непрерывная цепь в изобутане содержит только три атома углерода, предпочтительное название ИЮПАК 2-метилпропан, но местный житель (2-) обычно опускается в общей номенклатуре как избыточный; C2 - единственное положение в цепи пропана, где может находиться метильный заместитель, не изменяя основную цепь и не образуя конституциональный изомер. п-бутан.
использованная литература
- ^ а б Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 652. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
Названия «изобутан», «изопентан» и «неопентан» больше не рекомендуются.
- ^ "Растворимость в воде". PubChem. Национальный центр биотехнологической информации. Получено 6 апреля 2017.
- ^ «CDC - Карманный справочник NIOSH по химической опасности - изобутан». CDC - Карманный справочник NIOSH по химической опасности. CDC. Получено 28 декабря 2018.
- ^ а б Запись в базе данных веществ GESTIS Институт охраны труда и здоровья
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0350". Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Патентные часы, 31 июля 2006 г.». Архивировано из оригинал 11 марта 2007 г.. Получено 8 августа, 2006.
- ^ Бипин В. Вора; Джозеф А. Кокал; Пол Т. Баргер; Роберт Дж. Шмидт; Джеймс А. Джонсон (2003). «Алкилирование». Энциклопедия химической технологии Кирк-Отмера. Дои:10.1002 / 0471238961.0112112508011313.a01.pub2. ISBN 0471238961.
- ^ Кеннет С. Уайтли. «Полиэтилен». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a21_487.pub2.
- ^ Ритвельд, Уилл (2005-02-08). «Часто задаваемые вопросы о легких канистровых печах и топливе». Походный свет. Получено 2014-07-26.
- ^ «Европейская комиссия по модернизации хладагентов для стационарных применений» (PDF). Архивировано из оригинал (PDF) на 2009-08-05. Получено 2010-10-29.
- ^ Страница - 15 марта 2010 г. (2010-03-15). «ГринФриз». Гринпис. Получено 2013-01-02.
- ^ «Часто задаваемые вопросы об углеводородных хладагентах Агентства по охране окружающей среды США». Epa.gov. Получено 2010-10-29.
- ^ «Сборник заявлений о политике в отношении углеводородов и хладагентов, октябрь 2006 г.» (PDF). Архивировано из оригинал (PDF) на 2014-08-08. Получено 2014-08-01.
- ^ «Бюллетень MACS: использование углеводородного хладагента в транспортных средствах» (PDF). Архивировано из оригинал (PDF) на 2011-01-05. Получено 2010-10-29.
- ^ "Бюллетень Общества автомобильных инженеров по углеводородным хладагентам". Sae.org. 2005-04-27. Архивировано из оригинал на 2005-05-05. Получено 2010-10-29.
- ^ "Бюллетень труда Саскачевана по углеводородным хладагентам в транспортных средствах". Labour.gov.sk.ca. 2010-06-29. Архивировано из оригинал на 2009-07-01. Получено 2010-10-29.
- ^ VASA о законности и целесообразности хладагентов В архиве 13 января 2009 г. Wayback Machine
- ^ «Предупреждение правительства штата Квинсленд (Австралия) в отношении углеводородных хладагентов» (PDF). Energy.qld.gov.au. Архивировано из оригинал (PDF) на 2008-12-17. Получено 2010-10-29.
- ^ "Протокол парламента Нового Южного Уэльса (Австралия), 16 октября 1997 г.". Parliament.nsw.gov.au. 1997-10-16. Архивировано из оригинал 1 июля 2009 г.. Получено 2010-10-29.
- ^ "Протокол парламента Нового Южного Уэльса (Австралия), 29 июня 2000 г.". Parliament.nsw.gov.au. Архивировано из оригинал 22 мая 2005 г.. Получено 2010-10-29.
- ^ Панико, Р. и Пауэлл, У. Х., ред. (1994). Руководство по номенклатуре органических соединений ИЮПАК 1993 г.. Оксфорд: Blackwell Science. ISBN 0-632-03488-2. http://www.acdlabs.com/iupac/nomenclature/93/r93_679.htm