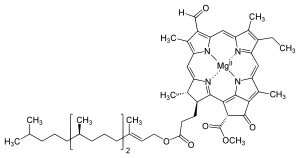
Хлорофилл - Chlorophyll


Хлорофилл (также хлорофил) является одним из нескольких связанных зеленых пигменты найдено в мезосомы из цианобактерии и в хлоропласты из водоросли и растения.[1] Его название происходит от Греческий слова χλωρός, хлорос («бледно-зеленый») и φύλλον, филлон ("лист").[2] Хлорофилл необходим в фотосинтез, позволяя растениям поглощать энергия от света.
Наиболее сильно хлорофиллы поглощают свет в синяя часть из электромагнитный спектр а также красная часть.[3] И наоборот, он плохо поглощает зеленые и почти зеленые части спектра, которые он отражает, создавая зеленый цвет хлорофилл-содержащих тканей. В фотосистемах зеленых растений существуют два типа хлорофилла: хлорофилл а и б.[4]
История
Хлорофилл был впервые выделен и назван Джозеф Бьенэме Кавенту и Пьер Жозеф Пеллетье в 1817 г.[5]Наличие магний в хлорофилле был открыт в 1906 г.,[6] и был первым обнаружением этого элемента в живой ткани.[7]
После первоначальной работы, проделанной немецким химиком Ричард Вильштеттер с 1905 по 1915 год, общая структура хлорофилла а был разъяснен Ганс Фишер в 1940 г. К 1960 г., когда большая часть стереохимия хлорофилла а был известен, Роберт Бернс Вудворд опубликовал полный синтез молекулы.[7][8] В 1967 году последнее оставшееся стереохимическое выяснение было завершено Ян Флеминг,[9] а в 1990 году Вудворд с соавторами опубликовали обновленный синтез.[10] Хлорофилл f было объявлено о присутствии в цианобактерии и другие кислородные микроорганизмы, образующие строматолиты в 2010;[11][12] молекулярная формула C55ЧАС70О6N4Mg и структура (2-формил ) -хлорофилл а были выведены на основе ЯМР, оптических и масс-спектров.[13]
Фотосинтез

Хлорофилл жизненно важен для фотосинтез, что позволяет растениям поглощать энергию из свет.[14]
Молекулы хлорофилла расположены внутри и вокруг фотосистемы которые встроены в тилакоид мембраны хлоропласты.[15] В этих комплексах хлорофилл выполняет три функции. Функция подавляющего большинства хлорофилла (до нескольких сотен молекул на фотосистему) заключается в поглощении света. Сделав это, эти же центры выполняют свою вторую функцию: передачу этой световой энергии посредством резонансная передача энергии к определенной паре хлорофилла в центр реакции фотосистем. Эта пара влияет на конечную функцию хлорофиллов, разделение зарядов, что приводит к биосинтезу. фотосистема II и фотосистема I, у которых есть свои отдельные реакционные центры, названные P680 и P700, соответственно. Эти центры названы по длине волны (в нанометры ) их максимума поглощения красного пика. Идентичность, функция и спектральные свойства типов хлорофилла в каждой фотосистеме различны и определяются друг другом и окружающей их белковой структурой. После извлечения из белка в растворитель (например, ацетон или же метанол ),[16][17][18] эти пигменты хлорофилла можно разделить на хлорофилл а и хлорофилл b.
Функция реакционного центра хлорофилла - поглощать световую энергию и передавать ее другим частям фотосистемы. Поглощенная энергия фотона передается электрону в процессе, называемом разделением зарядов. Удаление электрона из хлорофилла - это реакция окисления. Хлорофилл отдает электрон высокой энергии ряду молекулярных промежуточных продуктов, называемых электронная транспортная цепь. Заряженный реакционный центр хлорофилла (P680+) затем восстанавливается обратно в основное состояние, принимая электрон, оторванный от воды. Электрон, уменьшающий P680+ в конечном итоге происходит за счет окисления воды до O2 и H+ через несколько промежуточных звеньев. Эта реакция заключается в том, как фотосинтезирующие организмы, такие как растения, производят O2 газа, и является источником практически всех O2 в атмосфере Земли. Фотосистема I обычно работает последовательно с Фотосистемой II; таким образом, P700+ Фотосистема I обычно восстанавливается, поскольку она принимает электрон через множество промежуточных продуктов в тилакоидной мембране, электронами, поступающими, в конечном счете, из Фотосистемы II. Однако реакции переноса электронов в тилакоидных мембранах сложны, и источник электронов, используемый для восстановления P700+ может изменяться.
Электронный поток, создаваемый пигментами хлорофилла реакционного центра, используется для перекачки H+ ионов через тилакоидную мембрану, создавая хемиосмотический потенциал, используемый в основном в производстве АТФ (запасенная химическая энергия) или для снижения НАДФ+ к НАДФН. НАДФН - универсальный агент используется для снижения CO2 на сахара, а также другие биосинтетические реакции.
Хлорофилл-белковые комплексы реакционного центра способны непосредственно поглощать свет и выполнять процессы разделения зарядов без помощи других пигментов хлорофилла, но вероятность того, что это происходит при данной интенсивности света, мала. Таким образом, все другие хлорофиллы в фотосистеме и белки антенного пигмента совместно поглощают световую энергию и направляют ее в реакционный центр. Помимо хлорофилла а, есть и другие пигменты, называемые вспомогательные пигменты, которые встречаются в этих антенных комплексах пигмент-белок.
Химическая структура
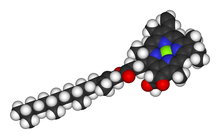
Хлорофиллы многочисленны по типу, но все они определяются наличием пятого кольца за четырьмя пирролоподобными кольцами. Большинство хлорофиллов классифицируются как хлорины, которые являются сокращенными родственниками порфирины (нашел в гемоглобин ). Они имеют общий путь биосинтеза с порфиринами, включая их предшественник. уропорфириноген III. В отличие от гемов, у которых железо в центре тетрапиррол кольцо, связывают хлорофиллы магний. Для структур, изображенных в этой статье, некоторые из лиганды прикреплен к Mg2+ центр опущены для ясности. Хлориновое кольцо может иметь различные боковые цепи, обычно в том числе длинные. фитол цепь. Наиболее распространенная форма у наземных растений - хлорофилл. а.
Структуры хлорофиллов кратко описаны ниже:[19][13]
| Хлорофилл а | Хлорофилл b | Хлорофилл c1 | Хлорофилл c2 | Хлорофилл d | Хлорофилл f[13] | |
|---|---|---|---|---|---|---|
| Молекулярная формула | C55ЧАС72О5N4Mg | C55ЧАС70О6N4Mg | C35ЧАС30О5N4Mg | C35ЧАС28О5N4Mg | C54ЧАС70О6N4Mg | C55ЧАС70О6N4Mg |
| Группа C2 | -CH3 | -CH3 | -CH3 | -CH3 | -CH3 | −CHO |
| Группа C3 | −CH = CH2 | −CH = CH2 | −CH = CH2 | −CH = CH2 | −CHO | −CH = CH2 |
| Группа C7 | -CH3 | −CHO | -CH3 | -CH3 | -CH3 | -CH3 |
| Группа C8 | -CH2CH3 | -CH2CH3 | -CH2CH3 | −CH = CH2 | -CH2CH3 | -CH2CH3 |
| Группа C17 | -CH2CH2COO − Phytyl | -CH2CH2COO − Phytyl | -CH = CHCOOH | -CH = CHCOOH | -CH2CH2COO − Phytyl | -CH2CH2COO − Phytyl |
| Связка C17-C18 | Одинокий (хлорин) | Одинокий (хлорин) | Двойной (порфирин) | Двойной (порфирин) | Одинокий (хлорин) | Одинокий (хлорин) |
| Вхождение | Универсальный | В основном растения | Различные водоросли | Различные водоросли | Цианобактерии | Цианобактерии |
- Структуры хлорофиллов

хлорофилл а
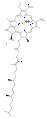
хлорофилл б
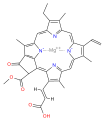
хлорофилл c1

хлорофилл c2
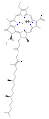
хлорофилл d

хлорофилл ж
Измерение содержания хлорофилла

Измерение поглощения света[как? ] осложняется растворителем, используемым для извлечения хлорофилла из растительного материала, что влияет на полученные значения,
- В диэтиловый эфир, хлорофилл а имеет приблизительные максимумы поглощения 430 нм и 662 нм, а хлорофилл б имеет приблизительные максимумы 453 нм и 642 нм.[20]
- Пики поглощения хлорофилла а находятся на 465 нм и 665 нм. Хлорофилл а флуоресценция при 673 нм (максимум) и 726 нм. Пик молярный коэффициент поглощения хлорофилла а превышает 105 M−1 см−1, который является одним из самых высоких для низкомолекулярных органических соединений.[21]
- В смеси 90% ацетон-вода длины волн пикового поглощения хлорофилла а составляют 430 нм и 664 нм; пики для хлорофилла б составляют 460 нм и 647 нм; пики для хлорофилла c1 - 442 нм и 630 нм; пики для хлорофилла c2 - 444 нм и 630 нм; пики для хлорофилла d составляют 401 нм, 455 нм и 696 нм.[22]
Измеряя поглощение света в красной и дальней красной областях, можно оценить концентрацию хлорофилла в листе.[23]
Коэффициент флуоресцентного излучения можно использовать для измерения содержания хлорофилла. Возбуждая хлорофилл а флуоресценция на более низкой длине волны, отношение испускания флуоресценции хлорофилла на 705±10 нм и 735±10 нм может обеспечить линейную зависимость содержания хлорофилла по сравнению с химическим тестированием. Соотношение F735/F700 предоставил значение корреляции р2 0,96 по сравнению с химическими испытаниями в диапазоне от 41 мг · м−2 до 675 мг · м−2. Гительсон также разработал формулу для прямого считывания содержания хлорофилла в мг / м3.−2. Формула обеспечивает надежный метод измерения содержания хлорофилла в 41 мг / м3.−2 до 675 мг · м−2 с соотношением р2 значение 0,95.[24]
Биосинтез
У некоторых растений хлорофилл получают из глутамат и синтезируется по разветвленной биосинтетический путь который делится с гем и сирохема.[25][26][27]Хлорофилл-синтаза[28] фермент, завершающий биосинтез хлорофилла а[29][30] катализируя реакцию EC 2.5.1.62
- хлорофиллид а + фитилдифосфат хлорофилл а + дифосфат
Это образует сложный эфир группы карбоновой кислоты в хлорофиллид а с 20 углеродом дитерпен алкоголь фитол.Хлорофилл б производится тем же ферментом, действующим на хлорофиллид б.
В Покрытосеменные растения, более поздние стадии биосинтетического пути зависят от света, и такие растения бледные (этиолированный ) если вырос в темноте.[нужна цитата ] Несосудистые растения и зеленые водоросли обладают дополнительным светонезависимым фермент и зеленеют даже в темноте.[нужна цитата ]
Сам хлорофилл обязан белки и может передавать поглощенную энергию в нужном направлении. Протохлорофиллид, один из биосинтетических промежуточных продуктов, встречается в основном в свободной форме и в условиях освещения действует как фотосенсибилизатор, образуя высокотоксичные свободные радикалы. Следовательно, растениям необходим эффективный механизм регулирования количества этого предшественника хлорофилла. У покрытосеменных это делается на этапе аминолевулиновая кислота (ALA), одно из промежуточных соединений в пути биосинтеза. Растения, которые питаются ALA, накапливают высокие и токсичные уровни протохлорофиллида; то же самое делают мутанты с поврежденной регуляторной системой.[31]
Старение и цикл хлорофилла
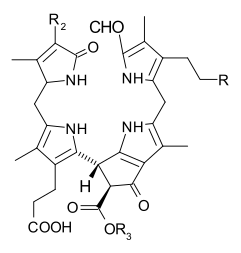
Процесс старение растений вовлекает разложение хлорофилла: например, фермент хлорофиллаза (EC 3.1.1.14 ) гидролизует боковая цепь фитила, чтобы обратить вспять реакцию, в которой хлорофиллы биосинтезируются из хлорофиллида а или же б. Поскольку хлорофиллид а может быть преобразован в хлорофиллид б и последний может быть повторно этерифицирован до хлорофилла б, эти процессы позволяют переключаться между хлорофиллами а и б. Кроме того, хлорофилл б можно напрямую уменьшить (через 71-гидроксихлорофилл а) обратно к хлорофиллу а, завершая цикл.[32][33]На более поздних стадиях старения хлорофиллиды превращаются в группу бесцветных тетрапирролы известные как нефлуоресцентные катаболиты хлорофилла (NCC) с общей структурой:
Эти соединения также были обнаружены в созревающих фруктах, и они дают характерные осенние краски к лиственный растения.[33][34]
Дефектная среда может вызвать хлороз
Хлороз это состояние, в котором листья вырабатывают недостаточно хлорофилла, делая их желтыми. Хлороз может быть вызван дефицитом питательных веществ утюг - называется хлорозом железа - или из-за нехватки магний или же азот. PH почвы иногда играет роль в хлорозе, вызванном питательными веществами; многие растения приспособлены к росту в почвах с определенным уровнем pH, и от этого может зависеть их способность поглощать питательные вещества из почвы.[35] Хлороз также может быть вызван патогенами, включая вирусы, бактерии и грибковые инфекции, или насекомыми, сосущими сок.[нужна цитата ]
Дополнительное светопоглощение антоцианов

Антоцианы другие растительные пигменты. Характер поглощения, ответственный за красный цвет антоцианов может дополнять цвет зеленого хлорофилла в фотосинтетически активных тканях, таких как молодые Quercus coccifera листья. Он может защитить листья от нападения пожирателей растений, которых может привлечь зеленый цвет.[36]
Распределение
Карты хлорофилла показывают миллиграммы хлорофилла на кубический метр морской воды каждый месяц. Места с очень низким содержанием хлорофилла, что указывает на очень низкое количество фитопланктон, синие. Места, где концентрация хлорофилла была высокой, что означает рост многих фитопланктона, окрашены в желтый цвет. Наблюдения производятся спектрорадиометром среднего разрешения (MODIS) на спутнике НАСА Aqua. Земля темно-серая, а места, где MODIS не мог собрать данные из-за морского льда, полярной темноты или облаков, светло-серые. Самые высокие концентрации хлорофилла там, где крошечные обитающие на поверхности океанские растения процветающий, находятся в холодных полярных водах или в местах, где океанские течения выносят холодную воду на поверхность, например, вокруг экватора и вдоль берегов континентов. Фитопланктон стимулируется не самой холодной водой. Вместо этого низкие температуры часто являются признаком того, что вода поднялась на поверхность из глубин океана, неся питательные вещества, накопившиеся с течением времени. В полярных водах питательные вещества накапливаются в поверхностных водах в темные зимние месяцы, когда растения не могут расти. Когда весной и летом возвращается солнечный свет, растения цветут в высокой концентрации.[37]
Кулинарное использование
Синтетический хлорофилл зарегистрирован как краситель пищевой добавки, а его Номер E является E140. Повара используют хлорофилл для окрашивания в зеленый цвет различных продуктов и напитков, например пасты и спиртных напитков. Абсент приобретает свой зеленый цвет естественным образом из-за хлорофилла, внесенного через большое разнообразие трав, используемых при его производстве.[38] Хлорофилл не растворяется в воде, и его сначала смешивают с небольшим количеством растительное масло получить желаемое решение.[нужна цитата ]
Биологическое использование
Исследование, проведенное в 2002 году, показало, что «листья, подвергавшиеся воздействию сильного света, содержат деградированные основные антенные белки, в отличие от тех, которые хранятся в темноте, что согласуется с исследованиями освещения изолированные белки ". Это показалось авторам как поддержка гипотеза который "активный кислород виды играют роль in vivo «в краткосрочном поведении растений.[39]
Смотрите также
- Бактериохлорофилл, родственные соединения фототрофных бактерий
- Хлорофиллин, полусинтетическое производное хлорофилла
- Максимум глубокого хлорофилла
- Расти свет, лампа, способствующая фотосинтезу
- Флуоресценция хлорофилла, для измерения стресса растений
Рекомендации
- ^ Мэй П. «Хлорофилл». Бристольский университет.
- ^ «хлорофилл». Интернет-словарь этимологии.
- ^ Muneer S, Ким EJ, Park JS, Lee JH (март 2014 г.). «Влияние зеленых, красных и синих светодиодов на белки мультибелкового комплекса и фотосинтетическую активность при различной интенсивности света в листьях салата (Lactuca sativa L.)». Международный журнал молекулярных наук. 15 (3): 4657–70. Дои:10.3390 / ijms15034657. ЧВК 3975419. PMID 24642884.
- ^ Speer BR (1997). «Фотосинтетические пигменты». Глоссарий UCMP (онлайн). Музей палеонтологии Калифорнийского университета. Получено 2010-07-17.
- ^ Видеть:
- Делепин М (Сентябрь 1951 г.). «Джозеф Пеллетье и Джозеф Кавенту». Журнал химического образования. 28 (9): 454. Bibcode:1951JChEd..28..454D. Дои:10.1021 / ed028p454.
- Пеллетье и Кавенту (1817 г.) "Notice sur la matière verte des feuilles" (Обратите внимание на зеленый материал в листьях), Journal de Pharmacie, 3 : 486-491. На стр. 490 авторы предлагают новое название хлорофиллу. С п. 490: "Nous n'avons aucun droit pour nommer une entity connue depuis long temps, et à l'histoire de laquelle nous n'avons ajouté que quelques faits; cependant nous proposerons, sans y mettre aucune important, le nom de" хлорофил, де хлор, couleur, et φυλλον, feuille: ce nom indiquerait le rôle qu'elle joue dans la nature ". (Мы не имеем права называть вещество, [которое] было] известно давно и к истории которого мы добавили лишь несколько фактов; однако мы предложим, не придавая этому значения, название хлорофилл, из хлор, цвет и φυλλον, лист: это имя указывает на роль, которую он играет в природе.)
- ^ Willstätter R (1906). "Zur Kenntniss der Zusammensetzung des Chlorophylls" [Вклад в знание состава хлорофилла]. Annalen der Chemie (на немецком). 350 (1–2): 48–82. Дои:10.1002 / jlac.19063500103.
С п. 49: "Das Hauptproduct der alkalischen Hydrolyse bilden tiefgrüne Alkalisalze. В ihnen liegen complexe Magnesiumverbindungen vor, die das Metall in einer gegen Alkali auch bei hoher Temperatur merkwürdig widestandsfähigen Bindung enthalten". (Глубокие зеленые щелочные соли образуют основной продукт щелочного гидролиза. В них присутствуют сложные соединения магния, которые содержат металл в связи, чрезвычайно устойчивой к щелочам даже при высокой температуре.)
- ^ а б Мотильва М (2008). «Хлорофиллы - от функциональности в продуктах питания до актуальности для здоровья». 5-й конгресс по пигментам в продуктах питания - за качество и здоровье (Распечатать). Университет Хельсинки. ISBN 978-952-10-4846-3.
- ^ Woodward RB, Ayer WA, Beaton JM, Bickelhaupt F, Bonnett R, Buchschacher P и др. (Июль 1960 г.). «Полный синтез хлорофилла» (PDF). Журнал Американского химического общества. 82 (14): 3800–3802. Дои:10.1021 / ja01499a093.
- ^ Флеминг I (14 октября 1967 г.). «Абсолютная конфигурация и структура хлорофилла». Природа. 216 (5111): 151–152. Bibcode:1967Натура.216..151F. Дои:10.1038 / 216151a0. S2CID 4262313.
- ^ Woodward RB, Ayer WA, Beaton JM, Bickelhaupt F, Bonnett R, Buchschacher P и др. (1990). «Полный синтез хлорофилла а». Тетраэдр. 46 (22): 7599–7659. Дои:10.1016 / 0040-4020 (90) 80003-Z.
- ^ Джабр Ф (август 2010 г.). "Новая форма хлорофилла?". Scientific American.
- ^ Инфракрасный хлорофилл может стимулировать солнечные батареи. Новый ученый. 19 августа, 2010. Проверено 15 апреля 2012 г.
- ^ а б c Чен, Мин; Шлип, Мартин; Willows, Роберт Д.; Цай, Чжэн-Ли; Neilan, Brett A .; Шеер, Хьюго (2010). «Красный смещенный хлорофилл: рис. 1». Наука. 329 (5997): 1318–1319. Дои:10.1126 / science.1191127. PMID 20724585. S2CID 206527174.
- ^ Картер Дж. С. (1996). «Фотосинтез». Университет Цинциннати. Архивировано из оригинал на 29.06.2013.
- ^ Природа (5 июля 2013 г.). «Блок 1.3. Фотосинтетические клетки». Основы клеточной биологии. nature.com.
- ^ Маркер AF (1972). «Использование ацетона и метанола в оценке хлорофилла в присутствии феофитина в растениях». Пресноводная биология. 2 (4): 361–385. Дои:10.1111 / j.1365-2427.1972.tb00377.x.
- ^ Джеффри С.В., Шибата (февраль 1969 г.). «Некоторые спектральные характеристики хлорофилла c из Tridacna crocea Zooxanthellae». Биологический бюллетень. 136 (1): 54–62. Дои:10.2307/1539668. JSTOR 1539668.
- ^ Гилпин Л. (21 марта 2001 г.). «Методы анализа придонного фотосинтетического пигмента». Школа наук о жизни, Университет Напьера. Архивировано из оригинал 14 апреля 2008 г.. Получено 2010-07-17.
- ^ Шеер, Хьюго (2006). «Обзор хлорофиллов и бактериохлорофиллов: биохимия, биофизика, функции и приложения». Хлорофиллы и бактериохлорофиллы. Достижения в фотосинтезе и дыхании. 25. С. 1–26. Дои:10.1007/1-4020-4516-6_1. ISBN 978-1-4020-4515-8.
- ^ Гросс Дж (1991). Пигменты в овощах: хлорофиллы и каротиноиды.. Ван Ностранд Рейнхольд. ISBN 978-0442006570.
- ^ Порра Р.Дж., Томпсон В.А., Криедеманн П.Е. (1989). «Определение точных коэффициентов экстинкции и одновременных уравнений для анализа хлорофиллов a и b, экстрагированных четырьмя различными растворителями: проверка концентрации стандартов хлорофилла с помощью атомно-абсорбционной спектроскопии». Biochimica et Biophysica Acta (BBA) - Биоэнергетика. 975 (3): 384–394. Дои:10.1016 / S0005-2728 (89) 80347-0.
- ^ Ларкум А.В., Дуглас С., Рэйвен Дж. А., ред. (2003). Фотосинтез в водорослях. Лондон: Клувер. ISBN 978-0-7923-6333-0.
- ^ Кейт Т., Перкинс Т.Д. (сентябрь 2003 г.). «Джозеф Пеллетье и Джозеф Кавенту». Журнал физиологии деревьев. 23 (15): 1077–1079. Дои:10.1093 / treephys / 23.15.1077. PMID 12975132.
- ^ Гительсон А.А., Бушманн С., Лихтенталер Н.К. (1999). "Коэффициент флуоресценции хлорофилла F735/F700 как точный показатель содержания хлорофилла в растениях ». Remote Sens. Enviro. 69 (3): 296–302. Bibcode:1999RSEnv..69..296G. Дои:10.1016 / S0034-4257 (99) 00023-1.
- ^ Баттерсби, А. Р. (2000). «Тетрапирролы: пигменты жизни. Обзор тысячелетия». Nat. Prod. Представитель. 17 (6): 507–526. Дои:10.1039 / B002635M. PMID 11152419.
- ^ Ахтар, М. (2007). «Модификация ацетатных и пропионатных боковых цепей во время биосинтеза гема и хлорофиллов: механистические и стереохимические исследования». Ciba Foundation Symposium 180 - Биосинтез тетрапиррольных пигментов. Симпозиумы Фонда Новартис. 180. С. 131–155. Дои:10.1002 / 9780470514535.ch8. ISBN 9780470514535. PMID 7842850.
- ^ Уиллоуз, Роберт Д. (2003). «Биосинтез хлорофиллов из протопорфирина IX». Отчеты о натуральных продуктах. 20 (6): 327–341. Дои:10.1039 / B110549N. PMID 12828371.
- ^ Schmid, H.C .; Рассадина, В .; Oster, U .; Schoch, S .; Рюдигер, В. (2002). «Предварительная загрузка хлорофилл-синтазы тетрапренилдифосфатом является обязательным этапом биосинтеза хлорофилла» (PDF). Биологическая химия. 383 (11): 1769–78. Дои:10.1515 / BC.2002.198. PMID 12530542. S2CID 3099209.
- ^ Экхардт, Ульрих; Гримм, Бернхард; Гортенштайнер, Стефан (2004). «Последние достижения в биосинтезе и распаде хлорофилла у высших растений». Молекулярная биология растений. 56 (1): 1–14. Дои:10.1007 / s11103-004-2331-3. PMID 15604725. S2CID 21174896.
- ^ Болливар, Дэвид В. (2007). «Последние достижения в биосинтезе хлорофилла». Фотосинтез Исследования. 90 (2): 173–194. Дои:10.1007 / s11120-006-9076-6. PMID 17370354. S2CID 23808539.
- ^ Мескаускене Р., Натер М., Гослинг Д., Кесслер Ф., op den Camp R, Апель К. (октябрь 2001 г.). «Грипп: негативный регулятор биосинтеза хлорофилла у Arabidopsis thaliana». Труды Национальной академии наук Соединенных Штатов Америки. 98 (22): 12826–31. Bibcode:2001ПНАС ... 9812826М. Дои:10.1073 / pnas.221252798. JSTOR 3056990. ЧВК 60138. PMID 11606728.
- ^ «Цикл хлорофилла». IUBMB. 2011 г.. Получено 2020-06-04.
- ^ а б Хёртенштайнер, С. (2006). «Деградация хлорофилла во время старения». Ежегодный обзор биологии растений. 57: 55–77. Дои:10.1146 / annurev.arplant.57.032905.105212. PMID 16669755.
- ^ Мюллер Т., Ульрих М., Онгания К.Х., Кройтлер Б. (2007). «Бесцветные тетрапиррольные катаболиты хлорофилла, обнаруженные в созревающих фруктах, являются эффективными антиоксидантами». Angewandte Chemie. 46 (45): 8699–702. Дои:10.1002 / anie.200703587. ЧВК 2912502. PMID 17943948.
- ^ Duble RL. «Железный хлороз в дерновине». Техасский университет A&M. Получено 2010-07-17.
- ^ Карагеоргу П., Манетас Ю. (май 2006 г.). «Важность быть красной в молодости: антоцианы и защита молодых листьев Quercus coccifera от травоядных насекомых и избытка света». Физиология деревьев. 26 (5): 613–21. Дои:10.1093 / treephys / 26.5.613. PMID 16452075.
- ^ Хлорофилл: Глобальные карты. Earthobservatory.nasa.gov. Проверено 2 февраля 2014.
- ^ Адамс Дж (2004). Ужасный абсент: история дьявола в бутылке. Соединенное Королевство: И. Б. Таурис, 2004. стр. 22. ISBN 978-1860649202.
- ^ Золла, Лелло; Ринальдуччи, Сара (2002). «Участие активных форм кислорода в деградации светособирающих белков при световых стрессах †». Биохимия. 41 (48): 14391–14402. Дои:10.1021 / bi0265776. PMID 12450406.