Каротиноид - Carotenoid
Каротиноиды (/kəˈрɒтɪпɔɪd/), также называемый тетратерпеноиды, желтые, оранжевые и красные органический пигменты которые производятся растениями и водорослями, а также некоторыми бактериями и грибами.[1] Каротиноиды придают характерный цвет тыквы, морковь, кукуруза, помидоры, канарейки, фламинго, лосось, лобстер, креветки и нарциссы.[1] Каротиноиды могут вырабатываться всеми этими организмами из жиров и других основных органических метаболических блоков. Единственные наземные членистоногие, которые, как известно, производят каротиноиды, это тля, и паутинный клещ, который приобрел способность и гены от грибов.[2][3][4] Он также продуцируется эндосимбиотическими бактериями белокрылки.[5] Каротиноиды из рациона откладываются в жировых тканях животных,[1] и исключительно плотоядные животные получают соединения из животного жира. В рационе человека поглощение каротиноидов улучшается при употреблении с жиром в еде.[6] Приготовление овощей, содержащих каротиноиды, в масле увеличивает количество каротиноидов биодоступность.[1][6]
Известно более 1100 каротиноидов.[7] которые можно разделить на два класса: ксантофиллы (которые содержат кислород) и каротины (которые являются чистыми углеводородами и не содержат кислорода).[1] Все производные из тетратерпены, что означает, что они производятся из 8 изопрен молекул и содержат 40 атомов углерода. Как правило, каротиноиды поглощают волны с длиной волны от 400 до 550 нанометров (от фиолетового до зеленого света). Это приводит к тому, что соединения становятся ярко-желтыми, оранжевыми или красными. Каротиноиды являются доминирующим пигментом в окраске осенних листьев около 15-30% древесных пород,[1] но многие цвета растений, особенно красные и пурпурные, связаны с полифенолы.

Каротиноиды выполняют две ключевые роли в растениях и водорослях: они поглощают световую энергию для использования в фотосинтезе и обеспечивают фотозащита через нефотохимическая закалка.[8] Каротиноиды, содержащие незамещенные бета-иононовые кольца (включая бета-каротин, альфа-каротин, бета-криптоксантин, и гамма-каротин ) имеют витамин А активность (это означает, что они могут быть преобразованы в ретинол ). В глаза, лютеин, мезо-зеаксантин, и зеаксантин присутствуют как макулярные пигменты чье значение для зрительной функции по состоянию на 2016 год остается ниже клинические исследования.[1][9]
Биосинтез

Основными строительными блоками каротиноидов являются изопентенилдифосфат (IPP) и диметилаллилдифосфат (DMAPP).[10] Эти два изомера изопрена используются для создания различных соединений в зависимости от биологического пути, используемого для синтеза изомеров.[11] Известно, что растения используют два различных пути для продукции IPP: цитозольный путь мевалоновой кислоты (MVA) и пластидный метилэритритол-4-фосфат (MEP).[10] У животных производство холестерина начинается с создания IPP и DMAPP с использованием MVA.[11] На заводах по производству каротиноидов используйте MEP для создания IPP и DMAPP.[10] Путь MEP приводит к смеси IPP: DMAPP в соотношении 5: 1.[11] IPP и DMAPP претерпевают несколько реакций, в результате которых образуется главный предшественник каротиноидов, геранилгеранил дифосфат (GGPP). GGPP может быть преобразован в каротины или ксантофиллы, пройдя ряд различных этапов пути биосинтеза каротиноидов.[10]
Путь MEP
Глицеральдегид 3-фосфат и пируват, промежуточные звенья фотосинтез, превращаются в дезокси-D-ксилулозо-5-фосфат (DXP) с использованием катализатора DXP-синтаза (DXS). DXP редуктоизомераза уменьшает и перестраивает молекулы в DXP[10] в присутствии НАДФН,[11] формирование MEP.[10] Затем MEP превращается в 4- (цитидин 5’-дифосфо) -2-C-метил-D-эритрит (CDP-ME) в присутствии CTP через фермент MEP цитидилилтрансферазу. CDP-ME затем конвертируется в присутствии АТФ на 2-фосфо-4- (цитидин 5’-дифосфо) -2-C-метил-D-эритритол (CDP-ME2P). Превращение в CDP-ME2P катализируется ферментом CDP-ME киназа. Затем CDP-ME2P превращается в 2-C-метил-D-эритритол 2,4-циклодифосфат (MECDP). Эта реакция происходит, когда MECDP-синтаза катализирует реакцию и CMP удаляется из молекулы CDP-ME2P. Затем MECDP превращается в (e) -4-гидрокси-3-метилбут-2-ен-1-илдифосфат (HMBDP) через HMBDP-синтаза в присутствии флаводоксин и НАДФН. HMBDP сводится к IPP при наличии ферредоксин и НАДФН ферментом HMBDP редуктаза. Последние два этапа с участием HMBPD-синтазы и редуктазы могут происходить только полностью. анаэробный среды. После этого IPP может изомеризовать в DMAPP через изомеразу IPP.[11]
Путь биосинтеза каротиноидов
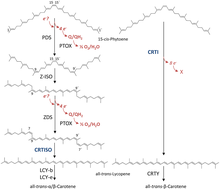
Две молекулы GGPP конденсируются через фитоенсинтаза (PSY), образуя 15-цис изомер из фитоен. Последующее преобразование в полностью транс-ликопин зависит от организма. Бактерии и грибы используют единственный фермент, бактериальная фитоенодесатураза (CRTI) для катализа. Однако растения и цианобактерии используют для этого четыре фермента.[12] Первый из этих ферментов - это фитоиндесатураза растительного типа который вводит две дополнительные двойные связи в 15-цис-фитоен посредством дегидрирование и изомеризует две существующие двойные связи из транс в снг производство 9,15,9’-три-цис-ζ-каротина. Центральная двойная связь этого три-цис-ζ-каротина изомеризуется зета-каротина изомераза Z-ISO и полученный 9,9'-ди-цис-ζ-каротин снова дегидрируют через ζ-каротин десатураза (ZDS). Это снова вводит две двойные связи, в результате чего получается 7,9,7 ’, 9’-тетра-цис-ликопин. CRTISO, изомераза каротиноидов, необходима для преобразования СНГ -ликопин в все-транс ликопин в присутствии восстановленного FAD.
Этот полностью транс-ликопин подвергается циклизации; циклизация приводит к разнообразию каротиноидов, которое можно различить по концевым группам. Может быть либо бета кольцо или эпсилон-кольцо, каждое из которых генерируется отдельным ферментом (ликопин бета-циклаза [beta-LCY] или ликопин-эпсилон-циклаза [эпсилон-LCY]). Альфа-каротин образуется, когда полностью трансликопин сначала вступает в реакцию с эпсилон-LCY, а затем во вторую реакцию с бета-LCY; в то время как бета-каротин производится двумя реакциями с бета-LCY. Альфа- и бета-каротин - самые распространенные каротиноиды в растении. фотосистемы но они все еще могут быть преобразованы в ксантофиллы с помощью бета-гидролазы и эпсилон-гидролазы, что приводит к образованию различных ксантофиллов.[10]
Регулирование
Считается, что как DXS, так и DXR являются ферментами, определяющими скорость, что позволяет им регулировать уровень каротиноидов.[10] Это было обнаружено в эксперименте, в котором DXS и DXR были генетически сверхэкспрессированы, что привело к повышенной экспрессии каротиноидов в полученных проростках.[10] Также считается, что шапероны J-белка (J20) и белка теплового шока 70 (Hsp70) участвуют в посттранскрипционной регуляции активности DXS, так что мутанты с дефектной активностью J20 проявляют пониженную активность фермента DXS при накоплении неактивного белка DXS.[13] Регулирование также может быть вызвано внешними токсины которые влияют на ферменты и белки, необходимые для синтеза. Кетокломазон получают из гербициды наносится на почву и связывается с DXP-синтазой.[11] Это ингибирует DXP-синтазу, предотвращая синтез DXP и останавливая путь MEP.[11] Использование этого токсина приводит к снижению уровня каротиноидов в растениях, выращиваемых в загрязненной почве.[11] Фосмидомицин, антибиотик, это конкурентный ингибитор DXP-редуктоизомеразы из-за его структуры, аналогичной ферменту.[11] Применение указанного антибиотика предотвращает снижение DXP, снова останавливая путь MEP.[11]
Структура и функции
Структура каротиноидов придает биологические способности, в том числе фотосинтез, фотозащита, окраска растений и клеточная сигнализация.
Общая структура каротиноида представляет собой полиен цепь, состоящая из 9-11 двойных связей и, возможно, оканчивающаяся кольцами. Эта структура сопряженные двойные связи приводит к высокому восстановительному потенциалу или способности переносить электроны по всей молекуле.[14] Каротиноиды могут передавать энергию возбуждения одним из двух способов: 1) синглет-синглетная передача энергии от каротиноида к хлорофилл 2) триплет-триплетный перенос энергии от хлорофилла к каротиноиду. Синглет-синглетный перенос энергии представляет собой передачу более низкого энергетического состояния и используется во время фотосинтеза.[15] Длина полиенового хвоста обеспечивает поглощение света в фотосинтетическом диапазоне; как только он поглощает энергию, он становится возбужденным, а затем передает возбужденные электроны в хлорофилл для фотосинтеза.[14] Триплет-триплетный перенос является более высоким энергетическим состоянием и необходим для фотозащиты.[15] И свет, и кислород производят вредные вещества во время фотосинтеза, причем самые разрушительные из них активные формы кислорода (ROS). Поскольку эти высокоэнергетические АФК производятся в хлорофилле, энергия передается полиеновому хвосту каротиноида и претерпевает серию реакций, в которых электроны перемещаются между каротиноидными связями, чтобы найти наиболее сбалансированное состояние (состояние с наименьшей энергией) для каротиноида.[14]
Длина каротиноидов также играет роль в окраске растений, поскольку длина полиенового хвоста определяет, какие длины волн света будет поглощать растение. Волны, которые не поглощаются, отражаются и являются цветом растения.[14] Следовательно, разные виды будут содержать каротиноиды с разной длиной хвоста, что позволяет им поглощать и отражать разные цвета.[14]
Каротиноиды также участвуют в различных типах клеточной передачи сигналов.[15] Они могут сигнализировать о производстве абсцизовая кислота, регулирующий рост растений, покой семян, созревание эмбриона и прорастание, деление клеток удлинение, рост цветков и реакции на стресс.[16]
Характеристики

Каротиноиды относятся к категории тетратерпеноиды (т.е. они содержат 40 атомов углерода и состоят из четырех терпен единиц, каждая из которых содержит 10 атомов углерода). Структурно каротиноиды имеют вид полиен углеводородная цепь, которая иногда заканчивается кольцами и может иметь или не иметь присоединенные дополнительные атомы кислорода.
- Каротиноиды с молекулами, содержащими кислород, такие как лютеин и зеаксантин, известны как ксантофиллы.
- Неоксигенированные (бескислородные) каротиноиды, такие как α-каротин, β-каротин, и ликопин, известны как каротины. Каротины обычно содержат только углерод и водород (т.е. углеводороды ) и находятся в подклассе непредельные углеводороды.
Их цвет, варьирующийся от бледно-желтого через ярко-оранжевый до темно-красного, напрямую связан с их структурой. Ксантофиллы часто желтые, отсюда и название их класса. В двойные углерод-углеродные связи взаимодействуют друг с другом в процессе, называемом спряжение, что позволяет электронам в молекуле свободно перемещаться по этим участкам молекулы. По мере увеличения количества сопряженных двойных связей электроны, связанные с сопряженными системами, имеют больше места для перемещения и требуют меньше энергии для изменения состояния. Это приводит к уменьшению диапазона энергий света, поглощаемого молекулой. По мере того, как большее количество длин волн света поглощается из более длинного конца видимого спектра, соединения приобретают все более красный вид.
Каротиноиды обычно липофильный из-за наличия длительного ненасыщенный алифатический цепи, как в некоторых жирные кислоты. Физиологическое всасывание этих жирорастворимые витамины в организме человека и других организмов напрямую зависит от наличия жиров и желчные соли.[1]
Еда
Бета-каротин, нашел в тыквы, сладкий картофель, морковь и зимний сквош, отвечает за их оранжево-желтый цвет.[1] Сушеная морковь содержит наибольшее количество каротина из всех продуктов на 100-граммовую порцию, измеренное в эквивалентах активности ретинола (эквиваленты провитамина А).[17] вьетнамский gac фрукты содержат самую высокую известную концентрацию каротиноидов ликопин.[18] Хотя зеленый, капуста, шпинат, капуста зелень, и зелень репы содержат значительное количество бета-каротина.[1] Диета фламинго богат каротиноидами, придающими перьям этих птиц оранжевый цвет.[19]
Физиологические эффекты
Обзоры эпидемиологический Исследования, направленные на поиск корреляции между потреблением каротиноидов с пищей и клиническими результатами, пришли к различным выводам:
- Обзор 2015 года показал, что продукты с высоким содержанием каротиноидов, по-видимому, защищают от рак головы и шеи.[20]
- Еще один обзор 2015 года, посвященный тому, могут ли каретеноиды предотвращать рак простаты обнаружили, что, хотя несколько исследований показали, что корреляция между диетами, богатыми каротиноидами, по-видимому, оказывает защитный эффект, недостаточно доказательств, чтобы определить, связано ли это с каротиноидами как таковыми.[21]
- Обзор 2014 года не выявил корреляции между потреблением продуктов с высоким содержанием каротиноидов и витамина А и риском заражения. болезнь Паркинсона.[22]
- В другом обзоре 2014 г. не было обнаружено противоречивых результатов в исследованиях потребления каротиноидов с пищей и риска их получения. рак молочной железы.[23]
Каротиноиды также являются важными компонентами темно-коричневого пигмента. меланин, который содержится в волосах, коже и глазах. Меланин поглощает свет высокой энергии и защищает эти органы от внутриклеточного повреждения.
- Несколько исследований показали положительное влияние диеты с высоким содержанием каротиноидов на текстуру, чистоту, цвет, прочность и эластичность кожи.[24][25][26]
- Исследование 1994 года показало, что диета с высоким содержанием каротиноидов помогает уменьшить симптомы напряжение глаз (сухость глаз, головные боли и помутнение зрения) и улучшить ночное зрение.[27][28]
Люди и другие животные в основном не способны синтезировать каротиноиды и должны получать их с пищей. Каротиноиды - обычная и часто декоративная особенность животных. Например, розовый цвет лосось, и красный цвет приготовленных лобстеры и чешуйки желтого морфа обыкновенные настенные ящерицы связаны с каротиноидами.[29][нужна цитата ] Было высказано предположение, что каротиноиды используются в декоративных элементах (крайние примеры см. тупик птицы), потому что, учитывая их физиологические и химические свойства, они могут использоваться в качестве видимых индикаторов индивидуального здоровья и, следовательно, используются животными при выборе потенциальных партнеров.[30]
Цвета растений


Наиболее распространенные каротиноиды включают ликопин и предшественник витамина А β-каротин. В растениях ксантофилл лютеин является наиболее распространенным каротиноидом, и его роль в предотвращении возрастных заболеваний глаз в настоящее время изучается.[9] Лютеин и другие каротиноидные пигменты, обнаруженные в зрелых листьях, часто не очевидны из-за маскирующего присутствия хлорофилл. Когда хлорофилл отсутствует, как в осенней листве, преобладают желтые и оранжевые цвета каротиноидов. По той же причине каротиноидные цвета часто преобладают в спелых фруктах после того, как они становятся невидимыми из-за исчезновения хлорофилла.
Каротиноиды отвечают за ярко-желтый и оранжевый оттенок. лиственный листва (например, умирающая Осенние листья ) определенных пород древесины как гикори, пепел, клен, желтый тополь, осина, береза, черная вишня, платан, тополь, сассафрас, и ольха. Каротиноиды являются доминирующим пигментом в окраске осенних листьев около 15-30% древесных пород.[31] Однако красный, пурпурный и их смешанные комбинации, которые украшают осеннюю листву, обычно происходят из другой группы пигментов в клетках, называемых антоцианы. В отличие от каротиноидов, эти пигменты не присутствуют в листе на протяжении всего вегетационного периода, но активно вырабатываются к концу лета.[32]
Ароматические химикаты
Продукты распада каротиноидов, такие как иононы, дамасконы и дамасценоны также являются важными ароматизирующими химическими веществами, которые широко используются в духи и парфюмерная промышленность. И β-дамасценон, и β-ионон, хотя и имеют низкую концентрацию в Роза Дистилляты являются основными веществами, вызывающими запах цветов. На самом деле сладкие цветочные запахи присутствуют в черный чай, в возрасте табак, виноград, и много фрукты происходят из-за ароматических соединений, возникающих в результате распада каротиноидов.
Болезнь
Некоторые каротиноиды производятся бактериями для защиты от окислительной иммунной атаки. Золотой пигмент, придающий некоторые оттенки Золотистый стафилококк их имя (aureus = золотой) - это каротиноид, называемый стафилоксантин. Этот каротиноид является фактором вирулентности с антиоксидант действие, которое помогает микробу избежать смерти активные формы кислорода используется иммунной системой хозяина.[33]
Каротиноиды природного происхождения
- Углеводороды
- Ликоперсен 7,8,11,12,15,7 ', 8', 11 ', 12', 15'-декагидро-γ, γ-каротин
- Фитофлуен
- Ликопин
- Гексагидроликопин 15-СНГ-7,8,11,12,7 ', 8'-гексагидро-γ, γ-каротин
- Торулене 3 ', 4'-Дидегидро-β, γ-каротин
- α-Zeacarotene 7 ', 8'-дигидро-ε, γ-каротин
- бета-каротин
- Спирты
- Аллоксантин
- Бактерируберин 2,2'-Бис (3-гидрокси-3-метилбутил) -3,4,3 ', 4'-тетрадегидро-1,2,1', 2'-тетрагидро-γ, γ-каротин-1,1 ' -диол
- Синтиаксантин
- Пектеноксантин
- Криптомонаксантин (3R, 3'R) -7,8,7 ', 8'-Тетрадегидро-β, β-каротин-3,3'-диол
- Crustaxanthin β, -каротен-3,4,3 ', 4'-тетрол
- Газаниаксантин (3R) -5'-цис-β, γ-каротин-3-ол
- ОН-хлоробактен 1 ', 2'-дигидро-f, γ-каротин-1'-ол
- Лороксантин β, ε-каротин-3,19,3'-триол
- Лютеин (3R, 3′R, 6′R) -β, ε-каротин-3,3′-диол
- Ликоксантин γ, γ-каротин-16-ол
- Родопин 1,2-дигидро-γ, γ-каротин-1-ол
- Родопинол a.k.a. Вармингол 13-СНГ-1,2-дигидро-γ, γ-каротин-1,20-диол
- Сапроксантин 3 ', 4'-Дидегидро-1', 2'-дигидро-β, γ-каротин-3,1'-диол
- Зеаксантин
- Гликозиды
- Осцилаксантин 2,2'-Бис (β-L-рамнопиранозилокси) -3,4,3 ', 4'-тетрадегидро-1,2,1', 2'-тетрагидро-γ, γ-каротин-1,1'-диол
- Флейксантофилл 1 '- (β-D-глюкопиранозилокси) -3', 4'-дидегидро-1 ', 2'-дигидро-β, γ-каротин-2'-ол
- Эфиры
- Родовибрин 1'-Метокси-3 ', 4'-дидегидро-1,2,1', 2'-тетрагидро-γ, γ-каротин-1-ол
- Сфероиден 1-Метокси-3,4-дидегидро-1,2,7 ', 8'-тетрагидро-γ, γ-каротин
- Эпоксиды
- Диадиноксантин 5,6-эпокси-7 ', 8'-дидегидро-5,6-дигидро-каротин-3,3-диол
- Лютеоксантин 5,6: 5 ', 8'-Диэпокси-5,6,5', 8'-тетрагидро-β, β-каротин-3,3'-диол
- Мутатоксантин
- Цитроксантин
- Зеаксантин фураноксид 5,8-эпокси-5,8-дигидро-β, β-каротин-3,3'-диол
- Неохром 5 ', 8'-Эпокси-6,7-дидегидро-5,6,5', 8'-тетрагидро-β, β-каротин-3,5,3'-триол
- Foliachrome
- Троллихром
- Вочериаксантин 5 ', 6'-эпокси-6,7-дидегидро-5,6,5', 6'-тетрагидро-β, β-каротин-3,5,19,3'-тетрол
- Альдегиды
- Родопинал
- Warmingone 13-цис-1-гидрокси-1,2-дигидро-γ, γ-каротин-20-al
- Торуларходинальдегид 3 ', 4'-Дидегидро-β, γ-каротин-16'-аль
- Кислоты и сложные эфиры кислот
- Torularhodin 3 ', 4'-Дидегидро-β, γ-каротин-16'-овая кислота
- Метиловый эфир торулародина Метил 3 ', 4'-дидегидро-β, γ-каротин-16'-оат
- Кетоны
- Astacene
- Астаксантин
- Кантаксантин[34] также известный как афаницин, хлореллаксантин β, β-каротин-4,4'-дион
- Капсантин (3R, 3'S, 5'R) -3,3'-Дигидрокси-β, κ-каротин-6'-он
- Капсорубин (3S, 5R, 3'S, 5'R) -3,3'-Дигидрокси-κ, κ-каротин-6,6'-дион
- Криптокапсин (3'R, 5'R) -3'-Гидрокси-β, κ-каротин-6'-он
- 2,2'-дикетоспириллоксантин 1,1'-Диметокси-3,4,3 ', 4'-тетрадегидро-1,2,1', 2'-тетрагидро-γ, γ-каротин-2,2'-дион
- Эхиненон β, β-каротин-4-он
- 3'-гидроксиэхиненон
- Флексиксантин 3,1'-дигидрокси-3 ', 4'-дидегидро-1', 2'-дигидро-β, γ-каротин-4-он
- 3-ОН-Кантаксантин, он же Адонирубин, также известный как Адонирубин Феникоксантин 3-гидрокси-β, β-каротин-4,4'-дион
- Гидроксисфериоденон 1'-Гидрокси-1-метокси-3,4-дидегидро-1,2,1 ', 2', 7 ', 8'-гексагидро-γ, γ-каротин-2-он
- Океноне 1'-Метокси-1 ', 2'-дигидро-c, γ-каротин-4'-он
- Пектенолон 3,3'-дигидрокси-7 ', 8'-дидегидро-β, β-каротин-4-он
- Фениконон a.k.a. Дегидроадонирубин 3-гидрокси-2,3-дидегидро-β, β-каротин-4,4'-дион
- Феникоптерон β, ε-каротин-4-он
- Рубиксантон 3-гидрокси-β, γ-каротин-4'-он
- Сифонаксантин 3,19,3'-Тригидрокси-7,8-дигидро-β, ε-каротин-8-он
- Сложные эфиры спиртов
- Astacein 3,3'-Биспальмитоилокси-2,3,2 ', 3'-тетрадегидро-β, β-каротин-4,4'-дион или 3,3'-дигидрокси-2,3,2', 3'-тетрадегидро -β, β-каротин-4,4'-дипальмитат диона
- Фукоксантин 3'-Ацетокси-5,6-эпокси-3,5'-дигидрокси-6 ', 7'-дидегидро-5,6,7,8,5', 6'-гексагидро-β, β-каротин-8- один
- Изофукоксантин 3'-Ацетокси-3,5,5'-тригидрокси-6 ', 7'-дидегидро-5,8,5', 6'-тетрагидро-β, β-каротин-8-он
- Физалин
- Зеаксантин (3R, 3'R) -3,3'-Биспальмитоилокси-β, β-каротин или (3R, 3'R) -β, β-каротин-3,3'-диол
- Siphonein 3,3'-дигидрокси-19-лауроилокси-7,8-дигидро-β, ε-каротин-8-он или 3,19,3'-тригидрокси-7,8-дигидро-β, ε-каротин-8- один 19-лаурат
- Апокаротиноиды
- β-Апо-2'-каротенал 3 ', 4'-Дидегидро-2'-апо-b-каротин-2'-аль
- Апо-2-ликопенал
- Апо-6'-ликопенал 6'-Апо-у-каротин-6'-аль
- Азафринальдегид 5,6-дигидрокси-5,6-дигидро-10'-апо-β-каротин-10'-al
- Биксин 6'-Метил-водород 9'-цис-6,6'-диапокаротен-6,6'-диоат
- Цитранаксантин 5 ', 6'-дигидро-5'-апо-β-каротин-6'-он или 5', 6'-дигидро-5'-апо-18'-нор-β-каротин-6'-он или 6 '-метил-6'-апо-β-каротин-6'-он
- Кроцетин 8,8'-Диапо-8,8'-каротендиовая кислота
- Кроцетинсемиальдегид 8'-оксо-8,8'-диапо-8-каротиновая кислота
- Crocin Дигентиобиозил 8,8'-диапо-8,8'-каротендиоат
- Гопкинсиаксантин 3-гидрокси-7,8-дидегидро-7 ', 8'-дигидро-7'-апо-b-каротин-4,8'-дион или 3-гидрокси-8'-метил-7,8-дидегидро-8 '-апо-b-каротин-4,8'-дион
- Метил апо-6'-ликопеноат Метил 6'-апо-у-каротин-6'-оат
- Парацентрон 3,5-дигидрокси-6,7-дидегидро-5,6,7 ', 8'-тетрагидро-7'-апо-b-каротин-8'-он или 3,5-дигидрокси-8'-метил-6 , 7-дидегидро-5,6-дигидро-8'-апо-b-каротин-8'-он
- Синтаксантин 7 ', 8'-дигидро-7'-апо-b-каротин-8'-он или 8'-метил-8'-апо-b-каротин-8'-он
- Нор- и секокаротиноиды
- Актиниоэритрин 3,3'-бисацилокси-2,2'-динор-b, b-каротин-4,4'-дион
- β-каротенон 5,6: 5 ', 6'-Дисеко-b, b-каротин-5,6,5', 6'-тетрон
- Перидинин 3'-Ацетокси-5,6-эпокси-3,5'-дигидрокси-6 ', 7'-дидегидро-5,6,5', 6'-тетрагидро-12 ', 13', 20'-тринор-b , b-каротин-19,11-олид
- Пирроксантининол 5,6-эпокси-3,3'-дигидрокси-7 ', 8'-дидегидро-5,6-дигидро-12', 13 ', 20'-тринор-b, b-каротин-19,11-олид
- Семи-α-каротенон 5,6-Seco-b, е-каротин-5,6-дион
- Семи-β-каротенон 5,6-секо-b, b-каротин-5,6-дион или 5 ', 6'-секо-b, b-каротин-5', 6'-дион
- Трифазиаксантин 3-Гидроксисеми-b-каротенон 3'-Гидрокси-5,6-секо-b, b-каротин-5,6-дион или 3-гидрокси-5 ', 6'-секо-b, b-каротин-5' , 6'-дион
- Ретро-каротиноиды и ретро-апо-каротиноиды
- Эшшольцксантин 4 ', 5'-Дидегидро-4,5'-ретро-b, b-каротин-3,3'-диол
- Eschscholtzxanthone 3'-гидрокси-4 ', 5'-дидегидро-4,5'-ретро-b, b-каротин-3-он
- Родоксантин 4 ', 5'-Дидегидро-4,5'-ретро-b, b-каротин-3,3'-дион
- Тангераксантин 3-гидрокси-5'-метил-4,5'-ретро-5'-апо-b-каротин-5'-он или 3-гидрокси-4,5'-ретро-5'-апо-b-каротин- 5'-один
- Высшие каротиноиды
- Нонапреноксантин 2- (4-гидрокси-3-метил-2-бутенил) -7 ', 8', 11 ', 12'-тетрагидро-е, у-каротин
- Декапреноксантин 2,2'-Бис (4-гидрокси-3-метил-2-бутенил) -e, е-каротин
- C.p. 450 2- [4-гидрокси-3- (гидроксиметил) -2-бутенил] -2 '- (3-метил-2-бутенил) -b, b-каротин
- C.p. 473 2 '- (4-Гидрокси-3-метил-2-бутенил) -2- (3-метил-2-бутенил) -3', 4'-дидегидро-1 ', 2'-дигидро-β, γ-каротин -1'-ол
- Бактерируберин 2,2'-Бис (3-гидрокси-3-метилбутил) -3,4,3 ', 4'-тетрадегидро-1,2,1', 2'-тетрагидро-γ, γ-каротин-1,1 ' -диол
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я j «Каротиноиды». Информационный центр по микронутриентам, Институт Линуса Полинга, Университет штата Орегон. 1 августа 2016 г.. Получено 17 апреля 2019.
- ^ Моран Н.А., Ярвик Т. (2010).«Боковой перенос генов от грибов лежит в основе продукции каротиноидов у тлей». Наука. 328 (5978): 624–7. Bibcode:2010Sci ... 328..624M. Дои:10.1126 / science.1187113. PMID 20431015. S2CID 14785276.
- ^ Боран Алтынчичек; Дженнифер Л. Ковач; Николь М. Херардо (2011). "Горизонтально перенесенные гены грибковых каротиноидов у двухпятнистого паутинного клеща Tetranychus urticae". Письма о биологии. 8 (2): 253–257. Дои:10.1098 / рсбл.2011.0704. ЧВК 3297373. PMID 21920958.
- ^ Новакова Э., Моран Н.А. (2012). «Диверсификация генов биосинтеза каротиноидов у тлей после древнего переноса от грибка». Мол Биол Эвол. 29 (1): 313–23. Дои:10.1093 / molbev / msr206. PMID 21878683.
- ^ Слоан ДБ, Моран Н.А. (2012). «Эндосимбиотические бактерии как источник каротиноидов белокрылки». Biol Lett. 8 (6): 986–9. Дои:10.1098 / rsbl.2012.0664. ЧВК 3497135. PMID 22977066.
- ^ а б Машурабад, Пурна Чандра; Палика, Равиндранад; Юрва, Иветт Вильда; Bhaskarachary, K .; Пуллахандам, Рагху (3 января 2017 г.). «Диетический жировой состав, пищевая матрица и относительная полярность модулируют мицелларизацию и кишечное поглощение каротиноидов из овощей и фруктов». Журнал пищевой науки и технологий. 54 (2): 333–341. Дои:10.1007 / s13197-016-2466-7. ISSN 0022-1155. ЧВК 5306026. PMID 28242932.
- ^ Ябузаки, Дзюнко (01.01.2017). «База данных каротиноидов: структуры, химические отпечатки пальцев и распределение среди организмов». База данных. 2017 (1). Дои:10.1093 / база данных / bax004. ЧВК 5574413. PMID 28365725.
- ^ Армстронг Г.А., Херст Дж. Э. (1996). «Каротиноиды 2: Генетика и молекулярная биология биосинтеза каротиноидных пигментов». FASEB J. 10 (2): 228–37. Дои:10.1096 / fasebj.10.2.8641556. PMID 8641556. S2CID 22385652.
- ^ а б Бернштейн, П. С .; Ли, Б; Вачали, П. П .; Горусупуди, А; Shyam, R; Хенриксен, Б. С .; Нолан, Дж. М. (2015). «Лютеин, зеаксантин и мезо-зеаксантин: фундаментальные и клинические исследования, лежащие в основе диетических вмешательств на основе каротиноидов против глазных заболеваний». Прогресс в исследованиях сетчатки и глаз. 50: 34–66. Дои:10.1016 / j.preteyeres.2015.10.003. ЧВК 4698241. PMID 26541886.
- ^ а б c d е ж грамм час я Нисар, Назия; Ли, Ли; Лу, Шань; Кхин, Най Чи; Погсон, Барри Дж. (05.01.2015). «Метаболизм каротиноидов в растениях». Молекулярный завод. Метаболизм растений и синтетическая биология. 8 (1): 68–82. Дои:10.1016 / j.molp.2014.12.007. PMID 25578273.
- ^ а б c d е ж грамм час я j КУЗУЯМА, Томохиса; СЕТО, Харуо (09.03.2012). «Два разных пути для основных метаболических предшественников биосинтеза изопреноидов». Труды Японской академии. Серия B, Физические и биологические науки. 88 (3): 41–52. Bibcode:2012PJAB ... 88 ... 41K. Дои:10.2183 / pjab.88.41. ISSN 0386-2208. ЧВК 3365244. PMID 22450534.
- ^ Моисей, Александр Р .; Аль-Бабили, Салим; Вюрцель, Элеонора Т. (31 октября 2013 г.). «Механистические аспекты биосинтеза каротиноидов». Химические обзоры. 114 (1): 164–93. Дои:10.1021 / cr400106y. ЧВК 3898671. PMID 24175570.
- ^ Нисар, Назия; Ли, Ли; Лу, Шань; Чихин, Нет; Погсон, Барри Дж. (5 января 2015 г.). «Метаболизм каротиноидов в растениях». Молекулярный завод. 8 (1): 68–82. Дои:10.1016 / j.molp.2014.12.007. PMID 25578273.
- ^ а б c d е Вершинин, Александр (1999-01-01). «Биологические функции каротиноидов - разнообразие и эволюция». БиоФакторы. 10 (2–3): 99–104. Дои:10.1002 / биоф.5520100203. ISSN 1872-8081. PMID 10609869. S2CID 24408277.
- ^ а б c Когделл, Р. Дж. (1978-11-30). «Каротиноиды в фотосинтезе». Фил. Пер. R. Soc. Лондон. B. 284 (1002): 569–579. Bibcode:1978RSPTB.284..569C. Дои:10.1098 / рстб.1978.0090. ISSN 0080-4622.
- ^ Финкельштейн, Рут (01.11.2013). «Синтез абсцизовой кислоты и ответ». Книга арабидопсиса / Американское общество биологов растений. 11: e0166. Дои:10.1199 / таб.0166. ISSN 1543-8120. ЧВК 3833200. PMID 24273463.
- ^ «Продукты с самым высоким эквивалентом активности ретинола». Nutritiondata.self.com. Получено 2015-12-04.
- ^ Tran, X. T .; Парки, С. Э .; Roach, P.D .; Golding, J. B .; Нгуен, М. Х. (2015). «Влияние зрелости на физико-химические свойства плодов Gac (Momordica cochinchinensis Spreng.)». Пищевая наука и питание. 4 (2): 305–314. Дои:10.1002 / фсн3.291. ЧВК 4779482. PMID 27004120.
- ^ Йим, К. Дж .; Квон, Дж; Cha, I.T .; О, К. С .; Песня, Х. С .; Lee, H.W .; Rhee, J. K .; Сонг, Э. Дж .; Rho, J. R .; Seo, M. L .; Choi, J. S .; Choi, H.J .; Ли, С. Дж .; Nam, Y. D .; Ро, С. В. (2015). «Появление жизнеспособных краснопигментированных галоархей в оперении фламинго в неволе». Научные отчеты. 5: 16425. Bibcode:2015НатСР ... 516425Y. Дои:10.1038 / srep16425. ЧВК 4639753. PMID 26553382.
- ^ Леончини; Источники, природные; Голова; Рак шеи; и другие. (Июль 2015). «Систематический обзор и метаанализ эпидемиологических исследований». Биомаркеры эпидемиологии рака Пред.. 24 (7): 1003–11. Дои:10.1158 / 1055-9965.EPI-15-0053. PMID 25873578. S2CID 21131127.
- ^ Соареш Нда, C; и другие. (Октябрь 2015 г.). «Противораковые свойства каротиноидов при раке простаты. Обзор». Гистол Гистопатол. 30 (10): 1143–54. Дои:10.14670 / HH-11-635. PMID 26058846.
- ^ Такеда, А; и другие. (2014). «Витамин А и каротиноиды и риск болезни Паркинсона: систематический обзор и метаанализ». Нейроэпидемиология. 42 (1): 25–38. Дои:10.1159/000355849. PMID 24356061. S2CID 12396064.
- ^ Chajès, V; Ромье, I (январь 2014 г.). «Питание и рак груди». Maturitas. 77 (1): 7–11. Дои:10.1016 / j.maturitas.2013.10.004. PMID 24215727.
- ^ Схаген, СК; и другие. (2012). ""Василики А. Зампели, Евгения Макрантонаки, Христос К. Зубулис, «Открытие связи между питанием и старением кожи». Дерматоэндокринол. 4 (3): 298–307. Дои:10.4161 / derm.22876. ЧВК 3583891. PMID 23467449.
- ^ Папас, А (2009). «Взаимосвязь диеты и прыщей». Дерматоэндокринол. 1 (5): 262–267. Дои:10.4161 / derm.1.5.10192. ЧВК 2836431. PMID 20808513.
- ^ Чжи Фу, Y; Родос, G; Симмонс, LW (2017). «Каротиноид бета-каротин улучшает цвет лица, привлекательность и воспринимаемое здоровье, но не реальное здоровье у людей». Поведенческая экология. 28 (2): 570–578. Дои:10.1093 / beheco / arw188. S2CID 90683989.
- ^ Roh S, Weiter JJ ,. 1994., Легкое повреждение глаза., J Fla Med Assoc. 1994 Апрель; 81 (4): 248-51.
- ^ Розановска М. и др., Светоиндуцированное повреждение сетчатки. http://photobiology.info/Rozanowska.html
- ^ Сакки, Роберто (4 июня 2013 г.). «Изменение цвета полиморфной обыкновенной настенной ящерицы (Podarcis muralis): анализ с использованием цветовой системы RGB». Zoologischer Anzeiger. 252 (4): 431–439. Дои:10.1016 / j.jcz.2013.03.001.
- ^ Уайтхед Р.Д., Озакинчи Г., Перретт Д.И. (2012). «Привлекательный цвет кожи: использование полового отбора для улучшения диеты и здоровья». Evol Psychol. 10 (5): 842–54. Дои:10.1177/147470491201000507. PMID 23253790. S2CID 8655801.
- ^ Аркетти, Марко; Деринг, Томас Ф .; Hagen, Snorre B .; Хьюз, Николь М .; Кожа, Саймон Р .; Ли, Дэвид В .; Лев-Ядун, Симха; Манетас, Яннис; Угам, Хелен Дж. (2011). «Раскрытие эволюции осенних красок: междисциплинарный подход». Тенденции в экологии и эволюции. 24 (3): 166–73. Дои:10.1016 / j.tree.2008.10.006. PMID 19178979.
- ^ Дэвис, Кевин М., изд. (2004). Растительные пигменты и манипуляции с ними. Ежегодные обзоры растений. 14. Оксфорд: издательство Blackwell Publishing. п. 6. ISBN 978-1-4051-1737-1.
- ^ Лю Г.Й., Эссекс А., Бьюкенен Дж. Т. и др. (2005). «Золотой пигмент Staphylococcus aureus препятствует уничтожению нейтрофилов и способствует вирулентности благодаря своей антиоксидантной активности». J. Exp. Med. 202 (2): 209–15. Дои:10.1084 / jem.20050846. ЧВК 2213009. PMID 16009720.
- ^ Чхве, Сеён; Ку, Санго (2005). «Эффективный синтез кето-каротиноидов кантаксантина, астаксантина и астацена». J. Org. Chem. 70 (8): 3328–3331. Дои:10.1021 / jo050101l. PMID 15823009.
внешняя ссылка
- Каротиноидные терпеноиды
- Каротиноиды как предшественники ароматизаторов и ароматизаторов
- Каротиноидный ген у тли
- Международное каротиноидное общество
- Каротиноиды в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)

