Полифенол - Википедия - Polyphenol
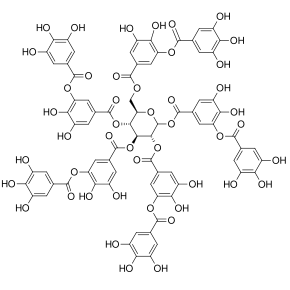
Полифенолы (/ˌпɒляˈжяпoʊл,-пɒл/) представляют собой большое семейство встречающихся в природе органические соединения характеризуется множеством фенол единицы.[1] Они многочисленны в растениях и разнообразны по строению.[1][2][3] Полифенолы включают флавоноиды, дубильная кислота, и эллагитаннин, некоторые из которых исторически использовались как красители и для дубление одежды.
Определение термина полифенол

Термин полифенол четко не определен, но в целом принято считать, что это натуральные продукты, «имеющие структуру полифенола (т.е. несколько гидроксильных групп на ароматических кольцах)», включая четыре основных класса: «фенольные кислоты, флавоноиды, стильбены и лигнаны». .[4]
- Флавоноиды включают флавоны, флавонолы, флаванолы, флаваноны, изофлавоны, проантоцианидины и антоцианы. Особенно много флаваноидов в продуктах питания катехин (чай, фрукты), гесперетин (цитрусовые), цианидин (красные фрукты и ягоды), Daidzein (соя ), проантоцианидины (яблоко, виноград, какао) и кверцетин (лук, чай, яблоки).[2]
- Феноловая кислота включает кофейная кислота
- Лигнаны полифенолы, полученные из фенилаланин нашел в семя льна и другие крупы.
Определение полифенолов "WBSSH"
Определение Уайта-Бэйта-Смита-Суэйна-Хаслама (WBSSH)[5] охарактеризованы структурные характеристики, общие для фенольных соединений растений, используемых в дубление (то есть дубильные вещества).[6] Что касается свойств, WBSSH описывает полифенолы следующим образом:
- в целом умеренно вода соединения
- с молекулярной массой 500–4000 Да
- с> 12 фенольными гидроксильными группами
- с 5–7 ароматическими кольцами на 1000 Да
Что касается структур, WBSSH выделяет два структурных семейства, которые обладают следующими свойствами:
- проантоцианидины и его производные
- галлоил и гексагидроксидифеноиловые эфиры и их производные
Определение полифенолов Quideau
По словам Стефана Кидо, термин «полифенол» относится к соединениям, полученным из шикимат /фенилпропаноид и / или поликетид путь, содержащий более одной фенольной единицы и лишенный азотсодержащих функций.
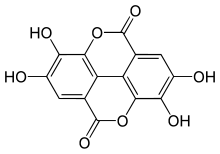
Эллаговая кислота (M.W. 302, справа), молекула, лежащая в основе природных фенольных соединений различных размеров, сама по себе не является полифенолом по определению WBSSH, а по определению Куидо. В малиновый эллагитаннин (M.W. ~ 2450),[7] с другой стороны, с его 14 галловая кислота фрагментов (большинство в компонентах типа эллаговой кислоты) и более 40 фенольных гидроксильных групп соответствует критериям обоих определений полифенола. Другие примеры соединений, которые подпадают под определения WBSSH и Quideau, включают черный чай теафлавин-3-галлат показано ниже, и гидролизуемый танин, дубильная кислота, показано выше.

Строение и биосинтез
Конструктивные особенности
Полифенолы часто представляют собой более крупные молекулы (макромолекулы ). Их верхний предел молекулярной массы составляет около 800 Дальтон, что дает возможность быстро диффундировать через клеточные мембраны, чтобы они могли достигать внутриклеточных участков действия или оставаться в виде пигментов, когда клетка старости. Следовательно, биосинтезируются многие более крупные полифенолы. на месте от полифенолов меньшего размера до негидролизуемых танинов, которые остаются неоткрытыми в растительной матрице. Большинство полифенолов содержат повторяющиеся фенольные фрагменты пирокатехола, резорцина, пирогаллола и флороглюцина, связанные между собой сложные эфиры (гидролизуемые таннины) или более стабильные связи C-C (негидролизуемые конденсированные танины ). Проантоцианидины в основном полимерные единицы катехин и эпикатехин.

Полифенолы часто имеют функциональные группы за пределами гидроксильные группы. Эфир сложный эфир связи обычны, как и карбоновые кислоты.

Химические свойства
Полифенолы реактивный виды к окисление, отсюда их описание как антиоксиданты in vitro.[8]
Использует
Некоторые полифенолы традиционно используются как красители. Например, в Индийский субконтинент, то гранат чистить, с высоким содержанием дубильных веществ и других полифенолов или его сока, используется при крашении несинтетических тканей.[9]
Полифенолы, особенно дубильные вещества, традиционно использовались для дубления кожи, а сегодня также в качестве прекурсоров в зеленая химия[10] в частности, для производства пластмасс или смол путем полимеризации с[11] или без использования формальдегид[12] или же клеи для ДСП.[13] Обычно цель состоит в том, чтобы использовать растительные остатки винограда, оливок (называемых выжимки ) или же орех пекан снаряды остались после обработки.[14]
Пирогаллол и пирокатехин - одни из самых старых фотографические разработчики.[15]:25
Биология
Считается, что полифенолы играют разнообразную роль в экологии растений. Эти функции включают:[16]
- Высвобождение и подавление гормонов роста, таких как ауксин.
- УФ-экраны для защиты от ионизирующего излучения и окрашивания (растительные пигменты ).[4]
- Сдерживание травоядных (сенсорные свойства).
- Профилактика микробных инфекций (фитоалексины ).[4][17]
- Сигнальные молекулы в процессе созревания и других процессов роста.
Встречаемость в природе
Самые распространенные полифенолы - это конденсированные танины, встречается практически во всех семействах растений. Более крупные полифенолы часто концентрируются в тканях листьев, эпидермисе, слоях коры, цветах и плодах, но также играют важную роль в разложении лесной подстилки и круговоротах питательных веществ в экологии леса. Абсолютные концентрации общих фенолов в тканях растений сильно различаются в зависимости от литературных источников, типа полифенолов и анализа; они находятся в диапазоне 1-25% от суммы природные фенолы и полифенолы в пересчете на массу сухих зеленых листьев.[18]
Высокий уровень полифенолов в некоторых лесах может объяснить их естественное происхождение. сохранение против гнили.[19]
Лен и Myriophyllum spicatum (подводное водное растение) выделяют полифенолы, которые участвуют в аллелопатический взаимодействия.[20][21]
Полифенолы также содержатся в животных. В членистоногие Такие как насекомые[22] и ракообразные[23] полифенолы играют роль в эпикутикула закалка (склеротизация ). Затвердение кутикулы происходит из-за наличия полифенолоксидаза.[24] У ракообразных существует вторая оксидазная активность, приводящая к образованию кутикулы. пигментация.[25] По-видимому, дубление полифенолами не происходит. паукообразные кутикула.[26]
Биосинтез и обмен веществ
Полифенолы включают в себя более мелкие детали и строительные блоки из более простых природные фенолы, которые происходят из фенилпропаноид путь фенольных кислот или шикимовая кислота путь для галлотанины и аналоги. Флавоноиды и производные кофейной кислоты биосинтезируются из фенилаланин и малонил-КоА. Сложные галлотанины развиваются через in vitro окисление 1,2,3,4,6-пентагаллоил-глюкоза или процессы димеризации, приводящие к гидролизуемым танинам. Для антоцианидинов, предшественников биосинтеза конденсированных танинов, дигидрофлавонолредуктаза и лейкоантоцианидин редуктаза (LAR) являются ключевыми ферментами с последующим добавлением катехиновых и эпикатехиновых частей для получения более крупных негидролизуемых танинов.[27]
Гликозилированная форма образуется из глюкозилтрансфераза активность и увеличивает растворимость полифенолов.[28]
Полифенолоксидаза (PPO) - это фермент, катализирующий окисление о-дифенолы производить о-хиноны. Именно быстрая полимеризация о-хинонов с образованием черных, коричневых или красных полифенольных пигментов является причиной подрумянивание фруктов. У насекомых ППО служит для укрепления кутикулы.[29]
Содержание в пище
Полифенолы составляют до 0,2-0,3% сырого веса многих фруктов, винограда и ягод. Потребление общих порций вина, шоколада, бобовые или чай также может способствовать примерно одному грамму потребления в день.[2][30] Согласно обзору полифенолов 2005 года:
Наиболее важными источниками питания являются товары, широко потребляемые в больших количествах, такие как фрукты и овощи, зеленый чай, черный чай, красное вино, кофе, шоколад, оливки и оливковое масло первого отжима. Травы и специи, орехи и водоросли также потенциально важны для обеспечения определенных полифенолов. Некоторые полифенолы специфичны для определенных продуктов питания (флаваноны в цитрусовых, изофлавоны в сое, флоридзин в яблоках); тогда как другие, такие как кверцетин, содержатся во всех растительных продуктах, таких как фрукты, овощи, злаки, бобовые, чай и вино.[31]
Некоторые полифенолы считаются антинутриенты - соединения, препятствующие всасыванию основные питательные вещества - особенно ионы железа и других металлов, которые могут связываться с пищеварительные ферменты и другие белки, особенно в жвачные животные.[32]
При сравнении методов приготовления фенольные и каротиноид уровни в овощах лучше сохранялись пропаривание в сравнении с жарка.[33] Полифенолы из вина, пива и различных безалкогольных соковых напитков можно удалить с помощью оклейка, вещества, которые обычно добавляются во время или ближе к завершению процесса пивоварения.[нужна цитата ]
Потенциальное воздействие на здоровье
Хотя воздействие на здоровье может быть связано с употреблением полифенолов в пище,[34] обширный метаболизм полифенолов в кишечнике и печени и их неопределенная судьба как метаболитов, которые быстро выводятся с мочой, не позволяют определить их биологические эффекты.[2] Поскольку метаболизм полифенолов невозможно оценить in vivo, нет Рекомендуемая диета (DRI) установленные или рекомендуемые уровни.[2]
В США Управление по контролю за продуктами и лекарствами (FDA) выпустило руководство по маркировке производителей, согласно которому полифенолы нельзя упоминать в качестве питательных антиоксидантов, если физиологический существуют доказательства, подтверждающие такую квалификацию, и значение DRI установлено.[35][36] Кроме того, поскольку предполагаемые утверждения о пользе для здоровья определенных продуктов, обогащенных полифенолами, остаются недоказанными,[37] заявления о здоровье полифенолов на этикетках продуктов запрещены FDA[36] и EFSA.[38] Однако во время 21-го века, EFSA признало определенные заявления о пользе для здоровья определенных продуктов полифенолов, таких как какао[39] и оливковое масло.[40]
По сравнению с действием полифенолов in vitro, возможные функции in vivo остаются неизвестными из-за 1) отсутствия подтвержденных in vivo биомаркеры;[2] 2) долгосрочные исследования, не продемонстрировавшие эффекты с механизм действия, чувствительность и специфичность или же эффективность;[2] и 3) недопустимые применения высоких нефизиологических тестовых концентраций в исследованиях in vitro, которые впоследствии не имеют отношения к дизайну экспериментов in vivo.[31]
Методы анализа
Сенсорные свойства
Что касается еды и напитков, причина терпкость не до конца изучен, но это измеряется химически как способность вещества осаждать белки.[41]
Обзор, опубликованный в 2005 году, показал, что терпкость увеличивается, а горечь уменьшается со средней степенью полимеризация. Сообщалось, что для водорастворимых полифенолов для осаждения белка требуются молекулярные массы от 500 до 3000. Однако молекулы меньшего размера могут по-прежнему обладать вяжущими свойствами, вероятно, из-за образования неосаждаемых комплексов с белками или сшивания белков простыми фенолами, имеющими 1,2-дигидрокси- или 1,2,3-тригидроксигруппы.[42] Конфигурации флавоноидов также могут вызывать значительные различия в сенсорных свойствах, например эпикатехин более горький и вяжущий, чем его хиральный изомер катехин. Напротив, гидроксикоричные кислоты не обладают вяжущими свойствами, но имеют горький вкус.[43]
Анализ
Методы анализа: фитохимия: добыча, изоляция, структурное объяснение,[44] тогда количественная оценка.
Добыча
Добыча полифенолов[45] может выполняться с использованием растворителя, такого как вода, горячая вода, метанол, метанол / муравьиная кислота, метанол / вода / уксусная или муравьиная кислота. Жидкостно-жидкостная экстракция также может быть выполнено или противоточная хроматография. Твердофазная экстракция также может изготавливаться на картриджах сорбента С18. Другие методы - ультразвуковая экстракция, экстракция с обратным холодильником, экстракция с помощью микроволн,[46] критический диоксид углерода,[14][47] экстракция жидкости под давлением[48] или использование этанола в иммерсионном экстракторе.[49] Условия экстракции (температура, время экстракции, отношение растворителя к сырью, растворитель и концентрации) должны быть оптимизированы.
Высокие уровни полифенолов, которые в основном содержатся в кожуре и семенах фруктов, могут отражать только измеренный извлекаемый полифенолы (EPP), содержащиеся в фруктах, которые также могут содержать неэкстрагируемые полифенолы. Черный чай содержит большое количество полифенолов и составляет 20% от его веса.[50]
Концентрация может производиться ультрафильтрация.[51] Очистка может быть достигнута препаративная хроматография.
Методы анализа

Фосфомолибденовая кислота используется как реагент для окрашивания фенолов в тонкослойная хроматография. Полифенолы можно изучить спектроскопия, особенно в ультрафиолетовой области, фракционирование или же бумажная хроматография. Их также можно проанализировать с помощью химических характеристик.
Инструментальная химия анализы включают разделение к высокоэффективная жидкостная хроматография (ВЭЖХ), и особенно обращенно-фазовая жидкостная хроматография (RPLC), может быть соединен с масс-спектрометрии.[14] Очищенные соединения можно идентифицировать с помощью ядерный магнитный резонанс.
Микроскопический анализ
В Реагент DMACA представляет собой гистологический краситель, специфичный для полифенолов, используемых в микроскопических исследованиях. В автофлуоресценция полифенолов, особенно для локализации лигнина и Суберин. Там, где флуоресценции самих молекул недостаточно для визуализации с помощью световой микроскопии, традиционно использовался DPBA (2-аминоэтиловый эфир дифенилборной кислоты, также называемый реагентом Натурстоффа), по крайней мере, в растениеводство, чтобы усилить сигнал флуоресценции.[52]
Количественная оценка
Содержание полифенолов можно количественно определить путем разделения / выделения. объемное титрование. Окислитель, перманганат, используется для окисления стандартных концентраций танинов с известными концентрациями, что дает стандартная кривая. Затем содержание таннина неизвестного вещества выражается в эквиваленте соответствующего гидролизуемого или конденсированного таннина.[53]
Некоторые методы количественного определения общего содержания полифенолов основаны на колориметрический измерения. Некоторые тесты относительно специфичны для полифенолов (например, тест Портера). Общее количество фенолов (или антиоксидантный эффект) можно измерить с помощью Реакция Фолина-Чокальте.[14] Результаты обычно выражаются в эквиваленте галловой кислоты. Полифенолы редко оцениваются антитело технологии.[54]
Другие тесты измеряют антиоксидантную способность фракции. Некоторые используют ABTS радикальный катион который реагирует на большинство антиоксидантов, включая фенолы, тиолы и Витамин С.[55] Во время этой реакции синий катион-радикал ABTS превращается обратно в свою бесцветную нейтральную форму. За реакцией можно следить спектрофотометрически. Этот анализ часто называют Эквивалентная антиоксидантная способность Trolox (TEAC) анализ. Реакционная способность различных протестированных антиоксидантов сравнивается с реакционной способностью Тролокс, который является витамин Е аналог.
Другие анализы антиоксидантной способности, в которых Trolox используется в качестве стандарта, включают: дифенилпикрилгидразил (DPPH), абсорбционная способность кислородных радикалов (ORAC),[56] железо-восстановительная способность плазмы (FRAP)[57] анализы или ингибирование катализируемых медью in vitro человек липопротеин низкой плотности окисление.[58]
Новые методы, включая использование биосенсоры может помочь контролировать содержание полифенолов в пище.[59]
Результаты количественного анализа, полученные с помощью детектор с диодной матрицей -Связанная ВЭЖХ обычно приводится как относительная, а не абсолютные значения поскольку отсутствуют коммерчески доступные стандарты для всех полифенольных молекул.
Этимология
Название происходит от Древнегреческий слово πολύς (полус, что означает «много, много») и слово фенол, которое относится к химической структуре, образованной присоединением к ароматическому бензоид (фенил ) позвонить в гидроксил (-ОН) группа, которая содержится в спиртах (отсюда -ol суффикс). Термин полифенол используется по крайней мере с 1894 года.[60]
Смотрите также
Рекомендации
- ^ а б Quideau, S.P .; Deffieux, D .; Douat-Casassus, C.L .; Пуйсегу, Л. (2011). «Полифенолы растений: химические свойства, биологическая активность и синтез». Angewandte Chemie International Edition. 50 (3): 586–621. Дои:10.1002 / anie.201000044. PMID 21226137.
- ^ а б c d е ж грамм «Флавоноиды». Информационный центр по микронутриентам, Институт Линуса Полинга, Государственный университет Орегона. 1 февраля 2016 г.. Получено 28 октября 2020.
- ^ Нонака, Г. (1989). «Выделение и выяснение структуры дубильных веществ» (PDF). Pure Appl. Chem. 61 (3): 357–360. Дои:10.1351 / pac198961030357. S2CID 84226096.
- ^ а б c Манах, Клодин; Скальберт, Огюстен; Моран, Кристина; Ремези, Кристиан; Хименес, Лилиана (1 мая 2004 г.). «Полифенолы: источники пищи и биодоступность». Американский журнал клинического питания. 79 (5): 727–747. Дои:10.1093 / ajcn / 79.5.727. ISSN 0002-9165. PMID 15113710.
- ^ Haslam, E .; Цай, Ю. (1994). «Растительные полифенолы (растительные дубильные вещества): метаболизм галловой кислоты». Отчеты о натуральных продуктах. 11 (1): 41–66. Дои:10.1039 / NP9941100041. PMID 15206456.
- ^ Практические полифенолы, Эдвин Хаслам, 1998 г., ISBN 0-521-46513-3
- ^ Сердечно-сосудистые заболевания и фитохимические вещества. Анонимный. C. Hamilton et al.
- ^ Сантос, M.A; Bonilla Venceslada, J.L; Мартин Мартин, A; Гарсия Гарсия, я (2005). «Оценка селективности озона при удалении полифенолов из барды». Журнал химической технологии и биотехнологии. 80 (4): 433–438. Дои:10.1002 / jctb.1222. ИНИСТ:16622840.
- ^ К. К. Джиндал; Р. К. Шарма (2004). Последние тенденции в садоводстве в Гималаях. Indus Publishing. ISBN 978-81-7387-162-7.
... кора дерева и кожура фруктов обычно используются в аюрведе ... также используются для окрашивания ...
- ^ Полшеттивар, Вивек; Варма, Раджендер С. (2008). «Экологичный и быстрый синтез биоактивных гетероциклов с использованием микроволнового излучения». Чистая и прикладная химия. 80 (4): 777–90. Дои:10.1351 / pac200880040777. S2CID 11940026.
- ^ Hillis, W. E .; Урбах, Г. (1959). «Реакция полифенолов с формальдегидом». Журнал прикладной химии. 9 (12): 665–673. Дои:10.1002 / jctb.5010091207.
- ^ Фукуока, Токума; Уяма, Хироши; Кобаяси, Широ (2003). "Синтез полифенолов сверхвысокой молекулярной массы окислительным связыванием". Макромолекулы. 36 (22): 8213–5. Bibcode:2003MaMol..36.8213F. Дои:10.1021 / ma034803t.
- ^ Пицци, А .; Valenezuela, J .; Вестермейер, К. (1994). «Клеи на основе танина сосны и ореха пекана для наружных ДСП с низким выделением формальдегида, быстрое прессование». Holz Als Roh- und Werkstoff. 52 (5): 311–5. Дои:10.1007 / BF02621421. S2CID 36500389.
- ^ а б c d Айзпуруа-Олайзола, Ойер; Ормазабал, Маркел; Вальехо, Азиер; Оливарес, Майтан; Наварро, Патрисия; Etxebarria, Нестор; Усобиага, Аресац (2015). "Оптимизация сверхкритических жидкостей последовательной экстракции жирных кислот и полифенолов из Vitis Винифера Виноград Отходы ». Журнал пищевой науки. 80 (1): E101–7. Дои:10.1111/1750-3841.12715. PMID 25471637.
- ^ Стивен Г. Анчелл и Билл Труп (1998). Поваренная книга по проявлению пленки. ISBN 978-0240802770.
- ^ В. Латтанцио и др. (2006). «Роль фенольных соединений в механизмах устойчивости растений к грибковым патогенам и насекомым» (и ссылки в нем). Фитохимия: Достижения в исследованиях, 23–67. ISBN 81-308-0034-9.
- ^ Хубер, В; Эберл, L; Feucht, W; Польстер, Дж (2003). «Влияние полифенолов на формирование бактериальной биопленки и кворум-зондирование». Z. Naturforsch. C. 58 (11–12): 879–84. Дои:10.1515 / znc-2003-11-1224. PMID 14713169. S2CID 25764128.
- ^ Hättenschwiler, Стефан; Витаусек, Питер М (2000). «Роль полифенолов в круговороте питательных веществ наземных экосистем». Тенденции в экологии и эволюции. 15 (6): 238–243. Дои:10.1016 / S0169-5347 (00) 01861-9. PMID 10802549.
- ^ Харт, Джон Х .; Хиллис, В. Э. (1974). «Ингибирование древесных грибов с помощью стильбенов и других полифенолов в Eucalyptus sideroxylon». Фитопатология. 64 (7): 939–48. Дои:10.1094 / Фито-64-939.
- ^ Попа, В; Думитру, М; Вольф, я; Ангел, Н. (2008). «Лигнин и полифенолы как аллелохимические вещества». Промышленные культуры и продукты. 27 (2): 144–9. Дои:10.1016 / j.indcrop.2007.07.019.
- ^ Накаи, S (2000). «Выделяемые Myriophyllum spicatum аллелопатические полифенолы, подавляющие рост сине-зеленых водорослей Microcystis aeruginosa». Водные исследования. 34 (11): 3026–32. Дои:10.1016 / S0043-1354 (00) 00039-7.
- ^ Вигглсворт, В. Б. (1988). «Источник липидов и полифенолов для кутикулы насекомых: роль жирового тела, эноцитов и эноцитоидов». Ткани и клетки. 20 (6): 919–932. Дои:10.1016 / 0040-8166 (88) 90033-X. PMID 18620248.
- ^ Деннелл, Р. (1947). «Возникновение и значение фенольного затвердевания в новообразованной кутикуле Crustacea decapoda». Труды Королевского общества B: биологические науки. 134 (877): 485–503. Bibcode:1947РСПСБ.134..485Д. Дои:10.1098 / rspb.1947.0027. PMID 20265564.
- ^ Локк, М .; Кришнан, Н. (1971). «Распределение фенолоксидаз и полифенолов при образовании кутикулы». Ткани и клетки. 3 (1): 103–126. Дои:10.1016 / S0040-8166 (71) 80034-4. PMID 18631545.
- ^ Кришнан, Г. (сентябрь 1951 г.). «Фенольное дубление и пигментация кутикулы у Carcinus maenas». Ежеквартальный журнал микроскопической науки. 92 (19): 333–342.
- ^ Кришнан, Г. (сентябрь 1954 г.). "Эпикутикула паукообразного, Palamneus swammerdami". Ежеквартальный журнал микроскопической науки. 95 (31): 371–381.
- ^ Таннер, Грегори Дж; Франки, Кэти Т; Абрахамс, Шарон; Уотсон, Джон М; Ларкин, Филип Дж; Эштон, Энтони Р. (2003). «Биосинтез проантоцианидина в растениях». Журнал биологической химии. 278 (34): 31647–56. Дои:10.1074 / jbc.M302783200. PMID 12788945.
- ^ Краснов, М. Н .; Мерфи, Т. М. (2004). «Глюкозилирующая активность полифенолов в клеточных суспензиях винограда (Vitis vinifera)». Журнал сельскохозяйственной и пищевой химии. 52 (11): 3467–3472. Дои:10.1021 / jf035234r. PMID 15161217.
- ^ Малек, С. Р. А. (1961). «Полифенолы и их производные хинона в кутикуле пустынной саранчи Schistocerca gregaria (Forskål)». Сравнительная биохимия и физиология. 2: 35–77. Дои:10.1016 / 0010-406X (61) 90071-8.
- ^ Pandey, K. B .; Ризви, С. И. (2009). «Полифенолы растений как диетические антиоксиданты для здоровья и болезней человека». Окислительная медицина и клеточное долголетие. 2 (5): 270–278. Дои:10.4161 / oxim.2.5.9498. ЧВК 2835915. PMID 20716914.
- ^ а б d'Archivio, M; Filesi, C; Varì, R; Scazzocchio, B; Маселла, Р. (2010). «Биодоступность полифенолов: состояние и противоречия». Международный журнал молекулярных наук. 11 (4): 1321–1342. Дои:10.3390 / ijms11041321. ЧВК 2871118. PMID 20480022.
- ^ Л. Меннен; и другие. (Январь 2005 г.). «Риски и безопасность потребления полифенолов». Am J Clin Nutr. 81 (1): 3265–3295. Дои:10.1093 / ajcn / 81.1.326S. PMID 15640498.
- ^ Мильо С., Кьяваро Е., Висконти А., Фольяно В., Пеллегрини Н. (2008). «Влияние различных способов приготовления на пищевые и физико-химические характеристики выбранных овощей». J Agric Food Chem. 56 (1): 139–47. Дои:10.1021 / jf072304b. PMID 18069785.
- ^ Скальберт, А; Манах, С; Моран, С; Ремези, C; Хименес, L (2005). «Диетические полифенолы и профилактика заболеваний». Критические обзоры в области пищевой науки и питания. 45 (4): 287–306. Дои:10.1080/1040869059096. ISSN 1040-8398. PMID 16047496. S2CID 15475614.
- ^ «Руководство для промышленности: маркировка пищевых продуктов; заявления о содержании питательных веществ; определение« высокой эффективности »и определение« антиоксидант »для использования в заявках на содержание питательных веществ для пищевых добавок и обычных пищевых продуктов; руководство по соблюдению требований для малых предприятий». Центр безопасности пищевых продуктов и прикладного питания Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. Июль 2008 г.. Получено 2 октября 2017.
- ^ а б Гросс, Пол (1 марта 2009 г.). «Новые роли полифенолов. Отчет из трех частей о текущих нормах и состоянии науки». Мир нутрицевтиков.
- ^ Холливелл Б. (2007). «Диетические полифенолы: хорошо, плохо или безразлично для вашего здоровья?». Cardiovasc Res. 73 (2): 341–347. Дои:10.1016 / j.cardiores.2006.10.004. PMID 17141749.
- ^ "Научное заключение по обоснованию заявлений о пользе для здоровья, связанных с: флавоноидами и аскорбиновой кислотой во фруктовых соках, включая ягодные соки (ID 1186); флавоноидами из цитрусовых (ID 1471); флавоноидами из Citrus paradisi Macfad. (ID 3324, 3325); флавоноидами (Я БЫ". Журнал EFSA. 9 (4): 2082. Апрель 2011 г. Дои:10.2903 / j.efsa.2011.2082. Сложить резюме.
- ^ "Научное заключение по изменению разрешения на заявление о пользе для здоровья, связанное с флаванолами какао и поддержанием нормальной эндотелий-зависимой вазодилатации в соответствии со статьей 13 (5) Регламента (ЕС) № 1924/2006 по запросу в соответствии со статьей 19 Регламент (ЕС) № 1924/2006 ". Журнал EFSA. 12 (5). Май 2014. Дои:10.2903 / j.efsa.2014.3654.
- ^ «Научное заключение по обоснованию заявлений о пользе для здоровья, связанных с полифенолами оливок и защитой частиц ЛПНП от окислительного повреждения (ID 1333, 1638, 1639, 1696, 2865), поддержанием нормальной концентрации холестерина ЛПВП в крови (ID 1639), сохранить». Журнал EFSA. 9 (4): 2033. Апрель 2011. Дои:10.2903 / j.efsa.2011.2033.
- ^ Персонал, Сенсорное общество. Основные вкусы: терпкость В архиве 27 сентября 2013 г. Wayback Machine
- ^ Lesschaeve I, Благородный AC (2005). «Полифенолы: факторы, влияющие на их сенсорные свойства и их влияние на предпочтения в еде и напитках». Am J Clin Nutr. 81 (1): 330S – 335S. Дои:10.1093 / ajcn / 81.1.330S. PMID 15640499.
- ^ Hufnagel JC, Hofmann T (2008). «Оросенсорная идентификация терпких ощущений во рту и горьких соединений в красном вине». J Agric Food Chem. 56 (4): 1376–1386. Дои:10.1021 / jf073031n. PMID 18193832.
- ^ Owen, R.W .; Haubner, R .; Hull, W. E .; Erben, G .; Spiegelhalder, B .; Bartsch, H .; Хабер, Б. (2003). «Выделение и выяснение структуры основных индивидуальных полифенолов в волокнах рожкового дерева». Пищевая и химическая токсикология. 41 (12): 1727–1738. Дои:10.1016 / S0278-6915 (03) 00200-X. PMID 14563398.
- ^ Эскрибано-Байлон, Мария Тереза; Сантос-Буэльга, Селестино (2003). «Извлечение полифенолов из пищевых продуктов» (PDF). В Сантос-Буэльге, Селестино; Уильямсон, Гэри (ред.). Методы анализа полифенолов. Королевское химическое общество. С. 1–16. ISBN 978-0-85404-580-8.
- ^ Пан, X (2003). «Экстракция полифенолов чая и чайного кофеина из листьев зеленого чая с помощью микроволновой печи». Химическая инженерия и обработка. 42 (2): 129–33. Дои:10.1016 / S0255-2701 (02) 00037-5.
- ^ Пальма, М; Тейлор, Л. (1999). «Извлечение полифенольных соединений из косточек винограда с помощью двуокиси углерода, близкой к критической». Журнал хроматографии А. 849 (1): 117–24. Дои:10.1016 / S0021-9673 (99) 00569-5. PMID 10444839.
- ^ Alonsosalces, R; Корта, Э; Барранко, А; Berrueta, L; Галло, B; Висенте, Ф (2001). «Жидкая экстракция под давлением для определения полифенолов в яблоке». Журнал хроматографии А. 933 (1–2): 37–43. Дои:10.1016 / S0021-9673 (01) 01212-2. PMID 11758745.
- ^ Sineiro, J .; Domínguez, H .; Núñez, M. J .; Лема, Дж. М. (1996). «Экстракция полифенолов этанолом в иммерсионном экстракторе. Эффект пульсирующего потока». Журнал Американского общества химиков-нефтяников. 73 (9): 1121–5. Дои:10.1007 / BF02523372. S2CID 96009875.
- ^ Арранц, Сара; Саура-Каликсто, Фульхенсио; Шаха, Шика; Крун, Пол А. (2009). «Высокое содержание неэкстрагируемых полифенолов во фруктах свидетельствует о недооценке содержания полифенолов в растительной пище». Журнал сельскохозяйственной и пищевой химии. 57 (16): 7298–303. Дои:10.1021 / jf9016652. HDL:10261/82508. PMID 19637929.
- ^ Nawaz, H; Ши, Дж; Mittal, G; Какуда, Y (2006). «Извлечение полифенолов из виноградных косточек и концентрирование с помощью ультрафильтрации». Технология разделения и очистки. 48 (2): 176–81. Дои:10.1016 / j.seppur.2005.07.006.
- ^ Ferrara BT, Thompson EP (февраль 2019 г.). «Метод визуализации флуоресценции флавоноидных терапевтических средств. in vivo в модельном эукариоте Dictyostelium discoideum". Биотехнологии (Бумага). 66 (2): 65–71. Дои:10.2144 / btn-2018-0084. PMID 30744410.

- ^ Темпель, А. С. (1982). «Таниновые методы измерения». Журнал химической экологии. 8 (10): 1289–1298. Дои:10.1007 / BF00987762. PMID 24414735. S2CID 39848160.
- ^ Gani, M .; McGuinness, B.J .; Да Виес, А. П. (1998). «Моноклональные антитела против полифенолов чая: новый иммуноанализ для обнаружения полифенолов в биологических жидкостях». Пищевая и сельскохозяйственная иммунология. 10: 13–22. Дои:10.1080/09540109809354964.
- ^ Уокер, Ричард Б .; Эверетт, Джейс Д. (2009). «Сравнительная скорость реакции различных антиоксидантов с радикальным катионом ABTS». Журнал сельскохозяйственной и пищевой химии. 57 (4): 1156–61. Дои:10.1021 / jf8026765. PMID 19199590.
- ^ Рой, Молей К.; Коидэ, Мотоки; Rao, Theertham P; Окубо, Цутому; Огасавара, Ютака; Джунджа, Лех Р. (2010). «Сравнение анализа ORAC и DPPH для оценки антиоксидантной способности чайных настоев: взаимосвязь между общим содержанием полифенолов и индивидуальным содержанием катехинов». Международный журнал пищевых наук и питания. 61 (2): 109–24. Дои:10.3109/09637480903292601. PMID 20109129. S2CID 1929167.
- ^ Pulido, R .; Браво, L .; Саура-Каликсто, Ф. (2000). «Антиоксидантная активность диетических полифенолов, определенная с помощью модифицированного анализа восстановления железо / антиоксидантной силы». Журнал сельскохозяйственной и пищевой химии. 48 (8): 3396–3402. Дои:10.1021 / jf9913458. HDL:10261/112476. PMID 10956123.
- ^ Мейер, А. С .; Yi, O. S .; Пирсон, Д. А .; Waterhouse, A. L .; Франкель, Э. Н. (1997). «Ингибирование окисления липопротеинов низкой плотности человека в отношении состава фенольных антиоксидантов в винограде (Vitis vinifera)». Журнал сельскохозяйственной и пищевой химии. 45 (5): 1638–1643. Дои:10.1021 / jf960721a.
- ^ Мелло, L; Сотомайор, Мария дель Пилар Табоада; Кубота, Лауро Тацуо (2003). «Амперометрический биосенсор на основе HRP для определения полифенолов в экстракте овощей». Датчики и исполнительные механизмы B: химические. 96 (3): 636–45. Дои:10.1016 / j.snb.2003.07.008.
- ^ «Полифенол». Merriam-Webster, Inc., 2019 г.. Получено 23 февраля 2019.

