Тиол - Thiol

А тиол (/ˈθаɪɒл/)[1] или производное тиола есть ли сероорганическое соединение формы R-SH, где R представляет собой алкил или другие органические заместитель. Сама функциональная группа –SH обозначается как тиоловая группа или сульфгидрильная группаили сульфанильную группу. Тиолы - аналог серы спирты (то есть сера занимает место кислорода в гидроксил группа алкоголя), а слово чемодан тио- + алкоголь, причем первое слово происходит от Греческий θεῖον (теион), что означает «сера».[2]
Многие тиолы имеют резкий запах, напоминающий запах чеснока или тухлых яиц. Тиолы используются как одоранты чтобы помочь в обнаружении натуральный газ (который в чистом виде не имеет запаха), а «запах природного газа» обусловлен запахом тиола, используемого в качестве одоранта. Тиолы иногда называют меркаптаны.[3][4] Термин «меркаптан» /мərˈkæптæп/[5] был введен в 1832 г. Уильям Кристофер Цейс и получен из латинский mercurio captāns (улавливает ртуть)[6] поскольку тиолат группа (RS−) очень прочно связывается с Меркурий соединения.[7]
Структура и склеивание
Тиолы структуры R-SH называются алкантиолами или алкилтиолами, в которых алкил группа (R) прикреплена к сульфгидрил группа (SH).[8] Тиолы и спирты имеют аналогичную связь. Поскольку сера является более крупным элементом, чем кислород, длина связи C-S - обычно около 180 пикометров - примерно на 40 пикометров длиннее типичной связи C-O. Углы C-S-H приближаются к 90 °, тогда как угол для группы C-O-H более тупой. В твердом или жидком состоянии водородная связь между отдельными тиоловыми группами слабая, основная сила сцепления Ван-дер-Ваальсовы взаимодействия между сильно поляризуемыми центрами двухвалентной серы.
Связь S-H намного слабее, чем связь O-H, что отражено в их соответствующих энергия диссоциации связи (BDE). Для CH3S-H, БДЭ составляет 366 кДж / моль (87 ккал / моль), а для CH3O-H, БДЭ составляет 440 кДж / моль (110 ккал / моль).[9]
Из-за небольшой разницы в электроотрицательность серы и водорода, связь S-H умеренно полярный. Напротив, связи O-H в гидроксильных группах более полярны. Тиолы имеют более низкую дипольный момент относительно их соответствующих спиртов.
Номенклатура
Есть несколько способов назвать алкилтиолы:
- Суффикс -тиол добавляется к названию алкана. Этот метод почти идентичен называть алкоголь и используется ИЮПАК, например CH3SH будет метантиол.
- Слово меркаптан заменяет алкоголь в названии эквивалентного спиртового соединения. Пример: CH3SH будет метилмеркаптаном, так же как CH3ОН называется метиловым спиртом.
- Период, термин сульфгидрил- или меркапто- используется как префикс, например меркаптопурин.
Физические свойства
Запах
Многие тиолы обладают сильными запахи напоминая чеснок. Запах тиолов, особенно низкомолекулярных, часто бывает сильным и отталкивающим. Спрей скунсы состоит в основном из низкомолекулярных тиолов и производных.[10][11][12][13][14] Эти соединения обнаруживаются человеческим носом в концентрациях всего 10 частей на миллиард.[15] Человек потеть содержит (р)/(S) -3-метил-3-меркапто-1-ол (MSH), обнаруживаемый при концентрации 2 частей на миллиард и имеющий фруктовый, лук -подобный запах. (Метилтио) метантиол (MeSCH2SH; MTMT) представляет собой летучий тиол с сильным запахом, также обнаруживаемый на уровне частей на миллиард, обнаруженный у мужчин. мышь моча. Лоуренс К. Кац и коллеги показали, что MTMT функционировал как семиохимический, активируя определенные обонятельные сенсорные нейроны мыши, привлекая самок мышей.[16] Было показано, что медь требуется для специфического обонятельного рецептора мыши, MOR244-3, который очень чувствителен к MTMT, а также к различным другим тиолам и родственным соединениям.[17] Обонятельный рецептор человека, OR2T11, был идентифицирован, который в присутствии меди очень чувствителен к запахам газа (см. ниже) этантиол и т-бутилмеркаптан а также другие тиолы с низким молекулярным весом, включая аллилмеркаптан найдено в человеке чеснок дыхание, и сильно пахнущий циклический сульфид тиетан.[18]
Тиолы также отвечают за класс вина вина вызвано непреднамеренной реакцией между серой и дрожжи и "зловонный" запах пива, подвергшегося воздействию ультрафиолета.
Не все тиолы имеют неприятный запах. Например, фуран-2-илметантиол способствует аромату жареного кофе, в то время как грейпфрутовый меркаптан, а монотерпеноид тиол, отвечает за характерный запах грейпфрут. Эффект последнего соединения присутствует только при низких концентрациях. Чистый меркаптан имеет неприятный запах.
Натуральный газ дистрибьюторы были обязаны добавлять тиолы, первоначально этантиол, чтобы натуральный газ (который, естественно, не имеет запаха) после смертельного Взрыв в новой лондонской школе в Нью-Лондон, Техас, в 1937 году. До этого события многие газораспределители производили одорированный газ. Большинство используемых в настоящее время одорантов газа содержат смеси меркаптанов и сульфидов, с т-бутилмеркаптан в качестве основного компонента запаха в природном газе и этантиол в сжиженном углеводородном газе (СУГ, пропан).[19] В ситуациях, когда тиолы используются в коммерческой промышленности, например, в танкерах для сжиженного нефтяного газа и в системах обработки сыпучих материалов, для уничтожения запаха используется катализатор окисления. Катализатор окисления на основе меди нейтрализует летучие тиолы и превращает их в инертные продукты.
Точки кипения и растворимость
Тиолы мало связаны с водородная связь, как с молекулами воды, так и между собой. Следовательно, у них меньше точки кипения и меньше растворимый в воде и других полярные растворители чем у спиртов аналогичной молекулярной массы. По этой же причине тиолы и их соответствующие сульфидные функциональные группы изомеры имеют аналогичные характеристики растворимости и температуры кипения, в то время как то же самое нельзя сказать о спиртах и их соответствующих изомерных простых эфирах.
Склеивание
Связь S-H в тиолах слабая по сравнению со связью O-H в спиртах. Для CH3X − H, энтальпии связи равны 365.07±2,1 ккал / моль для X = S и 440.2±3,0 ккал / моль для X = O.[20] Отщепление атома водорода от тиола дает тиильный радикал с формулой RS•, где R = алкил или арил.
Характеристика
Летучие тиолы легко и почти безошибочно обнаруживаются по их характерному запаху. S-специфические анализаторы для газовые хроматографы полезны. Спектроскопические индикаторы - D2O-заменяемый SЧАС сигнал в 1ЧАС ЯМР спектр (33S есть ЯМР -активен, но сигналы для двухвалентной серы очень широки и мало полезны[21]). В νSH полоса появляется около 2400 см−1 в ИК-спектр.[3] в нитропруссидная реакция, свободные тиоловые группы реагируют с нитропруссид натрия и гидроксид аммония придать красный цвет.
Подготовка
В промышленности метантиол получают по реакции сероводород с участием метанол. Этот метод используется для промышленного синтеза метантиол:
- CH3ОН + Н2S → CH3SH + H2О
Такие реакции проводятся в присутствии кислотных катализаторов. Другой основной путь получения тиолов включает добавление сероводорода к алкенам. Такие реакции обычно проводят в присутствии кислоты. катализатор или УФ-свет. Также использовалось замещение галогенидов с использованием подходящего органического галогенида и сероводорода натрия.[22]
Другой метод включает алкилирование гидросульфид натрия.
- RX + NaSH → RSH + NaX (X = Cl, Br, I)
Этот метод используется для производства тиогликолевая кислота от хлоруксусная кислота.
Лабораторные методы
В общем, в типичном лабораторном масштабе прямая реакция галогеналкан с гидросульфидом натрия вэффективен за счет конкурирующего образования сульфидов. Вместо этого алкилгалогениды превращаются в тиолы через S-алкилирование тиомочевина. Этот многоэтапный процесс с одним горшком протекает через посредство изотиоурония соль, который гидролизуется на отдельной стадии:[23][24]
- CH3CH2Br + SC (NH2)2 → [CH3CH2SC (NH2)2] Br
- [CH3CH2SC (NH2)2] Br + NaOH → CH3CH2SH + OC (NH2)2 + NaBr
Путь тиомочевины хорошо работает с первичными галогенидами, особенно активированными. Вторичные и третичные тиолы получить труднее. Вторичные тиолы могут быть получены из кетона через соответствующие дитиокеталы.[25] Родственный двухэтапный процесс включает алкилирование тиосульфата с образованием тиосульфоната ("Бунте соль ") с последующим гидролизом. Метод иллюстрируется одним синтезом тиогликолевая кислота:
- ClCH2CO2H + Na2S2О3 → Na [O3S2CH2CO2H] + NaCl
- Na [O3S2CH2CO2H] + H2O → HSCH2CO2Н + NaHSO4
Литийорганические соединения и Реактивы Гриньяра реагируют с серой с образованием тиолатов, которые легко гидролизуются:[26]
- RLi + S → RSLi
- RSLi + HCl → RSH + LiCl
Фенолы можно превратить в тиофенолы путем перегруппировки их О-арилдиалкилтиокарбаматы.[27]
Тиолы получают восстановительным деалкилированием сульфидов, особенно производных бензила и тиоацеталей.[28]
Тиофенолы производятся S-арилирование или замена уходящей группы диазония на сульфгидрильный анион (SH−):[29][30]
- ArN2+ + SH− → АрШ + Н2
Реакции
Сродни химии спиртов, тиолы образуют сульфиды, тиоацетали, и тиоэфиры, которые аналогичны эфиры, ацетали, и сложные эфиры соответственно. Тиолы и спирты также сильно различаются по своей реакционной способности, тиолы окисляются легче, чем спирты. Тиолаты являются более сильными нуклеофилами, чем соответствующие алкоксиды.
S-Алкилирование
Тиолы, или более конкретно их сопряженные основания, легко алкилируются с образованием сульфидов:
- RSH + R′Br + B → RSR ′ + [HB] Br (B = база)
Кислотность
Тиолы легко депротонируются.[31] По сравнению со спиртами тиолы более кислые. Сопряженное основание тиола называется тиолат. Бутантиол имеет пKа 10,5 против 15 для бутанола. Тиофенол имеет пKа из 6 против 10 для фенол. Сильнокислый тиол - это пентафтортиофенол (C6F5SH) с пKа из 2,68. Таким образом, тиолаты могут быть получены из тиолов обработкой гидроксидами щелочных металлов.

Редокс
Тиолы, особенно в присутствии основания, легко окисленный реагентами, такими как бром и йод дать органический дисульфид (R − S − S − R).
- 2 R − SH + Br2 → R − S − S − R + 2 HBr
Окисление более мощными реагентами, такими как гипохлорит натрия или пероксид водорода может также дать сульфоновые кислоты (RSO3ЧАС).
- R − SH + 3 H2О2 → RSO3H + 3 H2О
Окисление также может осуществляться кислородом в присутствии катализаторов:[32]
- 2 R – SH +1⁄2 О2 → RS − SR + H2О
Тиолы участвуют в тиол-дисульфидном обмене:
- RS-SR + 2 R'SH → 2 RSH + R'S-SR '
Эта реакция важна по своей природе.
Комплексообразование с ионами металлов
С ионами металлов тиолаты действуют как лиганды с образованием тиолатные комплексы переходных металлов. Период, термин меркаптан происходит из латинский ртутные каптаны (улавливает ртуть)[6] потому что тиолатная группа так сильно связана с Меркурий соединения. Согласно с теория жесткой / мягкой кислоты / основания (HSAB), сера - относительно мягкий (поляризуемый) атом. Это объясняет тенденцию тиолов связываться с мягкими элементами и ионами, такими как ртуть, свинец или кадмий. Стабильность тиолатов металлов сопоставима со стабильностью соответствующих сульфидных минералов.
Тиоксантаты
Реакция взаимодействия тиолатов с сероуглерод давать тиоксантат (RSCS−
2).
Тиильные радикалы
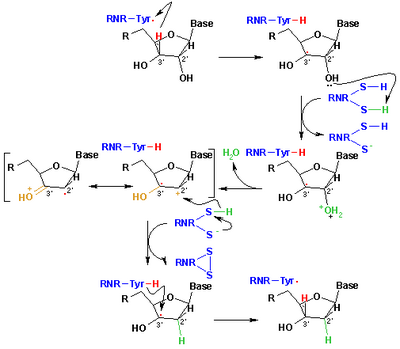
Свободные радикалы производные от меркаптанов, называемые тиильные радикалы, обычно используются для объяснения реакций в органическая химия и биохимия. У них есть формула RS• где R представляет собой органический заместитель, такой как алкил или арил.[4] Они возникают или могут быть сгенерированы рядом маршрутов, но основным методом является абстрагирование H-атома от тиолов. Другой метод предполагает гомолиз органических дисульфидов.[33] В биологии тиильные радикалы ответственны за образование дезоксирибонуклеиновых кислот, строительных блоков для ДНК. Это преобразование катализируется рибонуклеотидредуктаза (см. рисунок).[34] Промежуточные продукты тиила также образуются путем окисления глутатион, антиоксидант в биологии. Тиильные радикалы (сероцентрированные) могут превращаться в углеродные радикалы через водород обмен атомами равновесие. Формирование углерод -центрированные радикалы могут привести к повреждению белков из-за образования C -C связи или фрагментация основной цепи.[35]
Из-за слабости связи S-H тиолы могут функционировать как мусорщики из свободные радикалы.[36]
Биологическое значение
Цистеин и цистин
Как функциональная группа аминокислота цистеин, тиоловая группа играет очень важную роль в биологии. Когда тиоловые группы двух остатков цистеина (как в мономерах или составляющих единицах) сближаются друг с другом в процессе белок складной, реакция окисления может создать цистин блок с дисульфидная связь (-S-S-). Дисульфидные связи могут способствовать третичная структура если цистеины являются частью того же пептид цепочке или внести свой вклад в четвертичная структура мультиэлементных белков, образуя довольно прочные ковалентные связи между различными пептидными цепями. Физическое проявление цистеин-цистинового равновесия обеспечивается выпрямление волос технологии.[37]
Сульфгидрильные группы в активный сайт из фермент может сформировать нековалентные связи с ферментом субстрат а также способствуя ковалентной каталитическая активность в каталитические триады. Остатки цистеина активного центра являются функциональной единицей в цистеиновая протеаза каталитические триады. Остатки цистеина также могут реагировать с ионами тяжелых металлов (Zn2+, Компакт диск2+, Pb2+, Hg2+, Ag+) из-за высокого сродства мягкого сульфида к мягкому металлу (см. жесткие и мягкие кислоты и основания ). Это может деформировать и инактивировать белок и является одним из механизмов отравление тяжелыми металлами.
Препараты, содержащие тиоловые группы6-меркаптопурин (противоопухолевый) Каптоприл (антигипертензивный) D-пеницилламин (противоартритный) Ауротиолат натрия (противоартритный)[38]
Кофакторы
Много кофакторы (вспомогательные молекулы, не основанные на белках) содержат тиолы. Биосинтез и разложение жирных кислот и связанных с ними длинноцепочечных углеводородов осуществляется на каркасе, который закрепляет растущую цепь через тиоэфир, полученный из тиола. Коэнзим А. В биосинтез из метан, главный углеводород на Земле возникает в результате реакции, опосредованной коэнзим М, 2-меркаптоэтилсульфоновая кислота. Тиолаты, конъюгированные основания, полученные из тиолов, образуют прочные комплексы со многими ионами металлов, особенно с теми, которые классифицируются как мягкие. Стабильность тиолатов металлов сопоставима со стабильностью соответствующих сульфидных минералов.
В скунсах
Защитный спрей скунсы состоит в основном из низкомолекулярных тиолов и производных с неприятным запахом, защищающих скунса от хищников. Совы могут охотиться на скунсов, так как у них отсутствует обоняние.[39]
Примеры тиолов
- Метантиол - CH3SH [метилмеркаптан]
- Этантиол - С2ЧАС5SH [этилмеркаптан]
- 1-пропантиол - С3ЧАС7SH [п-пропилмеркаптан]
- 2-пропантиол - CH3CH (SH) CH3 [2C3 меркаптан]
- Аллил меркаптан - CH2= CHCH2SH [2-пропентиол]
- Бутантиол - С4ЧАС9SH [п-бутилмеркаптан]
- терт-Бутилмеркаптан - (CH3)3CSH [т-бутилмеркаптан]
- Пентантиолы - С5ЧАС11SH [пентилмеркаптан]
- Тиофенол - С6ЧАС5SH
- Димеркаптоянтарная кислота
- Тиоуксусная кислота
- Коэнзим А
- Глутатион
- Металлотионеин
- Цистеин
- 2-меркаптоэтанол
- Дитиотреитол /дитиоэритрит (ан эпимерный пара)
- 2-меркаптоиндол
- Грейпфрутовый меркаптан
- Фуран-2-илметантиол
- 3-меркаптопропан-1,2-диол
- 3-меркапто-1-пропансульфоновая кислота
- 1-гексадекантиол
- Пентахлорбензолтиол
Смотрите также
использованная литература
- ^ Справочник по словарю: тиол В архиве 2013-04-11 в Wayback Machine
- ^ θεῖον В архиве 2017-05-10 в Wayback Machine, Генри Джордж Лидделл, Роберт Скотт, Греко-английский лексикон
- ^ а б Патай, Саул, изд. (1974). Химия тиоловой группы. Лондон: Уайли. ISBN 978-0-471-66949-4.
- ^ а б Р. Дж. Кремлин (1996). Введение в химию сероорганических соединений. Чичестер: Джон Уайли и сыновья. ISBN 978-0-471-95512-2.
- ^ Справочник по словарю: меркаптан В архиве 2012-11-13 в Wayback Machine
- ^ а б Оксфордские американские словари (Mac OS X Leopard ).
- ^ Увидеть:
- Цейзе, Уильям Кристофер (1834). "Mercaptanet, med bemaerkninger over nogle andre nye producter из svovelvinsyresaltene, som og af den tunge vinolie, ved sulfureter" [Меркаптан, с замечаниями о некоторых других новых продуктах солей этилгидросульфата, а также тяжелого винного масла с помощью сероводорода]. Kongelige Danske Videnskabers Selskabs Skrifter. 4-я серия (на датском языке). 6: 1–70. На стр. 13 изобретено слово «меркаптан».
- Немецкий перевод: Цейзе, В. К. (1834). "Das Mercaptan, nebst Bermerkungen über einige neue Producte aus der Einwirkung der Sulfurete auf weinschwefelsaure Salze und auf das Weinöl" [Меркаптан вместе с комментариями к некоторым новым продуктам воздействия сероводорода на соли этилсульфата ((C2ЧАС5) HSO4) и тяжелое винное масло (смесь диэтилсульфата, диэтилсульфита и полимеризованного этилена)]. Annalen der Physik und Chemie. 2-я серия (на немецком языке). 31 (24): 369–431. С п. 378: "… Nenne ich den vom Quecksilber aufgenommenen Stoff Меркаптум (фон: Corpus mercurio captum) … " (… Я называю вещество [которое] поглощается ртутью «меркаптом» (от: тело (вещество) [которое] было поглощено ртутью)…)
- Немецкий перевод перепечатан на:Цейзе, В. К. (1834). "Das Mercaptan, nebst Bemerkungen über einige andere neue Erzeugnisse der Wirkung schwefelweinsaurer Salze, wie auch des schweren Weinöls auf Sulphurete". Journal für Praktische Chemie. 1 (1): 257–268, 345–356, 396–413, 457–475. Дои:10.1002 / prac.18340010154.
- Обобщено в: Цейзе, В. К. (1834). "Ueber das Mercaptan" [О меркаптане]. Annalen der Pharmacie. 11 (1): 1–10. Дои:10.1002 / jlac.18340110102. В архиве из оригинала от 20.03.2015.
- Цейзе, Уильям Кристофер (1834). "Sur le mercaptan; avec des monitoring sur d'autres производит результирующее действие сульфовинатов ainsi que de l'huile de vin, sur desulfures Metalliques" [О меркаптане; с наблюдениями за другими продуктами, возникающими в результате действия сульфовинатов [обычно этилгидросульфата], а также винного масла [смеси диэтилсульфата и полимеров этилена] на сульфиды металлов]. Annales de Chimie et de Physique. 56: 87–97. В архиве из оригинала от 20.03.2015. «Меркаптан» (этилтиол) был открыт в 1834 году датским профессором химии. Уильям Кристофер Цейс (1789–1847). Он назвал это «меркаптан», сокращение от «corpus mercurio captans» (вещества, улавливающего ртуть) [стр. 88], потому что он бурно реагировал с оксидом ртути (II) («дейтоксид ртути») [стр. 92].
- Статья в Annales de Chimie et de Physique (1834) была переведена из немецкой статьи: Цейзе, В. К. (1834). "Das Mercaptan, nebst Bemerkungen über einige neue Producte aus der Einwirkung der Sulfurete auf weinschwefelsaure Salze und auf das Weinöl". Annalen der Physik und Chemie. 107 (27): 369–431. Bibcode:1834AnP ... 107..369Z. Дои:10.1002 / andp.18341072402. В архиве из оригинала от 20.03.2015.
- ^ «Алканетиолы». Королевское химическое общество. Получено 4 сентября 2019.
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 0-8493-0487-3.
- ^ Андерсен К. К .; Бернштейн Д. Т. (1978). "Некоторые химические составляющие запаха полосатого скунса (Мефит, мефит)". Журнал химической экологии. 1 (4): 493–499. Дои:10.1007 / BF00988589. S2CID 9451251.
- ^ Андерсен К. К., Бернштейн Д. Т .; Бернштейн (1978). «1-Бутантиол и полосатый скунс». Журнал химического образования. 55 (3): 159–160. Bibcode:1978JChEd..55..159A. Дои:10.1021 / ed055p159.
- ^ Андерсен К. К .; Бернштейн Д. Т .; Карет Р. Л .; Романчик Л. Дж. Младший (1982). "Химические составляющие защитного секрета полосатого скунса (Мефит, мефит)". Тетраэдр. 38 (13): 1965–1970. Дои:10.1016 / 0040-4020 (82) 80046-X.
- ^ Wood W. F .; Соллерс Б.Г .; Драгу Г. А .; Драгу Дж. У. (2002). "Летучие компоненты в защитных аэрозолях скунса с капюшоном, Mephitis macroura". Журнал химической экологии. 28 (9): 1865–70. Дои:10.1023 / А: 1020573404341. PMID 12449512. S2CID 19217201.
- ^ Уильям Ф. Вуд. «Химия Skunk Spray». Кафедра химии, Государственный университет Гумбольдта. В архиве из оригинала 8 октября 2010 г.. Получено 2 января, 2008.
- ^ Олдрич, Т. (1896 г.). "Химическое исследование секрета анальных желез Мефитигный мефит (Скунс обыкновенный), с замечаниями о физиологических свойствах этого секрета ». J. Exp. Med. 1 (2): 323–340. Дои:10.1084 / jem.1.2.323. ЧВК 2117909. PMID 19866801.
- ^ Лин, Дайю; Чжан, Шаочжун; Блок, Эрик; Кац, Лоуренс К. (2005). «Кодирование социальных сигналов в основной обонятельной луковице мыши». Природа. 434 (7032): 470–477. Bibcode:2005Натура.434..470л. Дои:10.1038 / природа03414. PMID 15724148. S2CID 162036.
- ^ Дуань, Сюйфан; Блок, Эрик; Ли, Чжэнь; Коннелли, Тимоти; Чжан, Цзянь; Хуанг, Чжимин; Су, Сюбо; Пан, Йи; и другие. (2012). «Решающая роль меди в обнаружении запахов, координирующих металл». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 109 (9): 3492–3497. Bibcode:2012PNAS..109.3492D. Дои:10.1073 / pnas.1111297109. ЧВК 3295281. PMID 22328155.
- ^ «Медный ключ к нашей чувствительности к неприятному запаху тухлых яиц». chemistryworld.com. В архиве с оригинала 10 мая 2017 г.. Получено 3 мая 2018.
- ^ Робертс, Дж. С., изд. (1997). Энциклопедия химической технологии Кирка-Отмера. Вайнхайм: Wiley-VCH.[страница нужна ]
- ^ Luo, Y.-R .; Ченг, Ж.-П. (2017). «Связанные энергии диссоциации». В Дж. Р. Рамбле (ред.). Справочник по химии и физике. CRC Press.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Человек, Паскаль П. «Справочные материалы по ЯМР серы-33». www.pascal-man.com. В архиве с оригинала 23 августа 2017 г.. Получено 3 мая 2018.
- ^ Джон С. Робертс, "Тиолс", в Энциклопедия химической технологии Кирка-Отмера, 1997, Wiley-VCH, Weinheim. Дои:10.1002 / 0471238961.2008091518150205.a01
- ^ Speziale, A. J. (1963). «Этанедитиол». Органический синтез.; Коллективный объем, 4, п. 401.
- ^ Urquhart, G.G .; Гейтс, мл., J. W .; Коннор, Ральф (1941). «н-Додецил Меркаптан». Орг. Синтезатор. 21: 36. Дои:10.15227 / orgsyn.021.0036.
- ^ С. Р. Уилсон, Г. М. Георгиадис (1990). «Мекаптаны из тиокеталей: циклододецил меркаптан». Органический синтез.; Коллективный объем, 7, п. 124.
- ^ Э. Джонс и И. М. Муди (1990). «2-Тиофентиол». Органический синтез.; Коллективный объем, 6, п. 979.
- ^ Мелвин С. Ньюман и Фредерик В. Хетцель (1990). «Тиофенолы из фенолов: 2-нафталинтиол». Органический синтез.; Коллективный объем, 6, п. 824.
- ^ Эрнест Л. Элиэль, Джозеф Э. Линч, Фумитака Куме и Стивен В. Фрай (1993). «Хиральный 1,3-оксатиан из (+) - пулегона: гексагидро-4,4,7-триметил-4ЧАС-1,3-бензоксатиин ». Органический синтез.CS1 maint: несколько имен: список авторов (ссылка на сайт); Коллективный объем, 8, п. 302
- ^ Казем-Ростами, Масуд; Хазаеи, Ардешир; Мусави-Заре, Ахмад; Баят, Мохаммад; Saednia, Shahnaz (2012). «Новый синтез тиофенолов из родственных триазенов в мягких условиях». Synlett. 23 (13): 1893–1896. Дои:10.1055 / с-0032-1316557.
- ^ Лейкарт, Рудольф (1890). "Eine neue Methode zur Darstellung aromatischer Mercaptane" [Новый метод получения ароматических меркаптанов]. Journal für Praktische Chemie. 2-я серия (на немецком языке). 41: 179–224. Дои:10.1002 / prac.18900410114.
- ^ М. Э. Алонсо и Х. Арагона (1978). «Сульфидный синтез в получении несимметричных диалкилдисульфидов: втор-бутил-изопропилдисульфид». Орг. Синтезатор. 58: 147. Дои:10.15227 / orgsyn.058.0147.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Ахмадуллина, А.Г .; Кижаев, Б. В .; Нургалиева, Г.М .; Хрущева, И.К .; Шабаева, А. С .; и другие. (1993). «Гетерогенно-каталитическая демеркаптизация легкого углеводородного сырья».. Химия и технология топлив и масел. 29 (3): 108–109. Дои:10.1007 / bf00728009. S2CID 97292021. В архиве из оригинала от 15.08.2011.
- ^ Рой, Катрин-Мария (2005). «Тиолы и органические сульфиды». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a26_767.
- ^ Стуббе, Джоанна; Nocera, Daniel G .; Yee, Cyril S .; Чанг, Мишель С. Ю. (2003). «Радикальное инициирование в рибонуклеотидредуктазе класса I: перенос электронов с протонами на большие расстояния?». Chem. Rev. 103 (6): 2167–2202. Дои:10.1021 / cr020421u. PMID 12797828.
- ^ Хофштеттер, Дастин; Наузер, Томас; Коппенол, Виллем Х. (2010). «Равновесия водородного обмена в радикалах глутатиона: константы скорости». Chem. Res. Токсикол. 23 (10): 1596–1600. Дои:10.1021 / tx100185k. ЧВК 2956374. PMID 20882988.
- ^ Кох, Кэмерон Дж .; Парламент, Мэтью Б .; Браун, Дж. Мартин; Уртасун, Рауль С. (2010). «Химические модификаторы радиационного ответа». Учебник радиационной онкологии имени Лейбеля и Филлипса. Эльзевир. С. 55–68. Дои:10.1016 / b978-1-4160-5897-7.00004-4. ISBN 978-1-4160-5897-7.
Сульфгидрилы являются поглотителями свободных радикалов, защищая химические повреждения, вызванные ионизирующим излучением или алкилирующими агентами.
- ^ Рис, Урри; и другие. (2011). Кэмпбелл Биология (Девятое изд.). Нью-Йорк: Пирсон Бенджамин Каммингс. стр.65, 83.
- ^ Малле, Э (2007). «Миелопероксидаза: цель для разработки новых лекарств?». Британский журнал фармакологии. 152 (6): 838–854. Дои:10.1038 / sj.bjp.0707358. ЧВК 2078229. PMID 17592500.
- ^ "Понимание сов - Доверие сов". theowlstrust.org. В архиве из оригинала 5 февраля 2018 г.. Получено 3 мая 2018.
внешние ссылки
- Меркаптаны (или тиолы) в Периодическая таблица видео (Ноттингемский университет)
- Приложения, свойства и синтез ω-функционализированных н-алкантиолов и дисульфидов - строительных блоков самоорганизующихся монослоев Д. Витт, Р. Клайн, П. Барски, Б.А. Гжибовски в Северо-Западном университете.
- Меркаптан, Колумбийской электронной энциклопедией.
- Что такое Меркаптан?, компанией Columbia Gas из Пенсильвании и Мэриленда.
- Что такое химическое вещество с наихудшим запахом?, автор: About Chemistry.
