Рибонуклеотидредуктаза - Ribonucleotide reductase
| рибонуклеозид-дифосфатредуктаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 1.17.4.1 | ||||||||
| Количество CAS | 9047-64-7sy | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Рибонуклеотидредуктаза (RNR), также известный как рибонуклеотиддифосфатредуктаза (rNDP), является фермент что катализирует образование дезоксирибонуклеотиды из рибонуклеотиды.[1] Он катализирует это образование, удаляя 2'-гидроксильную группу рибозного кольца нуклеозиддифосфатов. Это восстановление производит дезоксирибонуклеотиды.[2] Дезоксирибонуклеотиды, в свою очередь, используются в синтезе ДНК. Реакция, катализируемая RNR, строго сохраняется у всех живых организмов.[3] Кроме того, RNR играет критическую роль в регулировании общей скорости синтеза ДНК, так что соотношение ДНК к клеточной массе поддерживается на постоянном уровне во время деление клеток и Ремонт ДНК.[4] Несколько необычной особенностью фермента RNR является то, что он катализирует реакцию, протекающую через свободный радикал механизм действия.[5][6] Подложки для РНР: ADP, ВВП, CDP и UDP. dTDP (диокситимидиндифосфат) синтезируется другим ферментом (тимидилаткиназа ) из дТМФ (дезокситимидинмонофосфат).
Структура
Рибонуклеотидредуктазы делятся на три класса. Ферменты RNR класса I состоят из большой альфа-субъединицы и малых бета-субъединиц, которые связываются, образуя активную гетеродимерный тетрамер. Уменьшая NDP до 2'-dNDP, фермент катализирует синтез de novo дезоксирибонуклеотидов (dNTP), которые являются предшественниками синтеза ДНК и необходимы для распространение клеток.[7] RNR класса II образуют 5'-дезоксиаденозильный радикал путем гомолитического расщепления связи C-Co в аденозилкобаламине. Кроме того, RNR класса III содержат стабильный глицильный радикал.[8]
Люди несут RNR класса I. Альфа-субъединица кодируется геном RRM1, тогда как существуют две изоформы бета-субъединицы, кодируемые генами RRM2 и RRM2B:
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Каждая альфа класса I мономер состоит из трех домены:[9]
- один преимущественно спиральный домен, содержащий 220 N-концевой остатки,
- вторая большая десятицепочечная α / β структура, содержащая 480 остатков,
- и третья небольшая пятицепочечная α / β структура, содержащая 70 остатков.
В Pfam, второй домен был интерпретирован как два отдельных домена:
- более короткий полностью альфа-N-концевой домен,
- и более длинный бочкообразный С-концевой домен.
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Субъединица бета класса I обычно содержит биметаллический центр и стабильную тирозил радикальный. У человека бета-субъединица зависит от кофактора ди-железа. В Кишечная палочка, тирозильный радикал находится в положении 122 (Y122), обеспечивая стабильный радикал для субъединиц RNR2 класса I.[13] В A. aegypti, этот тирозильный радикал находится в положении 184 (Y184).[14] Тирозильный радикал глубоко погружен внутри белка в гидрофобную среду, расположенную близко к центру железа, который используется для стабилизации тирозильного радикала. В структуре двух μ-оксо-связанных железов преобладают лиганды, которые служат сайтами связывания железа: четыре карбоксилата [аспартат (D146), глутамат (E177, E240 и E274)] и два гистидины (H180 и H277).[14] Ассоциация происходит между C-концом RNR2 и C-конец РНР1.[9] Ферментативная активность зависит от ассоциации субъединиц RNR1 и RNR2. Активный центр состоит из активных дитиольных групп из RNR1, а также из диферрического центра и тирозильного радикала из субъединицы RNR2.
Другие остатки RNR2, такие как аспартат (D273), триптофан (W48) и тирозин (Y356) дополнительно стабилизируют тирозильный радикал в активном центре, тем самым обеспечивая перенос электронов.[9] Эти остатки помогают переносить радикальный электрон от тирозина (Y122) RNR2 к цистеин (C439) из RNR1. Перенос электрона начинается с тирозина RNR2 (Y122) и продолжается в RNR2 на триптофан (W48), который отделен от тирозина RNR1 (Y731) на 2,5 нанометры. Перенос электронов от RNR2 к RNR1 происходит через тирозин (от Y356 до Y731) и продолжается через тирозин (Y730) к цистеину (C439) в активном сайте.[15] Сайт-ориентированные мутации первичной структуры RNR указывают на то, что все упомянутые выше остатки участвуют в переносе свободного радикала на большие расстояния к активному сайту.[9]
В A. aegypti комаров, RNR1 сохраняет большинство важных аминокислотных остатков, включая аспартат (D64) и валин (V292 или V284), которые необходимы для аллостерическая регуляция; пролин (P210 и P610), лейцин (L453 и L473), и метионин (M603) остатки, расположенные в гидрофобном активном сайте; остатки цистеина (C225, C436 и C451), которые участвуют в удалении атома водорода и переносе радикального электрона в активный центр; цистеин (C225 и C436), аспарагин (N434) и глутаматные (E441) остатки, которые связывают рибонуклеотидный субстрат; остатки тирозина (Y723 и Y743), которые определяют перенос радикалов; и остатки цистеина (C838 и C841), которые используются для регенерации дитиоловых групп в активном центре.[14]
Функция

Фермент рибонуклеотидредуктаза (RNR) катализирует синтез dNDP de novo.[16] Катализ рибонуклеозид-5’-дифосфатов (NDP) включает восстановление 2’-углерода рибозо-5-фосфат с образованием восстановленных 2’-дезоксипроизводным 2’-дезоксирибонуклеозид 5’-дифосфатов (дНДФ). Это уменьшение начинается с образования свободных радикалов. После однократного восстановления для RNR требуются электроны, пожертвованные дитиоловыми группами белка. тиоредоксин. Регенерация тиоредоксина происходит, когда никотинамидадениндинуклеотидфосфат (НАДФН ) обеспечивает два атома водорода, которые используются для уменьшения дисульфид группы тиоредоксина.
Три класса RNR имеют схожие механизмы восстановления NDP, но отличаются доменом, который генерирует свободный радикал, конкретный металл в металлопротеин структура и доноры электронов. Все занятия используют свободнорадикальную химию.[9] Редуктазы класса I используют центр железа с превращением двухвалентного железа в трехвалентное для образования свободного тирозильного радикала. Восстановление субстратов NDP происходит в аэробных условиях. Редуктазы класса I делятся на IA и IB из-за различий в регуляции. Редуктазы класса IA распространены в эукариоты, эубактерии, бактериофаги, и вирусы. Редуктазы класса IB обнаружены у эубактерий. Редуктазы класса IB могут также использовать радикал, образующийся при стабилизации двухъядерного марганец центр. Редуктазы класса II генерируют свободные радикалы 5’-дезоксиаденозильный радикал из кобаламин (кофермент B12) и имеют более простую структуру, чем редуктазы классов I и III. Восстановление NDP или рибонуклеотид-5’-трифосфатов (NTP) происходит при любом аэробный или анаэробные условия. Редуктазы II класса распространены в архебактерии, эубактерии и бактериофаги. Редуктазы класса III используют радикал глицина, образующийся с помощью S-аденозил метионин и центр железной серы. Снижение NTP ограничивается анаэробными условиями. Редуктазы класса III распространены в архебактериях, эубактериях и бактериофагах.[9][14] Организмы не ограничиваются одним классом ферментов. Например, Кишечная палочка имеют RNR как I, так и III класса.
Каталитический восстановительный механизм
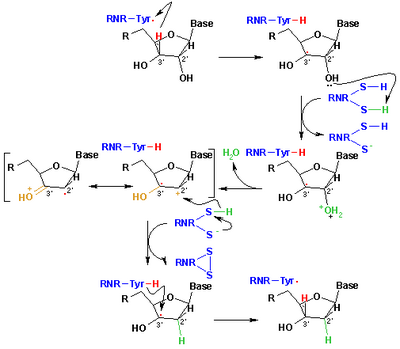
Механизм, который в настоящее время принят для восстановления рибонуклеотидов до дезоксирибонуклеотидов, изображен на следующей схеме. Первый шаг включает отрыв 3’-H субстрата 1 радикалом Cys439. Впоследствии реакция включает отщепление одной молекулы воды от углерода C-2 ’рибонуклеотида, катализируемое Cys225 и Glu441. На третьем этапе происходит перенос атома водорода от Cys225 к углероду C-2 ’2’-кетильного радикала 3 после предыдущего переноса протона от Cys462 к Cys225. В конце этой стадии получают анион-радикальный дисульфидный мостик и промежуточный кетон 4 с закрытой оболочкой. Этот промежуточный продукт был идентифицирован во время превращения нескольких 2’-замещенных аналогов субстрата, а также с природным субстратом.[17] взаимодействуя с мутантами фермента. Следующим этапом является окисление анионного дисульфидного мостика с сопутствующим восстановлением субстрата с образованием 5. Спиновая плотность смещается от атомов серы к атому C-3 'субстрата с одновременным переносом протона от Glu441 на углерод C. -3 '. Последний этап является обратным первому этапу и включает перенос водорода от Cys439 к C-3 ’, регенерирование исходного радикала и получение конечного продукта 6.
Теоретические модели некоторых этапов этих механизмов с использованием полной модели белка R1 можно найти в исследованиях, проведенных Cerqueira. и другие..[18][19]
Регулирование

RNR класса I включает субъединицы RNR1 и RNR2, которые могут связываться с образованием гетеродимерного тетрамера.[5] RNR1 содержит оба аллостерических сайта, опосредуя регуляцию субстратной специфичности и активности.[11] В зависимости от аллостерической конфигурации один из четырех рибонуклеотидов связывается с активным сайтом.
Регулирование RNR предназначено для поддержания сбалансированного количества dNTP. Связывание эффекторных молекул увеличивает или снижает активность РНР. Когда АТФ связывается с сайтом аллостерической активности, он активирует RNR. Напротив, когда dATP связывается с этим сайтом, он деактивирует RNR.[9] Помимо контроля активности, аллостерический механизм также регулирует специфичность субстрата и гарантирует, что фермент продуцирует равное количество каждого dNTP для синтеза ДНК.[9] Во всех классах связывание АТФ или дАТФ с аллостерическим сайтом индуцирует восстановление цитидин-5’-дифосфата (ЦДФ) и уридин-5’-дифосфата (УДФ); 2’-дезоксигуанозин-5’-трифосфат (dGTP) индуцирует восстановление аденозин-5’-дифосфата (ADP); и 2’-дезокситимидин-5’-трифосфат (dTTP) индуцирует уменьшение гуанозин-5’-дифосфата (GDP) (рис. 1).
Редуктазы класса IB не ингибируются dATP, потому что им не хватает примерно 50 N-концевых аминокислот, необходимых для сайта аллостерической активности.[20] Кроме того, важно, чтобы активность рибонуклеотидредуктазы находилась под транскрипционным и посттранскрипционным контролем, поскольку синтез ДНК без повреждений зависит от сбалансированного пула дезоксирибонуклеотидов.[21] Эукариотические клетки с редуктазами класса IA имеют механизм отрицательного контроля, чтобы выключить синтез dNTPs по мере их накопления. Этот механизм защищает клетку от токсических и мутагенных эффектов, которые могут возникнуть в результате перепроизводства dNTP, поскольку изменения в сбалансированных пулах dNTP приводят к повреждению ДНК и гибели клеток.[22][23] Хотя избыточная продукция dNTP или их несбалансированная поставка может привести к неправильному включению нуклеотидов в ДНК, поставка dNTPs может позволить репарацию ДНК. p53R2 представляет собой небольшую субъединицу рибонуклеотидредуктазы, которая может вызывать такую репарацию. Изменения в этом p53-индуцированном гомологе R2 могут вызывать истощение митохондриальной ДНК, и, следовательно, p53R2 служит основным фактором поставки dNTP.[24]
RNR может использовать морфеин модель аллостерическая регуляция.[25]
Ингибиторы RNR1 и RNR2
Обычно ингибиторы RNR класса I можно разделить на три основные группы: ингибиторы трансляции, которые блокируют синтез фермента; ингибиторы димеризации, которые предотвращают ассоциацию двух субъединиц RNR (R1 и R2); и каталитические ингибиторы, которые инактивируют субъединицу R1 и / или субъединицу R2.[18]
RNR класса I может подавляться пептиды аналогично C-конец РНР2. Эти пептиды могут конкурировать с RNR2 за связывание с RNR1, и в результате RNR1 не образует ферментативно активного комплекса с RNR2.[26][27] Хотя C-конец белков RNR2 отличается у разных видов, RNR2 может взаимодействовать с RNR1 у разных видов.[28] Когда C-конец RNR2 мыши был заменен на Кишечная палочка С-концевых (7 или 33) аминокислотных остатков RNR2, химерная субъединица RNR2 все еще связывается с субъединицами RNR1 мыши. Однако им не хватает ферментативной активности, вероятно, из-за удаления остатков, участвующих в переносе свободнорадикального электрона от RNR2 к субъединице RNR1.[27]
Небольшие пептиды могут специфически ингибировать связывание субъединиц RNR2 с RNR1, если они имеют значительное сходство с С-концом нормального RNR2.[29] Это ингибирование связывания RNR2 с RNR1 было успешно протестировано на RNR вируса простого герпеса (HSV). Когда в конкурентных анализах использовали олигомер из 7 аминокислот (GAVVNDL), укороченный от С-конца субъединицы RNR2, это препятствовало образованию ферментативно активного комплекса с RNR1 нормальным RNR2.[30] Другие малые пептидные ингибиторы, подобные С-концу RNR2, также успешно применялись для ингибирования ферментативной активности HSV RNR и, следовательно, репликации HSV.[31] В мышах модели стромальный кератит и неоваскуляризация роговицы (HSV глазное заболевание ), небольшой C-концевой аналог RNR2 BILD 1263, как сообщается, ингибирует RNR и эффективен в предотвращении этих заболеваний.[32] В некоторых случаях, хотя лечение небольшими аналогами С-конца не может остановить распространение болезни, они все же могут помочь в исцелении. в ацикловир -резистентный HSV (PAAr5), небольшой пептидный ингибитор BILD 1633, как сообщается, в 5-10 раз более эффективен, чем BILD 1263, против кожной инфекции PAAr5.[33] Комбинированная терапия (BILD 1633 и ацикловир) более эффективна для лечения местных повреждений у мышей. Эти данные предполагают, что небольшие пептидные ингибиторы, которые конкурируют с RNR2 за связывание с RNR1, полезны для предотвращения распространения HSV.
Галлий ингибирует RNR2, заменяя Fe3+ на активном сайте. Мальтолат галлия представляет собой пероральную биодоступную форму галлия, которая использует эту ингибирующую активность для лечения рака, инфекций и других заболеваний.[34]
Наркотики гидроксимочевина[35] и Мотексафин гадолиний мешают действию этого фермента.[36]
Рекомендации
- ^ Элледж С.Дж., Чжоу З., Аллен Дж.Б. (март 1992 г.). «Рибонуклеотидредуктаза: регуляция, регуляция, регуляция». Тенденции в биохимических науках. 17 (3): 119–23. Дои:10.1016/0968-0004(92)90249-9. PMID 1412696.
- ^ Сниден Дж. Л., Леб Л. А. (сентябрь 2004 г.). «Мутации в субъединице R2 рибонуклеотидредуктазы, которые придают устойчивость к гидроксимочевине». Журнал биологической химии. 279 (39): 40723–8. Дои:10.1074 / jbc.M402699200. PMID 15262976.
- ^ Торрентс Э., Алой П., Гиберт И., Родригес-Треллес Ф (август 2002 г.). «Рибонуклеотидредуктазы: дивергентная эволюция древнего фермента». Журнал молекулярной эволюции. 55 (2): 138–52. Дои:10.1007 / s00239-002-2311-7. PMID 12107591. S2CID 24603578.
- ^ Херрик Дж., Склави Б. (январь 2007 г.). «Рибонуклеотидредуктаза и регуляция репликации ДНК: старая история и древнее наследие». Молекулярная микробиология. 63 (1): 22–34. Дои:10.1111 / j.1365-2958.2006.05493.x. PMID 17229208. S2CID 9473163.
- ^ а б Эклунд Х., Эрикссон М., Улин Ю., Нордлунд П., Логан Д. (август 1997 г.). «Рибонуклеотидредуктаза - структурные исследования радикального фермента». Биологическая химия. 378 (8): 821–5. Дои:10.1515 / bchm.1997.378.8.815. PMID 9377477.
- ^ Стуббе Дж., Риггс-Геласко П. (ноябрь 1998 г.). «Использование свободных радикалов: образование и функция тирозильного радикала в рибонуклеотидредуктазе». Тенденции в биохимических науках. 23 (11): 438–43. Дои:10.1016 / S0968-0004 (98) 01296-1. PMID 9852763.
- ^ Fairman JW, Wijerathna SR, Ahmad MF, Xu H, Nakano R, Jha S, Prendergast J, Welin RM, Flodin S, Roos A, Nordlund P, Li Z, Walz T., Dealwis CG (март 2011 г.). «Структурная основа аллостерической регуляции рибонуклеотидредуктазы человека путем нуклеотид-индуцированной олигомеризации». Структурная и молекулярная биология природы. 18 (3): 316–22. Дои:10.1038 / nsmb.2007. ЧВК 3101628. PMID 21336276.
- ^ Ларссон К.М., Джордан А., Элиассон Р., Райхард П., Логан Д. Т., Нордлунд П. (ноябрь 2004 г.). «Структурный механизм регуляции специфичности аллостерического субстрата в рибонуклеотидредуктазе». Структурная и молекулярная биология природы. 11 (11): 1142–9. Дои:10.1038 / nsmb838. PMID 15475969. S2CID 1025702.
- ^ а б c d е ж грамм час Джордан А, Райхард П. (1998). «Рибонуклеотидредуктазы». Ежегодный обзор биохимии. 67 (1): 71–98. Дои:10.1146 / annurev.biochem.67.1.71. PMID 9759483.
- ^ а б PDB: 1PEU; Uppsten M, Färnegårdh M, Jordan A, Eliasson R, Eklund H, Uhlin U (июнь 2003 г.). «Структура большой субъединицы рибонуклеотидредуктазы Ib класса из Salmonella typhimurium и ее комплексов с аллостерическими эффекторами». Журнал молекулярной биологии. 330 (1): 87–97. Дои:10.1016 / S0022-2836 (03) 00538-2. PMID 12818204.
- ^ а б Улин У, Эклунд Х (август 1994 г.). «Структура белка рибонуклеотидредуктазы R1». Природа. 370 (6490): 533–9. Дои:10.1038 / 370533a0. PMID 8052308. S2CID 8940689.
- ^ Нордлунд П., Эклунд Х (июль 1993 г.). «Структура и функция белка R2 рибонуклеотидредуктазы Escherichia coli». Журнал молекулярной биологии. 232 (1): 123–64. Дои:10.1006 / jmbi.1993.1374. PMID 8331655.
- ^ Högbom M, Andersson ME, Nordlund P (март 2001 г.). «Кристаллические структуры окисленных биядерных центров марганца в Mn-замещенной рибонуклеотидредуктазе класса I из Escherichia coli: карбоксилатные сдвиги с последствиями для активации O2 и генерации радикалов». Журнал биологической неорганической химии. 6 (3): 315–23. Дои:10.1007 / s007750000205. PMID 11315567. S2CID 20748553.
- ^ а б c d Pham DQ, Blachuta BJ, Nichol H, Winzerling JJ (сентябрь 2002 г.). "Субъединицы рибонуклеотидредуктазы комара желтой лихорадки, Aedes aegypti: клонирование и экспрессия". Биохимия и молекулярная биология насекомых. 32 (9): 1037–44. Дои:10.1016 / S0965-1748 (02) 00041-3. PMID 12213240.
- ^ Чанг М.С., Йи С.С., Стуббе Дж., Носера Д.Г. (май 2004 г.). «Включение рибонуклеотидредуктазы за счет инициируемого светом образования аминокислотных радикалов». Труды Национальной академии наук Соединенных Штатов Америки. 101 (18): 6882–7. Дои:10.1073 / pnas.0401718101. ЧВК 406436. PMID 15123822.
- ^ Кокс М, Нельсон Д.Р. (2008). Принципы биохимии Ленингера. Сан-Франциско: В. Х. Фриман. ISBN 978-0-7167-7108-1.
- ^ Cerqueira NM, Фернандес PA, Eriksson LA, Ramos MJ (декабрь 2004 г.). «Активация рибонуклеотидов ферментом рибонуклеотидредуктазой: понимание роли фермента». Журнал вычислительной химии. 25 (16): 2031–7. Дои:10.1002 / jcc.20127. PMID 15481089. S2CID 19665974.
- ^ а б Серкейра Н.М., Перейра С., Фернандес ПА, Рамос М.Дж. (2005). «Обзор ингибиторов рибонуклеотидредуктазы: привлекательная мишень в противоопухолевой терапии». Современная лекарственная химия. 12 (11): 1283–94. Дои:10.2174/0929867054020981. PMID 15974997.
- ^ Cerqueira NM, Fernandes PA, Eriksson LA, Ramos MJ (март 2006 г.). «Дегидратация рибонуклеотидов, катализируемая рибонуклеотидредуктазой: роль фермента». Биофизический журнал. 90 (6): 2109–19. Дои:10.1529 / biophysj.104.054627. ЧВК 1386789. PMID 16361339.
- ^ Элиассон Р., Понтис Е., Джордан А., Райхард П. (октябрь 1996 г.). «Аллостерическая регуляция третьей рибонуклеотидредуктазы (фермент NrdEF) из энтеробактерий». Журнал биологической химии. 271 (43): 26582–7. Дои:10.1074 / jbc.271.43.26582. PMID 8900130.
- ^ Thelander L (июнь 2007 г.). «Рибонуклеотидредуктаза и синтез митохондриальной ДНК». Природа Генетика. 39 (6): 703–4. Дои:10.1038 / ng0607-703. PMID 17534360. S2CID 22565931.
- ^ Кунц Б.А. (1988). «Мутагенез и дисбаланс пула дезоксирибонуклеотидов». Мутационные исследования. 200 (1–2): 133–47. Дои:10.1016/0027-5107(88)90076-0. PMID 3292903.
- ^ Меут М (апрель 1989 г.). «Молекулярная основа мутаций, вызванных дисбалансом пула дезоксирибонуклеозидтрифосфата в клетках млекопитающих». Экспериментальные исследования клеток. 181 (2): 305–16. Дои:10.1016/0014-4827(89)90090-6. PMID 2647496.
- ^ Бурдон А., Минай Л., Серр В., Джейс Дж. П., Сарци Е., Обер С., Кретьен Д., де Лонле П., Паки-Флюклингер В., Аракава Н., Накамура И., Мюнних А., Рётиг А. (июнь 2007 г.). «Мутация RRM2B, кодирующей p53-контролируемую рибонуклеотидредуктазу (p53R2), вызывает серьезное истощение митохондриальной ДНК». Природа Генетика. 39 (6): 776–80. Дои:10,1038 / нг2040. PMID 17486094. S2CID 22103978.
- ^ Селвуд Т., Джаффе Е.К. (март 2012 г.). «Динамические диссоциирующие гомоолигомеры и контроль функции белка». Архивы биохимии и биофизики. 519 (2): 131–43. Дои:10.1016 / j.abb.2011.11.020. ЧВК 3298769. PMID 22182754.
- ^ Climent I, Sjöberg BM, Huang CY (май 1991 г.). «Карбоксиконцевые пептиды в качестве зондов для взаимодействия субъединиц рибонуклеотидредуктазы Escherichia coli: кинетический анализ исследований ингибирования». Биохимия. 30 (21): 5164–71. Дои:10.1021 / bi00235a008. PMID 2036382.
- ^ а б Хаманн С.С., Лентаинг С., Ли Л.С., Салем Дж. С., Ян Ф. Д., Куперман Б.С. (март 1998 г.). «Химерные ингибиторы малых субъединиц рибонуклеотидредуктазы млекопитающих: двойная функция С-конца R2?». Белковая инженерия. 11 (3): 219–24. Дои:10.1093 / белок / 11.3.219. PMID 9613846.
- ^ Cosentino G, Lavallée P, Rakhit S, Plante R, Gaudette Y, Lawetz C, Whitehead PW, Duceppe JS, Lépine-Frenette C, Dansereau N (январь 1991). «Специфическое ингибирование рибонуклеотидредуктаз пептидами, соответствующими С-концу их второй субъединицы». Биохимия и клеточная биология. 69 (1): 79–83. Дои:10.1139 / o91-011. PMID 2043345.
- ^ Куперман Б.С. (2003). «Олигопептидное ингибирование рибонуклеотидредуктаз класса I». Биополимеры. 71 (2): 117–31. Дои:10.1002 / bip.10397. PMID 12767114. S2CID 25196379.
- ^ Филатов Д., Ингемарсон Р., Грэслунд А., Теландер Л. (август 1992 г.). "Роль карбоксильного конца малой субъединицы рибонуклеотидредуктазы вируса простого герпеса во взаимодействии субъединиц и формировании структуры железо-тирозильный центр". Журнал биологической химии. 267 (22): 15816–22. PMID 1322407.
- ^ Коэн Э.А., Годро П, Бразо П, Ланжелье Y (1986).«Специфическое ингибирование рибонуклеотидредуктазы вируса герпеса нонапептидом, происходящим от карбоксильного конца субъединицы 2». Природа. 321 (6068): 441–3. Дои:10.1038 / 321441a0. PMID 3012360. S2CID 4238076.
- ^ Брандт Ч.Р., Спенсер Б., Имеш П., Гарно М., Дезиель Р. (май 1996 г.). «Оценка ингибитора пептидомиметической рибонуклеотидредуктазы на мышиной модели глазного заболевания вируса простого герпеса 1 типа». Противомикробные препараты и химиотерапия. 40 (5): 1078–84. Дои:10.1128 / aac.40.5.1078. ЧВК 163269. PMID 8723444.
- ^ Дуан Дж., Льюцци М., Пэрис В., Ламберт М., Лавц К., Мосс Н., Харамилло Дж., Готье Дж., Дезиель Р., Кордингли М.Г. (июль 1998 г.). «Противовирусная активность селективного ингибитора рибонуклеотидредуктазы против ацикловиррезистентного вируса простого герпеса типа 1 in vivo». Противомикробные препараты и химиотерапия. 42 (7): 1629–35. Дои:10.1128 / aac.42.7.1629. ЧВК 105657. PMID 9660995.
- ^ Бернштейн Л.Р. (декабрь 1998 г.). «Механизмы терапевтического действия галлия» (PDF). Фармакологические обзоры. 50 (4): 665–82. PMID 9860806.
- ^ «Информация по EC 1.17.4.1 - рибонуклеозиддифосфатредуктаза». Бренда. Получено 25 июля 2015.
- ^ Хашеми С.И., Унгерштедт Дж.С., Захеди Аввал Ф., Холмгрен А. (апрель 2006 г.). «Мотексафин гадолиний, опухоль-селективный препарат, нацеленный на тиоредоксинредуктазу и рибонуклеотидредуктазу». Журнал биологической химии. 281 (16): 10691–7. Дои:10.1074 / jbc.M511373200. PMID 16481328.
внешняя ссылка
- Рибонуклеотид + редуктазы в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- База данных рибонуклеотидредуктазы (RNRdb)