Мышьяк - Arsenic
 | |||||||||||||||||||||||||||||
| Мышьяк | |||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение |
| ||||||||||||||||||||||||||||
| Аллотропы | серый (чаще всего), желтый, черный | ||||||||||||||||||||||||||||
| Внешность | металлический серый | ||||||||||||||||||||||||||||
| Стандартный атомный вес Аr, std(В качестве) | 74.921595(6)[1] | ||||||||||||||||||||||||||||
| Мышьяк в периодическая таблица | |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
| Атомный номер (Z) | 33 | ||||||||||||||||||||||||||||
| Группа | группа 15 (пниктогены) | ||||||||||||||||||||||||||||
| Период | период 4 | ||||||||||||||||||||||||||||
| Блокировать | p-блок | ||||||||||||||||||||||||||||
| Категория элемента | Металлоид | ||||||||||||||||||||||||||||
| Электронная конфигурация | [Ar ] 3d10 4 с2 4p3 | ||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 5 | ||||||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||||||
| Фаза вSTP | твердый | ||||||||||||||||||||||||||||
| Точка сублимации | 887 К (615 ° С, 1137 ° F) | ||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | 5,727 г / см3 | ||||||||||||||||||||||||||||
| в жидком состоянии (приm.p.) | 5,22 г / см3 | ||||||||||||||||||||||||||||
| Тройная точка | 1090 К, 3628 кПа[2] | ||||||||||||||||||||||||||||
| Критическая точка | 1673 К,? МПа | ||||||||||||||||||||||||||||
| Теплота плавления | серый: 24,44кДж / моль | ||||||||||||||||||||||||||||
| Теплота испарения | 34,76 кДж / моль (т) | ||||||||||||||||||||||||||||
| Молярная теплоемкость | 24,64 Дж / (моль · К) | ||||||||||||||||||||||||||||
Давление газа
| |||||||||||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||||||||||
| Состояния окисления | −3, −2, −1, 0,[3] +1,[4] +2, +3, +4, +5 (мягко кислый окись) | ||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,18 | ||||||||||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||||||||||
| Радиус атома | эмпирические: 119вечера | ||||||||||||||||||||||||||||
| Ковалентный радиус | 119 ± 16 часов | ||||||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 185 вечера | ||||||||||||||||||||||||||||
| Другие свойства | |||||||||||||||||||||||||||||
| Естественное явление | изначальный | ||||||||||||||||||||||||||||
| Кристальная структура | ромбоэдрический | ||||||||||||||||||||||||||||
| Тепловое расширение | 5,6 мкм / (м · К)[5] (вr.t.) | ||||||||||||||||||||||||||||
| Теплопроводность | 50,2 Вт / (м · К) | ||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 333 нОм · м (при 20 ° C) | ||||||||||||||||||||||||||||
| Магнитный заказ | диамагнитный[6] | ||||||||||||||||||||||||||||
| Магнитная восприимчивость | −5.5·10−6 см3/ моль[7] | ||||||||||||||||||||||||||||
| Модуль для младших | 8 ГПа | ||||||||||||||||||||||||||||
| Объемный модуль | 22 ГПа | ||||||||||||||||||||||||||||
| Твердость по Моосу | 3.5 | ||||||||||||||||||||||||||||
| Твердость по Бринеллю | 1440 МПа | ||||||||||||||||||||||||||||
| Количество CAS | 7440-38-2 | ||||||||||||||||||||||||||||
| История | |||||||||||||||||||||||||||||
| Открытие | Арабские алхимики (до 815 г.) | ||||||||||||||||||||||||||||
| Главный изотопы мышьяка | |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
Мышьяк это химический элемент с символ В качестве и атомный номер 33. Мышьяк содержится во многих минералах, обычно в сочетании с сера и металлы, но и как чистый элементаль кристалл. Мышьяк - это металлоид. Он имеет различные аллотропы, но только серая форма, имеющая металлический вид, важна для промышленности.
В основном мышьяк используется в сплавах вести (например, в автомобильные аккумуляторы и боеприпасы ). Мышьяк - распространенный n-тип присадка в полупроводник электронные устройства. Он также входит в состав III-V составной полупроводник арсенид галлия. Мышьяк и его соединения, особенно триоксид, используются в производстве пестициды, изделия из обработанной древесины, гербициды, и инсектициды. Эти применения сокращаются в связи с растущим признанием токсичности мышьяка и его соединений.[8]
Несколько видов бактерий могут использовать соединения мышьяка в качестве респираторных метаболиты. Следовые количества мышьяка необходимы диетический элемент у крыс, хомяков, коз, кур и, предположительно, у других видов. Роль в метаболизме человека неизвестна.[9][10][11] Тем не мение, отравление мышьяком возникает в многоклеточной жизни, если количество превышает необходимое. Загрязнение подземных вод мышьяком это проблема, которая затрагивает миллионы людей во всем мире.
В Соединенные Штаты ' Агентство по охране окружающей среды заявляет, что все формы мышьяка представляют серьезную опасность для здоровья человека.[12] Соединенные Штаты' Агентство регистрации токсичных веществ и заболеваний поставил мышьяк на первое место в Приоритетном списке 2001 г. Опасно Вещества на Суперфонд места.[13] Мышьяк относится к группе А канцероген.[12]
Характеристики
Физические характеристики
Три самых распространенных мышьяка аллотропы представляют собой серый, желтый и черный мышьяк, причем серый является наиболее распространенным.[14] Серый мышьяк (α-As, космическая группа р3m No. 166) имеет двухслойную структуру, состоящую из множества сцепленных, взъерошенных шестичленных колец. Из-за слабой связи между слоями серый мышьяк хрупкий и имеет относительно низкую Твердость по Моосу из 3.5. Ближайшие и следующие ближайшие соседи образуют искаженный октаэдрический комплекс, при этом три атома в одном двойном слое находятся немного ближе, чем три атома в следующем.[15] Эта относительно плотная упаковка обеспечивает высокую плотность 5,73 г / см.3.[16] Серый мышьяк - это полуметалл, но становится полупроводник с запрещенная зона 1,2–1,4 эВ в случае аморфизации.[17] Серый мышьяк также является наиболее стабильной формой. Желтый мышьяк мягкий и воскообразный, чем-то похож на тетрафосфор (п
4).[18] У обоих по четыре атома, расположенных в виде четырехгранный структура, в которой каждый атом связан с каждым из трех других атомов одинарной связью. Этот нестабильный аллотроп, будучи молекулярным, является наиболее летучим, наименее плотным и наиболее токсичным. Твердый желтый мышьяк получают путем быстрого охлаждения паров мышьяка. В качестве
4. На свету он быстро превращается в серый мышьяк. Желтая форма имеет плотность 1,97 г / см.3.[16] Черный мышьяк по структуре похож на черный фосфор.[16]Черный мышьяк также может образовываться при охлаждении пара до температуры около 100–220 ° C и при кристаллизации аморфного мышьяка в присутствии паров ртути.[19] Стекловидный и хрупкий. Это также плохой проводник.[20]
Изотопы
Мышьяк встречается в природе как моноизотопный элемент, состоящий из одной конюшни изотоп, 75В качестве.[21] По состоянию на 2003 год не менее 33 радиоизотопы также были синтезированы в диапазоне атомная масса от 60 до 92. Самым стабильным из них является 73Как и в случае с период полураспада 80,30 дней. Все остальные изотопы имеют период полураспада менее одного дня, за исключением 71В качестве (т1/2= 65,30 часов), 72В качестве (т1/2= 26,0 часов), 74В качестве (т1/2= 17,77 дней), 76В качестве (т1/2= 1,0942 дня), и 77В качестве (т1/2= 38,83 часа). Изотопы легче конюшни 75Как склонны распадаться β+ разлагаться, а те, что тяжелее, имеют тенденцию распадаться β− разлагаться, за некоторыми исключениями.
Не менее 10 ядерные изомеры были описаны, с атомной массой от 66 до 84. Наиболее стабильным изомером мышьяка является 68мКак и с периодом полураспада 111 секунд.[21]
Химия
Мышьяк имеет такую же электроотрицательность и энергию ионизации, что и его более легкий родственный фосфор, и, соответственно, легко образует ковалентные молекулы с большинством неметаллов. Хотя мышьяк стабилен в сухом воздухе, под воздействием влажности он образует золотисто-бронзовый налет, который в конечном итоге становится черным поверхностным слоем.[22] При нагревании на воздухе мышьяк окисляет к триоксид мышьяка; пары этой реакции имеют запах, напоминающий чеснок. Этот запах можно обнаружить при ударе арсенид минералы, такие как арсенопирит с молотком.[2] Он горит в кислороде с образованием триоксида мышьяка и пятиокись мышьяка, которые имеют ту же структуру, что и более известные соединения фосфора, и фтор, чтобы дать пентафторид мышьяка.[22] Мышьяк (и некоторые соединения мышьяка) возвышенный при нагревании при атмосферном давлении превращается непосредственно в газообразную форму без промежуточного жидкого состояния при 887 K (614 ° C).[2] В тройная точка составляет 3,63 МПа и 1090 К (820 ° C).[16][2] Мышьяк делает мышьяковая кислота с концентрированным азотная кислота, мышьяковистая кислота с разбавленной азотной кислотой и триоксид мышьяка с концентрированным серная кислота; однако он не реагирует с водой, щелочами или неокисляющими кислотами.[23] Мышьяк реагирует с металлами с образованием арсениды, хотя это не ионные соединения, содержащие As3− ион, поскольку образование такого аниона было бы сильно эндотермическим, и даже арсениды группы 1 обладают свойствами интерметаллид соединения.[22] Нравиться германий, селен, и бром, который как мышьяк преуспеть в серии 3D переходов, мышьяк гораздо менее стабилен в групповой степени окисления +5, чем его вертикальные соседи фосфор и сурьма, и, следовательно, пятиокись мышьяка и мышьяковая кислота являются сильными окислителями.[22]
Соединения
Соединения мышьяка в некоторых отношениях напоминают соединения мышьяка. фосфор который занимает то же группа (столбец) периодическая таблица. Самый распространенный состояния окисления для мышьяка: −3 в арсениды, которые представляют собой сплавоподобные интерметаллиды, +3 в арсениты, и +5 в арсенаты и большинство органических соединений мышьяка. Мышьяк также легко связывается с самим собой, как видно из квадрата As3−
4 ионы в минерале скуттерудит.[24] В +3 степень окисления, мышьяк обычно пирамидальный из-за влияния одинокая пара из электроны.[14]
Неорганические соединения
Одним из простейших соединений мышьяка является тригидрид, высокотоксичный, легковоспламеняющийся, пирофорный арсин (Пепел3). Это соединение обычно считается стабильным, поскольку при комнатной температуре оно медленно разлагается. При температуре 250–300 ° C происходит быстрое разложение до мышьяка и водорода.[25] Несколько факторов, например влажность, наличие света и уверенности катализаторы (а именно алюминий ) ускоряют разложение.[26] Он легко окисляется на воздухе с образованием триоксида мышьяка и воды, и аналогичные реакции происходят с сера и селен вместо кислород.[25]
Мышьяк бесцветный, без запаха, кристаллический оксиды В качестве2О3 ("белый мышьяк ") и В качестве2О5 которые гигроскопичный и легко растворяется в воде с образованием кислых растворов. Мышьяковая (V) кислота слабая кислота, и соли называются арсенаты,[27] самый распространенный загрязнение подземных вод мышьяком, и проблема, которая затрагивает многих людей. Синтетические арсенаты включают Зеленый Шееле (арсенат меди, кислый арсенат меди), арсенат кальция, и арсенат свинца. Эти три были использованы как сельскохозяйственный инсектициды и яды.
Этапы протонирования между арсенатом и мышьяковой кислотой аналогичны этапам между фосфат и фосфорная кислота. В отличие от фосфористая кислота, мышьяковистая кислота является действительно трехосновным, с формулой As (OH)3.[27]
Известно большое количество сернистых соединений мышьяка. Орпимент (В качестве2S3 ) и реальгар (В качестве4S4 ) довольно многочисленны и ранее использовались в качестве красящих пигментов. В As4S10, мышьяк имеет формальную степень окисления +2 в As4S4 который содержит связи As-As, так что общая ковалентность As по-прежнему равна 3.[28] И орпимент, и реальгар, а также As4S3, имеют аналоги селена; аналогичный As2Te3 известен как минерал калгурлиит,[29] и анион As2Te− известен как лиганд в кобальт комплексы.[30]
Все тригалогениды мышьяка (III) хорошо известны, за исключением неизвестного астатида. Пентафторид мышьяка (AsF5) является единственным важным пентагалогенидом, отражающим более низкую стабильность степени окисления +5; даже в этом случае это очень сильный фторирующий и окисляющий агент. (The пентахлорид стабилен только ниже -50 ° C, при этой температуре он разлагается до трихлорида с выделением газообразного хлора.[16])
Сплавы
Мышьяк используется в качестве элемента группы 5 в Полупроводники III-V арсенид галлия, арсенид индия, и арсенид алюминия.[31] Счетчик валентных электронов GaAs такой же, как у пары атомов Si, но ленточная структура полностью отличается, что приводит к отличным объемным свойствам.[32] Другие сплавы мышьяка включают полупроводник II-V. арсенид кадмия.[33]
Мышьякоорганические соединения
Известно большое разнообразие органических соединений мышьяка. Некоторые из них были разработаны как боевые отравляющие вещества во время Первой мировой войны, в том числе везиканты Такие как люизит и рвотные агенты, такие как адамсит.[34][35][36] Какодиловая кислота, представляющий исторический и практический интерес, вытекает из метилирование триоксида мышьяка, реакция, не имеющая аналогов в химии фосфора. В самом деле, какодил был первым известным металлоорганическим соединением (хотя мышьяк не является настоящим металлом) и был назван от греческого κακωδἰα «вонять» своим неприятным запахом; это очень ядовито.[37]
Возникновение и производство

Мышьяк составляет около 1,5промилле (0,00015%) от земной коры, и является 53-м по численности элементом. Типичные фоновые концентрации мышьяка не превышают 3 нг / м3.3 в атмосфере; 100 мг / кг в почве; и 10 мкг / л в пресной воде.
Минералы с формулой MAsS и MAs2 (M = Fe, Ni, Co ) являются основными коммерческими источниками мышьяка вместе с Realgar (минерал сульфид мышьяка) и самородный (элементарный) мышьяк. Иллюстративный минерал арсенопирит (Fe В качествеS ), что структурно связано с железный пирит. Известны многие второстепенные минералы, содержащие As. Мышьяк также встречается в окружающей среде в различных органических формах.[38]

В 2014 году Китай был крупнейшим производителем белого мышьяка с почти 70% мировой долей, за ним следовал Марокко, Россия, и Бельгия, согласно Британская геологическая служба и Геологическая служба США.[40] Большинство предприятий по переработке мышьяка в США и Европе закрылись из-за экологических проблем. Мышьяк содержится в пыли плавильных заводов медь, золото, и вести в плавильных печах и извлекается в основном из пыли от рафинирования меди.[41]
На жарка арсенопирит в воздухе, мышьяк возгоняется в виде оксида мышьяка (III), оставляя оксиды железа,[38] при обжиге без воздуха образуется серый мышьяк. Дальнейшая очистка от серы и других халькогенов достигается за счет сублимация в вакууме, в атмосфере водорода или перегонкой из расплавленной свинцово-мышьяковой смеси.[42]
| Классифицировать | Страна | 2014 В качестве2О3 Производство[40] |
|---|---|---|
| 1 | 25000 т | |
| 2 | 8 800 т | |
| 3 | 1,500 т | |
| 4 | 1000 т | |
| 5 | 52 т | |
| 6 | 45 т | |
| — | Мировой итог (округлено) | 36 400 т |
История


Слово мышьяк берет свое начало в Сирийский слово ܠܐ ܙܐܦܢܝܐ (аль) зарника,[43][нужен лучший источник ] с арабского al-zarnīḵ الزرنيخ 'The орпимент ’На основе Персидский зар "золото" от слова زرنيخ зарних, что означает «желтый» (буквально «золотой») и, следовательно, «(желтый) orpiment». Он был принят в Греческий в качестве арсеникон (ἀρσενικόν), форма, которая народная этимология, являясь средней формой греческого слова арсеникос (ἀρσενικός), что означает «мужской», «мужественный». Греческое слово было принято на латыни как мышьяк, который по-французски стал мышьяк, от которого происходит английское слово «мышьяк».[43][нужен лучший источник ] Сульфиды мышьяка (арипимент, Realgar ) и оксиды были известны и использовались с древних времен.[44] Зосим (около 300 г. н.э.) описывает обжарку Sandarach (реальгар), чтобы получить облако мышьяка (триоксид мышьяка ), которую он затем уменьшает серому мышьяку.[45] Поскольку симптомы отравление мышьяком не очень специфичны, он часто использовался для убийство до появления Марш тест, чувствительный химический тест на его присутствие. (Другой менее чувствительный, но более общий тест - это Тест Рейнша...) Из-за его использования правящим классом для убийства друг друга, а также его силы и осторожности, мышьяк был назван «ядом королей» и «королем ядов».[46]

Вовремя Бронзовый век, мышьяк часто входил в состав бронза, что сделало сплав более твердым (т.н. "мышьяковая бронза ").[47][48]Выделение мышьяка было описано Джабир ибн Хайян до 815 г. н.э.[49] Альбертус Магнус (Альберт Великий, 1193–1280) позже изолировал элемент от соединения в 1250 году, нагревая мыло вместе с трисульфид мышьяка.[50] В 1649 г. Иоганн Шредер опубликовали два способа приготовления мышьяка.[51] Кристаллы элементарного (самородного) мышьяка встречаются в природе, хотя и редко.
Дымящаяся жидкость кадета (нечистый какодил ), часто называемый первым синтетическим металлоорганическое соединение, был синтезирован в 1760 г. Луи Клод Кадет де Гассикур по реакции ацетат калия с триоксид мышьяка.[52]

в Викторианская эпоха, «мышьяк» («белый мышьяк» или триоксид мышьяка) был смешан с уксус и мел и съедены женщинами, чтобы улучшить цвет лица их лиц, делая их кожу бледнее, показывая, что они не работали в поле.[53] Мышьяк также втирали в лицо и руки женщин, чтобы «улучшить их цвет лица». Случайное использование мышьяка при фальсификации пищевых продуктов привело к Брэдфорд сладкое отравление в 1858 году, в результате чего погибло около 20 человек.[54] В производстве обоев также стали использовать красители из мышьяка, которые, как считалось, увеличивают яркость пигмента.[55]
С момента их открытия широко использовались два пигмента мышьяка: Пэрис Грин и Зеленый Шееле. После того, как токсичность мышьяка стала широко известной, эти химические вещества стали реже использоваться в качестве пигментов и чаще в качестве инсектицидов. В 1860-х годах широко использовался мышьяк, побочный продукт производства красителей. Это была твердая смесь триоксида мышьяка, анилина, извести и закиси железа, нерастворимая в воде и очень токсичная при вдыхании или проглатывании.[56] Но позже он был заменен на другой краситель на основе мышьяка Paris Green.[57] С более глубоким пониманием механизма токсикологии, начиная с 1890-х годов, использовались два других соединения.[58] Арсенит извести и арсенат свинца широко использовались в качестве инсектицидов до открытия ДДТ в 1942 г.[59][60][61]
Приложения
Сельскохозяйственная
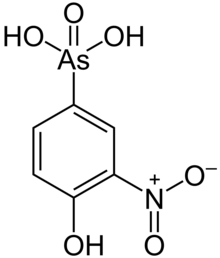
Токсичность мышьяка для насекомые, бактерии, и грибы привело к его использованию в качестве консерванта для древесины.[62] В 1930-х годах процесс обработки древесины хромированный арсенат меди (также известный как CCA или Таналит ) был изобретен, и на протяжении десятилетий эта обработка была самым широким промышленным применением мышьяка. Повышенное признание токсичности мышьяка привело к запрету ХАК в потребительских товарах в 2004 г., инициированному Евросоюз и США.[63][64] Однако CCA по-прежнему активно используется в других странах (например, на каучуковых плантациях Малайзии).[8]
Мышьяк также использовался в различных сельскохозяйственных инсектицидах и ядах. Например, арсенат свинца был обычным инсектицидом на фруктовые деревья,[65] но контакт с соединением иногда приводил к повреждение мозга среди работающих на опрыскивателях. Во второй половине 20 века метиларсенат натрия (MSMA) и динатрий метил арсенат (DSMA) - менее токсичные органические формы мышьяка - заменили арсенат свинца в сельском хозяйстве. В свою очередь, к 2013 году использование этих органических мышьяков было прекращено во всех видах сельскохозяйственной деятельности, кроме выращивания хлопка.[66]
Биогеохимия мышьяка сложна и включает различные процессы адсорбции и десорбции. Токсичность мышьяка связана с его растворимостью и зависит от pH. Арсенит (AsO3−
3) более растворим, чем арсенат (AsO3−
4) и более токсичен; однако при более низком pH арсенат становится более подвижным и токсичным. Было обнаружено, что добавление оксидов серы, фосфора и железа к почвам с высоким содержанием арсенита значительно снижает фитотоксичность мышьяка.[67]
Мышьяк используется в качестве кормовой добавки в домашняя птица и свиноводство, в частности, в США для увеличения веса, улучшения эффективность корма, и предотвратить болезнь.[68][69] Примером является роксарсон, который использовался как бройлер около 70% производителей бройлеров в США.[70] Alpharma, дочерняя компания Pfizer Inc., производящая роксарсон, добровольно приостановила продажу препарата в ответ на исследования, показавшие повышенные уровни неорганического мышьяка, канцерогена, у обработанных цыплят.[71] Преемник Alpharma, Зоэтис, продолжает продавать нитарсон, в первую очередь для индеек.[71]
Мышьяк намеренно добавлен в корм куры выращен для употребления в пищу. Органические соединения мышьяка менее токсичны, чем чистый мышьяк, и способствуют росту цыплят. В некоторых условиях мышьяк в гроши превращается в токсичную неорганическую форму.[72]
Исследование, проведенное в 2006 г. Австралийский скаковая лошадь Phar Lap, определили, что смерть известного чемпиона в 1932 году была вызвана передозировкой мышьяка. Сиднейский ветеринар Перси Сайкс заявил: «В те дни мышьяк был довольно распространенным тонизирующим средством, обычно принимавшимся в виде раствора (раствор Фаулера) ... Это было настолько распространено, что я считаю, что 90 процентов лошадей имели мышьяк. в их системе ".[73]
Медицинское использование
В течение 18, 19 и 20 веков ряд соединений мышьяка использовался в качестве лекарств, в том числе арсфенамин (к Пол Эрлих ) и триоксид мышьяка (к Томас Фаулер ).[74] Арсфенамин, а также неосальварсан, был указан для сифилис, но был вытеснен современным антибиотики. Однако мышьяки, такие как меларсопрол все еще используются для лечения трипаносомоз, поскольку, несмотря на то, что эти препараты обладают сильной токсичностью, болезнь почти всегда заканчивается летальным исходом, если ее не лечить.[75]
Триоксид мышьяка использовался различными способами за последние 500 лет, чаще всего для лечения рак, но также и в таких разнообразных лекарствах, как Решение Фаулера в псориаз.[76] Соединенные штаты Управление по контролю за продуктами и лекарствами в 2000 году одобрил это соединение для лечения пациентов с острый промиелоцитарный лейкоз что устойчиво к полностью транс-ретиноевая кислота.[77]
Недавно исследователи обнаружили опухоли, используя мышьяк-74 (излучатель позитронов). Этот изотоп дает более четкое ПЭТ сканирование изображения, чем предыдущий радиоактивный агент, йод -124, потому что организм имеет тенденцию доставлять йод к щитовидной железе, создавая сигнальный шум.[78]Наночастицы мышьяка продемонстрировал способность убивать раковые клетки с меньшим цитотоксичность чем другие составы мышьяка.[79]
В субтоксических дозах растворимые соединения мышьяка действуют как стимуляторы, и когда-то были популярны в малых дозах в качестве лекарства людьми в середине 18-19 веков.[16]
Сплавы
Основное применение мышьяка - его легирование свинцом. Свинцовые компоненты в автомобильные аккумуляторы усилены присутствием очень небольшого процента мышьяка.[8][80] Обезцинкование латуни (медно-цинковый сплав) значительно снижается при добавлении мышьяка.[81] «Мышьяковая медь, раскисленная фосфором» с содержанием мышьяка 0,3% имеет повышенную коррозионную стойкость в определенных средах.[82] Арсенид галлия это важный полупроводник материал, используемый в интегральные схемы. Схемы из GaAs намного быстрее (но и дороже), чем схемы, сделанные из кремний. В отличие от кремния GaAs имеет прямая запрещенная зона, и может использоваться в лазерные диоды и Светодиоды преобразовать электрические энергия прямо в свет.[8]
Военный
После Первая Мировая Война, Соединенные Штаты создали запас в 20 000 тонн вооруженный люизит (ClCH = CHAsCl2), органо-мышьяк пузырчатый (блистерный агент) и легкое раздражитель. Склад был нейтрализован отбеливателем и сброшен в Мексиканский залив в 1950-е гг.[83] Вовремя война во Вьетнаме, США использовали Агент синий, смесь какодилат натрия и его кислотная форма, как одна из радужные гербициды лишить северовьетнамских солдат листвы и риса.[84][85]
Другое использование
- Ацетоарсенит меди использовался в качестве зеленого пигмент известен под многими именами, в том числе Пэрис Грин и изумрудно-зеленый. Это вызвало многочисленные отравления мышьяком. Зеленый Шееле, арсенат меди, использовался в 19 веке как краситель в сладости.[86]
- Мышьяк используется в бронзовый[87] и пиротехника.
- До 2% произведенного мышьяка используется в свинцовых сплавах для свинцовый выстрел и пули.[88]
- В альфа-латунь в небольших количествах добавляют мышьяк, чтобы устойчивый к децинкификации. Этот сорт латуни используется в сантехнической арматуре и других влажных средах.[89]
- Мышьяк также используется для сохранения таксономических образцов.
- Мышьяк использовался как глушитель в керамике, создавая белые глазури.[90]
- До недавнего времени мышьяк использовался в оптическом стекле. Современные производители стекла под давлением защитников окружающей среды перестали использовать как мышьяк, так и вести.[91]
Биологическая роль
Бактерии
Некоторые виды бактерии получают свою энергию в отсутствие кислорода путем окисляющий различные виды топлива в то время как сокращение арсенат в арсенит. В окислительных условиях окружающей среды некоторые бактерии используют в качестве топлива арсенит, который они окисляют до арсената.[92] В ферменты вовлеченные известны как арсенат редуктазы (Арр).[93]
В 2008 году были обнаружены бактерии, использующие версию фотосинтез в отсутствие кислорода с арсенитами как доноры электронов, производя арсенаты (так же, как при обычном фотосинтезе вода используется в качестве донора электронов, производя молекулярный кислород). Исследователи предполагают, что на протяжении истории эти фотосинтезирующие организмы производили арсенаты, которые позволяли бактериям, восстанавливающим арсенат, процветать. Один напряжение PHS-1 был изолирован и относится к гаммапротеобактерии Ectothiorhodospira shaposhnikovii. Механизм неизвестен, но закодированный фермент Arr может действовать в обратном направлении по сравнению с известным ему. гомологи.[94]
В 2011 году было высказано предположение, что штамм Halomonadaceae можно было бы выращивать в отсутствие фосфора, если бы этот элемент был заменен мышьяком,[95] используя тот факт, что арсенат и фосфат анионы аналогичны структурно. Исследование было широко раскритиковано и впоследствии опровергнуто группами независимых исследователей.[96][97]
Незаменимый микроэлемент у высших животных
Некоторые данные свидетельствуют о том, что мышьяк является важным микроэлементом для птиц (куры) и млекопитающих (крысы, хомяки и козы). Тем не менее биологическая функция не известно.[98][99][100]
Наследственность
Мышьяк был связан с эпигенетические изменения наследственные изменения экспрессии генов, которые происходят без изменений в Последовательность ДНК. К ним относятся метилирование ДНК, модификация гистонов и РНК вмешательство. Токсичные уровни мышьяка вызывают значительное гиперметилирование ДНК генов-супрессоров опухолей p16 и p53, что увеличивает риск канцерогенез. Эти эпигенетические события были изучены in vitro используя человека почка клетки и in vivo используя крысу печень клетки и периферическая кровь лейкоциты в людях.[101] Масс-спектрометрия с индуктивно связанной плазмой (ICP-MS) используется для определения точных уровней внутриклеточного мышьяка и других оснований мышьяка, участвующих в эпигенетической модификации ДНК.[102] Исследования, изучающие мышьяк как эпигенетический фактор, могут быть использованы для разработки точных биомаркеров воздействия и восприимчивости.
Китайский тормозной папоротник (Pteris vittata ) гипераккумулирует мышьяк из почвы в листьях и имеет предполагаемое использование в фиторемедиация.[103]
Биометилирование
Неорганический мышьяк и его соединения, попадая в пищевая цепочка, прогрессивно метаболизируются в процессе метилирование.[104][105] Например, форма Scopulariopsis brevicaulis производит триметиларсин если присутствует неорганический мышьяк.[106] Органическое соединение арсенобетаин содержится в некоторых морских продуктах, таких как рыба и водоросли, а также в грибах в больших концентрациях. В среднем человек получает около 10–50 мкг / день. Значения около 1000 мкг не являются необычными после употребления рыбы или грибов, но есть небольшая опасность при употреблении в пищу рыбы, потому что это соединение мышьяка почти нетоксично.[107]
Экологические проблемы
Контакт
Естественные источники воздействия на человека включают вулканический пепел, выветривание минералов и руд и минерализованные грунтовые воды. Мышьяк также содержится в пище, воде, почве и воздухе.[108] Мышьяк усваивается всеми растениями, но больше он концентрируется в листовых овощах, рисе, яблочном и виноградном соке и морепродуктах.[109] Дополнительный путь воздействия - вдыхание атмосферных газов и пыли.[110]Вовремя Викторианская эпоха, мышьяк широко использовался в домашнем декоре, особенно в обоях.[111]
Встречается в питьевой воде
Обширное загрязнение подземных вод мышьяком привело к широкому распространению отравление мышьяком в Бангладеш[112] и соседние страны. По оценкам, около 57 миллионов человек в Бенгальском бассейне пьют. грунтовые воды с концентрацией мышьяка выше Всемирная организация здоровья стандарт 10 частей на миллиард (ч / млрд).[113] Однако исследование заболеваемости раком на Тайване[114] предположили, что значительное увеличение смертности от рака появляется только при уровнях выше 150 частей на миллиард. Мышьяк в грунтовых водах имеет естественное происхождение и выделяется из отложений в грунтовые воды в результате аноксические условия недр. Эти грунтовые воды использовались после местных и западных НПО и правительство Бангладеш провело масштабную мелкую трубу Что ж программа питьевой воды в конце двадцатого века. Эта программа была разработана для предотвращения питья загрязненных бактериями поверхностных вод, но не проверила содержание мышьяка в грунтовых водах. Многие другие страны и районы в Юго-Восточная Азия, Такие как Вьетнам и Камбоджа, имеют геологические среды, которые производят грунтовые воды с высоким содержанием мышьяка. Арсеникоз было сообщено в Накхонситхаммарат, Таиланд в 1987 г., а Река Чао Прайя вероятно, содержит высокие уровни растворенного мышьяка естественного происхождения, что не представляет проблемы для здоровья населения, поскольку большая часть населения использует воду в бутылках.[115] В Пакистане более 60 миллионов человек подвергаются воздействию питьевой воды, загрязненной мышьяком, о чем свидетельствует недавний доклад Наука. Команда Подгорского исследовала более 1200 проб, и более 66% проб превышали минимальный уровень загрязнения ВОЗ.[116]
В Соединенных Штатах мышьяк чаще всего встречается в грунтовых водах юго-запада.[117] Части Новая Англия, Мичиган, Висконсин, Миннесота а также известно, что реки Дакота имеют значительные концентрации мышьяка в грунтовых водах.[118] Повышенный уровень рака кожи был связан с воздействием мышьяка в Висконсине, даже на уровнях ниже 10 частей на миллиард стандарта питьевой воды.[119] Согласно недавнему фильму, финансируемому США Суперфонд миллионы частных скважин содержат неизвестные уровни мышьяка, а в некоторых районах США более 20% скважин могут содержать уровни, превышающие установленные пределы.[120]
Воздействие мышьяка на низком уровне в концентрациях 100 частей на миллиард (т.е.выше стандарта питьевой воды 10 частей на миллиард) ставит под угрозу первоначальный иммунный ответ на H1N1 или свиной грипп инфекция по мнению ученых, поддерживаемых NIEHS. Исследование, проведенное на лабораторных мышах, предполагает, что люди, подвергшиеся воздействию мышьяка в питьевой воде, могут подвергаться повышенному риску более серьезных заболеваний или смерти от вируса.[121]
Некоторые канадцы пьют воду, содержащую неорганический мышьяк. Воды из частных колодцев наиболее подвержены риску содержания неорганического мышьяка. Предварительный анализ воды из скважины обычно не позволяет определить содержание мышьяка. Исследователи из Геологической службы Канады смоделировали относительные вариации в потенциальной опасности природного мышьяка для провинции Нью-Брансуик. Это исследование имеет важное значение для питьевой воды и проблем со здоровьем, связанных с неорганическим мышьяком.[122]
Эпидемиологические данные из Чили показывает дозозависимую связь между хроническим воздействием мышьяка и различными формами рака, в частности, когда присутствуют другие факторы риска, такие как курение сигарет. Эти эффекты были продемонстрированы при загрязнении менее 50 частей на миллиард.[123] Мышьяк сам по себе входит в состав табачный дым.[124]
Анализ многочисленных эпидемиологических исследований воздействия неорганического мышьяка позволяет предположить небольшое, но измеримое увеличение риска рака мочевого пузыря на 10 частей на миллиард.[125] По словам Питера Равенскрофта с географического факультета Кембриджского университета,[126] примерно 80 миллионов человек во всем мире потребляют с питьевой водой от 10 до 50 частей на миллиард мышьяка. Если бы все они потребляли с питьевой водой ровно 10 частей на миллиард мышьяка, то приведенный ранее анализ нескольких эпидемиологических исследований предсказал бы еще 2000 случаев рака мочевого пузыря. Это представляет собой явную недооценку общего воздействия, поскольку оно не включает рак легких или кожи и явно недооценивает воздействие. Те, кто подвергается воздействию мышьяка с уровнями выше действующего стандарта ВОЗ, должны взвесить затраты и выгоды от лечения мышьяком.
Ранние (1973) оценки процессов удаления растворенного мышьяка из питьевой воды показали эффективность соосаждения с оксидами железа или алюминия. В частности, было обнаружено, что железо в качестве коагулянта удаляет мышьяк с эффективностью, превышающей 90%.[127][128] Несколько систем адсорбционных сред были одобрены для использования в местах обслуживания в исследовании, финансируемом Агентство по охране окружающей среды США (Агентство по охране окружающей среды США) и Национальный фонд науки (NSF). Группа европейских и индийских ученых и инженеров построила шесть заводов по переработке мышьяка в Западная Бенгалия основан на методе восстановления на месте (технология SAR). В этой технологии не используются химические вещества, и мышьяк остается в нерастворимой форме (состояние +5) в подземной зоне за счет подпитки аэрированной воды в водоносный горизонт и развития зоны окисления, которая поддерживает микроорганизмы, окисляющие мышьяк. Этот процесс не приводит к образованию потока отходов или осадка и является относительно дешевым.[129]
Еще один эффективный и недорогой способ избежать загрязнения мышьяком - это прокладывать колодцы на глубину 500 футов или глубже, чтобы достичь более чистой воды. Недавнее исследование 2011 года, финансируемое Программой исследований Суперфонда Национального института экологических наук США, показывает, что глубокие отложения могут удалить мышьяк и вывести его из обращения. В этом процессе называется адсорбция, мышьяк прилипает к поверхности частиц глубоких отложений и естественным образом удаляется из грунтовых вод.[130]
Магнитное разделение мышьяка в очень слабом магнитном поле градиенты с большой площадью поверхности и монодисперсный магнетит (Fe3О4) нанокристаллы были продемонстрированы в очистке воды в местах потребления. Использование высокой удельной поверхности Fe3О4 нанокристаллов резко сократилась масса отходов, связанных с удалением мышьяка из воды.[131]
Эпидемиологические исследования показали наличие корреляции между хроническим потреблением питьевой воды, загрязненной мышьяком, и частотой всех основных причин смертности.[132] В литературе указывается, что воздействие мышьяка является причиной патогенеза диабета.[133]
Недавно было показано, что фильтры на основе соломы снижают содержание мышьяка в воде до 3 мкг / л. Это может найти применение в областях, где питьевая вода добывается из-под земли. водоносные горизонты.[134]
Сан-Педро-де-Атакама
На протяжении нескольких веков люди Сан-Педро-де-Атакама в Чили пили воду, загрязненную мышьяком, и некоторые данные свидетельствуют о том, что у них выработался определенный иммунитет.[135][136][137]
Карты опасностей для загрязненных подземных вод
Около одной трети населения мира пьет воду из подземных источников. Из них около 10 процентов, примерно 300 миллионов человек, получают воду из ресурсов подземных вод, загрязненных вредными для здоровья уровнями мышьяка или фторида.[138] Эти микроэлементы происходят в основном из минералов и ионов земли.[139][140]
Редокс-превращение мышьяка в природных водах
Мышьяк уникален среди следов металлоиды и оксианион-образующие следы металлов (например, As, Se, Sb, Mo, V, Cr, U, Re). Он чувствителен к мобилизации при значениях pH, типичных для природных вод (pH 6,5–8,5), как в окислительных, так и в восстановительных условиях. Мышьяк может присутствовать в окружающей среде в нескольких степенях окисления (−3, 0, +3 и +5), но в природных водах он чаще всего встречается в неорганических формах в виде оксианионов трехвалентного арсенита [As (III)] или пятивалентного арсената [As (V)]. Органические формы мышьяка образуются в результате биологической активности, в основном в поверхностных водах, но редко имеют количественное значение. Однако органические соединения мышьяка могут образовываться там, где на воду в значительной степени влияет промышленное загрязнение.[141]
Мышьяк можно солюбилизировать различными способами. Когда pH высокий, мышьяк может высвобождаться из участков связывания на поверхности, которые теряют свой положительный заряд. Когда уровень воды падает и сульфид минералы подвергаются воздействию воздуха, мышьяк, заключенный в сульфидных минералах, может попадать в воду. Когда в воде присутствует органический углерод, бактерии питаются путем прямого восстановления As (V) до As (III) или путем восстановления элемента в месте связывания, высвобождая неорганический мышьяк.[142]
На превращения мышьяка в водной среде влияют pH, восстановительно-окислительный потенциал, концентрация органических веществ, а также концентрации и формы других элементов, особенно железа и марганца. Основными факторами являются pH и окислительно-восстановительный потенциал. Как правило, основными формами мышьяка в кислородных условиях являются H3AsO4, H2AsO4−, HAsO42−, и AsO43− при pH 2, 2–7, 7–11 и 11 соответственно. В восстановительных условиях H3AsO4 преобладает при pH 2–9.
Окисление и восстановление влияют на миграцию мышьяка в подземных средах. Арсенит является наиболее стабильной растворимой формой мышьяка в восстановительной среде, а арсенат, который менее подвижен, чем арсенит, доминирует в окислительных средах при нейтральном pH. Следовательно, мышьяк может быть более подвижным в восстановительных условиях. Восстановительная среда также богата органическими веществами, которые могут повысить растворимость соединений мышьяка. В результате адсорбция мышьяка уменьшается, а растворенный мышьяк накапливается в грунтовых водах. Вот почему содержание мышьяка в восстановительной среде выше, чем в окислительной.[143]
Присутствие серы - еще один фактор, влияющий на превращение мышьяка в природной воде. Мышьяк может осадок при образовании сульфидов металлов. Таким образом, мышьяк удаляется из воды, и его подвижность уменьшается. Когда присутствует кислород, бактерии окисляют восстановленную серу для выработки энергии, потенциально выделяя связанный мышьяк.
Окислительно-восстановительные реакции с участием Fe также являются важными факторами в судьбе мышьяка в водных системах. Восстановление оксигидроксидов железа играет ключевую роль в выделении мышьяка в воду. Таким образом, мышьяк может быть обогащен водой с повышенными концентрациями Fe.[144] В окислительных условиях мышьяк может мобилизоваться из пирит или оксиды железа, особенно при повышенном pH. В восстановительных условиях мышьяк может быть мобилизован путем восстановительной десорбции или растворения, когда он связан с оксидами железа. Восстановительная десорбция происходит при двух обстоятельствах. Во-первых, арсенат восстанавливается до арсенита, который менее сильно адсорбируется на оксидах железа. Другой результат - изменение заряда на поверхности минерала, которое приводит к десорбции связанного мышьяка.[145]
Некоторые виды бактерий катализируют окислительно-восстановительные превращения мышьяка. Диссимиляционные арсенат-респираторные прокариоты (DARP) ускоряют восстановление As (V) до As (III). DARP использует As (V) в качестве акцептора электронов анаэробного дыхания и получает энергию для выживания. В этом процессе могут окисляться другие органические и неорганические вещества. Хемоавтотрофный окислители арсенита (CAO) и гетеротрофный окислители арсенита (HAO) превращают As (III) в As (V). CAO сочетают окисление As (III) с восстановлением кислорода или нитрата. Они используют полученную энергию, чтобы исправить производство органического углерода из CO.2. HAO не может получать энергию от окисления As (III). Этот процесс может быть мышьяком. детоксикация механизм бактерий.[146]
Равновесные термодинамические расчеты предсказывают, что концентрации As (V) должны быть больше, чем концентрации As (III) во всех условиях, кроме сильно восстанавливающих, т.е. когда SO42− сокращение происходит. Однако абиотические окислительно-восстановительные реакции мышьяка протекают медленно. Окисление As (III) растворенным O2 это особенно медленная реакция. Например, Джонсон и Пилсон (1975) дали период полураспада для оксигенации As (III) в морской воде от нескольких месяцев до года.[147] В других исследованиях соотношения As (V) / As (III) были стабильными в течение нескольких дней или недель во время отбора проб воды, когда не принимались особые меры для предотвращения окисления, что снова указывает на относительно низкие скорости окисления. Черри обнаружил в результате экспериментальных исследований, что соотношения As (V) / As (III) были стабильными в бескислородных растворах до 3 недель, но постепенные изменения происходили в течение более длительных периодов времени.[148] Было замечено, что образцы стерильной воды менее подвержены изменениям в составе, чем нестерильные образцы.[149] Оремланд обнаружил, что восстановление As (V) до As (III) в озере Моно быстро катализируется бактериями с константами скорости в диапазоне от 0,02 до 0,3 дня.−1.[150]
Консервация древесины в США
По состоянию на 2002 год предприятия промышленности США потребляли 19 600 метрических тонн мышьяка. Девяносто процентов из них было использовано для обработки древесины хромированный арсенат меди (CCA). В 2007 году 50% из 5280 метрических тонн потребления по-прежнему использовалось для этой цели.[41][151] В Соединенных Штатах добровольный отказ от мышьяка в производстве потребительских товаров, а также товаров для жилищного строительства и строительства общего назначения начался 31 декабря 2003 года, и в настоящее время используются альтернативные химические вещества, такие как Щелочная медь четвертичная, бораты, азол меди, ципроконазол, и пропиконазол.[152]
Хотя это приложение больше не выпускается, оно также является одним из самых важных для широкой публики. Подавляющее большинство пожилых обработанный давлением древесина была обработана CCA. Пиломатериалы CCA по-прежнему широко используются во многих странах и активно использовались во второй половине 20-го века в качестве строительных и наружных материалов. строительный материал. Хотя использование пиломатериалов CCA было запрещено во многих областях после того, как исследования показали, что мышьяк может вымываться из древесины в окружающую среду. почва (например, из-за оборудования детских площадок), опасность также представляет сжигание старой древесины CCA. Прямое или косвенное попадание в организм древесной золы от сожженных пиломатериалов из CCA привело к гибели животных и серьезным отравлениям у людей; смертельная доза для человека составляет примерно 20 граммов золы.[153] Пиломатериалы из лома CCA со строительных площадок и сносов могут быть непреднамеренно использованы при коммерческих и бытовых пожарах. Протоколы по безопасной утилизации пиломатериалов CCA не согласованы во всем мире. Широко распространен свалка утилизация такой древесины вызывает определенные опасения,[154] но другие исследования не показали загрязнения грунтовых вод мышьяком.[155][156]
Составление карты промышленных выбросов в США
Одним из инструментов, который отображает местонахождение (и другую информацию) выбросов мышьяка в Соединенных Штатах, является TOXMAP.[157] TOXMAP - это географическая информационная система (ГИС), разработанная Отделом специализированных информационных служб Национальная медицинская библиотека США (NLM) финансируется Федеральным правительством США. TOXMAP с размеченными картами Соединенных Штатов позволяет пользователям визуально исследовать данные из Агентство по охране окружающей среды США (EPA) Инвентаризация выбросов токсичных веществ и Программы фундаментальных исследований Суперфонда. Информация TOXMAP о химических веществах и состоянии окружающей среды взята из сети токсикологических данных NLM (TOXNET),[158] PubMed, и из других авторитетных источников.
Биоремедиация
Физические, химические и биологические методы использовались для восстановления воды, загрязненной мышьяком.[159] Биоремедиация считается рентабельной и экологически чистой.[160] Биологическая очистка грунтовых вод, загрязненных мышьяком, направлена на превращение арсенита, токсичной для человека формы мышьяка, в арсенат. Арсенат (степень окисления +5) является доминирующей формой мышьяка в поверхностных водах, в то время как арсенит (степень окисления +3) является доминирующей формой в гипоксической или бескислородной среде. Арсенит более растворим и подвижен, чем арсенат. Многие виды бактерий могут преобразовывать арсенит в арсенат в бескислородных условиях, используя арсенит в качестве донора электронов.[161] Это полезный метод восстановления грунтовых вод. Другой стратегией биоремедиации является использование растений, которые накапливают мышьяк в своих тканях через фиторемедиация но необходимо рассмотреть вопрос об утилизации зараженного растительного материала.
Биоремедиация требует тщательной оценки и проектирования в соответствии с существующими условиями. Некоторые сайты могут потребовать добавления акцептора электронов, в то время как другие требуют добавления микробов (биоаугментация ). Независимо от используемого метода, только постоянный мониторинг может предотвратить загрязнение в будущем.
Токсичность и меры предосторожности
| Опасности | |
|---|---|
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H301, H331, H350, H410[162] | |
Мышьяк и многие его соединения являются особенно сильнодействующими ядами.
Классификация
Элементарный мышьяк и соединения сульфата и триоксида мышьяка классифицируются как "токсичный "и" опасно для окружающей среды "в Евросоюз под директива 67/548 / EEC. Международное агентство по изучению рака (IARC) распознает мышьяк и неорганические соединения мышьяка как канцерогены 1 группы, а ЕС перечисляет триоксид мышьяка, пятиокись мышьяка, и арсенат соли категории 1 канцерогены.
Известно, что мышьяк вызывает арсеникоз когда он присутствует в питьевой воде, «наиболее распространенным видом является арсенат [HAsO2−
4; As (V)] и арсенит [H3AsO3; Как (III)] ".
Законные ограничения, еда и напитки
В США с 2006 года максимальная концентрация в питьевой воде, разрешенная Агентство по охране окружающей среды (EPA) составляет 10 частей на миллиард[163] и FDA установило тот же стандарт в 2005 году для бутилированной воды.[164] Департамент охраны окружающей среды Нью-Джерси установил лимит питьевой воды в размере 5 частей на миллиард в 2006 году.[165] В IDLH (непосредственно опасно для жизни и здоровья) значение для металлического мышьяка и неорганических соединений мышьяка составляет 5 мг / м3.3 (5 частей на миллиард). В Управление по охране труда установил допустимый предел воздействия (PEL) до средневзвешенного по времени (TWA) 0,01 мг / м3 (0,01 ppb), а Национальный институт охраны труда и здоровья (NIOSH) установил рекомендуемый предел воздействия (REL) до 15-минутного постоянного воздействия 0,002 мг / м3 (0,002 частей на миллиард).[166] PEL для органических соединений мышьяка составляет TWA 0,5 мг / м3.3.[167] (0,5 частей на миллиард).
В 2008 году, основываясь на текущих испытаниях широкого спектра американских продуктов питания на предмет токсичных химикатов,[168] Соединенные штаты. Управление по контролю за продуктами и лекарствами установил «уровень беспокойства» для неорганического мышьяка в яблочном и грушевом соках на уровне 23 частей на миллиард, исходя из неканцерогенных эффектов, и начал блокировать импорт продуктов, превышающих этот уровень; он также требовал отзыва несоответствующей отечественной продукции.[164] В 2011 г. Доктор Оз Телевизионное шоу транслировало программу, посвященную испытаниям, проведенным независимой лабораторией, нанятой продюсерами. Хотя методология оспаривалась (она не делала различий между органическим и неорганическим мышьяком), тесты показали уровни мышьяка до 36 частей на миллиард.[169] В ответ FDA проверило худший бренд из Доктор Унция показать и нашел гораздо более низкие уровни. Текущие испытания показали, что 95% образцов яблочного сока не соответствовали допустимому уровню. Позднее тестирование Потребительские отчеты показал уровень неорганического мышьяка чуть выше 10 частей на миллиард, и организация призвала родителей сократить потребление.[170] В июле 2013 года с учетом потребления детьми, хронического воздействия и канцерогенного эффекта FDA установило «уровень действия» для яблочного сока в 10 частей на миллиард, что соответствует стандарту для питьевой воды.[164]
Обеспокоенность по поводу содержания мышьяка в рисе в Бангладеш возникла в 2002 году, но в то время только в Австралии был законный предел для пищевых продуктов (один миллиграмм на килограмм).[171][172] Была выражена обеспокоенность по поводу того, что в 2005 году люди, которые ели рис из США, превышали стандарты ВОЗ по личному потреблению мышьяка.[173] В 2011 году Китайская Народная Республика установила пищевой стандарт на мышьяк в размере 150 частей на миллиард.[174]
В США в 2012 г. тестирование, проведенное отдельными группами исследователей в Исследовательском центре гигиены окружающей среды и профилактики заболеваний у детей в г. Дартмутский колледж (в начале года, уделяя особое внимание уровню мочеиспускания у детей)[175] и Потребительские отчеты (в ноябре)[176][177] обнаружили уровни мышьяка в рисе, что привело к призыву FDA установить ограничения.[178] FDA опубликовало некоторые результаты тестирования в сентябре 2012 г.[179][180] и по состоянию на июль 2013 года все еще собирает данные в поддержку нового потенциального регулирования. Он не рекомендовал никаких изменений в поведении потребителей.[181]
Consumer Reports рекомендуется:
- Что EPA и FDA исключают из производства продуктов питания удобрения, содержащие мышьяк, лекарства и пестициды;
- Чтобы FDA установило законный предел для пищевых продуктов;
- Эта промышленность изменила производственную практику для снижения уровней мышьяка, особенно в пищевых продуктах для детей; и
- Потребители проверяют запасы воды в доме, придерживаются разнообразной диеты и готовят рис с избытком воды, а затем сливают его (снижая содержание неорганического мышьяка примерно на треть вместе с небольшим снижением содержания витаминов).[177]
- Сторонники общественного здравоохранения, основанные на фактических данных, также рекомендуют, учитывая отсутствие регулирования или маркировки мышьяка в США, детям не следует есть не более 1,5 порций риса в неделю и не употреблять рисовое молоко как часть своего ежедневного рациона до 5 лет. .[182] Они также предлагают рекомендации для взрослых и младенцев о том, как ограничить воздействие мышьяка из риса, питьевой воды и фруктового сока.[182]
2014 год Всемирная организация здоровья была запланирована консультативная конференция для рассмотрения пределов 200–300 частей на миллиард для риса.[177]
Пределы профессионального воздействия
| Страна | Предел[183] |
|---|---|
| Аргентина | Подтвержденный канцероген для человека |
| Австралия | TWA 0,05 мг / м3 - канцероген |
| Бельгия | TWA 0,1 мг / м3 - канцероген |
| Болгария | Подтвержденный канцероген для человека |
| Колумбия | Подтвержденный канцероген для человека |
| Дания | TWA 0,01 мг / м3 |
| Финляндия | Канцероген |
| Египет | TWA 0,2 мг / м3 |
| Венгрия | Предел концентрации 0,01 мг / м3 - Кожа, канцероген |
| Индия | TWA 0,2 мг / м3 |
| Япония | Канцероген группы 1 |
| Иордания | Подтвержденный канцероген для человека |
| Мексика | TWA 0,2 мг / м3 |
| Новая Зеландия | TWA 0,05 мг / м3 - канцероген |
| Норвегия | TWA 0,02 мг / м3 |
| Филиппины | TWA 0,5 мг / м3 |
| Польша | TWA 0,01 мг / м3 |
| Сингапур | Подтвержденный канцероген для человека |
| Южная Корея | TWA 0,01 мг / м3[184][185] |
| Швеция | TWA 0,01 мг / м3 |
| Таиланд | TWA 0,5 мг / м3 |
| индюк | TWA 0,5 мг / м3 |
| объединенное Королевство | TWA 0,1 мг / м3 |
| Соединенные Штаты | TWA 0,01 мг / м3 |
| Вьетнам | Подтвержденный канцероген для человека |
Экотоксичность
Мышьяк биоаккумулятивный у многих организмов, в частности морских видов, но, по-видимому, он не оказывает значительного биоусиления в пищевых сетях. В загрязненных районах на рост растений может влиять поглощение корнями арсената, который является аналогом фосфата и поэтому легко переносится в тканях и клетках растений. На загрязненных территориях поглощение более токсичного иона арсенита (особенно в восстановительных условиях) вероятно в плохо дренированных почвах.
Токсичность для животных
| Сложный | Животное | LD50 | Маршрут |
|---|---|---|---|
| Мышьяк | Крыса | 763 мг / кг | устный |
| Мышьяк | Мышь | 145 мг / кг | устный |
| Арсенат кальция | Крыса | 20 мг / кг | устный |
| Арсенат кальция | Мышь | 794 мг / кг | устный |
| Арсенат кальция | Кролик | 50 мг / кг | устный |
| Арсенат кальция | Собака | 38 мг / кг | устный |
| Свинец арсенат | Кролик | 75 мг / кг | устный |
| Сложный | Животное | LD50[186] | Маршрут |
|---|---|---|---|
| Триоксид мышьяка (As (III)) | Мышь | 26 мг / кг | устный |
| Арсенит (As (III)) | Мышь | 8 мг / кг | я |
| Арсенат (As (V)) | Мышь | 21 мг / кг | я |
| ММА (как (III)) | Хомяк | 2 мг / кг | ip |
| ММА (как (V)) | Мышь | 916 мг / кг | устный |
| DMA (как (V)) | Мышь | 648 мг / кг | устный |
| im = вводится внутримышечно ip = вводится внутрибрюшинно | |||
Биологический механизм
Токсичность мышьяка обусловлена сродством оксидов мышьяка (III) к тиолы. Тиолы в форме цистеин остатки и кофакторы Такие как липоевая кислота и кофермент А, расположены на активных сайтах многих важных ферменты.[8]
Мышьяк разрушает АТФ производство через несколько механизмов. На уровне цикл лимонной кислоты, мышьяк подавляет липоевая кислота, который является кофактором для пируватдегидрогеназа. Арсенат, конкурируя с фосфатом, разъединяет окислительного фосфорилирования, тем самым подавляя связанное с энергией сокращение НАД +, митохондриальное дыхание и синтез АТФ. Также увеличивается производство перекиси водорода, которая, как предполагается, может образовывать активные формы кислорода и окислительный стресс. Эти метаболические помехи приводят к смерти от мультисистемной органная недостаточность. Предполагается, что органная недостаточность связана с некротический смерть клетки, а не апоптоз, так как запасы энергии были слишком истощены для возникновения апоптоза.[186]
Риски воздействия и устранение
Профессиональное облучение и отравление мышьяком может возникнуть у людей, работающих в отраслях, связанных с использованием неорганического мышьяка и его соединений, таких как консервирование древесины, производство стекла, сплавов цветных металлов и производство электронных полупроводников. Неорганический мышьяк также содержится в выбросах коксовых печей, связанных с металлургической промышленностью.[187]
Преобразование между As (III) и As (V) является важным фактором загрязнения окружающей среды мышьяком. Согласно Кроалу, Гралнику, Маласарну и Ньюману, «[] понимание [] того, что стимулирует окисление As (III) и / или ограничивает восстановление As (V), имеет отношение к биоремедиация загрязненных участков (Croal). Изучение хемолитоавтотрофных окислителей As (III) и гетеротрофных восстановителей As (V) может помочь понять процессы окисления и / или восстановления мышьяка.[188]
Уход
Возможно лечение хронического отравления мышьяком. Британский антилюизит (димеркапрол ) назначают в дозах от 5 мг / кг до 300 мг каждые 4 часа в первый день, затем каждые 6 часов во второй день и, наконец, каждые 8 часов в течение 8 дополнительных дней.[189] Однако США Агентство регистрации токсичных веществ и заболеваний (ATSDR) заявляет, что долгосрочные последствия воздействия мышьяка невозможно предсказать.[110] Кровь, моча, волосы и ногти могут быть проверены на мышьяк; однако эти тесты не могут предсказать возможные последствия для здоровья от воздействия.[110] Длительное воздействие и последующее выделение с мочой связывают с раком мочевого пузыря и почек, а также с раком печени, простаты, кожи, легких и полости носа.[190]
Смотрите также
Рекомендации
- ^ Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ а б c d Гекчен, Н. А (1989). «Система As (мышьяка)». Бык. Фазовые диаграммы сплавов. 10: 11–22. Дои:10.1007 / BF02882166.
- ^ Abraham, Mariham Y .; Ван, Юйчжун; Се, Яомин; Вэй, Пингжун; Шефер III, Генри Ф .; Schleyer, P. von R .; Робинсон, Грегори Х. (2010). «Карбеновая стабилизация ди мышьяка: от гипервалентности к аллотропии». Химия: европейский журнал. 16 (2): 432–5. Дои:10.1002 / chem.200902840. PMID 19937872.
- ^ Эллис, Бобби Д .; Макдональд, Чарльз Л. Б. (2004). «Стабилизированный йодид мышьяка (I): готовый источник фрагментов йодида мышьяка и полезный реагент для образования кластеров». Неорганическая химия. 43 (19): 5981–6. Дои:10.1021 / ic049281s. PMID 15360247.
- ^ Кверна, Фрэн (2002). Ссылка на ASM Ready: Тепловые свойства металлов. ASM International. С. 8–. ISBN 978-0-87170-768-0. pdf.
- ^ Лиде, Дэвид Р., изд. (2000). «Магнитная восприимчивость элементов и неорганических соединений». Справочник по химии и физике (PDF) (81 изд.). CRC Press. ISBN 0849304814.
- ^ Weast, Роберт (1984). CRC, Справочник по химии и физике. Бока-Ратон, Флорида: Издательство Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4.
- ^ а б c d е Grund, Sabina C .; Хануш, Куниберт; Вольф, Ханс Уве. «Мышьяк и соединения мышьяка». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a03_113.pub2.
- ^ Анке М. Мышьяк. В: Mertz W. ed., Микроэлементы в питании человека и животных, 5-е изд. Орландо, Флорида: Academic Press, 1986, 347–372
- ^ Утус, Эрик О. (1992). «Доказательства существенности мышьяка». Геохимия окружающей среды и здоровье. 14 (2): 55–58. Дои:10.1007 / BF01783629. PMID 24197927. S2CID 22882255.
- ^ Утус Э.О., Эссенция мышьяка и факторы, влияющие на ее важность. В: Chappell W.R., Abernathy C.O., Cothern C.R. eds., Arsenic Exposure and Health. Нортвуд, Великобритания: Письма о науке и технологиях, 1994, 199–208.
- ^ а б Дибьенду, Саркар; Датта, Рупали (2007). «Биогеохимия мышьяка в загрязненных почвах участков Суперфонда». EPA. Агентство по охране окружающей среды США. Получено 25 февраля 2018.
- ^ Карелтон, Джеймс (2007). «Итоговый отчет: биогеохимия мышьяка в загрязненных почвах участков Суперфонда». EPA. Агентство по охране окружающей среды США. Получено 25 февраля 2018.
- ^ а б Норман, Николас С. (1998). Химия мышьяка, сурьмы и висмута. Springer. п. 50. ISBN 978-0-7514-0389-3.
- ^ Биберг, Эгон; Виберг, Нильс; Холлеман, Арнольд Фредерик (2001). Неорганическая химия. Академическая пресса. ISBN 978-0-12-352651-9.
- ^ а б c d е ж Холлеман, Арнольд Ф .; Виберг, Эгон; Виберг, Нильс (1985). «Арсен». Lehrbuch der Anorganischen Chemie (на немецком языке) (91–100 изд.). Вальтер де Грюйтер. С. 675–681. ISBN 978-3-11-007511-3.
- ^ Маделунг, Отфрид (2004). Полупроводники: справочник данных. Birkhäuser. С. 410–. ISBN 978-3-540-40488-0.
- ^ Зайдл, Майкл; Балаж, Габор; Шеер, Манфред (22 марта 2019 г.). «Химия желтого мышьяка». Химические обзоры. 119 (14): 8406–8434. Дои:10.1021 / acs.chemrev.8b00713. PMID 30900440.
- ^ Антонатос, Николас; Люкса, Ян; Стурала, Иржи; Софер, Зденек (2020). «Черный мышьяк: новый метод синтеза путем каталитической кристаллизации мышьяковистого стекла». Наномасштаб. 12 (9): 5397–5401. Дои:10.1039 / C9NR09627B. PMID 31894222.
- ^ Факты об элементе мышьяка. chemicool.com
- ^ а б Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (2003), "ТогдаUBASE оценка ядерных и распадных свойств », Ядерная физика A, 729: 3–128, Bibcode:2003НуФА.729 .... 3А, Дои:10.1016 / j.nuclphysa.2003.11.001
- ^ а б c d Гринвуд и Эрншоу, стр. 552–4.
- ^ Чисхолм, Хью, изд. (1911). . Британская энциклопедия. 2 (11-е изд.). Издательство Кембриджского университета. С. 651–654.
- ^ Ухер, Цтирад (2001). "Глава 5 Скуттерудиты: Перспективные новые термоэлектрики". Последние тенденции в исследованиях термоэлектрических материалов I: Скуттерудиты: перспективные новые термоэлектрики. Полупроводники и полуметаллы. 69. С. 139–253. Дои:10.1016 / S0080-8784 (01) 80151-4. ISBN 978-0-12-752178-7.
- ^ а б Гринвуд и Эрншоу, стр. 557–8.
- ^ Национальный институт исследований и безопасности (2000 год). "Fichexicologique nº 53: Trihydrure d'arsenic" (PDF). Архивировано из оригинал (PDF) 26 ноября 2006 г.. Получено 6 сентября 2006. Цитировать журнал требует
| журнал =(помощь) - ^ а б Гринвуд и Эрншоу, стр. 572–8.
- ^ «Мышьяк: данные по сульфидному соединению мышьяка (II)». WebElements.com. В архиве из оригинала 11 декабря 2007 г.. Получено 10 декабря 2007.
- ^ "Калгурлиит". Миндат. Гудзоновский институт минералогии. 1993–2017 гг.. Получено 2 сентября 2017.
- ^ Гринвуд и Эрншоу, стр. 578–83.
- ^ Танака, А. (2004). «Токсичность арсенида индия, арсенида галлия и арсенида алюминия-галлия». Токсикология и прикладная фармакология. 198 (3): 405–11. Дои:10.1016 / j.taap.2003.10.019. PMID 15276420.
- ^ Оссичини, Стефано; Павеси, Лоренцо; Приоло, Франческо (1 января 2003 г.). Светоизлучающий кремний для микрофотоники. ISBN 978-3-540-40233-6. Получено 27 сентября 2013.
- ^ Din, M. B .; Гулд, Р. Д. (1998). Механизм сильнополевой проводимости тонких пленок испаренного арсенида кадмия. ICSE'98. 1998 Международная конференция IEEE по полупроводниковой электронике. Протоколы (Кат. № 98EX187). п. 168. Дои:10.1109 / SMELEC.1998.781173. ISBN 978-0-7803-4971-1. S2CID 110904915.
- ^ Эллисон, Хэнк Д. (2007). Справочник боевых химических и биологических агентов. CRC Press. ISBN 978-0-8493-1434-6.
- ^ Жирар, Джеймс (2010). Принципы химии окружающей среды. Джонс и Бартлетт Обучение. ISBN 978-0-7637-5939-1.
- ^ Сомани, Сату М. (2001). Боевые отравляющие вещества: токсичность на низких уровнях. CRC Press. ISBN 978-0-8493-0872-7.
- ^ Гринвуд, стр. 584
- ^ а б Матшуллат, Йорг (2000). «Мышьяк в геосфере - обзор». Наука об окружающей среде в целом. 249 (1–3): 297–312. Bibcode:2000СтЭн.249..297М. Дои:10.1016 / S0048-9697 (99) 00524-0. PMID 10813460.
- ^ Брукс, Уильям Э. "Обзор минерального сырья за 2007 год: мышьяк" (PDF). Геологическая служба США. В архиве (PDF) из оригинала 17 декабря 2008 г.. Получено 25 ноября 2008.
- ^ а б Эдельштейн, Даниэль Л. «Обзор минерального сырья за 2016 год: мышьяк» (PDF). Геологическая служба США. Получено 1 июля 2016.
- ^ а б Брукс, Уильям Э. «Ежегодник полезных ископаемых 2007: Мышьяк» (PDF). Геологическая служба США. В архиве (PDF) из оригинала 17 декабря 2008 г.. Получено 8 ноября 2008.
- ^ Уилан, Дж. М .; Struthers, J.D .; Дитценбергер, Дж. А. (1960). «Отделение серы, селена и теллура от мышьяка». Журнал Электрохимического общества. 107 (12): 982–985. Дои:10.1149/1.2427585.
- ^ а б Харпер, Дуглас. «мышьяк». Интернет-словарь этимологии. Получено 15 мая 2010.
- ^ Бентли, Рональд; Честин, Томас Г. (2002). "Мышьяк Куриоза и человечество". Химический педагог. 7 (2): 51–60. Дои:10.1007 / s00897020539a. S2CID 6831485.
- ^ Холмиард Джон Эрик (2007). Создатели химии. Читать книги. ISBN 978-1-4067-3275-7.
- ^ Vahidnia, A .; Van Der Voet, G. B .; Де Вольф, Ф. А. (2007). «Нейротоксичность мышьяка - обзор». Человек и экспериментальная токсикология. 26 (10): 823–32. Дои:10.1177/0960327107084539. PMID 18025055. S2CID 24138885.
- ^ Лехтман, Х. (1996). «Мышьяковая бронза: грязная медь или выбранный сплав? Взгляд из Америки». Журнал полевой археологии. 23 (4): 477–514. Дои:10.2307/530550. JSTOR 530550.
- ^ Чарльз, Дж. А. (1967). «Ранние мышьяковистые бронзы - металлургический взгляд». Американский журнал археологии. 71 (1): 21–26. Дои:10.2307/501586. JSTOR 501586.
- ^ Джордж Сартон, Введение в историю науки. «В его трудах [...] мы находим получение различных веществ (например, основного карбоната свинца, мышьяка и сурьмы из их сульфидов)».
- ^ Эмсли, Джон (2001). Строительные блоки природы: руководство по элементам от А до Я. Оксфорд: Oxford University Press. С. 43, 513, 529. ISBN 978-0-19-850341-5.
- ^ (Конт), Антуан-Франсуа де Фуркруа (1804). Общая система химических знаний и ее применение к явлениям природы и искусства. С. 84–.
- ^ Сейферт, Дитмар (2001). "Дымящаяся мышьяковая жидкость кадета и какодиловые соединения Бунзена". Металлоорганические соединения. 20 (8): 1488–1498. Дои:10.1021 / om0101947.
- ^ «Медийное объявление 48 - без заголовка». The Washington Post (1877–1922). 13 февраля 1898 г.
- ^ Тернер, Алан (1999). «Точка зрения: история на данный момент: обзор событий в области регулирования пищевых продуктов Великобритании и связанных с ней консультативных комитетов». Британский продовольственный журнал. 101 (4): 274–283. Дои:10.1108/00070709910272141.
- ^ Хоксли, Люсинда (2016). Укушенный ведьмой: обои и мышьяк в викторианском доме. Нью-Йорк: Темза и Гудзон.
- ^ "Лондонский пурпурный. (8012-74-6)", Химическая книга
- ^ Ланман, Сьюзан В. (2000). «Цвет в саду:« Злокачественный пурпурный ».'". История сада. 28 (2): 209–221. Дои:10.2307/1587270. JSTOR 1587270.
- ^ Холтон, Э. К. (1926). «Инсектициды и фунгициды». Промышленная и инженерная химия. 18 (9): 931–933. Дои:10.1021 / ie50201a018.
- ^ Мерфи, Э. А .; Окотт, М. (1998). «Оценка количества пестицидов, содержащих мышьяк, исторически использовавшихся в географической области». Наука об окружающей среде в целом. 218 (2–3): 89–101. Bibcode:1998ScTEn.218 ... 89M. Дои:10.1016 / S0048-9697 (98) 00180-6.
- ^ Марлат, К. Л. (1897). Важные инсектициды: инструкции по их приготовлению и применению. Министерство сельского хозяйства США. п.5.
- ^ Кассинджер, Рут (20 апреля 2010 г.). Рай под стеклом: любитель создает сад в зимнем саду. ISBN 978-0-06-199130-1.
- ^ Рахман, Ф. А .; Allan, D. L .; Rosen, C.J .; Садовский, М. Дж. (2004). «Доступность мышьяка из древесины, обработанной хромированным арсенатом меди (CCA)». Журнал качества окружающей среды. 33 (1): 173–80. Дои:10.2134 / jeq2004.0173. PMID 14964372.
- ^ Lichtfouse, Эрик (2004). «Электродиалитическое удаление Cu, Cr и As из древесины с резьбой». В Lichtfouse, Эрик; Шварцбауэр, Ян; Роберт, Дидье (ред.). Химия окружающей среды: зеленая химия и загрязнители в экосистемах. Берлин: Springer. ISBN 978-3-540-22860-8.
- ^ Мандал, Бадал Кумар; Судзуки, К. Т. (2002). «Мышьяк в мире: обзор». Таланта. 58 (1): 201–235. Дои:10.1016 / S0039-9140 (02) 00268-0. PMID 18968746.
- ^ Перьеа, Ф. Дж. (20–26 августа 1998 г.). Историческое использование инсектицидов на основе арсената свинца, приводившее к загрязнению почвы и влиянию на восстановление почвы. 16-й Всемирный конгресс почвоведов. Монпелье, Франция. Архивировано из оригинал 7 декабря 2008 г.
- ^ «органические мышьяки». EPA.
- ^ «Микроэлементы в почвах и растениях, третье издание». CRC Press. Архивировано из оригинал 21 августа 2016 г.. Получено 2 августа 2016.
- ^ Nachman, Keeve E .; Грэм, Джей П .; Прайс, Лэнс Б .; Силбергельд, Эллен К. (2005). «Мышьяк: препятствие на пути к потенциальным решениям по управлению отходами животноводства». Перспективы гигиены окружающей среды. 113 (9): 1123–1124. Дои:10.1289 / ehp.7834. ЧВК 1280389. PMID 16140615.
- ^ «Мышьяк» (PDF). Агентство регистрации токсичных веществ и заболеваний. Раздел 5.3, с. 310.
- ^ Джонс, Ф. Т. (2007). «Широкий взгляд на мышьяк». Птицеводство. 86 (1): 2–14. Дои:10.1093 / пс / 86.1.2. PMID 17179408.
- ^ а б Персонал (8 июня 2011 г.). «Вопросы и ответы относительно 3-нитро (роксарсон)». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 21 сентября 2012.
- ^ Грей, Теодор (3 апреля 2012 г.). «Мышьяк». В сером, Теодор; Манн, Ник (ред.). Элементы: визуальное исследование каждого известного атома во Вселенной. Книги Hachette. ISBN 978-1579128951.
- ^ «Заявление Phar Lap о мышьяке преждевременно: эксперт». ABC News-AU. 23 октября 2006 г.. Получено 14 июн 2016.
- ^ Жибо, Стефан; Жауэн, Жерар (2010). Препараты на основе мышьяка: от раствора Фаулера до современной противоопухолевой химиотерапии. Разделы металлоорганической химии. 32. С. 1–20. Bibcode:2010moc..book .... 1G. Дои:10.1007/978-3-642-13185-1_1. ISBN 978-3-642-13184-4.
- ^ Бюшер П., Чекки Г., Жамонно В., Приотто Г. (2017). «Африканский трипаносомоз человека». Ланцет. 390 (10110): 2397–2409. Дои:10.1016 / S0140-6736 (17) 31510-6. PMID 28673422. S2CID 4853616.CS1 maint: несколько имен: список авторов (связь)
- ^ Huet, P.M .; Guillaume, E .; Cote, J .; Légaré, A .; Lavoie, P .; Виалле, А. (1975). «Нецирротическая пресинусоидальная портальная гипертензия, связанная с хронической мышьяковой интоксикацией». Гастроэнтерология. 68 (5, ч. 1): 1270–1277. Дои:10.1016 / S0016-5085 (75) 80244-7. PMID 1126603.
- ^ Антман, Карен Х. (2001). "История использования триоксида мышьяка в терапии рака". Онколог. 6 (Дополнение 2): 1–2. Дои:10.1634 / theoncologist.6-suppl_2-1. PMID 11331433.
- ^ Jennewein, Марк; Льюис, М. А .; Zhao, D .; Цыганов, Э .; Славянский, Н .; He, J .; Watkins, L .; Кодибагкар, В. Д .; О'Келли, S .; Kulkarni, P .; Antich, P .; Hermanne, A .; Rösch, F .; Mason, R .; Торп, доктор наук (2008). «Визуализация сосудов солидных опухолей у крыс с радиоактивным антителом, меченным мышьяком, которое связывает экспонированный фосфатидилсерин». Клинические исследования рака. 14 (5): 1377–1385. Дои:10.1158 / 1078-0432.CCR-07-1516. ЧВК 3436070. PMID 18316558.
- ^ Субастри, Арираман; Арун, Вишванатан; Шарма, Прити; Preedia babu, Ezhuthupurakkal; Суяваран, Арумугам; Нитхьянантан, Субраманиям; Alshammari, Ghedeir M .; Аристатил, Балакришнан; Дхаруман, Венкатараман; Тирунавуккарасу, Чиннасами (1 ноября 2018 г.). «Синтез и характеристика наночастиц мышьяка и его взаимодействие с ДНК и цитотоксический потенциал на клетках рака груди». Химико-биологические взаимодействия. Нанотехнологии, биология и токсикология. 295: 73–83. Дои:10.1016 / j.cbi.2017.12.025. ISSN 0009-2797. PMID 29277637.
- ^ Багшоу, Н. Э. (1995). «Свинцовые сплавы: прошлое, настоящее и будущее». Журнал источников энергии. 53 (1): 25–30. Bibcode:1995JPS .... 53 ... 25B. Дои:10.1016 / 0378-7753 (94) 01973-У.
- ^ Джозеф, Гюнтер; Кундиг, Конрад Дж. А; Международная ассоциация меди (1999 г.). "Делегирование". Медь: торговля, производство, использование и состояние окружающей среды. С. 123–124. ISBN 978-0-87170-656-0.
- ^ Наяр (1997). The Metals Databook. п. 6. ISBN 978-0-07-462300-8.
- ^ «Блистерные агенты». Красный код - оружие массового поражения. Получено 15 мая 2010.
- ^ Вестинг, Артур Х. (1972). «Гербициды на войне: текущее состояние и сомнения в будущем». Биологическое сохранение. 4 (5): 322–327. Дои:10.1016/0006-3207(72)90043-2.
- ^ Вестинг, Артур Х. (1971). «Лесное хозяйство и война в Южном Вьетнаме». Журнал лесного хозяйства. 69: 777–783.
- ^ Тимбрелл, Джон (2005). "Желтое масло и зеленый цвет Шееле". Парадокс яда: химические вещества как друзья и враги. Издательство Оксфордского университета. ISBN 978-0-19-280495-2.
- ^ Cross, J.D .; Dale, I.M .; Leslie, A.C.D .; Смит, Х. (1979). «Промышленное воздействие мышьяка». Журнал радиоаналитической химии. 48 (1–2): 197–208. Дои:10.1007 / BF02519786. S2CID 93714157.
- ^ Гурусвами, Шивараман (1999). «XIV. Боеприпасы». Технические свойства и применение свинцовых сплавов. CRC Press. С. 569–570. ISBN 978-0-8247-8247-4.
- ^ Дэвис, Джозеф R; Справочник комитета, ASM International (1 августа 2001 г.). «Делегирование». Медь и медные сплавы. п. 390. ISBN 978-0-87170-726-0.
- ^ Пармели, Каллен В. (1947). Керамические глазури (3-е изд.). Бостон, США: Cahners Books. п. 61.
- ^ «Спрос на мышьяк и окружающая среда». Обзор технологий загрязнения 214: Отходы ртути и мышьяка: удаление, восстановление, обработка и удаление. Уильям Эндрю. 1993. стр. 68. ISBN 978-0-8155-1326-1.
- ^ Штольц, Джон Ф .; Басу, Партха; Сантини, Джоанн М .; Оремланд, Рональд С. (2006). «Мышьяк и селен в микробном метаболизме». Ежегодный обзор микробиологии. 60: 107–30. Дои:10.1146 / annurev.micro.60.080805.142053. PMID 16704340. S2CID 2575554.
- ^ Мухопадхьяй, Рита; Розен, Барри П .; Phung, Le T .; Сильвер, Саймон (2002). «Микробный мышьяк: от геоциклов до генов и ферментов». Обзор микробиологии FEMS. 26 (3): 311–25. Дои:10.1111 / j.1574-6976.2002.tb00617.x. PMID 12165430.
- ^ Kulp, T. R; Hoeft, S.E .; Asao, M .; Madigan, M.T .; Hollibaugh, J. T .; Fisher, J.C .; Stolz, J. F .; Culbertson, C.W .; Miller, L.G .; Оремланд, Р. С. (2008). «Мышьяк (III) питает аноксигенный фотосинтез в биопленках горячих источников из озера Моно, Калифорния». Наука. 321 (5891): 967–970. Bibcode:2008Наука ... 321..967K. Дои:10.1126 / science.1160799. PMID 18703741. S2CID 39479754. Сложить резюме – Chemistry World, 15 августа 2008 г..
- ^ Wolfe-Simon, F .; Blum, J. S .; Kulp, T. R .; Gordon, G.W .; Hoeft, S.E .; Pett-Ridge, J .; Stolz, J. F .; Webb, S.M .; Вебер, П. К. (3 июня 2011 г.). «Бактерия, которая может расти, используя мышьяк вместо фосфора» (PDF). Наука. 332 (6034): 1163–1166. Bibcode:2011Научный ... 332.1163W. Дои:10.1126 / science.1197258. PMID 21127214. S2CID 51834091.
- ^ Erb, T. J .; Kiefer, P .; Hattendorf, B .; Günther, D .; Ворхольт, Дж. А. (2012). «GFAJ-1 представляет собой арсенат-устойчивый и фосфатозависимый организм». Наука. 337 (6093): 467–70. Bibcode:2012Наука ... 337..467E. Дои:10.1126 / наука.1218455. PMID 22773139. S2CID 20229329.
- ^ Reaves, M. L .; Sinha, S .; Rabinowitz, J. D .; Кругляк, Л .; Редфилд, Р. Дж. (2012). «Отсутствие детектируемого арсената в ДНК из клеток GFAJ-1, выращенных арсенатом». Наука. 337 (6093): 470–3. arXiv:1201.6643. Bibcode:2012Научный ... 337..470R. Дои:10.1126 / наука.1219861. ЧВК 3845625. PMID 22773140.
- ^ Анке М. (1986) «Мышьяк», стр. 347–372 в Mertz W. (ed.), Микроэлементы в питании человека и животных, 5-е изд. Орландо, Флорида: Academic Press
- ^ Утус Э. (1992). «Доказательства существенности мышьяка». Environ Geochem Health. 14 (2): 55–8. Дои:10.1007 / BF01783629. PMID 24197927. S2CID 22882255.
- ^ Утус Э. (1994) «Сущность мышьяка и факторы, влияющие на его важность», стр. 199–208 в Chappell W.R., Abernathy C.O., Cothern C.R. (ред.) Воздействие мышьяка и здоровье. Нортвуд, Великобритания: Письма о науке и технологиях.
- ^ Baccarelli, A .; Боллати, В. (2009). «Эпигенетика и химия окружающей среды». Текущее мнение в педиатрии. 21 (2): 243–251. Дои:10.1097 / MOP.0b013e32832925cc. ЧВК 3035853. PMID 19663042.
- ^ Николис, I .; Curis, E .; Deschamps, P .; Беназет, С. (2009). «Лекарственное использование, метаболизм, фармакокинетика и мониторинг арсенита в человеческих волосах». Биохимия. 91 (10): 1260–7. Дои:10.1016 / j.biochi.2009.06.003. PMID 19527769.
- ^ Lombi, E .; Zhao, F.-J .; Fuhrmann, M .; Ma, L.Q .; МакГрат, С. П. (2002). «Распределение и видообразование мышьяка в листах гипераккумулятора Pteris vittata». Новый Фитолог. 156 (2): 195–203. Дои:10.1046 / j.1469-8137.2002.00512.x. JSTOR 1514012.
- ^ Сакураи, Теруаки Сакураи (2003). «Биометилирование мышьяка является детоксикационным событием». Журнал науки о здоровье. 49 (3): 171–178. Дои:10.1248 / jhs.49.171.
- ^ Reimer, K. J .; Koch, I .; Каллен, W.R. (2010). Мышьякорганические. Распространение и трансформация в окружающей среде. Ионы металлов в науках о жизни. 7. С. 165–229. Дои:10.1039/9781849730822-00165. ISBN 978-1-84755-177-1. PMID 20877808.
- ^ Бентли, Рональд; Честин, Т. Г. (2002). «Микробное метилирование металлоидов: мышьяка, сурьмы и висмута». Обзоры микробиологии и молекулярной биологии. 66 (2): 250–271. Дои:10.1128 / MMBR.66.2.250-271.2002. ЧВК 120786. PMID 12040126.
- ^ Каллен, Уильям Р .; Реймер, Кеннет Дж. (1989). «Видообразование мышьяка в окружающей среде». Химические обзоры. 89 (4): 713–764. Дои:10.1021 / cr00094a002. HDL:10214/2162.
- ^ «Тематические исследования в экологической медицине (CSEM), пути воздействия токсичности мышьяка» (PDF). Агентство регистрации токсичных веществ и заболеваний. Получено 15 мая 2010.
- ^ «Мышьяк в продуктах питания: часто задаваемые вопросы». 5 декабря 2011 г.. Получено 11 апреля 2010.
- ^ а б c Мышьяк. Агентство регистрации токсичных веществ и заболеваний (2009 г.).
- ^ https://www.youtube.com/watch?v=MvxnXOoFl20
- ^ Мехарг, Эндрю (2005). Ядовитая земля - как мышьяк вызвал самое массовое в мире отравление. Macmillan Science. ISBN 978-1-4039-4499-3.
- ^ Хенке, Кевин Р. (28 апреля 2009 г.). Мышьяк: химия окружающей среды, угрозы здоровью и обработка отходов. п. 317. ISBN 978-0-470-02758-5.
- ^ Lamm, S. H .; Энгель, А .; Penn, C.A .; Chen, R .; Фейнлейб М. (2006). «Замещающий фактор риска рака мышьяка в наборе данных на юго-западе Тайваня». Environ. Перспектива здоровья. 114 (7): 1077–82. Дои:10.1289 / ehp.8704. ЧВК 1513326. PMID 16835062.
- ^ Конхорст, Эндрю (2005). «Мышьяк в подземных водах в отдельных странах Южной и Юго-Восточной Азии: обзор». J Trop Med Паразитол. 28: 73. Архивировано с оригинал 10 января 2014 г.
- ^ «Мышьяк в питьевой воде угрожает 60 миллионам жителей Пакистана». Наука | AAAS. 23 августа 2017 г.. Получено 11 сентября 2017.
- ^ «Мышьяк в питьевой воде: 3. Встречаемость в водах США» (PDF). Архивировано из оригинал (PDF) 7 января 2010 г.. Получено 15 мая 2010.
- ^ Уэлч, Алан Х .; Вестджон, Д. Б.; Helsel, Dennis R .; Хэнти, Ричард Б. (2000). «Мышьяк в грунтовых водах США: наличие и геохимия». Грунтовые воды. 38 (4): 589–604. Дои:10.1111 / j.1745-6584.2000.tb00251.x.
- ^ Knobeloch, L.M .; Зиерольд, К. М .; Андерсон, Х.А. (2006). «Связь загрязненной мышьяком питьевой воды с распространением рака кожи в долине реки Фокс в Висконсине». J. Health Popul Nutr. 24 (2): 206–13. HDL:1807/50099. PMID 17195561.
- ^ «В малых дозах: мышьяк». Программа суперфонда исследований токсичных металлов Дартмута. Дартмутский колледж.
- ^ Courtney, D .; Ely, Kenneth H .; Enelow, Ричард I .; Гамильтон, Джошуа В. (2009). «Низкие дозы мышьяка нарушают иммунный ответ на инфекцию гриппа А in vivo». Перспективы гигиены окружающей среды. 117 (9): 1441–7. Дои:10.1289 / ehp.0900911. ЧВК 2737023. PMID 19750111.
- ^ Klassen, R.A .; Douma, S.L .; Ford, A .; Rencz, A .; Грунский, Е. (2009). «Геофизическое моделирование относительных вариаций потенциальной опасности природного мышьяка в Нью-Брансуике» (PDF). Геологическая служба Канады. Архивировано из оригинал (PDF) 2 мая 2013 г.. Получено 14 октября 2012.
- ^ Ferreccio, C .; Санча, А. М. (2006). «Воздействие мышьяка и его влияние на здоровье в Чили». J Health Popul Nutr. 24 (2): 164–75. HDL:1807/50095. PMID 17195557.
- ^ Талхаут, Рейнскье; Шульц, Томас; Флорек, Ева; Ван Бентем, Ян; Вестер, Пит; Опперхёйзен, Антун (2011). «Опасные соединения в табачном дыме». Международный журнал экологических исследований и общественного здравоохранения. 8 (12): 613–628. Дои:10.3390 / ijerph8020613. ЧВК 3084482. PMID 21556207.
- ^ Chu, H.A .; Кроуфорд-Браун, Д. Дж. (2006). «Неорганический мышьяк в питьевой воде и рак мочевого пузыря: метаанализ для оценки реакции на дозу». Int. J. Environ. Res. Здравоохранение. 3 (4): 316–22. Дои:10.3390 / ijerph2006030039. PMID 17159272.
- ^ «Мышьяк в питьевой воде рассматривается как угроза - USATODAY.com». USA Today. 30 августа 2007 г.. Получено 1 января 2008.
- ^ Галледж, Джон Х .; О'Коннор, Джон Т. (1973). «Удаление мышьяка (V) из воды адсорбцией на гидроксидах алюминия и железа». J. American Water Works Assn. 65 (8): 548–552. Дои:10.1002 / j.1551-8833.1973.tb01893.x.
- ^ О'Коннор, Дж. Т .; О'Коннор, Т. «Мышьяк в питьевой воде: 4. Методы удаления» (PDF). Архивировано из оригинал (PDF) 7 января 2010 г.
- ^ «Обработка мышьяком in situ». insituarsenic.org. Получено 13 мая 2010.
- ^ Radloff, K. A .; Zheng, Y .; Michael, H.A .; Stute, M .; Bostick, B.C .; Михайлов, И .; Границы, М .; Huq, M. R .; Choudhury, I .; Rahman, M .; Schlosser, P .; Ахмед, К .; Ван Гин, А. (2011). «Миграция мышьяка в глубокие подземные воды в Бангладеш под влиянием адсорбции и потребности в воде». Природа Геонауки. 4 (11): 793–798. Bibcode:2011NatGe ... 4..793R. Дои:10.1038 / ngeo1283. ЧВК 3269239. PMID 22308168.
- ^ Явуз, Кафер Т .; Mayo, J. T .; Yu, W. W .; Пракаш, А .; Falkner, J.C .; Йен, С .; Cong, L .; Шипли, Х. Дж .; Кан, А .; Томсон, М .; Natelson, D .; Колвин, В. Л. (2005). «Низкопольное магнитное разделение монодисперсного Fe.3О4 Нанокристаллы ». Наука. 314 (5801): 964–967. Дои:10.1126 / science.1131475. PMID 17095696. S2CID 23522459.
- ^ Meliker, J. R .; Wahl, R.L .; Cameron, L.L .; Нриагу, Дж. О. (2007). «Мышьяк в питьевой воде и цереброваскулярные заболевания, сахарный диабет и заболевание почек в Мичигане: стандартизованный анализ коэффициента смертности». Состояние окружающей среды. 6: 4. Дои:10.1186 / 1476-069X-6-4. ЧВК 1797014. PMID 17274811.
- ^ Цзэн, Цзинь-Сяо; Тай, Тонг-Юань; Чонг, Чун-Хим; Цзэн, Цзин-Пин; Лай, Мэй-Шу; Lin, Boniface J .; Чиу, Хун-И; Сюэ, Ю-Мэй; Сюй, Куанг-Хун; Чен, К. Дж. (2000). «Долгосрочное воздействие мышьяка и заболеваемость инсулинозависимым сахарным диабетом: когортное исследование в деревнях с гиперэндемией арсениаза на Тайване». Перспективы гигиены окружающей среды. 108 (9): 847–51. Дои:10.1289 / ehp.00108847. ЧВК 2556925. PMID 11017889.
- ^ Газетная статья В архиве 17 апреля 2012 г. Wayback Machine (на венгерском языке) опубликовано Мадьяр Немзет 15 апреля 2012 г.
- ^ Геринг, П .; Апошиан, Х. В .; Mass, M.J .; Cebrián, M .; Beck, B.D .; Ваалкес, М. П. (1999). «Загадка канцерогенеза мышьяка: роль метаболизма». Токсикологические науки. 49 (1): 5–14. Дои:10.1093 / toxsci / 49.1.5. PMID 10367337.
- ^ Hopenhayn-Rich, C .; Biggs, M. L .; Smith, A.H .; Кальман, Д. А .; Мур, Л. Э. (1996). «Исследование метилирования населения, подвергающегося воздействию мышьяка в питьевой воде в окружающей среде». Перспективы гигиены окружающей среды. 104 (6): 620–628. Дои:10.1289 / ehp.96104620. ЧВК 1469390. PMID 8793350.
- ^ Smith, A.H .; Arroyo, A. P .; Mazumder, D. N .; Kosnett, M. J .; Эрнандес, А. Л .; Beeris, M .; Smith, M. M .; Мур, Л. Э. (2000). «Вызванные мышьяком поражения кожи у людей Атакаменьо в Северном Чили, несмотря на хорошее питание и столетия воздействия» (PDF). Перспективы гигиены окружающей среды. 108 (7): 617–620. Дои:10.1289 / ehp.00108617. ЧВК 1638201. PMID 10903614.
- ^ Eawag (2015) Справочник по геогенному загрязнению - Решение проблемы мышьяка и фторида в питьевой воде. C.A. Джонсон, А. Бретцлер (ред.), Швейцарский федеральный институт водных наук и технологий (Eawag), Дюбендорф, Швейцария. (загрузить: www.eawag.ch/en/research/humanwelfare/drinkingwater/wrq/geogenic-contamination-handbook/)
- ^ Амини М., Аббаспур К.К., Берг М., Винкель Л., Хуг С.Дж., Хоэн Э., Ян Х., Джонсон К.А. (2008). «Статистическое моделирование глобального геогенного загрязнения подземных вод мышьяком». Экологические науки и технологии. 42 (10): 3669–3675. Bibcode:2008EnST ... 42.3669A. Дои:10.1021 / es702859e. PMID 18546706.CS1 maint: несколько имен: список авторов (связь)
- ^ Винкель Л., Берг М., Амини М., Хуг С.Дж., Джонсон К.А. (2008). «Прогнозирование загрязнения мышьяком подземных вод в Юго-Восточной Азии по параметрам поверхности». Природа Геонауки. 1 (8): 536–542. Bibcode:2008NatGe ... 1..536Вт. Дои:10.1038 / ngeo254.CS1 maint: несколько имен: список авторов (связь)
- ^ Смедли, П. Л. (2002). «Обзор источника, поведения и распределения мышьяка в природных водах» (PDF). Прикладная геохимия. 17 (5): 517–568. Bibcode:2002ApGC ... 17..517S. Дои:10.1016 / S0883-2927 (02) 00018-5.
- ^ Как мышьяк попадает в грунтовые воды. Гражданской и экологической инженерии. Университет штата Мэн
- ^ Цзэн Чжаохуа, Чжан Чжилян (2002). «Образование элемента As в подземных водах и регулирующий фактор». Шанхайская геология 87 (3): 11–15.
- ^ Чжэн, Y; Stute, M; Ван Гин, А; Гавриэли, я; Дхар, Р; Симпсон, Х.Дж .; Schlosser, P; Ахмед, К.М. (2004). «Редокс-контроль мобилизации мышьяка в подземных водах Бангладеш». Прикладная геохимия. 19 (2): 201–214. Bibcode:2004ApGC ... 19..201Z. Дои:10.1016 / j.apgeochem.2003.09.007.
- ^ Томас, Мэри Энн (2007). «Связь мышьяка с окислительно-восстановительными условиями, глубиной и возрастом грунтовых вод в системе ледниковых водоносных горизонтов на севере Соединенных Штатов». Геологическая служба США, Вирджиния. С. 1–18.
- ^ Бин, Хонг (2006). «Влияние микробов на биогеохимию мышьякового механизма мобилизации мышьяка в подземных водах». Достижения в области наук о Земле. 21 (1): 77–82.
- ^ Джонсон, Д. Л; Пилсон, М. Э. К (1975). «Окисление арсенита в морской воде». Письма об окружающей среде. 8 (2): 157–171. Дои:10.1080/00139307509437429. PMID 236901.
- ^ Черри, Дж. А. (1979). «Виды мышьяка как индикатор окислительно-восстановительных условий в грунтовых водах». Современная гидрогеология - Мемориальный том Джорджа Берка Макси. Развитие науки о воде. 12. С. 373–392. Дои:10.1016 / S0167-5648 (09) 70027-9. ISBN 9780444418487.
- ^ Каллен, Уильям Р.; Реймер, Кеннет Дж (1989). «Видообразование мышьяка в окружающей среде». Химические обзоры. 89 (4): 713–764. Дои:10.1021 / cr00094a002. HDL:10214/2162.
- ^ Оремланд, Рональд С. (2000). «Бактериальное диссимиляционное восстановление арсената и сульфата в меромиктическом озере Моно, Калифорния». Geochimica et Cosmochimica Acta. 64 (18): 3073–3084. Bibcode:2000GeCoA..64.3073O. Дои:10.1016 / S0016-7037 (00) 00422-1.
- ^ Риз-младший, Роберт Г. "Товарные обзоры 2002: Мышьяк" (PDF). Геологическая служба США. В архиве (PDF) из оригинала 17 декабря 2008 г.. Получено 8 ноября 2008.
- ^ «Хромированный арсенат меди (ХАМ)». Агентство по охране окружающей среды США. 16 января 2014 г.. Получено 15 октября 2018.
- ^ «Безопасна ли сосна, обработанная CCA? - Хвойные породы». www.softwoods.com.au. Получено 24 февраля 2017.
- ^ Таунсенд, Тимоти Дж .; Соло-Габриэле, Елена (2 июня 2006 г.). Воздействие обработанной древесины на окружающую среду. CRC Press. ISBN 9781420006216.
- ^ Сакс, Дженнифер К .; Wannamaker, Эрик Дж .; Конклин, Скотт У .; Шупе, Тодд Ф .; Бек, Барбара Д. (1 января 2007 г.). «Оценка захоронения древесины, обработанной хромированным арсенатом меди (CCA), и потенциального воздействия на грунтовые воды: данные из Флориды». Атмосфера. 66 (3): 496–504. Bibcode:2007Чмсп..66..496С. Дои:10.1016 / j.chemosphere.2006.05.063. PMID 16870233.
- ^ BuildingOnline. "Удаление обработанной древесины CCA | Научный совет по консервантам древесины | Цель, обоснованность, научный анализ CCA". www.woodpreservativescience.org. Получено 16 июн 2016.
- ^ "Карта релизов TRI". Toxmap.nlm.nih.gov. Архивировано из оригинал 20 марта 2010 г.. Получено 23 марта 2010.
- ^ TOXNET - Базы данных по токсикологии, опасным химическим веществам, здоровью окружающей среды и выбросам токсичных веществ. Toxnet.nlm.nih.gov. Проверено 24 октября 2011.
- ^ Jain, C.K .; Сингх Р. Д. (2012). «Технологические варианты удаления мышьяка с особым акцентом на Юго-Восточную Азию». Журнал экологического менеджмента. 107: 1–8. Дои:10.1016 / j.jenvman.2012.04.016. PMID 22579769.
- ^ Геринг, П. (2013). «Биовосстановление воды, загрязненной мышьяком: последние достижения и перспективы на будущее». Загрязнение воды, воздуха и почвы. 224 (12): 1722. Bibcode:2013WASP..224.1722B. Дои:10.1007 / s11270-013-1722-y. S2CID 97563539.
- ^ Геринг, П. (2015). «Анаэробное окисление арсенита с электродом, выступающим в качестве единственного акцептора электронов: новый подход к биологической очистке грунтовых вод, загрязненных мышьяком». Журнал опасных материалов. 283: 617–622. Дои:10.1016 / j.jhazmat.2014.10.014. HDL:10256/11522. PMID 25464303.
- ^ «Мышьяк». Сигма Олдрич. 15 октября 2018 г.. Получено 15 октября 2018.
- ^ Правило мышьяка. НАС. Агентство по охране окружающей среды. Принято 22 января 2001 г .; вступает в силу 23 января 2006 г.
- ^ а б c «Вспомогательный документ об уровне действия мышьяка в яблочном соке». Fda.gov. Получено 21 августа 2013.
- ^ "Справочник домовладельца по мышьяку в питьевой воде". Департамент охраны окружающей среды Нью-Джерси. Получено 21 августа 2013.
- ^ Карманный справочник NIOSH по химической опасности. "#0038". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Карманный справочник NIOSH по химической опасности. "#0039". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Общее исследование диеты и Программа токсичных элементов
- ^ Коц, Дебора (14 сентября 2011 г.). «Есть ли в яблочном соке небезопасный уровень мышьяка? - The Boston Globe». Boston.com. Получено 21 августа 2013.
- ^ Морран, Крис. «Исследование, посвященное отчетам потребителей, обнаруживает высокий уровень мышьяка и свинца в некоторых фруктовых соках». Consumerist.com.
- ^ «Загрязнение мышьяком почв рисовых полей Бангладеш: влияние риса на потребление мышьяка: Nature News». Nature.com. 22 ноября 2002 г.. Получено 21 августа 2013.
- ^ «Загрязненные колодцы выливают мышьяк на продовольственные культуры». Новый ученый. 6 декабря 2002 г.. Получено 21 августа 2013.
- ^ Пеплоу, Марк (2 августа 2005 г.). «Американский рис может нести бремя мышьяка». Новости природы. Дои:10.1038 / news050801-5.
- ^ «Рис как источник воздействия мышьяка».
- ^ «EHP - Потребление риса и концентрация мышьяка в моче у детей в США». Ehp.niehs.nih.gov. Архивировано из оригинал 12 ноября 2014 г.. Получено 21 августа 2013.
- ^ «Высокий уровень мышьяка в рисе». ЭНЕРГЕТИЧЕСКИЙ ЯДЕРНЫЙ РЕАКТОР. 2 марта 2012 г.. Получено 21 августа 2013.
- ^ а б c "Мышьяк в вашей пище | Расследование сообщений потребителей". Consumerreports.org. 1 ноября 2012 г.. Получено 21 августа 2013.
- ^ Законодатели призывают FDA действовать в соответствии со стандартами мышьяка. Foodsafetynews.com (24 февраля 2012 г.). Проверено 23 мая 2012.
- ^ «FDA ищет ответы на вопрос о мышьяке в рисе». Fda.gov. 19 сентября 2012 г.. Получено 21 августа 2013.
- ^ «Мышьяк в рисе». Fda.gov. Получено 21 августа 2013.
- ^ «Вопросы и ответы: анализ мышьяка в рисе и рисовых продуктах FDA». Fda.gov. 21 марта 2013 г.. Получено 21 августа 2013.
- ^ а б «Мышьяк в рисе: что нужно знать». Калифорнийский университет в Беркли Велнес. Получено 3 сентября 2014.
- ^ «Мышьяк». RTECS. Национальный институт охраны труда и здоровья (NIOSH).
- ^ Корейское агентство по охране труда и технике безопасности В архиве 23 января 2017 г. Wayback Machine. kosha.or.kr
- ^ КОША ГИД H-120-2013. naver.com
- ^ а б Хьюз, Майкл Ф. (2002). «Токсичность мышьяка и возможные механизмы действия». Письма токсикологии. 133 (1): 1–16. Дои:10.1016 / S0378-4274 (02) 00084-X. PMID 12076506.
- ^ «OSHA Мышьяк». Администрация США по охране труда. В архиве из оригинала 12 октября 2007 г.. Получено 8 октября 2007.
- ^ Croal, Laura R .; Гралник, Джеффри А .; Маласарн, Давин; Ньюман, Дайан К. (2004). «Генетика геохимии». Ежегодный обзор генетики. 38: 175–206. Дои:10.1146 / annurev.genet.38.072902.091138. PMID 15568975.
- ^ Джаннини, А. Джеймс; Блэк, Генри Ричард; Гетче, Роджер Л. (1978). Справочник по психиатрическим, психогенным и соматопсихическим расстройствам. Нью-Гайд-Парк, штат Нью-Йорк: издательство Medical Examination Publishing Co., стр. 81–82. ISBN 978-0-87488-596-5.
- ^ Руководство по токсичности мышьяка (2007). Агентство США по регистрации токсичных веществ и заболеваний.
Библиография
- Эмсли, Джон (2011). «Мышьяк». Строительные блоки природы: руководство по элементам от А до Я. Оксфорд, Англия, Великобритания: Издательство Оксфордского университета. С. 47–55. ISBN 978-0-19-960563-7.
- Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- Ривертс, Джон (2015). Элементы загрязнения окружающей среды. Абингдон и Нью-Йорк, Рутледж. ISBN 978-0-41-585920-2.
дальнейшее чтение
- Джеймс Дж. Уортон (2011). Мышьяк век. Издательство Оксфордского университета. ISBN 978-0-19-960599-6.
внешняя ссылка
- Страница CTD по мышьяку и Страница CTD по мышьякам от База данных сравнительной токсикогеномики
- Отравление мышьяком: общие аспекты и хелатирующие агенты, к Гейр Бьёрклунд, Массимилиано Пеана и другие. Архивы токсикологии (2020) 94: 1879–1897.
- Небольшая доза токсикологии
- Мышьяк в грунтовых водах Книга о мышьяке в подземных водах IAH Нидерландское отделение и Нидерландское гидрологическое общество
- Фокус загрязнения: мышьяк посредством EPA.
- Критерии гигиены окружающей среды для мышьяка и соединений мышьяка, 2001 г. посредством ВОЗ.
- Капай, Саймон; Петерсон, Ганс; Либер, Карстен; Бхаттачарья, Просун (2006). «Влияние хронического отравления мышьяком на здоровье человека - обзор». Журнал экологической науки и здоровья, часть A. 41 (10): 2399–2428. Дои:10.1080/10934520600873571. PMID 17018421. S2CID 4659770.
- Национальный институт охраны труда и здоровья - страница Arsenic
- Мышьяк в Периодическая таблица видео (Ноттингемский университет)


