Никель - Nickel
 | |||||||||||||||||||||||||||||||||||||||||
| Никель | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Внешность | блестящий, металлический и серебристый с золотым оттенком | ||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес Аr, std(Ni) | 58.6934(4)[1] | ||||||||||||||||||||||||||||||||||||||||
| Никель в периодическая таблица | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Атомный номер (Z) | 28 | ||||||||||||||||||||||||||||||||||||||||
| Группа | группа 10 | ||||||||||||||||||||||||||||||||||||||||
| Период | период 4 | ||||||||||||||||||||||||||||||||||||||||
| Блокировать | d-блок | ||||||||||||||||||||||||||||||||||||||||
| Категория элемента | Переходный металл | ||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [Ar ] 3d8 4 с2 или же [Ar] 3d9 4 с1 | ||||||||||||||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 16, 2 или же 2, 8, 17, 1 | ||||||||||||||||||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||||||||||||||||||
| Фаза вSTP | твердый | ||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 1728 K (1455 ° С, 2651 ° F) | ||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 3003 К (2730 ° С, 4946 ° F) | ||||||||||||||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | 8,908 г / см3 | ||||||||||||||||||||||||||||||||||||||||
| в жидком состоянии (приm.p.) | 7,81 г / см3 | ||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 17.48 кДж / моль | ||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 379 кДж / моль | ||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 26,07 Дж / (моль · К) | ||||||||||||||||||||||||||||||||||||||||
Давление газа
| |||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||||||||||||||||||||||
| Состояния окисления | −2, −1, 0, +1,[2] +2, +3, +4[3] (мягко базовый окись) | ||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,91 | ||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||||||||||||||||||||||
| Радиус атома | эмпирические: 124вечера | ||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 124 ± 16 часов | ||||||||||||||||||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 163 вечера | ||||||||||||||||||||||||||||||||||||||||
| Другие свойства | |||||||||||||||||||||||||||||||||||||||||
| Естественное явление | изначальный | ||||||||||||||||||||||||||||||||||||||||
| Кристальная структура | гранецентрированная кубическая (fcc) | ||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкий стержень | 4900 м / с (приr.t.) | ||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 13,4 мкм / (м · К) (при 25 ° C) | ||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 90,9 Вт / (м · К) | ||||||||||||||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 69,3 нОм · м (при 20 ° C) | ||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | ферромагнитный | ||||||||||||||||||||||||||||||||||||||||
| Модуль для младших | 200 ГПа | ||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 76 ГПа | ||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 180 ГПа | ||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.31 | ||||||||||||||||||||||||||||||||||||||||
| Твердость по Моосу | 4.0 | ||||||||||||||||||||||||||||||||||||||||
| Твердость по Виккерсу | 638 МПа | ||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 667–1600 МПа | ||||||||||||||||||||||||||||||||||||||||
| Количество CAS | 7440-02-0 | ||||||||||||||||||||||||||||||||||||||||
| История | |||||||||||||||||||||||||||||||||||||||||
| Открытие и первая изоляция | Аксель Фредрик Кронштедт (1751) | ||||||||||||||||||||||||||||||||||||||||
| Главный изотопы никеля | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
Никель это химический элемент с символ Ni и атомный номер 28. Это серебристо-белый блестящий металл с легким золотистым оттенком. Никель относится к переходные металлы и тяжело и пластичный. Чистый никель, порошкообразный для максимизации реактивного площадь поверхности, проявляет значительную химическую активность, но более крупные куски медленно реагируют с воздухом под стандартные условия потому что на поверхности образуется оксидный слой, предотвращающий дальнейшую коррозию (пассивация ). Тем не менее, чистый родные никель находится в земной коре лишь в незначительных количествах, обычно в ультраосновные породы,[4][5] а в интерьерах больших никель-железные метеориты которые не подвергались воздействию кислорода вне атмосферы Земли.
Метеорный никель встречается в сочетании с утюг, отражение происхождения этих элементов как основных конечных продуктов нуклеосинтез сверхновой. Считается, что смесь железа и никеля составляет Внешний и внутренние ядра.[6]
Использование никеля (как натурального метеоритный никель-железный сплав) восходит к 3500 г. до н.э. Никель был впервые выделен и классифицирован как химический элемент в 1751 г. Аксель Фредрик Кронштедт, который изначально ошибочно принял руда для медь минеральная, на кобальтовых рудниках Лос, Хельсингланд, Швеция. Название элемента происходит от озорного спрайта из немецкой шахтерской мифологии, Никеля (похожего на Старый Ник ), олицетворявшего тот факт, что медно-никелевые руды сопротивляются переработке в медь. Экономически важным источником никеля является утюг руда лимонит, который часто содержит 1–2% никеля. К другим важным рудным минералам никеля относятся: пентландит и смесь богатых никелем природных силикатов, известных как гарниерит. Основные производственные площадки включают Садбери регион в Канада (который считается метеоритный источник), Новая Каледония в Тихий океан, и Норильск в Россия.
Никель медленно окисленный воздухом при комнатной температуре и считается устойчивым к коррозии. Исторически он использовался для покрытия железа и латунь, оборудование для нанесения покрытий и производство определенных сплавы которые сохраняют высокий серебристый блеск, например Немецкое серебро. Около 9% мирового производства никеля по-прежнему используется для антикоррозийного никелирования. Никелированные предметы иногда провоцируют аллергия на никель. Никель широко используется в монеты, хотя его растущая цена привела к некоторой замене его более дешевыми металлами в последние годы.
Никель - один из четырех элементов (остальные утюг, кобальт, и гадолиний )[7] которые ферромагнитный примерно при комнатной температуре. Алнико постоянный магниты частично на основе никеля имеют промежуточную прочность между постоянными магнитами на основе железа и редкоземельные магниты. В наше время металл ценен главным образом в сплавы; Около 68% мирового производства используется в производстве нержавеющей стали. Еще 10% используется для сплавов на основе никеля и меди, 7% - для легированных сталей, 3% - для литья, 9% - для гальваники и 4% - для других применений, включая быстрорастущий сектор аккумуляторных батарей,[8] в том числе в электрические транспортные средства (Электромобили).[9] В качестве соединения никель находит применение в различных нишах в химической промышленности, например в катализатор гидрирования, катоды для батарей, пигментов и обработки металлических поверхностей.[10] Никель является важным питательным веществом для некоторых микроорганизмов и растений, ферменты с никелем в качестве активный сайт.[11]
Характеристики
Атомно-физические свойства

Никель - это серебристо-белый металл с легким золотистым оттенком, который требует полировки. Это один из четырех элементов, которые обладают магнитными свойствами при комнатной температуре или близкой к ней, а остальные - железо. кобальт и гадолиний. Его Температура Кюри составляет 355 ° C (671 ° F), что означает, что объемный никель немагнитен выше этой температуры.[13] Элементарная ячейка никеля представляет собой гранецентрированный куб с параметром решетки 0,352 нм, что дает радиус атома 0,124 нм. Эта кристаллическая структура устойчива к давлению не менее 70 ГПа. Никель относится к переходным металлам. Он жесткий, податливый и пластичный, и имеет относительно высокий электрические и теплопроводность для переходных металлов.[14] Высота прочность на сжатие 34 ГПа, предсказанное для идеальных кристаллов, никогда не достигается в реальном массивном материале из-за образования и движения вывихи. Однако это было достигнуто в Ni наночастицы.[15]
Спор о конфигурации электронов
У атома никеля два электронные конфигурации, [Ar] 3d8 4 с2 и [Ar] 3d9 4 с1, которые очень близки по энергии - символ [Ar] относится к аргон -подобная структура ядра. Есть некоторые разногласия по поводу того, какая конфигурация имеет наименьшую энергию.[16] В учебниках химии электронная конфигурация никеля цитируется как [Ar] 4s.2 3D8,[17] что также может быть записано [Ar] 3d8 4 с2.[18] Эта конфигурация согласуется с Правило заказа энергии Маделунга, который предсказывает, что 4s заполняются раньше 3d. Это подтверждается экспериментальным фактом, что самое низкоэнергетическое состояние атома никеля - это 3d8 4 с2 уровень энергии, в частности 3d8(3F) 4 с2 3F, J = 4 уровень.[19]
Однако каждая из этих двух конфигураций распадается на несколько уровней энергии из-за тонкая структура,[19] и два набора энергетических уровней перекрываются. Средняя энергия состояний с конфигурацией [Ar] 3d9 4 с1 фактически ниже средней энергии состояний с конфигурацией [Ar] 3d8 4 с2. По этой причине в исследовательской литературе по атомным расчетам конфигурация основного состояния никеля цитируется как [Ar] 3d9 4 с1.[16]
Изотопы
Изотопы никеля варьируются в атомный вес от 48ты (48
Ni) до 78 ед. (78
Ni).
Природный никель состоит из пяти стабильных изотопы; 58
Ni, 60
Ni, 61
Ni, 62
Ni и 64
Ni, с 58
Ni самая многочисленная (68,077% природное изобилие ).
Никель-62 имеет наивысшее среднее энергия связи ядра на нуклон любого нуклид, при 8,7946 МэВ / нуклон.[20] [21] Его энергия связи больше, чем у обоих 56
Fe и 58
Fe, более распространенные элементы часто ошибочно упоминаются как имеющие наиболее прочно связанные нуклиды.[22] Хотя это, казалось бы, предсказывает, что никель-62 является самым распространенным тяжелым элементом во Вселенной, относительно высокая скорость фотодезинтеграция Из-за никеля в недрах звезд железо является самым распространенным.[22]
Стабильный изотоп никель-60 является дочерним продуктом потухший радионуклид 60
Fe, который распадается с периодом полураспада 2,6 миллиона лет. Потому что 60
Fe имеет такой длительный период полураспада, его стойкость в материалах в Солнечная система может генерировать наблюдаемые изменения в изотопном составе 60
Ni. Поэтому обилие 60
Ni присутствие во внеземном материале может дать представление о происхождении Солнечной системы и ее ранней истории.[нужна цитата ]
Не менее 26 никель радиоизотопы охарактеризованы, наиболее стабильное существо 59
Ni с период полураспада 76000 лет, 63
Ni со 100 лет, и 56
Ni с 6 дней. Все остальные радиоактивный изотопы имеют период полураспада менее 60 часов, а у большинства изотопов период полураспада менее 30 секунд. Этот элемент также имеет один мета-состояние.[23]
Радиоактивный никель-56 производится на заводе процесс горения кремния и позже выпущен в большом количестве во время тип Ia сверхновые. Форма кривая блеска этих сверхновых на промежуточных и поздних временах соответствует распаду через захват электронов никеля-56 в кобальт -56 и в конечном итоге до железа-56.[24] Никель-59 - долгожитель космогенный радионуклид с периодом полураспада 76000 лет. 59
Ni нашла множество приложений в изотопная геология. 59
Ni использовался для датирования земного возраста метеориты и определить содержание внеземной пыли во льду и осадок. Период полураспада никеля-78 был недавно измерен в 110 миллисекунд, и он считается важным изотопом в нуклеосинтез сверхновой элементов тяжелее железа.[25] Нуклид 48Ni, открытый в 1999 году, является самым богатым протонами изотопом тяжелых элементов из известных. С 28 протоны и 20 нейтроны, 48Ni "вдвойне магия ", как есть 78
Ni с 28 протонами и 50 нейтронами. Поэтому оба они необычайно стабильны для нуклидов с таким большим протон-нейтронный дисбаланс.[23][26]
Вхождение

На Земле никель чаще всего встречается в сочетании с сера и утюжить пентландит, с сера в миллерит, с мышьяк в минерале никелин, а с мышьяком и сера в никеле галенит.[27] Никель обычно содержится в железные метеориты как сплавы камасит и тенит. Присутствие никеля в метеоритах было впервые обнаружено в 1799 г. Жозеф-Луи Пруст, французский химик, работавший тогда в Испании. Пруст проанализировал образцы метеорита из Кампо-дель-Сьело (Аргентина), которые были получены в 1783 году Мигелем Рубином де Селисом, обнаружив в них присутствие никеля (около 10%) наряду с железом.[28]
Основная часть никеля составляет добыт из двух типов руда депозиты. Первый латерит, где основные рудно-минеральные смеси никелевые лимонит, (Fe, Ni) O (OH) и гарниерит (смесь различного водного никеля и богатых никелем силикатов). Второй - магматический сульфид месторождения, где основной рудный минерал пентландит: (Ni, Fe)
9S
8.[нужна цитата ]
Индонезия и Австралия имеют самые большие оценочные запасы, составляющие 46% от мировых.[29]
Выявленные наземные ресурсы во всем мире, содержащие в среднем 1% никеля или больше, содержат не менее 130 миллионов тонн никеля (примерно вдвое больше известных запасов). Около 60% находится в латериты и 40% в сульфидных месторождениях.[30]
На геофизический доказательств, считается, что большая часть никеля на Земле находится в внешний и внутренние ядра. Камасит и тенит встречаются в природе сплавы железа и никеля. Для камасита содержание сплава обычно составляет от 90:10 до 95: 5, хотя примеси (такие как кобальт или же углерод ), в то время как для тенита содержание никеля составляет от 20% до 65%. Камасит и тенит также встречаются в никель-железные метеориты.[31]
Соединения
Самый распространенный степень окисления никеля +2, а соединения Ni0, Ni+, а Ni3+ хорошо известны, а экзотические степени окисления Ni2−, Ni1−, а Ni4+ были произведены и изучены.[32]
Никель (0)

Тетракарбонил никеля (Ni (CO)
4), открытый Людвиг Монд,[33] представляет собой летучую высокотоксичную жидкость при комнатной температуре. При нагревании комплекс снова разлагается на никель и окись углерода:
- Ni (CO)
4 ⇌ Ni + 4 CO
Это поведение используется в Мондовский процесс для очистки никеля, как описано выше. Родственный комплекс никеля (0) бис (циклооктадиен) никель (0) является полезным катализатором в никельорганическая химия поскольку циклооктадиен (или же треска) лиганды легко вытесняются.
Никель (I)

2(CN)
6]4−
ион[34]
Комплексы никеля (I) встречаются редко, но одним из примеров является тетраэдрический комплекс NiBr (PPh3)3. Многие комплексы никеля (I) имеют связи Ni-Ni, например темно-красный диамагнитный K
4[Ni
2(CN)
6] подготовлен сокращением K
2[Ni
2(CN)
6] с амальгама натрия. Это соединение окисляется в воде, высвобождая ЧАС
2.[34]
Считается, что степень окисления никеля (I) важна для никельсодержащих ферментов, таких как [NiFe] -гидрогеназа, который катализирует обратимое восстановление протоны к ЧАС
2.[35]
Никель (II)

3)
6]2+
, [Ni (C2ЧАС4(NH2)2 )]2+, [NiCl
4]2−
, [Национальные институты здравоохранения США
2O)
6]2+

Никель (II) образует соединения со всеми распространенными анионами, включая сульфид, сульфат, карбонат, гидроксид, карбоксилаты и галогениды. Сульфат никеля (II) производится в больших количествах путем растворения металлического никеля или оксидов в серной кислоте с образованием гекса- и гептагидратов.[36] полезный для гальваника никель. Обычные соли никеля, такие как хлорид, нитрат и сульфат, растворяются в воде с образованием зеленых растворов металл aquo комплекс [Национальные институты здравоохранения США
2O)
6]2+
.
Четыре галогенида образуют соединения никеля, которые представляют собой твердые тела с молекулами, имеющими октаэдрические центры Ni. Никель (II) хлорид является наиболее распространенным, и его поведение иллюстрирует другие галогениды. Хлорид никеля (II) получают путем растворения никеля или его оксида в соляная кислота. Обычно встречается как зеленый гексагидрат, формула которого обычно записывается как NiCl2• 6H2О. При растворении в воде эта соль образует металл aquo комплекс [Национальные институты здравоохранения США
2O)
6]2+
. Обезвоживание NiCl2• 6H2O дает желтый безводный NiCl
2.
Некоторые четырехкоординатные комплексы никеля (II), например бис (трифенилфосфин) хлорид никеля, существуют как в тетраэдрической, так и в плоской квадратной геометрии. Тетраэдрические комплексы парамагнитный, а плоские квадратные комплексы диамагнитный. Обладая свойствами магнитного равновесия и образования октаэдрических комплексов, они контрастируют с двухвалентными комплексами более тяжелых металлов 10 группы, палладия (II) и платины (II), которые образуют только квадратно-плоскую геометрию.[32]
Никелоцен известен; у него есть счет электронов из 20, что делает его относительно нестабильным.
Никель (III) и (IV)

Известны многочисленные соединения Ni (III), первыми такими примерами являются тригалофосфины никеля (III) (NiIII(PPh3)ИКС3).[37] Кроме того, Ni (III) образует простые соли с фторидом[38] или же окись ионы. Ni (III) может быть стабилизирован σ-донорными лигандами, такими как тиолы и фосфины.[34]
Ni (IV) присутствует в смешанном оксиде BaNiO
3, а Ni (III) присутствует в гидроксид никеля, который используется как катод во многих перезаряжаемые батарейки, включая никель-кадмиевый, никель-железо, никель водород, и никель-металлогидрид, и используется некоторыми производителями в Литий-ионный батареи.[39] Ni (IV) остается редкой степенью окисления никеля, и на сегодняшний день известно очень мало соединений.[40][41][42][43]
История
Поскольку руды никеля легко спутать с рудами серебра, понимание этого металла и его использования датируется относительно недавним временем. Тем не менее, непреднамеренное использование никеля является древним, и его можно проследить до 3500 г. до н.э. Бронзы на территории современной Сирии было обнаружено 2% никеля.[44] Некоторые древние китайские рукописи предполагают, что «белая медь» (мельхиор, известный как Байтонг) использовался там между 1700 и 1400 гг. до н. э. Эта белая медь из Пактонга была экспортирована в Великобританию еще в 17 веке, но содержание никеля в этом сплаве не было обнаружено до 1822 года.[45] Монеты из медно-никелевого сплава чеканили бактрийские короли. Агафокл, Евтидем II, и Панталеон во II веке до нашей эры, возможно, из китайского мельхиора.[46]

В средневековой Германии красный минерал был найден в Эрцгебирге (Рудные горы), напоминавшие медную руду. Однако, когда горняки не смогли извлечь из него медь, они обвинили в этом вредного спрайта немецкой мифологии Никель (похожий на Старый Ник ), чтобы окружить медь. Они назвали эту руду Купферникель из немецкого Купфер для меди.[47][48][49][50] Эта руда теперь известна как никелин, никель арсенид. В 1751 году барон Аксель Фредрик Кронштедт пытался извлечь медь из купферникеля на кобальт мой в Шведский деревня Лос, и вместо этого произвел белый металл, который он назвал в честь духа, давшего название минералу, никель.[51] В современном немецком языке купферникель или купфер-никель обозначают сплав. мельхиор.[14]
Первоначально единственным источником никеля был редкий купферникель. Начиная с 1824 г., никель был получен как побочный продукт синий кобальт производство. Первая крупномасштабная выплавка никеля началась в Норвегии в 1848 году из богатых никелем пирротин. Введение никеля в производство стали в 1889 г. увеличило спрос на никель, и никелевые месторождения Новая Каледония, открытый в 1865 году, обеспечил большую часть мировых запасов в период с 1875 по 1915 год. Открытие крупных месторождений в Бассейн Садбери, Канада в 1883 г., в Норильск-Талнах, Россия в 1920 г., а в Меренский риф Южная Африка в 1924 году сделала возможным крупномасштабное производство никеля.[45]
Чеканка

За исключением вышеупомянутых бактрийских монет, никель не входил в состав монет до середины XIX века.
Канада
99,9% никелевые монеты по пять центов были поражены в Канаде (крупнейшем в мире производителе никеля в то время) в невоенные годы с 1922 по 1981 год; содержание металла сделало эти монеты магнитными.[52] В период военного времени 1942–45 никель был удален из канадских и американских монет, чтобы сохранить его для производства брони.[48][53] С 1968 года Канада использовала 99,9% никеля в своих дорогостоящих монетах до 2000 года.
Швейцария
Монеты из почти чистого никеля впервые были использованы в 1881 году в Швейцарии.[54]
объединенное Королевство
Бирмингем подделал никелевые монеты в c. 1833 для торговли в Малайе.[55]
Соединенные Штаты
В Соединенных Штатах термин «никель» или «никель» первоначально применялся к медно-никелевым продуктам. Летающий орел цент, который заменил медь на 12% никеля 1857–58, затем Индийская голова цент того же сплава с 1859 по 1864 год. Еще позже, в 1865 году, термин обозначал трехцентовый никель, с никелем увеличилась до 25%. В 1866 г. пятицентовая защитная никель (25% никеля, 75% меди) присвоили это обозначение. Наряду с пропорцией сплава этот термин используется до сих пор в Соединенных Штатах.
Текущее использование
В 21 веке высокая цена на никель привела к некоторой замене металла в монетах по всему миру. Монеты, все еще изготовленные из никелевых сплавов, бывают одно- и двух-евро монеты, 5 ¢, 10 50, 25 и 50 ¢ Монеты США и 20 пенсов, 50 пенсов, 1 фунт стерлингов и 2 фунта стерлингов Монеты Великобритании. Никелевый сплав в британских монетах номиналом 5 и 10 пенсов был заменен на никелированную сталь с 2012 года, что вызвало у некоторых людей проблемы с аллергией и вызвало общественные споры.[54]
Мировое производство
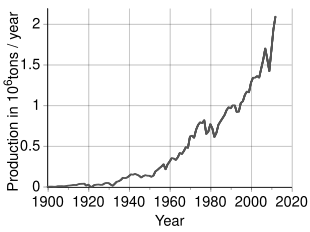

По оценкам, во всем мире добывается более 2,7 миллионов тонн (т) никеля в год, причем Индонезия (800000 т), Филиппины (420 000 т),[57] Россия (270 000 т), Новая Каледония (220 000 т), Австралия (180 000 т) и Канада (180000 т) - крупнейшие производители по состоянию на 2019 год.[58] Крупнейшие месторождения никеля за пределами России расположены в г. Финляндия и Греция. Выявленные наземные ресурсы, содержащие в среднем 1% никеля или более, содержат не менее 130 миллионов тонн никеля. Примерно 60% находится в латеритах и 40% - в сульфидных месторождениях. Кроме того, обширные глубоководные ресурсы никеля находятся в марганцевых корках и конкрециях, покрывающих большие площади дна океана, особенно в Тихом океане.[59]
Единственное место в Соединенных Штатах, где добыча никеля рентабельна, - это Риддл, Орегон, где несколько квадратных миль никельсодержащих гарниерит расположены поверхностные отложения. Шахта закрылась в 1987 году.[60][61] В Проект шахты орла это новый никелевый рудник в Мичиган с верхний полуостров. Строительство было завершено в 2013 году, а эксплуатация началась в третьем квартале 2014 года.[62] За первый полный год эксплуатации на руднике Игл было добыто 18 000 тонн.[62]
Экстракция и очистка
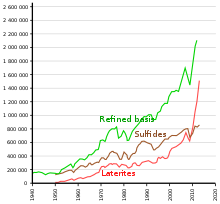
Никель получают через добывающая металлургия: он извлекается из руды обычными процессами обжига и восстановления, которые дают металл чистотой более 75%. Во многих нержавеющая сталь В зависимости от примесей можно использовать никель с чистотой 75% без дополнительной очистки.
Традиционно большая часть сульфидных руд перерабатывалась с использованием пирометаллургический методы для создания матовый для дальнейшей доработки. Последние достижения в гидрометаллургическая техника привело к значительно более чистому продукту из металлического никеля. Большинство сульфидных месторождений традиционно обрабатывались путем обогащения через пенная флотация процесс, за которым следует пирометаллургический добыча. В гидрометаллургических процессах сульфидные никелевые руды концентрируются путем флотации (дифференциальная флотация, если соотношение Ni / Fe слишком низкое), а затем плавятся. Никелевый штейн дополнительно обрабатывается Процесс Шерритта-Гордона. Сначала удаляют медь, добавляя сероводород, оставляя концентрат кобальта и никеля. Затем для разделения кобальта и никеля используется экстракция растворителем, при этом конечное содержание никеля превышает 99%.

Электрорафинирование
Второй распространенный процесс рафинирования - это выщелачивание металлического штейна в раствор соли никеля с последующим электролитическим извлечением никеля из раствора путем нанесения его на катод в качестве электролитического никеля.
Мондовский процесс

Самый чистый металл получают из оксида никеля Мондовский процесс, который достигает чистоты более 99,99%.[63] Процесс был запатентован Людвигом Мондом и использовался в промышленности еще до начала 20-го века. В этом процессе никель реагирует с монооксид углерода в присутствии серного катализатора при температуре около 40–80 ° C с образованием карбонил никеля. Железо дает пентакарбонил железа тоже, но эта реакция медленная. При необходимости никель можно отделить перегонкой. Дикобальт октакарбонил также образуется при перегонке никеля в качестве побочного продукта, но разлагается до тетракобальт додекакарбонил при температуре реакции с получением нелетучего твердого вещества.[64]
Никель получают из карбонила никеля одним из двух способов. Его можно пропускать через большую камеру при высоких температурах, в которой постоянно перемешиваются десятки тысяч никелевых сфер, называемых гранулами. Карбонил разлагается и осаждает чистый никель на никелевых сферах. В альтернативном процессе карбонил никеля разлагается в меньшей камере при 230 ° C с образованием мелкодисперсного никелевого порошка. Окись углерода как побочный продукт рециркулируется и используется повторно. Продукт из высокочистого никеля известен как «карбонильный никель».[65]
Ценность металла
Рыночная цена на никель росла в течение 2006 года и в первые месяцы 2007 года; по состоянию на 5 апреля 2007 года металл торговался по нас $52,300/тонна или 1,47 доллара за унцию.[66] Впоследствии цена резко упала, и по состоянию на сентябрь 2017 года металл торговался по цене 11000 долларов за тонну, или 0,31 доллара за унцию.[67]
В Никелевая монета США содержит 0,04 унции (1,1 г) никеля, который по цене апреля 2007 года стоил 6,5 цента, а также 3,75 грамма меди стоимостью около 3 центов, при общей стоимости металла более 9 центов. Поскольку номинальная стоимость никеля составляет 5 центов, это сделало его привлекательной целью для плавки для людей, желающих продать металлы с прибылью. Тем не менее Монетный двор США, предвидя эту практику, 14 декабря 2006 г. ввели новые временные правила, подлежащие общественному обсуждению в течение 30 дней, которые криминализировали плавку и экспорт центов и никеля.[68] Нарушители могут быть наказаны штрафом до 10 000 долларов и / или лишены свободы на срок до пяти лет.
По состоянию на 19 сентября 2013 г. стоимость плавки американского никеля (включая медь и никель) составляет 0,045 доллара США, что составляет 90% от номинальной стоимости.[69]
Приложения

В настоящее время мировое производство никеля используется следующим образом: 68% производится из нержавеющей стали; 10% в цветных металлах сплавы; 9% в гальваника; 7% в легированной стали; 3% в литейных цехах; и 4% других видов использования (включая батареи).[8]
Никель используется во многих конкретных и узнаваемых промышленных и потребительских товарах, в том числе нержавеющая сталь, алнико магниты, чеканка, перезаряжаемые батарейки, струны электрогитары, капсюли микрофонов, обшивка сантехники,[70] и специальные сплавы, такие как пермаллой, Элинвар, и инвар. Используется для гальваники и как зеленый оттенок в стекле. Никель является преимущественно легируемым металлом, и его основное применение - в никелевых сталях и никелевых чугунах, где он обычно увеличивает предел прочности на разрыв, ударную вязкость и предел упругости. Он широко используется во многих других сплавах, включая никелевые латуни и бронзы, а также сплавы с медью, хромом, алюминием, свинцом, кобальтом, серебром и золотом (Инконель, Инколой, Монель, Нимоник ).[71]

Поскольку никель устойчив к коррозии, он иногда использовался вместо декоративного серебра. Никель также иногда использовался в некоторых странах после 1859 года в качестве дешевого металла для чеканки монет (см. Выше), но в последние годы 20 века его заменили более дешевым металлом. нержавеющая сталь (т.е. железные) сплавы, за исключением США и Канады.
Никель является отличным легирующим агентом для некоторых драгоценных металлов и используется в пробирный огонь как коллекционер элементы платиновой группы (PGE). Таким образом, никель способен полностью собирать все шесть элементов ЭПГ из руд и частично собирать золото. Никелевые рудники с высокой производительностью могут также заниматься извлечением ЭПГ (в первую очередь платина и палладий ); примерами являются Норильск в России и бассейн Садбери в Канаде.
Пена никель или никелевая сетка используется в газодиффузионные электроды за щелочные топливные элементы.[72][73]
Никель и его сплавы часто используются в качестве катализаторов гидрирование реакции. Никель Ренея тонкоизмельченный никель-алюминиевый сплав является одной из распространенных форм, хотя также используются родственные катализаторы, включая катализаторы типа Ренея.
Никель является природным магнитострикционным материалом, а это означает, что в присутствии магнитное поле материал претерпевает небольшое изменение длины.[74][75] В магнитострикция никеля составляет порядка 50 частей на миллион и имеет отрицательное значение, что указывает на его сокращение.
Никель используется в качестве связующего в цементированных карбид вольфрама или в твердосплавной промышленности и используются в пропорциях от 6% до 12% по весу. Никель делает карбид вольфрама магнитным и повышает коррозионную стойкость склеиваемых деталей, хотя твердость меньше, чем у кобальтовых связок.[76]
63
Ni, с этими период полураспада 100,1 года, полезен в Критрон устройства как бета-частица (высокоскоростной электрон ) эмиттер сделать ионизация с помощью поддерживающего электрода надежнее.[77]
Около 27% всего производства никеля предназначено для машиностроения, 10% - для строительства, 14% - для трубных изделий, 20% - для металлических изделий, 14% - для транспорта, 11% - для электронных товаров и 5% - для других целей.[8]
Никель Ренея широко используется для гидрирование из ненасыщенный масла сделать маргарин, а некачественный маргарин и остатки масла могут содержать никель в виде загрязнитель. Forte et al. обнаружили, что у пациентов с диабетом 2 типа содержание Ni в крови составляет 0,89 нг / мл по сравнению с 0,77 нг / мл в контрольной группе.[78]
Биологическая роль
Хотя никель не был признан до 1970-х годов, известно, что он играет важную роль в биологии некоторых растений. эубактерии, архебактерии, и грибы.[79][80][81] Никелевые ферменты, такие как уреаза считаются факторами вирулентности у некоторых организмов.[82][83] Уреаза катализирует гидролиз мочевина с образованием аммиака и карбамат.[80][79] В NiFe гидрогеназы может катализировать окисление ЧАС
2 с образованием протонов и электронов, а также может катализировать обратную реакцию, восстановление протонов с образованием газообразного водорода.[80][79] Кофермент никель-тетрапиррол, кофактор F430, присутствует в метил коэнзим М редуктаза, которая может катализировать образование метана или обратную реакцию в метаногенный археи (в +1 степень окисления).[84] Один из ферментов дегидрогеназы монооксида углерода состоит из кластера Fe-Ni-S.[85] Другие никельсодержащие ферменты включают редкий класс бактерий: супероксиддисмутаза[86] и глиоксалаза I ферменты бактерий и некоторых паразитарных эукариот трипаносомальный паразиты[87] (у высших организмов, включая дрожжи и млекопитающих, этот фермент содержит двухвалентный Zn2+).[88][89][90][91][92]
Пищевой никель может влиять на здоровье человека из-за заражения никель-зависимыми бактериями, но также возможно, что никель является важным питательным веществом для бактерий, проживающих в толстом кишечнике, фактически функционируя как пребиотик.[93] Институт медицины США не подтвердил, что никель является важным питательным веществом для человека, поэтому ни Рекомендуется диетическое пособие (RDA) и адекватного потребления не установлено. В Допустимый верхний уровень всасывания диетического никеля составляет 1000 мкг / день в виде растворимых солей никеля. Потребление с пищей оценивается от 70 до 100 мкг / день, при этом всасывается менее 10%. То, что всасывается, выводится с мочой.[94] Относительно большое количество никеля - сравнимое с расчетным средним потреблением, указанным выше - выщелачивание в пищу, приготовленную из нержавеющей стали. Например, количество никеля, выщелоченного после 10 циклов варки в одной порции томатного соуса, составляет в среднем 88 мкг.[95][96]
Никель выделился из Сибирские ловушки предполагается, что извержения вулканов способствуют росту Methanosarcina, род эвриархеотических архей, которые производили метан во время Пермско-триасовое вымирание, крупнейшее событие вымирания за всю историю наблюдений.[97]
Токсичность
| Опасности | |
|---|---|
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H317, H351, H372, H402, H412 | |
| P201, P202, P260, P264, P270, P272, P273, P280, P302 + 352, P308 + 313, P333 + 313, P363, P405, P501[98] | |
| NFPA 704 (огненный алмаз) | |
Основным источником воздействия никеля является оральное потребление, поскольку никель необходим для растений.[99] Никель естественным образом содержится как в пище, так и в воде, и его количество может увеличиваться человеком. загрязнение. Например, никелированные краны может загрязнять воду и почву; добыча полезных ископаемых и при плавке никель может попасть в Сточные Воды; никель – сталь сплав Посуда и посуда с никелевым пигментом могут выделять никель в пищу. Атмосфера может быть загрязнена переработкой никелевой руды и ископаемое топливо горение. Люди могут поглощать никель непосредственно из табачный дым и контакт кожи с украшениями, шампуни, моющие средства и монеты. Менее распространенная форма хронического воздействия - через гемодиализ поскольку следы ионов никеля могут абсорбироваться в плазму из хелатирующий действие альбумин.
Среднесуточное воздействие не представляет угрозы для здоровья человека. Большая часть никеля, ежедневно всасываемого людьми, удаляется почками и выводится из организма с мочой или выводится через желудочно-кишечный тракт, не всасываясь. Никель не является кумулятивным ядом, но большие дозы или хроническое вдыхание могут быть токсичными, даже канцерогенный, и составляют профессиональный риск.[100]
Соединения никеля классифицируются как канцерогены для человека.[101][102][103][104] на основании повышенного риска респираторного рака, наблюдаемого в эпидемиологических исследованиях у рабочих завода по переработке сульфидных руд.[105] Это подтверждается положительными результатами биотестов NTP с субсульфидом Ni и оксидом Ni на крысах и мышах.[106][107] Данные о людях и животных неизменно указывают на отсутствие канцерогенности при пероральном пути воздействия и ограничивают канцерогенность соединений никеля для респираторных опухолей после вдыхания.[108][109] Металлический никель классифицируется как подозреваемый канцероген;[101][102][103] существует согласованность между отсутствием повышенного риска рака дыхательных путей у рабочих, преимущественно подвергающихся воздействию металлического никеля[105] и отсутствие респираторных опухолей в исследовании канцерогенности ингаляционного воздействия порошка металлического никеля на крысах.[110] В исследованиях ингаляций на грызунах с различными соединениями никеля и металлическим никелем наблюдалось усиление воспалений легких с гиперплазией или фиброзом бронхиальных лимфатических узлов и без них.[104][106][110][111] В исследованиях на крысах пероральный прием водорастворимых солей никеля может вызвать эффекты перинатальной смертности у беременных животных.[112] Неясно, актуальны ли эти эффекты для людей, поскольку эпидемиологические исследования женщин, подвергшихся высокому облучению, не показали неблагоприятных эффектов токсичности для развития.[113][114][115][116]
Люди могут подвергаться воздействию никеля на рабочем месте при вдыхании, проглатывании и контакте с кожей или глазами. В Управление по охране труда (OSHA) установил законный предел (допустимый предел воздействия ) для рабочего места при 1 мг / м3 за 8-часовой рабочий день, без учета карбонила никеля. В Национальный институт охраны труда и здоровья (NIOSH) указывает рекомендуемый предел воздействия (REL) 0,015 мг / м3 за 8-часовой рабочий день. При 10 мг / м3, никель сразу опасно для жизни и здоровья.[117] Карбонил никеля [Ni (CO)
4] - чрезвычайно токсичный газ. Токсичность карбонилов металлов зависит как от токсичности металла, так и от выделения газов. монооксид углерода из карбонильных функциональных групп; Карбонил никеля также взрывоопасен на воздухе.[118][119]
Сенсибилизированный люди могут показать контакт с кожей аллергия на никель известный как контакт дерматит. Сильно сенсибилизированные люди также могут реагировать на продукты с высоким содержанием никеля.[120] Чувствительность к никелю также может присутствовать у пациентов с помфоликс. Никель является наиболее подтвержденным контактным аллергеном во всем мире, отчасти из-за его использования в ювелирных изделиях. проколотые уши.[121] Аллергия на никель, поражающая проколотые уши, часто проявляется зудом и покраснением кожи. Многие серьги теперь изготавливаются без никеля или с никелем с низким уровнем высвобождения.[122] для решения этой проблемы. Допустимое количество продуктов, контактирующих с кожей человека, теперь регулируется Евросоюз. В 2002 году исследователи обнаружили, что никель, выпускаемый для монет достоинством 1 и 2 евро, намного превышает эти стандарты. Считается, что это результат гальванический реакция.[123] За никель проголосовали Аллерген года в 2008 году Американским обществом контактного дерматита.[124] В августе 2015 года Американская академия дерматологии приняла заявление о безопасности никеля: «По оценкам, контактный дерматит, включающий сенсибилизацию никелем, составляет около 1,918 миллиарда долларов и затрагивает почти 72,29 миллиона человек».[120]
Отчеты показывают, что как вызванная никелем активация фактора, индуцируемого гипоксией (HIF-1), так и повышающая регуляция генов, индуцируемых гипоксией, вызваны истощением внутриклеточного аскорбат. Добавление аскорбата в культуральную среду увеличивало внутриклеточный уровень аскорбата и обращало вспять как индуцированную металлами стабилизацию HIF-1- и HIF-1α-зависимой экспрессии гена.[125][126]
Рекомендации
- ^ Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ Пфиррманн, Стефан; Лимберг, Кристиан; Хервиг, Кристиан; Штёсер, Рейнхард; Цимер, Буркхард (2009). «Диядерный комплекс динитрогена никеля (I) и его восстановление в одноэлектронных шагах». Angewandte Chemie International Edition. 48 (18): 3357–61. Дои:10.1002 / anie.200805862. PMID 19322853.
- ^ Карнс, Мэтью; Бучелла, Даниэла; Chen, Judy Y.-C .; Рамирес, Артур П .; Турро, Николас Дж .; Наколлс, Колин; Штайгервальд, Майкл (2009). «Стабильный тетраалкильный комплекс никеля (IV)». Angewandte Chemie International Edition. 48 (2): 290–4. Дои:10.1002 / anie.200804435. PMID 19021174.
- ^ Энтони, Джон В .; Бидо, Ричард А .; Bladh, Kenneth W .; Николс, Монте С., ред. (1990). «Никель» (PDF). Справочник по минералогии. Vol. И. Шантильи, штат Вирджиния, США: Минералогическое общество Америки. ISBN 978-0962209703.
- ^ «Никель: информация и данные о минералах никеля». Mindat.org. В архиве из оригинала 3 марта 2016 г.. Получено 2 марта, 2016.
- ^ Стиксруд, Ларс; Васерман, Евгений; Коэн, Рональд (ноябрь 1997 г.). «Состав и температура внутреннего ядра Земли». Журнал геофизических исследований. 102 (B11): 24729–24740. Bibcode:1997JGR ... 10224729S. Дои:10.1029 / 97JB02125.
- ^ Coey, J. M. D .; Скумрыев, В .; Галлахер, К. (1999). «Редкоземельные металлы: действительно ли гадолиний ферромагнитен?». Природа. 401 (6748): 35–36. Bibcode:1999Натура 401 ... 35С. Дои:10.1038/43363. S2CID 4383791.
- ^ а б c «Использование никеля в обществе». Институт никеля. В архиве из оригинала от 21 сентября 2017 года.
- ^ Тредголд, Тим. «Золото горячее, но никель еще горячее, так как спрос на батареи для электромобилей растет». Forbes. Получено 14 октября, 2020.
- ^ «Соединения никеля - история изнутри». Институт никеля. Архивировано из оригинал 31 августа 2018 г.
- ^ Малруни, Скотт Б.; Хаузинджер, Роберт П. (1 июня 2003 г.). «Поглощение и использование никеля микроорганизмами». Обзор микробиологии FEMS. 27 (2–3): 239–261. Дои:10.1016 / S0168-6445 (03) 00042-1. ISSN 0168-6445. PMID 12829270.
- ^ Сиодзава, Хидэцугу; Брионес-Леон, Антонио; Доманов Олег; Цехнер, Георг; и другие. (2015). «Кластеры никеля, встроенные в углеродные нанотрубки как высокоэффективные магниты». Научные отчеты. 5: 15033. Bibcode:2015НатСР ... 515033С. Дои:10.1038 / srep15033. ЧВК 4602218. PMID 26459370.
- ^ Киттель, Чарльз (1996). Введение в физику твердого тела. Вайли. п. 449. ISBN 978-0-471-14286-7.
- ^ а б Hammond, C.R .; Лиде, К. Р. (2018). "Элементы". В Rumble, Джон Р. (ред.). CRC Справочник по химии и физике (99-е изд.). Бока-Ратон, Флорида: CRC Press. п. 4.22. ISBN 9781138561632.
- ^ Sharma, A .; Hickman, J .; Газит, Н .; Рабкин, Е .; Мишин Ю. (2018). «Наночастицы никеля установили новый рекорд прочности». Nature Communications. 9 (1): 4102. Bibcode:2018НатКо ... 9.4102S. Дои:10.1038 / s41467-018-06575-6. ЧВК 6173750. PMID 30291239.
- ^ а б Шерри, Эрик Р. (2007). Периодическая таблица Менделеева: ее история и ее значение. Издательство Оксфордского университета. стр.239 –240. ISBN 978-0-19-530573-9.
- ^ Мисслер, Г.Л., Тарр, Д.А. (1999) Неорганическая химия 2-е изд., Прентис – Холл. п. 38. ISBN 0138418918.
- ^ Петруччи, Р. Х. и др. (2002) Общая химия 8-е изд., Прентис-Холл. п. 950. ISBN 0130143294.
- ^ а б База данных атомного спектра NIST В архиве 20 марта 2011 г. Wayback Machine Чтобы прочитать уровни атомов никеля, введите «Ni I» в поле «Спектр» и нажмите «Получить данные».
- ^ Шертлефф, Ричард; Дерринг, Эдвард (1989). «Наиболее плотно связанные ядра». Американский журнал физики. 57 (6): 552. Bibcode:1989AmJPh..57..552S. Дои:10.1119/1.15970. В архиве из оригинала 14 мая 2011 г.. Получено 19 ноября, 2008.
- ^ «Ядерный синтез». hyperphysics.phy-astr.gsu.edu. Получено 15 октября, 2020.
- ^ а б Фьюэлл, М. П. (1995). «Атомный нуклид с самой высокой средней энергией связи». Американский журнал физики. 63 (7): 653. Bibcode:1995AmJPh..63..653F. Дои:10.1119/1.17828.
- ^ а б Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (2003), "ТогдаUBASE оценка ядерных и распадных свойств », Ядерная физика A, 729: 3–128, Bibcode:2003НуФА.729 .... 3А, Дои:10.1016 / j.nuclphysa.2003.11.001
- ^ Пагель, Бернард Эфраим Юлиус (1997). «Дальнейшие этапы горения: эволюция массивных звезд». Нуклеосинтез и химическая эволюция галактик. стр.154–160. ISBN 978-0-521-55958-4.
- ^ Кастельвекки, Давиде (22 апреля 2005 г.). "Атомные сокрушители пролили свет на сверхновые, Большой взрыв". Архивировано из оригинал 23 июля 2012 г.. Получено 19 ноября, 2008.
- ^ W, P. (23 октября 1999 г.). «Дебютирует дважды волшебный металл - изотоп никеля». Новости науки. Архивировано из оригинал 24 мая 2012 г.. Получено 29 сентября, 2006.
- ^ Национальный реестр загрязнителей - Информационный бюллетень по никелю и соединениям В архиве 8 декабря 2011 г. Wayback Machine. Npi.gov.au. Проверено 9 января, 2012.
- ^ Кальво, Мигель (2019). Construyendo la Tabla Periódica. Сарагоса, Испания: Prames. п. 118. ISBN 978-84-8321-908-9.
- ^ «Мировые запасы никеля по странам 2019». Statista. Получено 6 августа, 2020.
- ^ Кук, Питер Х. «Обзор минерального сырья за 2019 год: никель» (PDF). Геологическая служба США. В архиве (PDF) с оригинала 21 апреля 2019 г.. Получено 18 марта, 2019.
- ^ Расмуссен, К. Л .; Мальвин, Д. Дж .; Уоссон, Дж. Т. (1988). «Разделение микроэлементов между тэнитом и камаситом - Связь со скоростью охлаждения железных метеоритов». Метеоритика. 23 (2): a107–112. Bibcode:1988Metic..23..107R. Дои:10.1111 / j.1945-5100.1988.tb00905.x.
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ «Извлечение никеля из руд с помощью процесса Монда». Природа. 59 (1516): 63–64. 1898. Bibcode:1898Натура..59 ... 63.. Дои:10.1038 / 059063a0.
- ^ а б c Housecroft, C.E .; Шарп, А. Г. (2008). Неорганическая химия (3-е изд.). Прентис Холл. п. 729. ISBN 978-0-13-175553-6.
- ^ Housecroft, C.E .; Шарп, А. Г. (2012). Неорганическая химия (4-е изд.). Прентис Холл. п. 764. ISBN 978-0273742753.
- ^ Ласселлес, Кейт; Морган, Линдси Дж .; Николлс, Дэвид и Бейерсманн, Детмар (2005) «Соединения никеля» в Энциклопедия промышленной химии Ульмана. Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a17_235.pub2
- ^ Дженсен, К. А. (1936). "Zur Stereochemie des koordinativ vierwertigen Nickels". Zeitschrift für Anorganische und Allgemeine Chemie. 229 (3): 265–281. Дои:10.1002 / zaac.19362290304.
- ^ Court, T. L .; Голубь, М.Ф.А. (1973). «Фторсодержащие соединения никеля (III)». Журнал химического общества, Dalton Transactions (19): 1995. Дои:10.1039 / DT9730001995.
- ^ «Корпорация Imara запускает новую технологию литий-ионных аккумуляторов для приложений большой мощности». Конгресс зеленых автомобилей. 18 декабря 2008 г. В архиве с оригинала 22 декабря 2008 г.. Получено 22 января, 2009.
- ^ Спокойный, Александр М .; Ли, Тина С .; Фарха, Омар К .; Machan, Charles M .; Она, Чуньсин; Стерн, Шарлотта Л .; Marks, Tobin J .; Хапп, Джозеф Т .; Миркин, Чад А. (28 июня 2010 г.). «Электронная настройка окислительно-восстановительных челноков на основе бис (дикарболлида) никеля в сенсибилизированных красителями солнечных элементах». Энгью. Chem. Int. Эд. 49 (31): 5339–5343. Дои:10.1002 / anie.201002181. PMID 20586090.
- ^ Хоторн, М. Фредерик (1967). «(3) -1,2-Дикарболлильные комплексы никеля (III) и никеля (IV)». Журнал Американского химического общества. 89 (2): 470–471. Дои:10.1021 / ja00978a065.
- ^ Камассо, Н. М .; Сэнфорд, М. С. (2015). «Дизайн, синтез и реакции сочетания углерод-гетероатомов металлоорганических комплексов никеля (IV)». Наука. 347 (6227): 1218–20. Bibcode:2015Научный ... 347.1218C. CiteSeerX 10.1.1.897.9273. Дои:10.1126 / science.aaa4526. PMID 25766226. S2CID 206634533.
- ^ Baucom, E. I .; Драго, Р. С. (1971). «Комплексы никеля (II) и никеля (IV) и 2,6-диацетилпиридиндиоксима». Журнал Американского химического общества. 93 (24): 6469–6475. Дои:10.1021 / ja00753a022.
- ^ Розенберг, Сэмюэл Дж. (1968). Никель и его сплавы. Национальное бюро стандартов.
- ^ а б Макнил, Ян (1990). «Появление никеля». Энциклопедия истории техники. Тейлор и Фрэнсис. стр.96–100. ISBN 978-0-415-01306-2.
- ^ Нидхэм, Джозеф; Ван, Линг; Лу, Гвэй-Джен; Цзянь, Цуэн-сюинь; Кун, Дитер и Голас, Питер Дж. (1974) Наука и цивилизация в Китае В архиве 3 мая 2016 г. Wayback Machine. Издательство Кембриджского университета. ISBN 0-521-08571-3С. 237–250.
- ^ Словарь Chambers Twentieth Century, стр. 888, W&R Chambers Ltd., 1977.
- ^ а б Болдуин, У. Х. (1931). «История Никеля. I. Как« гномы старого Ника перехитрили ». Журнал химического образования. 8 (9): 1749. Bibcode:1931JChEd ... 8.1749B. Дои:10.1021 / ed008p1749.
- ^ Болдуин, У. Х. (1931). «История никеля. II. Никель достигает совершеннолетия». Журнал химического образования. 8 (10): 1954. Bibcode:1931JChEd ... 8.1954B. Дои:10.1021 / ed008p1954.
- ^ Болдуин, У. Х. (1931). «История никеля. III. Руда, штейн и металл». Журнал химического образования. 8 (12): 2325. Bibcode:1931JChEd ... 8.2325B. Дои:10.1021 / ed008p2325.
- ^ Недели, Мэри Эльвира (1932). «Открытие элементов: III. Некоторые металлы восемнадцатого века». Журнал химического образования. 9 (1): 22. Bibcode:1932JChEd ... 9 ... 22Вт. Дои:10.1021 / ed009p22.
- ^ «Трудолюбивая, стойкая - пятицентовая монета». Королевский канадский монетный двор. 2008 г. В архиве из оригинала 26 января 2009 г.. Получено 10 января, 2009.
- ^ Моллой, Билл (8 ноября 2001 г.). «Тенденции никеля в монетах - прошлое, настоящее и будущее». Институт никеля. Архивировано из оригинал 29 сентября 2006 г.. Получено 19 ноября, 2008.
- ^ а б Лэйси, Анна (22 июня 2013 г.). «Плохая копейка? Новые монеты и аллергия на никель». BBC Health Check. В архиве с оригинала 7 августа 2013 г.. Получено 25 июля, 2013.
- ^ "nikkelen dubbele wapenstuiver Utrecht". nederlandsemunten.nl. В архиве с оригинала 7 января 2015 г.. Получено 7 января, 2015.
- ^ Kelly, T.D .; Матос, Г. «Статистика никеля» (PDF). Геологическая служба США. В архиве (PDF) с оригинала 12 августа 2014 г.. Получено 11 августа, 2014.
- ^ «10 ведущих стран-производителей никеля | МНН». Сеть новостей инвестирования. 21 июля 2020 г.. Получено 6 августа, 2020.
- ^ «Таблица данных по никелю - Обзор минерального сырья за 2020 год» (PDF). Геологическая служба США. Получено 6 августа, 2020.
- ^ «Никель» (PDF). Геологическая служба США, сводки по минеральным ресурсам. Январь 2013. В архиве (PDF) из оригинала от 9 мая 2013 г.. Получено 20 сентября, 2013.
- ^ "Проект" Никель-Маунтин " (PDF). Бункер руды. 15 (10): 59–66. 1953. Архивировано с оригинал (PDF) 12 февраля 2012 г.. Получено 7 мая, 2015.
- ^ "Автор по окружающей среде: никель". Совет национальной безопасности. 2006. Архивировано с оригинал 28 августа 2006 г.. Получено 10 января, 2009.
- ^ а б «Операции и развитие». Lundin Mining Corporation. Архивировано из оригинал 18 ноября 2015 г.. Получено 10 августа, 2014.
- ^ Mond, L .; Langer, K .; Квинке, Ф. (1890). «Действие окиси углерода на никель». Журнал химического общества. 57: 749–753. Дои:10.1039 / CT8905700749.
- ^ Керфут, Дерек Г. Э. «Никель». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a17_157.
- ^ Нейков, Олег Д .; Набойченко Станислав; Гопиенко, Виктор Г и Фришберг, Ирина V (15 января 2009 г.). Справочник по порошкам цветных металлов: технологии и применение. Эльзевир. С. 371–. ISBN 978-1-85617-422-0. В архиве из оригинала 29 мая 2013 г.. Получено 9 января, 2012.
- ^ «Графики цен на никель на LME». Лондонская биржа металлов. Архивировано из оригинал 28 февраля 2009 г.. Получено 6 июня, 2009.
- ^ «Лондонская биржа металлов». LME.com. В архиве с оригинала от 20 сентября 2017 года.
- ^ Монетный двор США движется к ограничению экспорта и плавки монет В архиве 27 мая 2016 г. Wayback Machine, Монетный двор США, пресс-релиз, 14 декабря 2006 г.
- ^ «Таблица внутренней стоимости обращающихся монет США». Coininflation.com. В архиве из оригинала 17 июня 2016 г.. Получено 13 сентября, 2013.
- ^ Американская сантехническая практика: из инженерных записей (до 1887 года - инженер-сантехник). Избранная перепечатка статей, описывающих известные сантехнические установки в Соединенных Штатах, а также вопросы и ответы о проблемах, возникающих в водопроводе и канализации дома. С пятьюстами тридцатью шестью иллюстрациями. Инженерная запись. 1896. с.119. Получено 28 мая, 2016.
- ^ Дэвис, Джозеф Р. (2000). «Использование никеля». Справочник по специальности ASM: никель, кобальт и их сплавы. ASM International. С. 7–13. ISBN 978-0-87170-685-0.
- ^ Хартон, Владислав В. (2011). Электрохимия твердого тела II: электроды, интерфейсы и керамические мембраны. Wiley-VCH. стр. 166–. ISBN 978-3-527-32638-9. В архиве из оригинала 10 сентября 2015 г.. Получено 27 июня, 2015.
- ^ Bidault, F .; Brett, D. J. L .; Миддлтон, П. Х .; Брэндон, Н. «Новая конструкция катода для щелочных топливных элементов (AFC)» (PDF). Имперский колледж Лондон. Архивировано из оригинал (PDF) 20 июля 2011 г.
- ^ Обзор магнитострикционных материалов. Калифорнийский университет в Лос-Анджелесе.
- ^ Ангара, Рагхавендра (2009). Система привода высокочастотного высокоамплитудного магнитного поля для магнитострикционных приводов. Издательство диссертаций Уми. п. 5. ISBN 9781109187533.
- ^ Чебураева, Р. Ф .; Чапорова, И. Н .; Красина Т. И. (1992). «Структура и свойства твердых сплавов карбида вольфрама на легированной никелевой связке». Советская порошковая металлургия и металлокерамика. 31 (5): 423–425. Дои:10.1007 / BF00796252. S2CID 135714029.
- ^ "Krytron Pulse Power Switching Tubes". Кремниевые исследования. 2011. Архивировано с оригинал 16 июля 2011 г.
- ^ Хан, Абдул Рехман; Аван, раввин Фазли (8 января 2014 г.). «Металлы в патогенезе диабета 2 типа». Журнал диабета и метаболических нарушений. 13 (1): 16. Дои:10.1186/2251-6581-13-16. ЧВК 3916582. PMID 24401367.
- ^ а б c Астрид Сигель; Гельмут Сигель; Роланд К. О. Сигель, ред.(2008). Никель и его удивительное воздействие на природу. Ионы металлов в науках о жизни. 2. Вайли. ISBN 978-0-470-01671-8.
- ^ а б c Сидор, Эндрю; Замбл, Дебора (2013). Банчи, Лючия (ред.). Металломика никеля: общие темы, определяющие гомеостаз никеля. Ионы металлов в науках о жизни. 12. Дордрехт: Спрингер. С. 375–416. Дои:10.1007/978-94-007-5561-1_11. ISBN 978-94-007-5561-1. PMID 23595678.
- ^ Замбл, Дебора; Ровиньска-Жирек, Магдалена; Козловский, Хенрик (2017). Биологическая химия никеля. Королевское химическое общество. ISBN 978-1-78262-498-1.
- ^ Коваччи, Антонелло; Телфорд, Джон Л .; Джудиче, Джузеппе Дель; Парсонне, Джули; Раппуоли, Рино (21 мая 1999 г.). "Helicobacter pylori Вирулентность и генетическая география ». Наука. 284 (5418): 1328–1333. Bibcode:1999Научный ... 284.1328C. Дои:10.1126 / science.284.5418.1328. PMID 10334982. S2CID 10376008.
- ^ Кокс, Гэри М .; Мукерджи, Жан; Коул, Гарри Т .; Касадеваль, Артуро; Идеально, Джон Р. (1 февраля 2000 г.). «Уреаза как фактор вирулентности при экспериментальном криптококкозе». Инфекция и иммунитет. 68 (2): 443–448. Дои:10.1128 / IAI.68.2.443-448.2000. ЧВК 97161. PMID 10639402.
- ^ Стивен В., Рэгдейл (2014). "Глава 6. Биохимия редуктазы метил-коэнзим M: никелевый металлофермент, катализирующий заключительный этап синтеза и первый этап анаэробного окисления парникового газа метанаВ Питере М. Х. Кронеке; Марте Э. Соса Торрес (ред.). Металлическая биогеохимия газообразных соединений окружающей среды. Ионы металлов в науках о жизни. 14. Springer. С. 125–145. Дои:10.1007/978-94-017-9269-1_6. ISBN 978-94-017-9268-4. PMID 25416393.
- ^ Ван, Винсент К.-К .; Рэгсдейл, Стивен У .; Армстронг, Фрейзер А. (2014). «Глава 4. Исследование эффективных электрокаталитических взаимопревращений диоксида углерода и оксида углерода никельсодержащими дегидрогеназами оксида углерода». В Питере М. Кронек; Марта Э. Соса Торрес (ред.). Металлическая биогеохимия газообразных соединений окружающей среды. Ионы металлов в науках о жизни. 14. Springer. С. 71–97. Дои:10.1007/978-94-017-9269-1_4. ISBN 978-94-017-9268-4. ЧВК 4261625. PMID 25416391.
- ^ Szilagyi, R.K .; Bryngelson, P.A .; Maroney, M. J .; Hedman, B .; и другие. (2004). "Исследование поглощения рентгеновских лучей S K-Edge в Ni-содержащем активном центре супероксиддисмутазы: новое структурное понимание механизма". Журнал Американского химического общества. 126 (10): 3018–3019. Дои:10.1021 / ja039106v. PMID 15012109.
- ^ Greig N; Wyllie S; Vickers TJ; Fairlamb AH (2006). «Трипанотион-зависимая глиоксалаза I в Trypanosoma cruzi». Биохимический журнал. 400 (2): 217–23. Дои:10.1042 / BJ20060882. ЧВК 1652828. PMID 16958620.
- ^ Aronsson A-C; Marmstål E; Маннервик Б (1978). «Глиоксалаза I, металлофермент цинка млекопитающих и дрожжей». Сообщения о биохимических и биофизических исследованиях. 81 (4): 1235–1240. Дои:10.1016 / 0006-291X (78) 91268-8. PMID 352355.
- ^ Ridderström M; Маннервик Б (1996). «Оптимизированная гетерологичная экспрессия человеческого фермента цинка глиоксалазы I». Биохимический журнал. 314 (Pt 2): 463–467. Дои:10.1042 / bj3140463. ЧВК 1217073. PMID 8670058.
- ^ Сен-Жан AP; Филлипс КР; Creighton DJ; Стоун MJ (1998). «Активные мономерные и димерные формы глиоксалазы I Pseudomonas putida: свидетельства обмена 3D-доменами». Биохимия. 37 (29): 10345–10353. Дои:10.1021 / bi980868q. PMID 9671502.
- ^ Торнали, П. Дж. (2003). «Глиоксалаза I - структура, функция и критическая роль в ферментативной защите от гликирования». Сделки Биохимического Общества. 31 (Pt 6): 1343–1348. Дои:10.1042 / BST0311343. PMID 14641060.
- ^ Вандер Ягт DL (1989). «Неизвестное название главы». In D Дельфин; Р. Поулсон; О Аврамович (ред.). Коэнзимы и кофакторы VIII: глутатион, часть A. Нью-Йорк: Джон Уайли и сыновья.
- ^ Замбелли, Барбара; Чурли, Стефано (2013). «Глава 10. Никель: и здоровье человека». В Астрид Сигель; Гельмут Сигель; Роланд К. О. Сигель (ред.). Взаимосвязь между ионами эссенциальных металлов и заболеваниями человека. Ионы металлов в науках о жизни. 13. Springer. С. 321–357. Дои:10.1007/978-94-007-7500-8_10. ISBN 978-94-007-7499-5. PMID 24470096.
- ^ Никель. В: Рекомендуемая диета для витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и меди В архиве 22 сентября 2017 г. Wayback Machine. Национальная академия прессы. 2001, стр. 521–529.
- ^ Камеруд К.Л .; Хобби К.А.; Андерсон К.А. (28 августа 2013 г.). «Нержавеющая сталь выщелачивает никель и хром в продукты во время приготовления». Журнал сельскохозяйственной и пищевой химии. 61 (39): 9495–501. Дои:10.1021 / jf402400v. ЧВК 4284091. PMID 23984718.
- ^ Flint GN; Packirisamy S (1997). «Чистота пищи, приготовленной в посуде из нержавеющей стали». Пищевые добавки и загрязняющие вещества. 14 (2): 115–26. Дои:10.1080/02652039709374506. PMID 9102344.
- ^ Ширбер, Майкл (27 июля 2014 г.). «Инновации микробов, возможно, положили начало крупнейшему вымиранию на Земле». Space.com. Журнал астробиологии. В архиве из оригинала 29 июля 2014 г.. Получено 29 июля, 2014.
.... Этот всплеск никеля позволил метаногенам взлететь.
- ^ «Никель 203904». Сигма Олдрич. В архиве с оригинала 26 января 2020 г.. Получено 26 января, 2020.
- ^ Хабер, Линн Т; Бейтс, Хадсон К.; Аллен, Брюс С; Винсент, Мелисса Дж; Оллер, Адриана Р. (2017). «Получение справочного значения пероральной токсичности для никеля». Нормативная токсикология и фармакология. 87: S1 – S18. Дои:10.1016 / j.yrtph.2017.03.011. PMID 28300623.
- ^ Буттисе, Клаудио (2015). «Соединения никеля». В Colditz, Graham A. (ed.). Энциклопедия рака и общества SAGE (Второе изд.). Таузенд Оукс: SAGE Publications, Inc., стр. 828–831. ISBN 9781483345734.
- ^ а б МАИР (2012). «Никель и никелевые соединения» В архиве 20 сентября 2017 г. Wayback Machine в IARC Monogr Eval Cancinog Risks Hum. Объем 100С. С. 169–218 ..
- ^ а б Регламент (ЕС) № 1272/2008 Европейского парламента и Совета от 16 декабря 2008 г. о классификации, маркировке и упаковке веществ и смесей, изменяющий и отменяющий Директивы 67/548 / EEC и 1999/45 / EC и изменяющий Регламент ( ЕС) № 1907/2006 [OJ L 353, 31.12.2008, стр. 1]. Приложение VI. В архиве 14 марта 2019 г. Wayback Machine. Доступ 13 июля 2017 г.
- ^ а б Согласованная на глобальном уровне система классификации и маркировки химических веществ (СГС) В архиве 29 августа 2017 г. Wayback Machine, 5-е изд., ООН, Нью-Йорк и Женева, 2013 г.
- ^ а б Национальная токсикологическая программа. (2016). «Отчет о канцерогенных веществах» В архиве 20 сентября 2017 г. Wayback Machine, 14-е изд. Research Triangle Park, NC: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения.
- ^ а б «Отчет Международного комитета по канцерогенезу никеля у человека». Скандинавский журнал труда, окружающей среды и здоровья. 16 (1 Спецификация): 1–82. 1990 г. Дои:10.5271 / sjweh.1813. JSTOR 40965957. PMID 2185539.
- ^ а б Национальная токсикологическая программа (1996). «Исследования токсикологии и канцерогенеза субсульфида никеля (CAS № 12035-72-2) у крыс F344 и мышей B6C3F1 (исследования при вдыхании)». Серия технических отчетов Национальной токсикологической программы. 453: 1–365. PMID 12594522.
- ^ Национальная токсикологическая программа (1996). «Исследования токсикологии и канцерогенеза NTP оксида никеля (CAS № 1313-99-1) у крыс F344 и мышей B6C3F1 (исследования при вдыхании)». Серия технических отчетов Национальной программы токсикологии. 451: 1–381. PMID 12594524.
- ^ Cogliano, V.J; Baan, R; Straif, K; Гросс, Й; Лауби-Секретан, B; Эль-Гиссасси, ф. Бувар, V; Бенбрахим-Таллаа, L; Guha, N; Фримен, C; Галичет, L; Уайлд, С. П. (2011). «Предотвратимые воздействия, связанные с раком человека». Журнал JNCI Национального института рака. 103 (24): 1827–39. Дои:10.1093 / jnci / djr483. ЧВК 3243677. PMID 22158127.
- ^ Heim, K. E; Бейтс, Х.К .; Раш, Р. Э; Оллер, А. Р. (2007). «Исследование оральной канцерогенности с гексагидратом сульфата никеля на крысах Fischer 344». Токсикология и прикладная фармакология. 224 (2): 126–37. Дои:10.1016 / j.taap.2007.06.024. PMID 17692353.
- ^ а б Oller, A.R; Киркпатрик, Д. Т; Радовский А; Бейтс, H.K (2008). «Исследование канцерогенности при вдыхании порошка металлического никеля на крысах линии Wistar». Токсикология и прикладная фармакология. 233 (2): 262–75. Дои:10.1016 / j.taap.2008.08.017. PMID 18822311.
- ^ Национальная токсикологическая программа (1996). «Исследования токсикологии и канцерогенеза NTP гексагидрата сульфата никеля (№ CAS 10101-97-0) у крыс F344 и мышей B6C3F1 (исследования при вдыхании)». Серия технических отчетов Национальной программы токсикологии. 454: 1–380. PMID 12587012.
- ^ Springborn Laboratories Inc. (2000). «Исследование репродуктивной токсичности двух поколений для перорального приема (через желудочный зонд) на крысах Sprague-Dawley с гексагидратом сульфата никеля». Заключительный отчет. Springborn Laboratories Inc., Спенсервиль. Исследование SLI № 3472.4.
- ^ Вактшельд, А; Талыкова, Л. В; Чащин, В.П .; Nieboer, E; Thomassen, Y; Одланд, Дж. О (2006). «Пороки развития половых органов у новорожденных у работниц никелеводства». Скандинавский журнал труда, окружающей среды и здоровья. 32 (1): 41–50. Дои:10.5271 / sjweh.975. PMID 16539171.
- ^ Вактшельд, А; Талыкова, Л. В; Чащин, В.П .; Odland, Jon Ø; Nieboer, E (2008). «Самопроизвольные аборты среди работниц нефтеперерабатывающих заводов, подвергшихся воздействию никеля». Международный журнал исследований в области гигиены окружающей среды. 18 (2): 99–115. Дои:10.1080/09603120701498295. PMID 18365800. S2CID 24791972.
- ^ Вактшельд, А; Талыкова, Л. В; Чащин, В.П .; Odland, J. O; Nieboer, E (2007). «Малолетние для гестационного возраста новорожденные работницы нефтеперерабатывающего завода, подвергшиеся воздействию никеля». Международный журнал медицины труда и гигиены окружающей среды. 20 (4): 327–38. Дои:10.2478 / v10001-007-0034-0. PMID 18165195. S2CID 1439478.
- ^ Вактшельд, А; Талыкова, Л. В; Чащин, В.П .; Odland, J. O; Nieboer, E (2008). «Материнское воздействие никеля и врожденные дефекты опорно-двигательный аппарат». Американский журнал промышленной медицины. 51 (11): 825–33. Дои:10.1002 / ajim.20609. PMID 18655106.
- ^ "CDC - Карманный справочник NIOSH по химической опасности - металлический никель и другие соединения (как Ni)". www.cdc.gov. В архиве с оригинала 18 июля 2017 г.. Получено 20 ноября, 2015.
- ^ Стеллман, Жанна Магер (1998). Энциклопедия по охране труда: химия, промышленность и профессии. Международная организация труда. С. 133–. ISBN 978-92-2-109816-4. В архиве из оригинала 29 мая 2013 г.. Получено 9 января, 2012.
- ^ Barceloux, Donald G .; Barceloux, Дональд (1999). «Никель». Клиническая токсикология. 37 (2): 239–258. Дои:10.1081 / CLT-100102423. PMID 10382559.
- ^ а б Заявление о позиции по чувствительности к никелю В архиве 8 сентября 2015 г. Wayback Machine. Американская академия дерматологии (22 августа 2015 г.)
- ^ Thyssen J. P .; Linneberg A .; Menné T .; Йохансен Дж. Д. (2007). «Эпидемиология контактной аллергии среди населения в целом - распространенность и основные выводы». Контактный дерматит. 57 (5): 287–99. Дои:10.1111 / j.1600-0536.2007.01220.x. PMID 17937743. S2CID 44890665.
- ^ Воздействие на кожу: никелевые сплавы В архиве 22 февраля 2016 г. Wayback Machine Ассоциация экологических исследований производителей никеля (NiPERA), по состоянию на 11 февраля 2016 г.
- ^ Nestle, O .; Speidel, H .; Шпейдель, М. О. (2002). «Высокий выпуск никеля из монет номиналом 1 и 2 евро». Природа. 419 (6903): 132. Bibcode:2002Натура.419..132Н. Дои:10.1038 / 419132a. PMID 12226655. S2CID 52866209.
- ^ Доу, Ли (3 июня 2008 г.). «Никель назван контактным аллергеном 2008 года». Информация об аллергии на никель. Архивировано из оригинал 3 февраля 2009 г.
- ^ Сальников, к .; Donald, S.P .; Bruick, R.K .; Житкович, А .; и другие. (Сентябрь 2004 г.). «Истощение внутриклеточного аскорбата канцерогенным металлом никелем и кобальтом приводит к индукции гипоксического стресса». Журнал биологической химии. 279 (39): 40337–44. Дои:10.1074 / jbc.M403057200. PMID 15271983.
- ^ Das, K. K .; Das, S. N .; Дхундаси, С. А. (2008). «Никель, его вредное воздействие на здоровье и окислительный стресс» (PDF). Индийский журнал медицинских исследований. 128 (4): 117–131. PMID 19106437. Архивировано из оригинал (PDF) 10 апреля 2009 г.. Получено 22 августа, 2011.
внешняя ссылка
- Никель в Периодическая таблица видео (Ноттингемский университет)
- CDC - Никель - Тема безопасности и гигиены труда NIOSH
- Гигиена труда при воздействии никеля на кожу в отраслях первичного производства пользователя GW Hughson. Институт медицины труда Отчет об исследовании TM / 04/05
- Гигиеническая оценка воздействия никеля на кожу в первичном производстве и основных отраслях промышленности. Отчет по фазе 2 пользователя GW Hughson. Институт медицины труда Отчет об исследовании TM / 05/06
- «Металл, который принес вам дешевые авиабилеты», BBC

