Бор - Википедия - Boron
 бор (β-ромбоэдрический)[1] | ||||||||||||||||
| Бор | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /ˈбɔːrɒп/ | |||||||||||||||
| Аллотропы | α-, β-ромбоэдрические, β-тетрагональные (и более ) | |||||||||||||||
| Внешность | Черно-коричневый | |||||||||||||||
| Стандартный атомный вес Аг, стд(В) | [10.806, 10.821] общепринятый:10.81 | |||||||||||||||
| Бор в периодическая таблица | ||||||||||||||||
| ||||||||||||||||
| Атомный номер (Z) | 5 | |||||||||||||||
| Группа | группа 13 (группа бора) | |||||||||||||||
| Период | период 2 | |||||||||||||||
| Блокировать | p-блок | |||||||||||||||
| Категория элемента | Металлоид | |||||||||||||||
| Электронная конфигурация | [Он ] 2 с2 2p1 | |||||||||||||||
| Электронов на оболочку | 2, 3 | |||||||||||||||
| Физические свойства | ||||||||||||||||
| Фаза вSTP | твердый | |||||||||||||||
| Температура плавления | 2349 K (2076 ° С, 3769 ° F) | |||||||||||||||
| Точка кипения | 4200 К (3927 ° C, 7101 ° F) | |||||||||||||||
| Плотность в жидком состоянии (приm.p.) | 2,08 г / см3 | |||||||||||||||
| Теплота плавления | 50.2 кДж / моль | |||||||||||||||
| Теплота испарения | 508 кДж / моль | |||||||||||||||
| Молярная теплоемкость | 11,087 Дж / (моль · К) | |||||||||||||||
Давление газа
| ||||||||||||||||
| Атомные свойства | ||||||||||||||||
| Состояния окисления | −5, −1, 0,[2] +1, +2, +3[3][4] (мягко кислый окись) | |||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,04 | |||||||||||||||
| Энергии ионизации |
| |||||||||||||||
| Радиус атома | эмпирические: 90вечера | |||||||||||||||
| Ковалентный радиус | 84 ± 15 часов | |||||||||||||||
| Радиус Ван-дер-Ваальса | 192 вечера | |||||||||||||||
| Другие свойства | ||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||
| Кристальная структура | ромбоэдрический | |||||||||||||||
| Скорость звука тонкий стержень | 16200 м / с (при 20 ° C) | |||||||||||||||
| Тепловое расширение | β-форма: 5–7 мкм / (м · К) (при 25 ° C)[5] | |||||||||||||||
| Теплопроводность | 27,4 Вт / (м · К) | |||||||||||||||
| Удельное электрическое сопротивление | ~106 Ом · м (при 20 ° C) | |||||||||||||||
| Магнитный заказ | диамагнитный[6] | |||||||||||||||
| Магнитная восприимчивость | −6.7·10−6 см3/ моль[6] | |||||||||||||||
| Твердость по Моосу | ~9.5 | |||||||||||||||
| Количество CAS | 7440-42-8 | |||||||||||||||
| История | ||||||||||||||||
| Открытие | Жозеф Луи Гей-Люссак и Луи Жак Тенар[7] (30 июня 1808 г.) | |||||||||||||||
| Первая изоляция | Хэмфри Дэви[8] (9 июля 1808 г.) | |||||||||||||||
| Главный изотопы бора | ||||||||||||||||
| ||||||||||||||||
| 10В природных образцах содержание B составляет 19,1–20,3%, остальное составляет 11Б.[10] | ||||||||||||||||
Бор это химический элемент с символ B и атомный номер 5. Произведено полностью расщепление космических лучей и сверхновые а не звездный нуклеосинтез, это элемент с низким содержанием Солнечная система и в земной коры.[11] Он составляет около 0,001 процента от веса земной коры.[12] Бор концентрируется на Земле благодаря растворимости в воде его наиболее распространенных природных соединений, боратные минералы. Они добываются промышленным способом как эвапориты, Такие как бура и кернит. Крупнейшие известные месторождения бора находятся в индюк, крупнейший производитель минералов бора.
Элементный бор - это металлоид что в небольших количествах содержится в метеороиды но химически несвязанный бор в естественных условиях не встречается на Земле. В промышленности очень чистый бор получается с трудом из-за загрязнения огнеупора углеродом или другими элементами. Несколько аллотропы бора существовать: аморфный бор - коричневый порошок; кристаллический бор от серебристого до черного, чрезвычайно твердый (около 9,5 на Шкала Мооса ) и бедный электрический проводник при комнатной температуре. Основное использование элементарного бора - это борные нити с приложениями, похожими на углеродные волокна в некоторых высокопрочных материалах.
Бор в основном используется в химических соединениях. Около половины всего потребляемого в мире бора составляет стекловолокно для изоляционных и конструкционных материалов. Следующее ведущее использование - в полимеры и керамика из высокопрочных, легких конструкционных и огнеупорных материалов. Боросиликатное стекло желательно из-за его большей прочности и устойчивости к тепловому удару, чем у обычного натриево-кальциевого стекла. Бор как перборат натрия используется как отбеливать. Небольшое количество бора используется как присадка в полупроводники, и реагент промежуточные звенья в синтез тонкой органической химии. Несколько борсодержащих органических фармацевтических препаратов используются или изучаются. Природный бор состоит из двух стабильных изотопов, один из которых (бор-10 ) имеет ряд применений в качестве улавливающего нейтроны агента.
В биологии бораты обладают низкой токсичностью для млекопитающих (аналогично столовая соль ), но более токсичны для членистоногие и используются как инсектициды. Борная кислота обладает умеренным антимикробным действием, известно несколько природных борсодержащих органических антибиотиков.[13] Бор является важным питательным веществом для растений и борсодержащими соединениями, такими как бура и борная кислота используются как удобрения в сельское хозяйство, хотя это требуется только в небольших количествах, а избыток токсичен. Соединения бора играют укрепляющую роль в клеточных стенках всех растений. Нет единого мнения о том, является ли бор важным питательным веществом для млекопитающих, включая человека, хотя есть некоторые свидетельства того, что он поддерживает здоровье костей.
История
Слово бор был придуман из бура, минерал, из которого он был выделен, по аналогии с углерод, на который бор похож по химическому составу.
Бура, ее минеральная форма, тогда известная как тинкал, глазури использовались в Китай с 300 г. н.э., и некоторое количество сырой буры попало на Запад, где алхимик Джабир ибн Хайян очевидно упомянул об этом в 700 г. Марко Поло вернул немного глазури в Италию в 13 веке. Агрикола, около 1600 г., сообщает об использовании буры в качестве флюса в металлургия. В 1777 г. борная кислота был признан в горячих источниках (софиони ) возле Флоренция, Италия, и стал известен как Sal sedativum, с преимущественно медицинским использованием. Редкий минерал называется сассолит, который находится в Сассо, Италия. Сассо был главным источником Европейский бура с 1827 по 1872 год, когда Американец источники заменили его.[14][15] Соединения бора использовались относительно редко до конца 1800-х годов, когда Фрэнсис Мэрион Смит с Компания Pacific Coast Borax впервые популяризировал и производил их в больших количествах по низкой цене.[16]
Бор не был признан элементом, пока он не был изолирован сэром Хэмфри Дэви[8] и по Жозеф Луи Гей-Люссак и Луи Жак Тенар.[7] В 1808 году Дэви заметил, что электрический ток, пропущенный через раствор боратов, вызывает образование коричневого осадка на одном из электродов. В своих последующих экспериментах он использовал калий для восстановления борной кислоты вместо электролиз. Он произвел достаточно бора, чтобы подтвердить новый элемент, и назвал элемент бораций.[8] Гей-Люссак и Тенар использовали железо для восстановления борной кислоты при высоких температурах. Окисляя бор воздухом, они показали, что борная кислота является продуктом окисления бора.[7][17] Йенс Якоб Берцелиус идентифицировал бор как элемент в 1824 году.[18] Возможно, впервые чистый бор был произведен американским химиком Иезекилем Вайнтраубом в 1909 году.[19][20][21]
Приготовление элементарного бора в лаборатории
Самые ранние способы получения элементарного бора включали восстановление оксид бора с металлами, такими как магний или же алюминий. Однако продукт почти всегда загрязнен бориды этих металлов. Чистый бор может быть получен восстановлением летучих галогенидов бора с помощью водород при высоких температурах. Сверхчистый бор для использования в полупроводниковой промышленности получают путем разложения диборан при высоких температурах и затем очищается зона плавки или же Чохральского процессы.[22]
Производство соединений бора не связано с образованием элементарного бора, но использует удобную доступность боратов.
Характеристики
Аллотропы

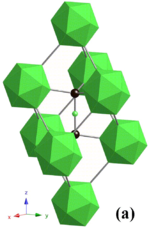
Бор похож на углерод в своей способности формировать стабильные ковалентно связанный молекулярные сети. Даже номинально неупорядоченный (аморфный ) бор содержит регулярный бор икосаэдры которые, однако, связаны между собой случайным образом без дальний заказ.[23][24] Кристаллический бор - очень твердый материал черного цвета с температурой плавления выше 2000 ° C. Он образует четыре основных полиморфы: α-ромбоэдрические и β-ромбоэдрические (α-R и β-R), γ и β-тетрагональные (β-T); Также существует α-тетрагональная фаза (α-T), но ее очень трудно получить без значительного загрязнения. Большинство фаз основаны на B12 икосаэдров, но γ-фаза может быть описана как каменная соль -типное расположение икосаэдров и B2 атомные пары.[25] Его можно получить путем сжатия других фаз бора до 12–20 ГПа и нагрева до 1500–1800 ° C; он остается стабильным после сброса температуры и давления. Фаза T производится при аналогичных давлениях, но более высоких температурах 1800–2200 ° C. Что касается фаз α и β, они могут сосуществовать в условия окружающей среды причем β-фаза более стабильна.[25][26][27] Сжатие бора выше 160 ГПа дает фазу бора с еще неизвестной структурой, и эта фаза представляет собой сверхпроводник при температурах 6–12 К.[28] Боросферы (фуллерен -подобный B40) молекулы) и борофен (предложил графен -подобная структура) были описаны в 2014 г.
| Борная фаза | α-R | β-R | γ | β-Т |
|---|---|---|---|---|
| Симметрия | Ромбоэдрический | Ромбоэдрический | Орторомбический | Тетрагональный |
| Атомы / элементарная ячейка[25] | 12 | ~105 | 28 | |
| Плотность (г / см3)[29][30][31][32] | 2.46 | 2.35 | 2.52 | 2.36 |
| Твердость по Виккерсу (ГПа)[33][34] | 42 | 45 | 50–58 | |
| Объемный модуль (ГПа)[34][35] | 185 | 224 | 227 | |
| Запрещенная зона (эВ)[34][36] | 2 | 1.6 | 2.1 |
Химия элемента
Элементарный бор встречается редко и плохо изучен, потому что чистый материал чрезвычайно сложно получить. Большинство исследований «бора» включают образцы, содержащие небольшое количество углерода. Химическое поведение бора напоминает поведение кремний больше, чем алюминий. Кристаллический бор химически инертен и устойчив к воздействию кипения. плавиковый или же соляная кислота. В мелком виде он медленно атакуется горячим концентрированным пероксид водорода, горячий концентрат азотная кислота, горячей серная кислота или горячая смесь серной и хромовые кислоты.[20]
Скорость окисления бора зависит от кристалличности, размера частиц, чистоты и температуры. Бор не реагирует с воздухом при комнатной температуре, но при более высоких температурах он горит с образованием триоксид бора:[37]
- 4 В + 3 О2 → 2 млрд2О3

Бор подвергается галогенированию с образованием тригалогенидов; Например,
- 2 комн. + 3 комн.2 → 2 BBr3
На практике трихлорид обычно получают из оксида.[37]
Атомная структура
Бор - самый легкий элемент, имеющий электрон в р-орбитальный в основном состоянии. Но, в отличие от большинства других p-элементы, он редко подчиняется Правило октета и обычно размещает только шесть электронов[38] (в трех молекулярные орбитали ) на его валентной оболочки. Бор является прототипом группа бора (в Группа ИЮПАК 13), хотя другими членами этой группы являются металлы и более типичные p-элементы (только алюминий в некоторой степени разделяет отвращение бора к правилу октетов).
Химические соединения

В наиболее известных соединениях бор имеет формальную степень окисления III. К ним относятся оксиды, сульфиды, нитриды и галогениды.[37]
Тригалогениды имеют плоскую тригональную структуру. Эти соединения Кислоты Льюиса в том, что они легко образуют аддукты с донорами электронных пар, которые называются Базы Льюиса. Например, фторид (F−) и трифторид бора (BF3) в сочетании, чтобы дать тетрафторборат анион, BF4−. Трифторид бора используется в нефтехимической промышленности в качестве катализатора. Галогениды реагируют с водой с образованием борная кислота.[37]
Бор встречается в природе на Земле почти полностью в виде различных оксидов B (III), часто связанных с другими элементами. Более ста боратные минералы содержат бор в степени окисления +3. Эти минералы в чем-то напоминают силикаты, хотя бор часто встречается не только в тетраэдрической координации с кислородом, но и в тригональной планарной конфигурации. В отличие от силикатов борные минералы никогда не содержат бор с координационным числом больше четырех. Типичный мотив представлен тетраборатными анионами обычного минерала бура, показанный слева. Формальный отрицательный заряд тетраэдрического боратного центра уравновешивается катионами металлов в минералах, таких как натрий (Na+) в буре.[37] Группа борат-силикатов турмалина также является очень важной группой борсодержащих минералов, и также известно, что ряд боросиликатов существует в природе.[39]
Бораны - это химические соединения бора и водорода с общей формулой BИксЧАСу. Эти соединения не встречаются в природе. Многие из боранов легко окисляются при контакте с воздухом, некоторые - бурно. Родительский член BH3 называется бораном, но он известен только в газообразном состоянии, и димеризуется с образованием диборана, B2ЧАС6. Все более крупные бораны состоят из многогранных кластеров бора, некоторые из которых существуют в виде изомеров. Например, изомеры B20ЧАС26 основаны на слиянии двух 10-атомных кластеров.
Наиболее важные бораны - диборан B2ЧАС6 и два его продукта пиролиза, пентаборан B5ЧАС9 и декаборана B10ЧАС14. Известно большое количество анионных гидридов бора, например [B12ЧАС12]2−.
Формальный степень окисления в боранах положительный и основан на предположении, что водород считается как -1, как в гидридах активных металлов. Тогда средняя степень окисления бора - это просто отношение водорода к бору в молекуле. Например, в диборане B2ЧАС6, степень окисления бора +3, но в декаборане B10ЧАС14, это 7/5 или +1,4. В этих соединениях степень окисления бора часто не является целым числом.
В нитриды бора отличаются разнообразием используемых в них структур. Они имеют структуры, аналогичные различным аллотропы углерода, включая графит, алмаз и нанотрубки. В алмазоподобной структуре, называемой кубическим нитридом бора (торговое название Боразон ), атомы бора существуют в тетраэдрической структуре атомов углерода в алмазе, но каждую четвертую связь B-N можно рассматривать как координировать ковалентную связь, где два электрона передаются атомом азота, который действует как База Льюиса к связи с Льюис кислый бор (III) центр. Кубический нитрид бора, помимо прочего, используется в качестве абразива, так как он имеет твердость, сравнимую с алмазом (два вещества могут оставлять царапины друг на друге). В составном аналоге графита BN, гексагональном нитриде бора (h-BN), положительно заряженные атомы бора и отрицательно заряженные атомы азота в каждой плоскости лежат рядом с противоположно заряженным атомом в следующей плоскости. Следовательно, графит и h-BN имеют очень разные свойства, хотя оба являются смазочными материалами, так как эти плоскости легко скользят друг мимо друга. Однако h-BN является относительно плохим проводником электричества и тепла в плоских направлениях.[40][41]
Борорганическая химия
Известно большое количество борорганических соединений, многие из которых используются в органический синтез. Многие производятся из гидроборирование, в котором работают диборан, B2ЧАС6, простой боран химический. Боровоорганические соединения (III) обычно бывают тетраэдрическими или тригонально плоскими, например, тетрафенилборат, [ДО Н.Э6ЧАС5)4]− против. трифенилборан, ДО Н.Э6ЧАС5)3. Однако несколько атомов бора, взаимодействуя друг с другом, имеют тенденцию образовывать новые додекаэдрические (12-сторонние) и икосаэдрические (20-сторонние) структуры, полностью состоящие из атомов бора или с различным количеством гетероатомов углерода.
Борорганические химические вещества используются в самых разных областях, включая карбид бора (см. ниже), сложная очень твердая керамика, состоящая из бор-углеродных кластерных анионов и катионов, чтобы карбораны, углерод-бор кластерная химия соединения, которые могут быть галогенированы с образованием реактивных структур, включая карборановая кислота, а суперкислотный. В качестве одного примера, карбораны образуют полезные молекулярные фрагменты, которые добавляют значительные количества бора к другим биохимическим веществам, чтобы синтезировать борсодержащие соединения для борная нейтронно-захватная терапия для рака.
Соединения B (I) и B (II)
Хотя в природе они не встречаются на Земле, бор образует множество стабильных соединений с формальной степенью окисления менее трех. Как и для многих ковалентных соединений, формальные состояния окисления часто не имеют большого значения. гидриды бора и бориды металлов. Галогениды также образуют производные B (I) и B (II). BF, изоэлектронный с N2, не могут быть выделены в сжатом виде, но B2F4 и B4Cl4 хорошо охарактеризованы.[42]

Бинарные соединения металла и бора, бориды металлов, содержат бор в отрицательной степени окисления. Иллюстративным является диборид магния (MgB2). Каждый атом бора имеет формальный заряд -1, а магнию соответствует формальный заряд +2. В этом материале центры бора являются тригонально плоскими с дополнительной двойной связью для каждого бора, образуя листы, похожие на углерод в графит. Однако, в отличие от гексагонального нитрида бора, у которого отсутствуют электроны в плоскости ковалентных атомов, делокализованные электроны в дибориде магния позволяют ему проводить электричество подобно изоэлектронному графиту. В 2001 году этот материал оказался высокотемпературным. сверхпроводник.[43][44] Это сверхпроводник, который находится в стадии активной разработки. Проект на ЦЕРН сделать MgB2 В результате были созданы сверхпроводящие испытательные кабели, способные выдерживать ток 20000 ампер для применения в распределительных сетях с чрезвычайно высоким током, таких как предполагаемая версия светосильного кабеля Большой адронный коллайдер.[45]
Некоторые другие бориды металлов находят специализированное применение в качестве твердых материалов для режущих инструментов.[46] Часто бор в боридах имеет фракционные степени окисления, такие как -1/3 в гексаборид кальция (Такси6).
Со структурной точки зрения наиболее отличительными химическими соединениями бора являются гидриды. В эту серию входят кластерные соединения dodecaborate (B
12ЧАС2−
12), декаборан (B10ЧАС14), а карбораны например, C2B10ЧАС12. Обычно такие соединения содержат бор с координационными числами больше четырех.[37]
Изотопы
Бор имеет два природных и стабильных изотопы, 11B (80,1%) и 10В (19,9%). Разница масс приводит к широкому диапазону значений δ11B значения, которые определяются как дробная разница между 11Группа 10B и традиционно выражается в частях на тысячу в природных водах в диапазоне от −16 до +59. Известно 13 изотопов бора, самый короткоживущий изотоп - это 7B который распадается через испускание протона и альфа-распад. Оно имеет период полураспада 3,5 × 10−22 с. Изотопное фракционирование бора контролируется реакциями обмена частиц бора B (OH)3 и [В (ОН)4]−. Изотопы бора также фракционируются при кристаллизации минералов, во время H2O фазовые изменения в гидротермальный систем, а во время гидротермальные изменения из камень. Последний эффект приводит к предпочтительному удалению [10В (ОН)4]− ион на глины. В результате получаются растворы, обогащенные 11В (ОН)3 и поэтому может нести ответственность за большие 11Обогащение морской водой B по сравнению с обоими океанический корка и континентальный корочка; эта разница может действовать как изотопная подпись.[47]
Экзотика 17B демонстрирует ядерный ореол, т.е. его радиус заметно больше, чем предсказывает модель капли жидкости.[48]
В 10Изотоп B полезен для улавливания тепловые нейтроны (видеть нейтронное сечение # Типичные сечения ). В атомная промышленность обогащает природный бор почти до чистого 10Б. Менее ценный побочный продукт, обедненный бор, почти чистый 11Б.
Коммерческое обогащение изотопов
Из-за своего высокого нейтронного сечения бор-10 часто используется для контроля деления в ядерных реакторах в качестве вещества, улавливающего нейтроны.[49] Было разработано несколько промышленных процессов обогащения; однако только фракционированная вакуумная перегонка диметиловый эфир присоединение трифторид бора (DME-BF3) и колоночная хроматография боратов.[50][51]
Обогащенный бор (бор-10)

Обогащенный бором или 10B используется как для защиты от излучения, так и является основным нуклидом, используемым в нейтронно-захватная терапия рака. В последнем ("борная нейтронно-захватная терапия" или BNCT) соединение, содержащее 10B включается в фармацевтический препарат, который избирательно поглощается злокачественной опухолью и тканями рядом с ней. Затем пациента лечат пучком нейтронов низкой энергии при относительно низкой дозе нейтронного излучения. Нейтроны, однако, вызывают энергетический и ближний вторичный альфа-частица и излучение тяжелых ионов лития-7, которые являются продуктами взаимодействия бор + нейтрон ядерная реакция, и это ионное излучение дополнительно бомбардирует опухоль, особенно изнутри опухолевых клеток.[52][53][54][55]
В ядерных реакторах 10B используется для контроля реактивности и в системы аварийного отключения. Он может выполнять любую функцию в виде боросиликатный стержни управления или как борная кислота. В реакторы с водой под давлением, 10B борная кислота добавляется в теплоноситель реактора при остановке установки на перегрузку. Затем он медленно отфильтровывается в течение многих месяцев, как делящийся материал израсходован, и топливо становится менее реактивным.[56]
В будущем пилотируемый межпланетный корабль, 10B теоретически играет роль конструкционного материала (как борные волокна или BN нанотрубка материал), который также будет играть особую роль в радиационной защите. Одна из трудностей в борьбе с космические лучи, которые в основном представляют собой протоны высоких энергий, заключается в том, что некоторое вторичное излучение от взаимодействия космических лучей и материалов космического корабля имеет высокую энергию раскол нейтроны. Такие нейтроны могут замедляться материалами с высоким содержанием легких элементов, такими как полиэтилен, но замедленные нейтроны продолжают представлять радиационную опасность, если они активно не поглощаются защитой. Среди легких элементов, поглощающих тепловые нейтроны, 6Ли и 10B представляют собой потенциальные конструкционные материалы космического корабля, которые служат как для механического усиления, так и для защиты от радиации.[57]
Обедненный бор (бор-11)
Радиационно-стойкие полупроводники
Космическое излучение будет производить вторичные нейтроны, если попадет в конструкции космического корабля. Эти нейтроны будут захвачены 10B, если он присутствует в космическом корабле полупроводники, производя гамма-луч, альфа-частица, а литий ион. Эти результирующие продукты распада могут затем облучать близлежащие полупроводниковые «чипы», вызывая потерю данных (переворот битов или одно событие расстроено ). В радиационно стойкий полупроводниковые конструкции, одна контрмера - использовать обедненный бор, который значительно обогащен 11B и почти не содержит 10Б. Это полезно, потому что 11B в значительной степени невосприимчив к радиационным повреждениям. Обедненный бор является побочным продуктом атомная промышленность.[56]
Протонно-борный синтез
11B также является кандидатом в качестве топлива для аневтронный синтез. При ударе протона с энергией около 500 кэВ, он производит три альфа-частицы и энергию 8,7 МэВ. Большинство других термоядерных реакций с участием водорода и гелия вызывают проникающее нейтронное излучение, которое ослабляет конструкции реактора и вызывает долговременную радиоактивность, тем самым подвергая опасности обслуживающий персонал. Тем не менее альфа-частицы из 11B-термоядерный синтез можно превратить непосредственно в электрическую энергию, и все излучение прекращается, как только отключается реактор.[58]
ЯМР-спектроскопия
Обе 10Группа 11B обладают ядерное вращение. Ядерный спин 10B равно 3, а у 11B - это 3/2. Таким образом, эти изотопы используются в ядерный магнитный резонанс спектроскопия; и спектрометры, специально приспособленные для обнаружения ядер бора-11, имеются в продаже. В 10Группа 11Ядра B также вызывают расщепление в резонансы прикрепленных ядер.[59]
Вхождение


Бор встречается редко во Вселенной и Солнечной системе из-за образования следов в Большой взрыв и в звездах. В небольших количествах образуется в расщепление космических лучей нуклеосинтез и может быть найден без комбинации в космическая пыль и метеороид материалы.
В среде Земли с высоким содержанием кислорода бор всегда полностью окислен до бората. Бор не появляется на Земле в элементарной форме. В лунном реголите были обнаружены очень маленькие следы элементарного бора.[60][61]
Хотя бор - относительно редкий элемент в земной коре, составляющий всего 0,001% от массы земной коры, он может быть сильно сконцентрирован под действием воды, в которой многие бораты растворимы. бура и борная кислота (иногда встречается в вулканический родниковые воды). Около сотни боратные минералы известны.
5 сентября 2017 года ученые сообщили, что Любопытство марсоход обнаружен бор, важный ингредиент для жизнь на земной шар, на планете Марс. Такое открытие, наряду с предыдущими открытиями о том, что вода могла присутствовать на древнем Марсе, еще больше подтверждает возможную раннюю обитаемость Кратер Гейла на Марсе.[62][63]
Производство
Экономически важными источниками бора являются минералы. колеманит, разорит (кернит ), улексит и тинкал. Вместе они составляют 90% добываемой борсодержащей руды. Крупнейшие известные месторождения буры в мире, многие из которых еще не освоены, находятся в Центральной и Западной Европе. индюк, включая провинции Эскишехир, Кютахья и Балыкесир.[64][65][66] Мировые доказанные запасы полезных ископаемых по бору превышают один миллиард метрических тонн при годовом производстве около четырех миллионов тонн.[67]
индюк и Соединенные Штаты являются крупнейшими производителями борных продуктов. Турция производит около половины мирового годового спроса за счет Eti Mine Works (турецкий: Eti Maden İşletmeleri) а турецкий государственный добыча полезных ископаемых и химикаты компания, специализирующаяся на продуктах из бора. Он держит государственная монополия по добыче боратные минералы в Турции, владеющей 72% известных мировых запасов.[68] В 2012 году он занимал 47% Поделиться производства мировых боратных минералов, опережая своего основного конкурента, Группа Рио Тинто.[69]
Почти четверть (23%) мирового производства бора приходится на Рио Тинто Боракс Шахта (также известный как Боракс-Бора в США) 35 ° 2′34,447 ″ с.ш. 117 ° 40′45,412 ″ з.д. / 35.04290194 ° с.ш.117.67928111 ° з.д. возле Борон, Калифорния.[70][71]
Тенденция рынка
Средняя стоимость кристаллического бора составляет 5 долларов за г.[72] Свободный бор в основном используется в производстве борных волокон, где он осаждается химическое осаждение из паровой фазы на вольфрам ядро (см. ниже). Волокна бора используются в легких композитных материалах, таких как высокопрочные ленты. Это использование составляет очень небольшую долю от общего использования бора. Бор вводится в полупроводники в виде соединений бора путем ионной имплантации.
Расчетное глобальное потребление бора (почти полностью в виде соединений бора) составляло около 4 миллионов тонн B2О3 в 2012 году. Мощности по добыче и переработке бора считаются достаточными для удовлетворения ожидаемых уровней роста в течение следующего десятилетия.
Форма потребления бора за последние годы изменилась. Использование руд типа колеманит отказался из-за опасений по поводу мышьяк содержание. Потребители перешли на использование очищенных боратов и борной кислоты с более низким содержанием загрязняющих веществ.
Растущий спрос на борную кислоту побудил ряд производителей инвестировать в дополнительные мощности. Турецкая государственная Eti Mine Works открыли новый завод борной кислоты производственной мощностью 100 000 тонн в год на Эмет в 2003 г. Группа Рио Тинто увеличил мощность завода по производству бора с 260 000 тонн в год в 2003 году до 310 000 тонн в год к маю 2005 года с планами по увеличению мощности до 366 000 тонн в год в 2006 году. Китайские производители бора не могут удовлетворить быстро растущий спрос на высокое качество бораты. Это привело к импорту тетрабората натрия (бура ) с 2000 по 2005 год увеличивалась стократно, а импорт борной кислоты увеличивался на 28% в год за тот же период.[73][74]
Рост мирового спроса был обусловлен высокими темпами роста в стекловолокно, стекловолокно и боросиликатный производство посуды. Быстрый рост производства армирующего борсодержащего стекловолокна в Азии остановил развитие не содержащего бор армирующего стекловолокна в Европе и США. Недавний рост цен на энергоносители может привести к более широкому использованию стекловолокна изоляционного качества с последующим ростом потребления бора. Roskill Consulting Group прогнозирует, что мировой спрос на бор будет расти на 3,4% в год и к 2010 году достигнет 21 миллиона тонн. Ожидается, что наибольший рост спроса будет в Азии, где спрос может увеличиваться в среднем на 5,7% в год.[73][75]
Приложения
Практически вся борная руда, добываемая на Земле, предназначена для переработки в борная кислота и пентагидрат тетрабората натрия. В Соединенных Штатах 70% бора используется для производства стекла и керамики.[76][77]Основное использование соединений бора в промышленном масштабе (около 46% конечного использования) приходится на производство стекловолокно для борсодержащих изоляционных и конструкционных стекловолокно, особенно в Азии. Бор добавляется в стекло в виде пентагидрата буры или оксида бора, чтобы влиять на прочность или флюсующие свойства стекловолокна.[78] Еще 10% мирового производства бора приходится на боросиликатное стекло как используется в высокопрочной посуде. Около 15% всего бора в мире используется в борной керамике, включая сверхтвердые материалы, обсуждаемые ниже. На сельское хозяйство приходится 11% мирового производства бора, а на отбеливатели и моющие средства - около 6%.[79]
Элементное борное волокно
Волокна бора (борные нити) - это высокопрочные, легкие материалы, которые используются в основном для аэрокосмический конструкции как составная часть композитные материалы, а также ограниченного производства потребительских и спортивных товаров, таких как гольф-клубы и удочки.[80][81] Волокна могут быть произведены химическое осаждение из паровой фазы бора на вольфрам нить.[82][83]
Волокна бора и пружины из кристаллического бора субмиллиметрового размера производятся лазер -помощь химическое осаждение из паровой фазы. Трансляция сфокусированного лазерного луча позволяет изготавливать даже сложные спиральные конструкции. Такие конструкции показывают хорошие механические свойства (модуль упругости 450 ГПа, деформация разрушения 3,7%, напряжение разрушения 17 ГПа) и могут применяться в качестве армирования керамики или в микромеханические системы.[84]
Борированное стекловолокно
Стекловолокно - это армированный волокном полимер сделано из пластик усиленный стекловолокно, обычно ткут в циновку. Стекловолокно, используемое в материале, изготовлено из различных типов стекла в зависимости от использования стекловолокна. Все эти стекла содержат кремнезем или силикат с различным количеством оксидов кальция, магния и иногда бора. Бор присутствует в виде боросиликата, буры или оксида бора и добавляется для повышения прочности стекла или в качестве флюса для снижения температуры плавления стекла. кремнезем, который слишком высок, чтобы его можно было легко обрабатывать в чистом виде для получения стекловолокна.
Стекло с высоким содержанием бора, используемое в стекловолокне, - это стекло E (названное от «электрического» использования, но в настоящее время наиболее распространенное стекловолокно для общего использования). Е-стекло - это алюмоборосиликатное стекло с содержанием оксидов щелочных металлов менее 1% по весу, которое в основном используется для изготовления стеклопластиков. Другие распространенные стекла с высоким содержанием бора включают C-стекло, известково-щелочное стекло с высоким содержанием оксида бора, используемое для изготовления штапельных стекловолокон и изоляции, и D-стекло, a боросиликатное стекло, названный из-за его низкого Dэлектрическая постоянная).[85]
Не все стекловолокна содержат бор, но в глобальном масштабе большая часть используемых стекловолокон действительно содержит его. Из-за повсеместного использования стекловолокна в строительстве и изоляции борсодержащие стекловолокна потребляют половину мирового производства бора и являются крупнейшим коммерческим рынком бора.
Боросиликатное стекло

Боросиликатное стекло, что обычно составляет 12–15% B2О3, 80% SiO2, и 2% Al2О3, имеет низкий коэффициент температурного расширения, давая ему хорошее сопротивление тепловой удар. Schott AG "Duran" и Owens-Corning товарный знак Pyrex два основных бренда этого стекла, которые используются как в лабораторная посуда и в потребительском посуда и формы для выпечки, главным образом для этого сопротивления.[86]
Карбид бора керамический
Некоторые соединения бора известны своей чрезвычайной твердостью и вязкостью.Карбид бора керамический материал, который получают разложением B2О3 с углеродом в электропечи:
- 2 млрд2О3 + 7 C → B4С + 6 СО
Структура карбида бора составляет лишь приблизительно B4C, и он показывает явное истощение углерода из этого предложенного стехиометрического соотношения. Это связано с его очень сложной структурой. Вещество можно увидеть с помощью эмпирическая формула B12C3 (т.е. с B12 додекаэдры являются мотивом), но с меньшим количеством углерода, как предполагалось, C3 единицы заменяются цепями C-B-C, а некоторые меньшие (B6) октаэдры также присутствуют (структурный анализ см. в статье о карбиде бора). Повторяющийся полимер плюс полукристаллическая структура карбида бора придает ему большую структурную прочность на вес. Он используется в танковая броня, бронежилеты, и многие другие структурные приложения.
Способность карбида бора поглощать нейтроны без образования долгоживущих радионуклиды (особенно в сочетании с дополнительным бором-10) делает материал привлекательным в качестве поглотитель нейтронного излучения, возникающего на атомных электростанциях.[88] Применение карбида бора в ядерной области включает в себя защиту, регулирующие стержни и запорные таблетки. В регулирующих стержнях карбид бора часто измельчается в порошок для увеличения площади его поверхности.[89]
Высокотвердые и абразивные составы
| Материал | Алмаз | кубический-BC2N | кубический-BC5 | кубический-БН | B4C | ReB2 |
|---|---|---|---|---|---|---|
| Твердость по Виккерсу (ГПа) | 115 | 76 | 71 | 62 | 38 | 22 |
| Вязкость разрушения (МПа м1⁄2) | 5.3 | 4.5 | 9.5 | 6.8 | 3.5 |
Порошки карбида бора и кубического нитрида бора широко используются в качестве абразивов. Нитрид бора материал изоэлектронен углерод. Подобно углю, он имеет как гексагональную (мягкий графитоподобный h-BN), так и кубическую (твердый, алмазоподобный c-BN) формы. h-BN используется как высокотемпературный компонент и смазка. c-BN, также известный под коммерческим названием боразон,[92] превосходный абразив. Его твердость лишь немного меньше, но его химическая стабильность выше, чем у алмаза. Гетеродиамон (также называемый BCN) - еще одно алмазоподобное соединение бора.
Металлургия
Бор добавлен в борсодержащие стали на уровне нескольких частей на миллион для повышения прокаливаемости. Более высокие проценты добавляются к сталям, используемым в атомная промышленность из-за способности бора поглощать нейтроны.
Бор может также повышать твердость поверхности сталей и сплавов за счет раздражающий. Дополнительно металл бориды используются для покрытия инструментов через химическое осаждение из паровой фазы или же физическое осаждение из паровой фазы. Имплантация ионов бора в металлы и сплавы посредством ионная имплантация или же ионно-лучевое осаждение, приводит к значительному увеличению поверхностного сопротивления и микротвердости. С этой же целью успешно применялось и лазерное легирование. Эти бориды являются альтернативой инструментам с алмазным покрытием, и их (обработанные) поверхности имеют свойства, аналогичные свойствам массивного борида.[93]
Например, диборид рения может производиться при атмосферном давлении, но является довольно дорогостоящим из-за содержания рения. Твердость ReB2 демонстрирует значительные анизотропия из-за гексагональной слоистой структуры. Его стоимость сопоставима с ценой карбид вольфрама, Карбид кремния, диборид титана или же диборид циркония.[91]Аналогично AlMgB14 + ТиБ2 композиты обладают высокой твердостью и износостойкостью и используются либо в объемном виде, либо в качестве покрытий для компонентов, подверженных воздействию высоких температур и износа.[94]
Составы моющих средств и отбеливатели
Бура используется в различных бытовых средствах для стирки и чистки,[95] в том числе "20 Mule Team Borax "усилитель белья и"Boraxo порошковое мыло для рук. Оно также присутствует в некоторых отбеливание зубов формулы.[77]
Перборат натрия служит источником активный кислород во многих моющие средства, стиральные порошки, чистящие средства, и прачечная отбеливает. Однако, несмотря на свое название, отбеливатель для стирки «Боратем» больше не содержит соединений бора. перкарбонат натрия вместо этого как отбеливающий агент.[96]
Инсектициды
Борная кислота используется в качестве инсектицида, особенно против муравьев, блох и тараканов.[97]
Полупроводники
Бор - полезный присадка для таких полупроводников, как кремний, германий, и Карбид кремния. Имея на один валентный электрон меньше, чем основной атом, он отдает дыра в результате чего р-тип проводимость. Традиционный метод введения бора в полупроводники - его атомная диффузия при высоких температурах. В этом процессе используется либо твердое тело (B2О3), жидкая (BBr3) или газообразных источников бора (B2ЧАС6 или BF3). Однако после 1970-х годов его в основном заменили на ion implantation, which relies mostly on BF3 as a boron source.[98] Boron trichloride gas is also an important chemical in semiconductor industry, however, not for doping but rather for плазменное травление of metals and their oxides.[99] Триэтилборан is also injected into осаждение из паровой фазы reactors as a boron source.[нужна цитата ] Examples are the plasma deposition of boron-containing hard carbon films, silicon nitride–boron nitride films, and for допинг из алмаз film with boron.[100]
Магниты
Boron is a component of neodymium magnets (Nd2Fe14B), which are among the strongest type of permanent magnet. These magnets are found in a variety of electromechanical and electronic devices, such as магнитно-резонансная томография (MRI) medical imaging systems, in compact and relatively small motors and приводы. As examples, computer HDDs (hard disk drives), CD (compact disk) and DVD (digital versatile disk) players rely on neodymium magnet motors to deliver intense rotary power in a remarkably compact package. In mobile phones 'Neo' magnets provide the magnetic field which allows tiny speakers to deliver appreciable audio power.[101]
Shielding and neutron absorber in nuclear reactors
Boron shielding is used as a control for ядерные реакторы, taking advantage of its high cross-section for neutron capture.[102]
В реакторы с водой под давлением a variable concentration of boronic acid in the cooling water is used as a нейтронный яд to compensate the variable reactivity of the fuel. When new rods are inserted the concentration of boronic acid is maximal, and is reduced during the lifetime.[103]
Other nonmedical uses
- Because of its distinctive green flame, amorphous boron is used in pyrotechnic flares.[104]
- Крахмал и казеин -based adhesives contain sodium tetraborate decahydrate (Na2B4О7·10 H2O)
- Some anti-corrosion systems contain borax.[105]
- Sodium borates are used as a flux for soldering silver and gold and with хлорид аммония for welding ferrous metals.[106] They are also fire retarding additives to plastics and rubber articles.[107]
- Борная кислота (also known as orthoboric acid) H3BO3 is used in the production of textile fiberglass and плоские дисплеи[77][108] и во многих PVAc - и PVOH -based adhesives.
- Триэтилборан is a substance which ignites the JP-7 fuel of the Пратт и Уитни J58 turbojet /прямоточный воздушно-реактивный двигатель engines powering the Локхид SR-71 Блэкберд.[109] It was also used to ignite the F-1 Engines на Сатурн V Rocket utilized by НАСА с Аполлон и Skylab programs from 1967 until 1973. Today SpaceX uses it to ignite the engines on their Сокол 9 ракета.[110] Triethylborane is suitable for this because of its пирофорный properties, especially the fact that it burns with a very high temperature.[111] Triethylborane is an industrial инициатор в радикальный reactions, where it is effective even at low temperatures.
- Borates are used as environmentally benign консерванты для древесины.[112]
Pharmaceutical and biological applications
Борная кислота has antiseptic, antifungal, and antiviral properties and for these reasons is applied as a water clarifier in swimming pool water treatment.[113] Mild solutions of boric acid have been used as eye antiseptics.
Бортезомиб (продается как Velcade и Cytomib). Boron appears as an active element in its first-approved organic pharmaceutical in the pharmaceutical bortezomib, a new class of drug called the proteasome inhibitors, which are active in myeloma and one form of lymphoma (it is in currently in experimental trials against other types of lymphoma). The boron atom in bortezomib binds the catalytic site of the 26S proteasome[114] with high affinity and specificity.
- A number of potential boronated pharmaceuticals using бор-10, have been prepared for use in boron neutron capture therapy (BNCT).[115]
- Some boron compounds show promise in treating артрит, though none have as yet been generally approved for the purpose.[116]
Тавабороле (продается как Kerydin) является Аминоацил тРНК синтетаза inhibitor which is used to treat toenail fungus. Он получил одобрение FDA в июле 2014 года.[117]
Dioxaborolane chemistry enables radioactive фторид (18F ) labeling of антитела или же красные кровяные тельца, which allows for позитронно-эмиссионная томография (PET) imaging of рак[118] и кровоизлияния,[119] соответственно. А ЧАСuman-Derived, граммenetic, пositron-emitting and Fluorescent (HD-GPF) reporter system uses a human protein, PSMA and non-immunogenic, and a small molecule that is positron-emitting (boron bound 18F ) and fluorescent for dual modality PET and fluorescence imaging of genome modified cells, e.g. рак, CRISPR / Cas9, или же CAR T -cells, in an entire mouse.[120]
Области исследований
Диборид магния это важный superconducting material with the transition temperature of 39 K. MgB2 wires are produced with the порошок в тюбике process and applied in superconducting magnets.[121][122]
Amorphous boron is used as a melting point depressant in nickel-chromium braze alloys.[123]
Шестиугольный нитрид бора forms atomically thin layers, which have been used to enhance the подвижность электронов в графен устройств.[124][125] It also forms nanotubular structures (BNNTs ), which have high strength, high chemical stability, and high теплопроводность, among its list of desirable properties.[126]
Биологическая роль
Boron is an essential plant питательное вещество, required primarily for maintaining the integrity of cell walls. However, high soil concentrations of greater than 1.0 промилле lead to marginal and tip necrosis in leaves as well as poor overall growth performance. Levels as low as 0.8 ppm produce these same symptoms in plants that are particularly sensitive to boron in the soil. Nearly all plants, even those somewhat tolerant of soil boron, will show at least some symptoms of boron toxicity when soil boron content is greater than 1.8 ppm. When this content exceeds 2.0 ppm, few plants will perform well and some may not survive.[127][128][129]
It is thought that boron plays several essential roles in animals, including humans, but the exact physiological role is poorly understood.[130][131] A small human trial published in 1987 reported on postmenopausal women first made boron deficient and then repleted with 3 mg/day. Boron supplementation markedly reduced urinary calcium excretion and elevated the serum concentrations of 17 beta-estradiol and testosterone.[132]
The U.S. Institute of Medicine has not confirmed that boron is an essential nutrient for humans, so neither a Recommended Dietary Allowance (RDA) nor an Adequate Intake have been established. Adult dietary intake is estimated at 0.9 to 1.4 mg/day, with about 90% absorbed. What is absorbed is mostly excreted in urine. The Tolerable Upper Intake Level for adults is 20 mg/day.[133]
In 2013, a hypothesis suggested it was possible that boron and molybdenum catalyzed the production of РНК на Марс with life being transported to Earth via a meteorite around 3 billion years ago.[134]
There exist several known boron-containing natural антибиотики. The first one found was boromycin, изолированные от стрептомицеты.[135][136]
Врожденная эндотелиальная дистрофия 2 типа, редкая форма дистрофия роговицы, is linked to mutations in SLC4A11 gene that encodes a transporter reportedly regulating the intracellular concentration of boron.[137]
Analytical quantification
For determination of boron content in food or materials, the колориметрический curcumin method используется. Boron is converted to boric acid or бораты and on reaction with куркумин in acidic solution, a red colored boron-хелат сложный, rosocyanine, сформирован.[138]
Health issues and toxicity
| Опасности | |
|---|---|
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H302[139] | |
| NFPA 704 (огненный алмаз) | |
Elemental boron, boron oxide, борная кислота, borates, and many борорганические соединения are relatively nontoxic to humans and animals (with toxicity similar to that of table salt). В LD50 (dose at which there is 50% mortality) for animals is about 6 g per kg of body weight. Substances with LD50 above 2 g are considered nontoxic. An intake of 4 g/day of boric acid was reported without incident, but more than this is considered toxic in more than a few doses. Intakes of more than 0.5 grams per day for 50 days cause minor digestive and other problems suggestive of toxicity.[141] Dietary supplementation of boron may be helpful for bone growth, wound healing, and antioxidant activity,[142] and insufficient amount of boron in diet may result in boron deficiency.
Single medical doses of 20 g of борная кислота за neutron capture therapy have been used without undue toxicity.
Boric acid is more toxic to insects than to mammals, and is routinely used as an insecticide.[97]
В бораны (boron hydrogen compounds) and similar gaseous compounds are quite poisonous. As usual, boron is not an element that is intrinsically poisonous, but the toxicity of these compounds depends on structure (for another example of this phenomenon, see фосфин ).[14][15] The boranes are also highly flammable and require special care when handling. Sodium borohydride presents a fire hazard owing to its reducing nature and the liberation of hydrogen on contact with acid. Boron halides are corrosive.[143]

Boron is necessary for plant growth, but an excess of boron is toxic to plants, and occurs particularly in acidic soil.[144][145] It presents as a yellowing from the tip inwards of the oldest leaves and black spots in barley leaves, but it can be confused with other stresses such as magnesium deficiency in other plants.[146]
Смотрите также
Рекомендации
- ^ Van Setten и другие. 2007, pp. 2460–1
- ^ Брауншвейг, H .; Dewhurst, R. D.; Hammond, K.; Mies, J.; Radacki, K.; Vargas, A. (2012). "Ambient-Temperature Isolation of a Compound with a Boron-Boron Triple Bond". Наука. 336 (6087): 1420–2. Bibcode:2012Sci...336.1420B. Дои:10.1126/science.1221138. PMID 22700924. S2CID 206540959.
- ^ Zhang, K.Q.; Guo, B .; Braun, V.; Dulick, M.; Bernath, P.F. (1995). "Infrared Emission Spectroscopy of BF and AIF" (PDF). J. Molecular Spectroscopy. 170 (1): 82. Bibcode:1995JMoSp.170...82Z. Дои:10.1006/jmsp.1995.1058.
- ^ Melanie Schroeder. Eigenschaften von borreichen Boriden und Scandium-Aluminium-Oxid-Carbiden (PDF) (на немецком). п. 139.
- ^ Holcombe Jr., C. E.; Smith, D. D.; Lorc, J. D.; Duerlesen, W. K.; Carpenter; D. A. (October 1973). "Physical-Chemical Properties of beta-Rhombohedral Boron". High Temp. Наука. 5 (5): 349–57.
- ^ а б Хейнс, Уильям М., изд. (2016). CRC Справочник по химии и физике (97th ed.). CRC Press. п. 4.127. ISBN 9781498754293.
- ^ а б c Gay Lussac, J.L. & Thenard, L.J. (1808). "Sur la décomposition et la recomposition de l'acide boracique". Annales de chimie. 68: 169–174.
- ^ а б c Davy H (1809). "An account of some new analytical researches on the nature of certain bodies, particularly the alkalies, phosphorus, sulphur, carbonaceous matter, and the acids hitherto undecomposed: with some general observations on chemical theory". Философские труды Лондонского королевского общества. 99: 39–104. Дои:10.1098 / рстл.1809.0005.
- ^ а б "Atomic Weights and Isotopic Compositions for All Elements". Национальный институт стандартов и технологий. Получено 21 сентября 2008.
- ^ Szegedi, S.; Váradi, M.; Buczkó, Cs. M.; Várnagy, M.; Sztaricskai, T. (1990). "Determination of boron in glass by neutron transmission method". Journal of Radioanalytical and Nuclear Chemistry Letters. 146 (3): 177. Дои:10.1007/BF02165219.
- ^ "Q & A: Where does the element Boron come from?". Physics.illinois.edu. Архивировано из оригинал 29 мая 2012 г.. Получено 4 декабря 2011.
- ^ "Boron". Britannica encyclopedia.
- ^ Irschik H, Schummer D, Gerth K, Höfle G, Reichenbach H (1995). "The tartrolons, new boron-containing antibiotics from a myxobacterium, Сорангиум целлюлозум". Журнал антибиотиков. 48 (1): 26–30. Дои:10.7164/antibiotics.48.26. PMID 7532644.
- ^ а б Garrett, Donald E. (1998). Borates: handbook of deposits, processing, properties, and use. Академическая пресса. pp. 102, 385–386. ISBN 978-0-12-276060-0.
- ^ а б Calvert, J. B. "Boron". Денверский университет. Получено 5 мая 2009.
- ^ Hildebrand, G. H. (1982) "Borax Pioneer: Francis Marion Smith." Сан-Диего: Книги Хауэлла-Норта. п. 267 ISBN 0-8310-7148-6
- ^ Weeks, Mary Elvira (1933). "XII. Other Elements Isolated with the Aid of Potassium and Sodium: Beryllium, Boron, Silicon and Aluminum". Открытие элементов. Истон, Пенсильвания: Журнал химического образования. п. 156. ISBN 978-0-7661-3872-8.
- ^ Berzelius produced boron by reducing a borofluoride salt; specifically, by heating potassium borofluoride with potassium metal. See: Berzelius, J. (1824) "Undersökning af flusspatssyran och dess märkvärdigaste föreningar" (Part 2) (Investigation of hydrofluoric acid and of its most noteworthy compounds), Kongliga Vetenskaps-Academiens Handlingar (Proceedings of the Royal Science Academy), vol. 12, pp. 46–98; see especially pp. 88ff. Reprinted in German as: Berzelius, J. J. (1824) "Untersuchungen über die Flußspathsäure und deren merkwürdigste Verbindungen", Poggendorff's Annalen der Physik und Chemie, т. 78, pages 113–150.
- ^ Weintraub, Ezekiel (1910). "Preparation and properties of pure boron". Transactions of the American Electrochemical Society. 16: 165–184.
- ^ а б Laubengayer, A. W.; Hurd, D. T.; Newkirk, A. E.; Hoard, J. L. (1943). "Boron. I. Preparation and Properties of Pure Crystalline Boron". Журнал Американского химического общества. 65 (10): 1924–1931. Дои:10.1021/ja01250a036.
- ^ Borchert, W.; Dietz, W .; Koelker, H. (1970). "Crystal Growth of Beta–Rhombohedrical Boron". Zeitschrift für Angewandte Physik. 29: 277. OSTI 4098583.
- ^ Berger, L. I. (1996). Semiconductor materials. CRC Press. стр.37–43. ISBN 978-0-8493-8912-2.
- ^ Delaplane, R.G.; Dahlborg, U.; Graneli, B.; Fischer, P.; Lundstrom, T. (1988). "A neutron diffraction study of amorphous boron". Журнал некристаллических твердых тел. 104 (2–3): 249–252. Bibcode:1988JNCS..104..249D. Дои:10.1016/0022-3093(88)90395-X.
- ^ R.G. Delaplane; Dahlborg, U.; Howells, W .; Lundstrom, T. (1988). "A neutron diffraction study of amorphous boron using a pulsed source". Журнал некристаллических твердых тел. 106 (1–3): 66–69. Bibcode:1988JNCS..106...66D. Дои:10.1016/0022-3093(88)90229-3.
- ^ а б c Oganov, A.R.; Chen J.; Gatti C.; Ma Y.-M.; Yu T.; Liu Z.; Glass C.W.; Ma Y.-Z.; Kurakevych O.O.; Solozhenko V.L. (2009). "Ionic high-pressure form of elemental boron" (PDF). Природа. 457 (7231): 863–867. arXiv:0911.3192. Bibcode:2009Natur.457..863O. Дои:10.1038/nature07736. PMID 19182772. S2CID 4412568.
- ^ van Setten M.J.; Uijttewaal M.A.; de Wijs G.A.; de Groot R.A. (2007). "Thermodynamic stability of boron: The role of defects and zero point motion" (PDF). Варенье. Chem. Soc. 129 (9): 2458–2465. Дои:10.1021/ja0631246. PMID 17295480.
- ^ Widom M.; Mihalkovic M. (2008). "Symmetry-broken crystal structure of elemental boron at low temperature". Phys. Ред. B. 77 (6): 064113. arXiv:0712.0530. Bibcode:2008PhRvB..77f4113W. Дои:10.1103/PhysRevB.77.064113. S2CID 27321818.
- ^ Eremets, M. I.; Struzhkin, V. V.; Mao, H.; Hemley, R. J. (2001). "Superconductivity in Boron". Наука. 293 (5528): 272–4. Bibcode:2001Sci...293..272E. Дои:10.1126/science.1062286. PMID 11452118. S2CID 23001035.
- ^ Wentorf, R. H. Jr (1 January 1965). "Boron: Another Form". Наука. 147 (3653): 49–50. Bibcode:1965Sci...147...49W. Дои:10.1126/science.147.3653.49. PMID 17799779. S2CID 20539654.
- ^ Hoard, J. L.; Sullenger, D. B.; Kennard, C. H. L.; Hughes, R. E. (1970). "The structure analysis of β-rhombohedral boron". J. Solid State Chem.. 1 (2): 268–277. Bibcode:1970JSSCh...1..268H. Дои:10.1016/0022-4596(70)90022-8.
- ^ Will, G.; Kiefer, B. (2001). "Electron Deformation Density in Rhombohedral a-Boron". Zeitschrift für Anorganische und Allgemeine Chemie. 627 (9): 2100. Дои:10.1002/1521-3749(200109)627:9<2100::AID-ZAAC2100>3.0.CO;2-G.
- ^ Talley, C. P.; LaPlaca, S.; Post, B. (1960). "A new polymorph of boron". Acta Crystallogr. 13 (3): 271–272. Дои:10.1107/S0365110X60000613.
- ^ Solozhenko, V. L.; Kurakevych, O. O.; Oganov, A. R. (2008). "On the hardness of a new boron phase, orthorhombic γ-B28". Journal of Superhard Materials. 30 (6): 428–429. arXiv:1101.2959. Дои:10.3103/S1063457608060117. S2CID 15066841.
- ^ а б c Zarechnaya, E. Yu.; Dubrovinsky, L.; Dubrovinskaia, N.; Filinchuk, Y.; Chernyshov, D.; Dmitriev, V.; Miyajima, N.; Эль Гореси, А .; и другие. (2009). "Superhard Semiconducting Optically Transparent High Pressure Phase of Boron". Phys. Rev. Lett. 102 (18): 185501. Bibcode:2009PhRvL.102r5501Z. Дои:10.1103/PhysRevLett.102.185501. PMID 19518885.
- ^ Nelmes, R. J.; Loveday, J. S.; Allan, D. R.; Hull, S.; Hamel, G.; Grima, P.; Hull, S. (1993). "Neutron- and x-ray-diffraction measurements of the bulk modulus of boron". Phys. Ред. B. 47 (13): 7668–7673. Bibcode:1993PhRvB..47.7668N. Дои:10.1103/PhysRevB.47.7668. PMID 10004773.
- ^ Madelung, O., ed. (1983). Landolt-Bornstein, New Series. 17e. Берлин: Springer-Verlag.
- ^ а б c d е ж Холлеман, Арнольд Ф .; Виберг, Эгон; Виберг, Нильс (1985). "Bor". Lehrbuch der Anorganischen Chemie (на немецком языке) (91–100 изд.). Вальтер де Грюйтер. pp. 814–864. ISBN 978-3-11-007511-3.
- ^ Key, Jessie A. (14 September 2014). "Violations of the Octet Rule". Introductory Chemistry. Получено 14 августа 2019.
- ^ "Mindat.org - Mines, Minerals and More". www.mindat.org.
- ^ Engler, M. (2007). "Hexagonal Boron Nitride (hBN) – Applications from Metallurgy to Cosmetics" (PDF). Cfi/Ber. DKG. 84: D25. ISSN 0173-9913.
- ^ Greim, Jochen & Schwetz, Karl A. (2005). "Boron Carbide, Boron Nitride, and Metal Borides". Boron Carbide, Boron Nitride, and Metal Borides, in Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH: Вайнхайм. Дои:10.1002/14356007.a04_295.pub2. ISBN 978-3527306732.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Jones, Morton E. & Marsh, Richard E. (1954). "The Preparation and Structure of Magnesium Boride, MgB2". Журнал Американского химического общества. 76 (5): 1434–1436. Дои:10.1021/ja01634a089.
- ^ Canfield, Paul C.; Крэбтри, Джордж У. (2003). "Magnesium Diboride: Better Late than Never" (PDF). Физика сегодня. 56 (3): 34–40. Bibcode:2003PhT....56c..34C. Дои:10.1063/1.1570770.
- ^ "Категория" Новости + статьи "не найдена - Сервер документов ЦЕРН". cds.cern.ch.
- ^ Cardarelli, François (2008). "Titanium Diboride". Materials handbook: A concise desktop reference. pp. 638–639. ISBN 978-1-84628-668-1.
- ^ Barth, S. (1997). "Boron isotopic analysis of natural fresh and saline waters by negative thermal ionization mass spectrometry". Химическая геология. 143 (3–4): 255–261. Bibcode:1997ChGeo.143..255B. Дои:10.1016/S0009-2541(97)00107-1.
- ^ Liu, Z. (2003). "Two-body and three-body halo nuclei". Наука Китай Физика, механика и астрономия. 46 (4): 441. Bibcode:2003ScChG..46..441L. Дои:10.1360/03yw0027. S2CID 121922481.
- ^ Steinbrück, Martin (2004). "Results of the B4C Control Rod Test QUENCH-07" (PDF). Forschungszentrum Karlsruhe in der Helmholtz-Gemeinschaft. Архивировано из оригинал (PDF) 19 июля 2011 г.
- ^ "Commissioning of Boron Enrichment Plant". Indira Gandhi Centre for Atomic Research. Архивировано из оригинал 8 декабря 2008 г.. Получено 21 сентября 2008.
- ^ Aida, Masao; Fujii, Yasuhiko; Okamoto, Makoto (1986). "Chromatographic Enrichment of 10B by Using Weak-Base Anion-Exchange Resin". Separation Science and Technology. 21 (6): 643–654. Дои:10.1080/01496398608056140. showing an enrichment from 18% to above 94%.
- ^ Barth, Rolf F. (2003). "A Critical Assessment of Boron Neutron Capture Therapy: An Overview". Журнал нейроонкологии. 62 (1): 1–5. Дои:10.1023/A:1023262817500. PMID 12749698. S2CID 31441665.
- ^ Coderre, Jeffrey A.; Morris, G. M. (1999). "The Radiation Biology of Boron Neutron Capture Therapy". Радиационные исследования. 151 (1): 1–18. Bibcode:1999RadR..151....1C. Дои:10.2307/3579742. JSTOR 3579742. PMID 9973079.
- ^ Barth, Rolf F.; S; F (1990). "Boron Neutron Capture Therapy of Cancer". Исследования рака. 50 (4): 1061–1070. PMID 2404588.
- ^ "Boron Neutron Capture Therapy – An Overview". Pharmainfo.net. 22 августа 2006 г. Архивировано с оригинал 23 июля 2011 г.. Получено 7 ноября 2011.
- ^ а б Duderstadt, James J.; Hamilton, Louis J. (1976). Nuclear Reactor Analysis. Wiley-Interscience. п.245. ISBN 978-0-471-22363-4.
- ^ Yu, J .; Chen, Y .; Elliman, R.G .; Petravic, M. (2006). "Isotopically Enriched 10BN Nanotubes" (PDF). Современные материалы. 18 (16): 2157–2160. Дои:10.1002/adma.200600231. Архивировано из оригинал (PDF) 3 августа 2008 г.
- ^ Nevins, W. M. (1998). "A Review of Confinement Requirements for Advanced Fuels". Журнал термоядерной энергии. 17 (1): 25–32. Bibcode:1998JFuE...17...25N. Дои:10.1023/A:1022513215080. S2CID 118229833.
- ^ "Boron NMR". BRUKER Biospin. Архивировано из оригинал 2 мая 2009 г.. Получено 5 мая 2009.
- ^ Mokhov, A.V., Kartashov, P.M., Gornostaeva, T.A., Asadulin, A.A., Bogatikov, O.A., 2013: Complex nanospherulites of zinc oxide and native amorphous boron in the Lunar regolith from Mare Crisium. Doklady Earth Sciences 448(1) 61-63
- ^ Миндат, http://www.mindat.org/min-43412.html
- ^ Gasda, Patrick J.; и другие. (5 September 2017). "In situ detection of boron by ChemCam on Mars" (PDF). Письма о геофизических исследованиях. 44 (17): 8739–8748. Bibcode:2017GeoRL..44.8739G. Дои:10.1002/2017GL074480.
- ^ Paoletta, Rae (6 September 2017). "Curiosity Has Discovered Something That Raises More Questions About Life on Mars". Gizmodo. Получено 6 сентября 2017.
- ^ Kistler, R. B. (1994). "Boron and Borates" (PDF). Промышленные полезные ископаемые и горные породы (6th ed.): 171–186.
- ^ Zbayolu, G.; Poslu, K. (1992). "Mining and Processing of Borates in Turkey". Обзор переработки полезных ископаемых и добывающей металлургии. 9 (1–4): 245–254. Дои:10.1080/08827509208952709.
- ^ Kar, Y.; Şen, Nejdet; Demİrbaş, Ayhan (2006). "Boron Minerals in Turkey, Their Application Areas and Importance for the Country's Economy". Minerals & Energy – Raw Materials Report. 20 (3–4): 2–10. Дои:10.1080/14041040500504293.
- ^ Global reserves chart. Проверено 14 августа 2014 года.
- ^ Şebnem Önder; Ayşe Eda Biçer & Işıl Selen Denemeç (September 2013). "Are certain minerals still under state monopoly?" (PDF). Mining Turkey. Получено 21 декабря 2013.
- ^ "Turkey as the global leader in boron export and production" (PDF). European Association of Service Providers for Persons with Disabilities Annual Conference 2013. Получено 18 декабря 2013.
- ^ "U.S. Borax Boron Mine". The Center for Land Use Interpretation, Ludb.clui.org. Архивировано из оригинал 11 февраля 2012 г.. Получено 26 апреля 2013.
- ^ "Boras". Rio Tinto. 10 апреля 2012 г. Архивировано с оригинал 18 сентября 2012 г.. Получено 26 апреля 2013.
- ^ "Boron Properties". Лос-Аламосская национальная лаборатория. Получено 18 сентября 2008.
- ^ а б The Economics of Boron (11-е изд.). Roskill Information Services, Ltd. 2006. ISBN 978-0-86214-516-3.
- ^ "Raw and Manufactured Materials 2006 Overview". Архивировано из оригинал 8 июля 2011 г.. Получено 5 мая 2009.
- ^ "Roskill reports: boron". Роскилл. Архивировано из оригинал on 4 October 2003. Получено 5 мая 2009.
- ^ "Boron: Statistics and Information". USGS. Получено 5 мая 2009.
- ^ а б c Хаммонд, К. Р. (2004). Элементы в Справочнике по химии и физике (81-е изд.). CRC press. ISBN 978-0-8493-0485-9.
- ^ [1] В архиве 6 октября 2014 г. Wayback Machine Discussion of various types of boron addition to glass fibers in fiberglass. Проверено 14 августа 2014 года.
- ^ Global end use of boron in 2011. Проверено 14 августа 2014 г.
- ^ Herring, H. W. (1966). "Selected Mechanical and Physical Properties of Boron Filaments" (PDF). НАСА. Получено 20 сентября 2008.
- ^ Layden, G. K. (1973). "Fracture behaviour of boron filaments". Журнал материаловедения. 8 (11): 1581–1589. Bibcode:1973JMatS...8.1581L. Дои:10.1007/BF00754893. S2CID 136959123.
- ^ Kostick, Dennis S. (2006). "Mineral Yearbook: Boron" (PDF). Геологическая служба США. Получено 20 сентября 2008.
- ^ Cooke, Theodore F. (1991). "Inorganic Fibers—A Literature Review". Журнал Американского керамического общества. 74 (12): 2959–2978. Дои:10.1111/j.1151-2916.1991.tb04289.x.
- ^ Johansson, S.; Schweitz, Jan-Åke; Westberg, Helena; Boman, Mats (1992). "Microfabrication of three-dimensional boron structures by laser chemical processing". Журнал прикладной физики. 72 (12): 5956–5963. Bibcode:1992JAP....72.5956J. Дои:10.1063/1.351904.
- ^ E. Fitzer; и другие. (2000). "Fibers, 5. Synthetic Inorganic". Энциклопедия промышленной химии Ульмана. Дои:10.1002/14356007.a11_001. ISBN 978-3527306732. Отсутствует или пусто
| название =(помощь) - ^ Pfaender, H. G. (1996). Schott guide to glass (2-е изд.). Springer. п.122. ISBN 978-0-412-62060-7.
- ^ Zhang F X; Xu F F; Mori T; Liu Q L; Sato A & Tanaka T (2001). "Crystal structure of new rare-earth boron-rich solids: REB28.5C4". J. Сплавы Compd. 329 (1–2): 168–172. Дои:10.1016 / S0925-8388 (01) 01581-X.
- ^ Fabrication and Evaluation of Urania-Alumina Fuel Elements and Boron Carbide Burnable Poison Elements, Wisnyi, L. G. and Taylor, K.M., in "ASTM Special Technical Publication No. 276: Materials in Nuclear Applications", Committee E-10 Staff, American Society for Testing Materials, 1959
- ^ Weimer, Alan W. (1997). Carbide, Nitride and Boride Materials Synthesis and Processing. Chapman & Hall (London, New York). ISBN 978-0-412-54060-8.
- ^ Solozhenko, V. L.; Kurakevych, Oleksandr O.; Le Godec, Yann; Mezouar, Mohamed; Mezouar, Mohamed (2009). "Ultimate Metastable Solubility of Boron in Diamond: Synthesis of Superhard Diamondlike BC5" (PDF). Phys. Rev. Lett. 102 (1): 015506. Bibcode:2009PhRvL.102a5506S. Дои:10.1103/PhysRevLett.102.015506. PMID 19257210.
- ^ а б Qin, Jiaqian; He, Duanwei; Wang, Jianghua; Fang, Leiming; Лей, Ли; Ли, Юнцзюнь; Hu, Juan; Kou, Zili; Bi, Yan (2008). "Is Rhenium Diboride a Superhard Material?". Современные материалы. 20 (24): 4780–4783. Дои:10.1002/adma.200801471.
- ^ Wentorf, R. H. (1957). "Cubic form of boron nitride". J. Chem. Phys. 26 (4): 956. Bibcode:1957JChPh..26..956W. Дои:10.1063/1.1745964.
- ^ Gogotsi, Y. Г., Андриевски, Р.А. (1999). Материаловедение карбидов, нитридов и боридов. Springer. стр.270. ISBN 978-0-7923-5707-0.
- ^ Шмидт, Юрген; Бёлинг, Мариан; Буркхардт, Ульрих; Гринь, Юрий (2007). «Получение диборида титана TiB.2 методом искрового плазменного спекания при низкой скорости нагрева ». Наука и технология перспективных материалов. 8 (5): 376–382. Bibcode:2007STAdM ... 8..376S. Дои:10.1016 / j.stam.2007.06.009.
- ^ Записывать в базе данных товаров для дома NLM
- ^ Томпсон, Р. (1974). «Промышленное применение соединений бора». Чистая и прикладная химия. 39 (4): 547. Дои:10.1351 / pac197439040547.
- ^ а б Klotz, J. H .; Moss, J. I .; Zhao, R .; Дэвис-младший, Л. Р .; Паттерсон, Р. С. (1994). «Оральная токсичность борной кислоты и других соединений бора для незрелых кошачьих блох (Siphonaptera: Pulicidae)». J. Econ. Энтомол. 87 (6): 1534–1536. Дои:10.1093 / jee / 87.6.1534. PMID 7836612.
- ^ Мэй, Гэри С .; Спанос, Костас Дж. (2006). Основы производства полупроводников и управления технологическими процессами. Джон Уайли и сыновья. стр.51 –54. ISBN 978-0-471-78406-7.
- ^ Шерер, Дж. Майкл (2005). Полупроводниковая промышленность: управление выхлопными газами. CRC Press. С. 39–60. ISBN 978-1-57444-720-0.
- ^ Zschech, Ehrenfried; Уилан, Кэролайн и Миколаджик, Томас (2005). Материалы для информационных технологий: устройства, межкомпонентные соединения и упаковка. Birkhäuser. п. 44. ISBN 978-1-85233-941-8.
- ^ Кэмпбелл, Питер (1996). Материалы для постоянных магнитов и их применение. Издательство Кембриджского университета. п. 45. ISBN 978-0-521-56688-9.
- ^ Мартин, Джеймс Э (2008). Физика для радиационной защиты: Справочник. С. 660–661. ISBN 978-3-527-61880-4.
- ^ Пастина, Б .; Isabey, J .; Хикель, Б. (1999). «Влияние химического состава воды на радиолиз воды теплоносителя первого контура в реакторах с водой под давлением». Журнал ядерных материалов. 264 (3): 309–318. Bibcode:1999JNuM..264..309P. Дои:10.1016 / S0022-3115 (98) 00494-2. ISSN 0022-3115.
- ^ Kosanke, B.J .; и другие. (2004). Пиротехническая химия. Журнал пиротехники. п. 419. ISBN 978-1-889526-15-7.
- ^ "Декагидрат буры". Получено 5 мая 2009.
- ^ Дэвис, А. С. (1992). Наука и практика сварки: наука и технология сварки. Издательство Кембриджского университета. п. 56. ISBN 978-0-521-43565-9.
- ^ Хоррокс, А. И Прайс, Д. (2001). Огнезащитные материалы. Woodhead Publishing Ltd. стр.55. ISBN 978-1-85573-419-7.
- ^ Ide, F. (2003). «Информационные технологии и полимеры. Плоский дисплей». Инженерные материалы. 51: 84. Архивировано с оригинал 13 марта 2012 г.. Получено 28 мая 2009.
- ^ «Локхид SR-71 Блэкберд». Музей авиации Мартовское поле. Архивировано из оригинал 4 марта 2000 г.. Получено 2009-05-05.
- ^ Центр состояния миссии, 2 июня 2010 г., 1905 г. по Гринвичу, Космический полет, дата обращения 2010-06-02, Цитата: «Фланцы будут соединять ракету с наземными резервуарами для хранения, содержащими жидкий кислород, керосиновое топливо, гелий, газообразный азот и источником зажигания первой ступени под названием триэтилалюминий-триэтилборан, более известный как TEA-TEB. "
- ^ Янг, А. (2008). Двигатель Saturn V F-1: история "Аполлона". Springer. п. 86. ISBN 978-0-387-09629-2.
- ^ Carr, J.M .; Дагган, П. Дж .; Humphrey, D.G .; Platts, J. A .; Тиндаль, Э. М. (2010). «Защитные свойства древесины четвертичных эфиров арилспиробората аммония, полученных из 2,3-диола нафталина, 2,2'-бифенола и 3-гидрокси-2-нафтойной кислоты». Австралийский химический журнал. 63 (10): 1423. Дои:10.1071 / CH10132.
- ^ "Борная кислота". Chemicalland21.com.
- ^ Bonvini P; Зорзи Э; Basso G; Розолен А (2007). «Опосредованное бортезомибом ингибирование 26S протеасомы вызывает остановку клеточного цикла и индуцирует апоптоз CD-30.+ анапластическая крупноклеточная лимфома ». Лейкемия. 21 (4): 838–42. Дои:10.1038 / sj.leu.2404528. PMID 17268529.
- ^ «Обзор фармацевтических препаратов нейтронозахватной терапии». Pharmainfo.net. 22 августа 2006 г. Архивировано с оригинал 23 июля 2011 г.. Получено 26 апреля 2013.
- ^ Трэверс, Ричард Л .; Ренни, Джордж; Ньюнхэм, Рекс (1990). «Бор и артрит: результаты двойного слепого пилотного исследования». Журнал диетической медицины. 1 (2): 127–132. Дои:10.3109/13590849009003147.
- ^ Томпсон, Шерил (8 июля 2014 г.). «FDA одобрило препарат на основе бора для лечения грибковых инфекций ногтей на ногах». зола. Получено 7 октября 2015.
- ^ Родригес, Эрик А .; Ван, Йе; Крисп, Джессика Л .; Вера, Дэвид Р .; Tsien, Roger Y .; Тинг, Ричард (27 апреля 2016 г.). «Новая химия диоксаборолана позволяет получать [18F] -излучающие позитроны, флуоресцентные [18F] -многодальные биомолекулы из твердой фазы». Биоконъюгат Химия. 27 (5): 1390–1399. Дои:10.1021 / acs.bioconjchem.6b00164. ЧВК 4916912. PMID 27064381.
- ^ Ван, Йе; Ань, Фэй-Фэй; Чан, Марк; Фридман, Бет; Родригес, Эрик А .; Tsien, Roger Y .; Арас, Омер; Тинг, Ричард (5 января 2017 г.). «18F-излучающие / флуоресцентно меченные эритроциты позволяют визуализировать внутреннее кровоизлияние в модели внутричерепного кровоизлияния у мышей». Журнал церебрального кровотока и метаболизма. 37 (3): 776–786. Дои:10.1177 / 0271678x16682510. ЧВК 5363488. PMID 28054494.
- ^ Го, Хуа; Харикришна, Коммиди; Ведвьяс, Йогиндра; Макклоски, Жаклин Э; Чжан, Вэйци; Чен, Нанди; Нурили, Фуад; Ву, Эми П; Сайман, Халук Б. (23 мая 2019 г.). «Флуоресцентный агент, излучающий [18 F] -позитрон для визуализации PMSA, позволяет генетическое сообщение в адоптивно перенесенных генетически модифицированных клетках». ACS Химическая биология. 14 (7): 1449–1459. Дои:10.1021 / acschembio.9b00160. ISSN 1554-8929. ЧВК 6775626. PMID 31120734.
- ^ Canfield, Paul C .; Крэбтри, Джордж У. (2003). «Диборид магния: лучше поздно, чем никогда» (PDF). Физика сегодня. 56 (3): 34–41. Bibcode:2003ФТ .... 56с..34С. Дои:10.1063/1.1570770. Архивировано из оригинал (PDF) 17 декабря 2008 г.. Получено 22 сентября 2008.
- ^ Браччини, Валерия; Нарделли, Д .; Penco, R .; Грассо, Г. (2007). "Разработка обработанного ex situ MgB2 провода и их приложения к магнитам ». Physica C: сверхпроводимость. 456 (1–2): 209–217. Bibcode:2007PhyC..456..209B. Дои:10.1016 / j.physc.2007.01.030.
- ^ Ву, Сяовэй; Chandel, R. S .; Ли, Ханг (2001). «Оценка переходной жидкофазной связи между суперсплавами на никелевой основе». Журнал материаловедения. 36 (6): 1539–1546. Bibcode:2001JMatS..36.1539W. Дои:10.1023 / А: 1017513200502. S2CID 134252793.
- ^ Dean, C. R .; Янг, А. Ф .; Meric, I .; Lee, C .; Wang, L .; Sorgenfrei, S .; Watanabe, K .; Taniguchi, T .; Kim, P .; Shepard, K. L .; Хон, Дж. (2010). «Подложки из нитрида бора для высококачественной графеновой электроники». Природа Нанотехнологии. 5 (10): 722–726. arXiv:1005.4917. Bibcode:2010НатНа ... 5..722Д. Дои:10.1038 / nnano.2010.172. PMID 20729834. S2CID 1493242.
- ^ Gannett, W .; Regan, W .; Watanabe, K .; Taniguchi, T .; Crommie, M. F .; Зеттл, А. (2010). «Подложки из нитрида бора для высокоподвижного графена, осажденного из газовой фазы». Письма по прикладной физике. 98 (24): 242105. arXiv:1105.4938. Bibcode:2011ApPhL..98x2105G. Дои:10.1063/1.3599708. S2CID 94765088.
- ^ Зеттл, Алекс; Коэн, Марвин (2010). «Физика нанотрубок нитрида бора». Физика сегодня. 63 (11): 34–38. Bibcode:2010ФТ .... 63к..34С. Дои:10.1063/1.3518210. S2CID 19773801.
- ^ Малер, Р.Л. «Основные микроэлементы растений. Бор в Айдахо» (PDF). Университет Айдахо. Архивировано из оригинал (PDF) 1 октября 2009 г.. Получено 5 мая 2009.
- ^ «Функции бора в питании растений» (PDF). U.S. Borax Inc. Архивировано с оригинал (PDF) 20 марта 2009 г.
- ^ Blevins, Dale G .; Лукашевский, К. М. (1998). «Функции бора в питании растений». Ежегодный обзор физиологии растений и молекулярной биологии растений. 49: 481–500. Дои:10.1146 / annurev.arplant.49.1.481. PMID 15012243.
- ^ «Бор». PDRhealth. Архивировано из оригинал 11 октября 2007 г.. Получено 18 сентября 2008.
- ^ Нильсен, Форрест Х. (1998). «Ультра-микроэлементы в питании: современные знания и предположения». Журнал микроэлементов в экспериментальной медицине. 11 (2–3): 251–274. Дои:10.1002 / (SICI) 1520-670X (1998) 11: 2/3 <251 :: AID-JTRA15> 3.0.CO; 2-Q.
- ^ Nielsen FH, Hunt CD, Mullen LM, Hunt JR (1987). «Влияние диетического бора на метаболизм минералов, эстрогена и тестостерона у женщин в постменопаузе». FASEB J. 1 (5): 394–7. Дои:10.1096 / fasebj.1.5.3678698. PMID 3678698. S2CID 93497977.
- ^ Бор. В: Нормы потребления витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и меди. Национальная академия прессы. 2001, стр. 510–521.
- ^ «Изначальным бульоном жизни был сухой марсианский суп из чашки». Новый ученый. 29 августа 2013 г.. Получено 29 августа 2013.
- ^ Hütter, R .; Keller-Schien, W .; Knüsel, F .; Прелог, В .; Роджерс младший, Г. К .; Suter, P .; Vogel, G .; Voser, W .; Зенер, Х. (1967). "Stoffwechselprodukte von Mikroorganismen. 57. Mitteilung. Boromycin". Helvetica Chimica Acta. 50 (6): 1533–1539. Дои:10.1002 / hlca.19670500612. PMID 6081908.
- ^ Dunitz, J. D .; Хоули, Д. М .; Miklos, D .; Уайт, Д. Н. Дж .; Берлин, Y .; Marusić, R .; Прелог В. (1971). «Состав боромицина». Helvetica Chimica Acta. 54 (6): 1709–1713. Дои:10.1002 / hlca.19710540624. PMID 5131791.
- ^ Vithana, En; Morgan, P; Sundaresan, P; Ebenezer, Nd; Tan, Dt; Мохамед, штат Мэриленд; Ананд, S; Хине, Ко; Венкатараман, Д; Yong, Vh; Сальто-Теллез, М; Венкатраман, А; Guo, K; Хемадеви, B; Шринивасан, М; Праджня, V; Хине, М; Кейси-младший; Inglehearn, Cf; Аунг, Т. (июль 2006 г.). «Мутации в котранспортере бората натрия SLC4A11 вызывают рецессивную врожденную наследственную эндотелиальную дистрофию (CHED2)». Природа Генетика. 38 (7): 755–7. Дои:10,1038 / ng1824. ISSN 1061-4036. PMID 16767101. S2CID 11112294.
- ^ Silverman, L .; Трего, Кэтрин (1953). «Коррекционно-колориметрическое микроопределение бора методом куркумин-ацетонового раствора». Анальный. Chem. 25 (11): 1639. Дои:10.1021 / ac60083a061.
- ^ «Бор 266620». Сигма-Олдрич.
- ^ «Паспорт безопасности данных - 266620». www.sigmaaldrich.com.
- ^ Нильсен, Форрест Х. (1997). «Бор в питании человека и животных». Растение и почва. 193 (2): 199–208. Дои:10.1023 / А: 1004276311956. S2CID 12163109. Получено 29 апреля 2018.
- ^ Пиццорно, Л. (август 2015 г.). "В боре нет ничего скучного". Интегративная медицина. 14 (4): 35–48. ЧВК 4712861. PMID 26770156.
- ^ «Критерии гигиены окружающей среды 204: бор». то IPCS. 1998. Получено 5 мая 2009.
- ^ Зекри, Монги; Обреза, Том. "Бор (B) и хлор (Cl) для цитрусовых деревьев" (PDF). Расширение МФСА. Университет Флориды. Получено 30 июн 2017.
- ^ К. И. Певерилл; Л. А. Воробей; Дуглас Дж. Рейтер (1999). Анализ почвы: руководство по интерпретации. Csiro Publishing. С. 309–311. ISBN 978-0-643-06376-1.
- ^ М. П. Рейнольдс (2001). Применение физиологии в селекции пшеницы. СИММИТ. п. 225. ISBN 978-970-648-077-4.
внешняя ссылка
- Бор в Периодическая таблица видео (Ноттингемский университет)
- Дж. Б. Калверт: Бор, 2004 г., частный сайт (заархивированная версия )