Триэтилборан - Википедия - Triethylborane
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Триэтилборан | |||
| Другие имена Триэтилборн, триэтилборн | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.002.383 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C6ЧАС15B | |||
| Молярная масса | 98,00 г / моль | ||
| Внешность | От бесцветной до бледно-желтой жидкости | ||
| Плотность | 0,677 г / см3 | ||
| Температура плавления | -93 ° С (-135 ° F, 180 К) | ||
| Точка кипения | 95 ° С (203 ° F, 368 К) | ||
| Непригодный; очень реактивный | |||
| Опасности | |||
| Главный опасности | Спонтанно воспламеняется на воздухе; вызывает ожоги | ||
| Паспорт безопасности | Внешний SDS | ||
| R-фразы (устарело) | R11 R14 / 15 R17 R19 R34 R35 R36 / 37 | ||
| S-фразы (устарело) | S6 S7 / 8 S16 S33 S36 / 37/39 S43 А S45 S29 | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | <-20 ° С (-4 ° F, 253 К) | ||
| -20 ° С (-4 ° F, 253 К) | |||
| Родственные соединения | |||
Родственные соединения |
| ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
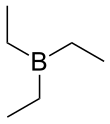
Триэтилборан (TEB), также называемый триэтилбор, является органоборан (соединение со связью B-C). Это бесцветный пирофорный жидкость. Его химическая формула (C2ЧАС5)3B, сокращенно Et3B. Растворим в органических растворителях. тетрагидрофуран и гексан.
Подготовка и состав
Триэтилборан получают по реакции триметилборат с триэтилалюминий:[1]
- Et3Al + (MeO)3B → Et3B + (MeO)3Al
Молекула мономерная, в отличие от H3B и Et3Al, которые склонны к димеризации. Имеет планарный БК3 основной.[1]
Приложения
Турбореактивный двигатель
Триэтилборан использовался для зажигания JP-7 топливо в Пратт и Уитни J58 турбореактивный /прямоточный воздушно-реактивный двигатель двигатели, питающие Локхид SR-71,[2] и его предшественник A-12 OXCART. Для этого подходит триэтилборан из-за его пирофорный свойства, особенно то, что горит при очень высокой температуре. Он был выбран в качестве метода зажигания из соображений надежности, а в случае с Blackbird, потому что JP-7 топливо имеет очень низкую летучесть и трудно воспламеняется. Обычные свечи зажигания создают высокий риск неисправности. Он использовался для запуска каждого двигателя и зажигания форсажные камеры.[3]
Ракета
Смешанный с 10–15% триэтилалюминий, он использовался перед стартом для зажигания Двигатели Ф-1 на Сатурн V ракета.[4]
В SpaceX Сокол 9 Ракета также использует смесь триэтилалюминий-триэтилборана в качестве воспламенителя первой и второй ступеней.[5]
Органическая химия
В промышленности триэтилборан используется в качестве инициатор в радикальный реакции, где он эффективен даже при низких температурах.[1] В качестве инициатора он может заменить некоторые оловоорганическое вещество соединения.
Реагирует с металлом енолирует, давая энокситриэтилбораты, которые могут быть алкилированы по α-углеродному атому кетона более селективно, чем в его отсутствие. Например, енолят от обработки циклогексанона гидрид калия при наличии триэтилборана дает 2-аллилциклогексанон с выходом 90%. Без него смесь продуктов содержит 43% моноаллилированного продукта, 31% диаллилированных циклогексанонов и 28% непрореагировавшего исходного материала.[6] Выбор основания и температуры влияет на то, будет ли производиться более или менее стабильный енолят, что позволяет контролировать положение заместителей. Начиная с 2-метилциклогексанона, реакция с гидридом калия и триэтилборана в ТГФ при комнатной температуре приводит к более замещенному (и более стабильному) енолату, тогда как реакция при -78 ° C с гексаметилдисилазид калия, KN [Si (CH
3)
3]
2 а триэтилборан дает менее замещенный (и менее стабильный) енолят. После реакции с йодистый метил первая смесь дает 2,2-диметилциклогексанон с выходом 90%, а вторая дает 2,6-диметилциклогексанон с выходом 93%.[6][7]

Он используется в Деоксигенация Бартона – Маккомби реакция деоксигенации спиртов. В сочетании с три-терт-бутоксиалюминийгидрид расщепляет эфиры. Например, ТГФ после гидролиза превращается в 1-бутанол. Он также продвигает определенные варианты Реформатский реакция.[8]
Триэтилборан является предшественником восстановителей триэтилборгидрида лития ("Супергидрид ") и триэтилборгидрид натрия.[9]
- MH + Et3B → MBHEt3 (М = Ли, Na)
Триэтилборан реагирует с метанолом с образованием диэтил (метокси) борана, который используется в качестве хелатирующего агента в Нарасака – Прасад сокращение для стереоселективной генерации син-1,3-диолы из β-гидроксикетонов.[10][11]
Безопасность
Триэтилборан сильно пирофорный, с самовоспламенение температура −20 ° C (−4 ° F),[12] горение характерным для соединений бора яблочно-зеленым пламенем. Таким образом, его обычно обрабатывают и хранят с помощью безвоздушные методы. Триэтилборан также очень токсичен при проглатывании, его ЛД50 составляет 235 мг / кг. [13] у подопытных крыс
Смотрите также
Рекомендации
- ^ а б c Brotherton, Роберт Дж .; Вебер, К. Джозеф; Guibert, Clarence R .; Литтл, Джон Л. (15 июня 2000 г.). «Соединения бора». Энциклопедия промышленной химии Ульмана. Wiley-VCH. Дои:10.1002 / 14356007.a04_309. ISBN 3527306730.
- ^ «Локхид SR-71 Блэкберд». Музей авиации Мартовское поле. Архивировано из оригинал на 2000-03-04. Получено 2009-05-05.
- ^ "Руководство по летной эксплуатации Lockheed SR-71 Blackbird". www.sr-71.org. Получено 2011-01-26.
- ^ А. Янг (2008). Двигатель Saturn V F-1: история "Аполлона". Springer. п. 86. ISBN 978-0-387-09629-2.
- ^ Центр состояния миссии, 2 июня 2010 г., 1905 г. по Гринвичу, Космический полет, дата обращения 2010-06-02, Цитата: «Фланцы будут соединять ракету с наземными резервуарами для хранения, содержащими жидкий кислород, керосиновое топливо, гелий, газообразный азот, и источником воспламенителя первой ступени под названием триэтилалюминий-триэтилборан, более известный как TEA-TEB. "
- ^ а б Крич, Дэвид, изд. (2008). «Энокситриэтилбораты и эноксидиэтилбораны». Реагенты для радикальной и радикально-ионной химии. Справочник реагентов для органического синтеза. 11. Джон Уайли и сыновья. ISBN 9780470065365.
- ^ Негиси, Эй-ичи; Чаттерджи, Сугата (1983). «Высокорегиоселективное получение« термодинамических »енолятов и их прямая характеристика с помощью ЯМР». Буквы Тетраэдра. 24 (13): 1341–1344. Дои:10.1016 / S0040-4039 (00) 81651-2.
- ^ Ямамото, Ёсинори; Ёсимицу, Такехико; Вуд, Джон Л.; Шахерер, Лаура Николь (15 марта 2007 г.). «Триэтилборан». Энциклопедия реагентов для органического синтеза. Вайли. Дои:10.1002 / 047084289X.rt219.pub3. ISBN 978-0471936237.
- ^ Binger, P .; Кёстер, Р. (1974). «Триэтилгидроборат натрия, тетраэтилборат натрия и триэтил-1-пропинилборат натрия». Неорганические синтезы. 15: 136–141. Дои:10.1002 / 9780470132463.ch31. ISBN 9780470132463.
- ^ Чен, Кау-Мин; Gunderson, Karl G .; Hardtmann, Goetz E .; Прасад, Капа; Репич, Олян; Шапиро, Майкл Дж. (1987). "Новый метод для На месте Получение алкоксидиалкилборанов и их использование для селективного получения 1,3-син Диолс ». Письма по химии. 16 (10): 1923–1926. Дои:10.1246 / кл.1987.1923.
- ^ Ян, Джаемун (2008). «Диастереоселективный Syn-Снижение уровня β-гидроксикетонов ». Шестичленные переходные состояния в органическом синтезе. Джон Уайли и сыновья. С. 151–155. ISBN 9780470199046.
- ^ Топливо и химикаты - Температура самовоспламенения
- ^ [1]