Аммиачно-боран - Ammonia borane
 | |
| Имена | |
|---|---|
| Название ИЮПАК Аммониотригидроборат[нужна цитата ] | |
| Другие имена Боразане[нужна цитата ] | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.170.890 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| BNH 6 | |
| Молярная масса | 30,865 г моль−1 |
| Внешность | Бесцветные кристаллы |
| Плотность | 780 мг мл−1 |
| Температура плавления | 104 ° С (219 ° F, 377 К) |
| Структура | |
| I4мм, четырехугольный | |
| Тетрагональный в B и N | |
| Тетрагидраль в B и N | |
| 5.2 D | |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| Родственные соединения | |
Родственные соединения | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
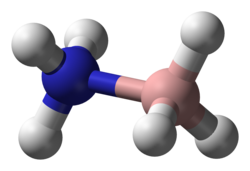
Аммиачно-боран (также систематически называемый амминетригидридобор), также называется боразан, это химическое соединение с формулой H3NBH3. Бесцветное или белое твердое вещество - простейший молекулярный бор -азот -гидрид соединение. Он привлек внимание как источник водород топливо, но в остальном представляет в первую очередь академический интерес.
Синтез
Реакция диборан с участием аммиак в основном дает диаммонийную соль [H2B (NH3)2]+(BH4)−. Аммиачный боран является основным продуктом, когда аддукт борана используется вместо диборана:[1]
- BH3(THF ) + NH3 → BH3NH3 + THF
Свойства и структура
Молекула принимает такую структуру, как этан, с чем это изоэлектронный. Расстояние B-N составляет 1,58 (2) Å. Расстояния B − H и N − H составляют 1,15 и 0,96 Å соответственно. Его сходство с этаном незначительно, поскольку аммиачный боран - твердое вещество, а этан - газ: их точки плавления различаются на 284 ° C. Это различие согласуется с высокополярной природой аммиачного борана. Атомы H, присоединенные к бору, гидридные, а атомы азота, присоединенные к азоту, несколько кислые.

Структура твердого тела свидетельствует о тесной ассоциации NЧАС и BЧАС центры. Ближайшее расстояние H − H составляет 1,990 Å, что можно сравнить с расстоянием связывания H − H 0,74 Å. Это взаимодействие называется дигидрогенная связь.[2][3] Первоначальный кристаллографический анализ этого соединения изменил назначение B и N. Обновленная структура была получена с улучшенными данными с использованием техники нейтронография это позволило расположить атомы водорода с большей точностью.
![Часть кристаллической структуры аммиачного борана [2]](http://upload.wikimedia.org/wikipedia/commons/thumb/9/93/Ammonia-borane-xtal-3D-balls.png/300px-Ammonia-borane-xtal-3D-balls.png)
Использует
Аммиачный боран был предложен в качестве носителя для хранения водород, например когда газ используется в качестве топлива для автомобилей. Его можно заставить выделять водород при нагревании, который сначала полимеризуется до (NH2BH2)п, затем в (NHBH)п,[4] который в конечном итоге разлагается на нитрид бора (BN) при температуре выше 1000 ° C.[5] Он более плотный по водороду, чем жидкий водород, а также способен существовать при нормальных температурах и давлениях.[6]
Аммиачный боран находит применение в органический синтез как стабильное на воздухе производное диборана.[7]
Аналогичные аминобораны
Многие аналоги приготовлены из первичных, вторичных и даже третичные амины:
- Боран трет-бутиламин (тBuNH2→ BH3)
- Боран триметиламин (Меня3N → BH3)
- Боран изопропиламин (яPrNH2 → BH3)
Первый аминный аддукт борана был получен из триметиламин. Боран трет-бутиламиновый комплекс получают реакцией боргидрида натрия с хлоридом трет-бутиламмония. Обычно аддукты более устойчивы с более основными аминами. Возможны также вариации по борному компоненту, хотя первичные и вторичные бораны встречаются реже.[8]
Кроме того, было приготовлено множество комплексов борана, в том числе боран диметилсульфид (Меня2S → BH3) и боран-тетрагидрофуран (THF → BH3).
использованная литература
- ^ Shore, S.G .; Боддекер, К. В. (1964). «Крупномасштабный синтез H2B (NH3)2+BH4− и H3NBH3". Неорганическая химия. 3 (6): 914–915. Дои:10.1021 / ic50016a038.
- ^ а б Klooster, W. T .; Koetzle, T. F .; Siegbahn, P.E.M .; Richardson, T. B .; Крэбтри, Р. Х. (1999). «Исследование дигидрогенной связи N − H ··· H − B, включая кристаллическую структуру BH.3NH3 методом нейтронографии ». Журнал Американского химического общества. 121 (27): 6337–6343. Дои:10.1021 / ja9825332.
- ^ Boese, R .; Niederprüm, N .; Блазер, Д. (1992). Maksic, Z. B .; Eckert-Masic, M. (ред.). Молекулы в естествознании и медицине. Чичестер, Англия: Эллис Хорвуд. ISBN 978-0135615980.
- ^ Gutowski, M .; Отри, Т. (2006). «Особенности: Водород попадает на борт». Мир химии. 3 (3).
- ^ Frueh, S .; Kellett, R .; Mallery, C .; Молтер; Т .; Willis, W. S .; King'ondu, C .; Суиб, С. Л. (2011). «Пиролитическое разложение аммиачного борана до нитрида бора». Неорганическая химия. 50 (3): 783–792. Дои:10.1021 / ic101020k. PMID 21182274.
- ^ Stephens, F. H .; Pons, V .; Бейкер, Р. Т. (2007). "Аммиак-Боран: Источник водорода по преимуществу?". Dalton Transactions. 2007 (25): 2613–2626. Дои:10.1039 / b703053c. PMID 17576485.
- ^ Эндрюс, Гленн С.; Neelamkavil, Santhosh F. (2008). «Боран-Аммиак». В пакете, Лео А. (ред.). Энциклопедия реагентов для органического синтеза. Нью-Йорк: Джон Уайли и сыновья. Дои:10.1002 / 047084289X.rb238.pub2. ISBN 0471936235.
- ^ Штаубиц, Энн; Робертсон, Аласдер П. М .; Манеры, Ян (2010). «Аммиак-боран и родственные соединения как источники дигидрогена». Химические обзоры. 110 (7): 4079–4124. Дои:10.1021 / cr100088b. PMID 20672860.
