Переходный металл - Transition metal
| Часть серия на |
| Периодическая таблица |
|---|
Формы периодической таблицы |
По структуре таблицы Менделеева |
Страницы данных для элементов
|
|
В химии термин переходный металл (или же переходный элемент) имеет три возможных определения:
- В ИЮПАК определение[1] определяет переходный металл как " элемент чей атом имеет частично заполненный d подоболочки, или которая может привести к катионы с неполным d суб-оболочка ".
- Многие ученые описывают «переходный металл» как любой элемент в d-блок из периодическая таблица, который включает группы с 3 по 12 периодической таблицы.[2][3] На практике f-блок лантаноид и актинид ряды также считаются переходными металлами и называются «внутренними переходными металлами».
- Хлопок и Уилкинсон[4] расширьте краткое определение IUPAC (см. выше), указав, какие элементы включены. Помимо элементов групп с 4 по 11, они добавляют скандий и иттрий в группе 3, которые имеют частично заполненный d суб-оболочка в металлическое состояние. Однако лантан и актиний в группе 3 классифицируются как лантаноиды и актиниды соответственно.
Английский химик Чарльз Бери (1890–1968) впервые использовал слово переход в этом контексте в 1921 году, когда он упомянул переходная серия элементов при изменении внутреннего слоя электронов (например п = 3 в 4-й строке периодической таблицы) из стабильной группы из 8 в одну из 18 или от 18 до 32.[5][6][7] Эти элементы теперь известны как d-блок.
Классификация
в d-блок, атомы элементов имеют от одного до десяти d электроны.
| Группа | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
|---|---|---|---|---|---|---|---|---|---|---|
| Период 4 | 21Sc | 22Ti | 23V | 24Cr | 25Mn | 26Fe | 27Co | 28Ni | 29Cu | 30Zn |
| 5 | 39Y | 40Zr | 41Nb | 42Пн | 43Tc | 44RU | 45Rh | 46Pd | 47Ag | 48CD |
| 6 | 57Ла | 72Hf | 73Та | 74W | 75Re | 76Операционные системы | 77Ir | 78Pt | 79Au | 80Hg |
| 7 | 89Ac | 104Rf | 105Db | 106Sg | 107Bh | 108Hs | 109Mt | 110Ds | 111Rg | 112Cn |
Элементы групп 4–11 обычно считаются переходными металлами, что подтверждается их типичным химическим составом, то есть большим диапазоном комплексных ионов в различных степенях окисления, окрашенными комплексами и каталитическими свойствами либо в качестве элемента, либо в виде ионов (или обоих). Sc и Y в группе 3 также обычно считаются переходными металлами. Однако элементы La – Lu и Ac – Lr и группа 12 привлекают разные определения разных авторов.
- Многие учебники по химии и печатные периодические таблицы классифицируют La и Ac как элементы группы 3 и переходные металлы, поскольку их атомные конфигурации в основном состоянии являются s2d1 как Sc и Y. Элементы Ce – Lu считаются "лантаноид "серия (или" лантаноид "согласно ИЮПАК) и Th – Lr как"актинид " серии.[8][9] Две серии вместе классифицируются как f-блок элементы, или (в старых источниках) как «внутренние переходные элементы».
- Некоторые учебники по неорганической химии включают La с лантаноидами и Ac с актинидами.[4][10][11] Эта классификация основана на сходстве химического поведения и определяет по 15 элементов в каждой из двух серий, даже если они соответствуют заполнению ж подоболочка, которая может содержать только 14 электронов.
- Третья классификация определяет элементы f-блока как La – Yb и Ac – No, при этом Lu и Lr помещаются в группу 3.[5] Это основано на Принцип Ауфбау (или правило Маделунга) для заполнения электронных подоболочек, в которых 4f заполняется перед 5d (и 5f перед 6d), так что подоболочка f фактически заполнена в Yb (и No), в то время как Lu (и Lr) имеет an [] s2ж14d1 конфигурация. Однако La и Ac являются исключениями из принципа Ауфбау с электронной конфигурацией [] s2d1 (не [] с2ж1 как предсказывает принцип Ауфбау), поэтому из атомных электронных конфигураций не ясно, следует ли считать La или Lu (Ac или Lr) переходными металлами.[12] Эту проблему можно решить, если учесть, что возбужденные состояния для свободного атома и иона могут стать основным состоянием в химической среде; La и Ac имеют пустые низколежащие f-подоболочки, заполненные Lu и Lr, поэтому возбуждение f-орбиталей возможно в La и Ac, но не в Lu или Lr.
Цинк, кадмий, и Меркурий обычно исключаются из переходных металлов,[5] поскольку у них есть электронная конфигурация [ ]d10s2, без неполных d ракушка.[13] в степень окисления +2, ионы имеют электронную конфигурацию []… d10. Хотя эти элементы могут существовать в других степенях окисления, включая степень окисления +1, как в двухатомном ионе Hg2+
2, у них еще есть полный d оболочка в этих степенях окисления. Таким образом, элементы группы 12 Zn, Cd и Hg могут быть отнесены к определенным критериям как постпереходные металлы в этом случае. Однако часто бывает удобно включить эти элементы в обсуждение переходных элементов. Например, при обсуждении энергия стабилизации кристаллического поля переходных элементов первого ряда удобно включать также элементы кальций и цинк, поскольку оба Ca2+
и Zn2+
имеют нулевое значение, с которым можно сравнивать значения для других ионов переходных металлов. Другой пример встречается в Серия Ирвинга – Уильямса констант устойчивости комплексов.
Недавний (хотя и оспариваемый и до сих пор не воспроизводимый независимо) синтез фторид ртути (IV) (HgF
4) был принят некоторыми, чтобы укрепить мнение о том, что элементы группы 12 следует рассматривать как переходные металлы,[14] но некоторые авторы до сих пор считают это соединение исключительным.[15] Копернициум Ожидается, что он сможет использовать свои d-электроны в химии, поскольку его 6d-подоболочка дестабилизирована сильным релятивистские эффекты из-за его очень высокого атомного номера, и как таковой, как ожидается, будет иметь поведение, подобное переходному металлу, когда он показывает более высокие степени окисления, чем +2 (которые точно не известны для более легких элементов группы 12).
Несмотря на то что мейтнерий, Дармштадтиум, и рентгений находятся в d-блоке и, как ожидается, будут вести себя как переходные металлы, аналогичные их более легким родственным соединениям. иридий, платина, и золото, экспериментально это пока не подтверждено.
Подклассы
Ранние переходные металлы находятся в левой части периодической таблицы от группы 3 к группе 7. Поздние переходные металлы находятся на правой стороне d-блока, от группы 8 до 11 (и 12, если это считается переходными металлами).
Электронная конфигурация
Общая электронная конфигурация d-блочные элементы - это (благородный газ ) (п − 1)d1–10нс0–2. Здесь «(благородный газ)» - это конфигурация последнего благородного газа, предшествующего рассматриваемому атому, а n - максимальное главное квантовое число занятой орбитали в этом атоме. Например, Ti (Z = 22) находится в периоде 4, так что n = 4, первые 18 электронов имеют такую же конфигурацию Ar в конце периода 3, а общая конфигурация (Ar) 3d24 с2. Переходные металлы периодов 6 и 7 также добавляют (п − 2)ж0–14 электроны, которые не указаны в таблицах ниже.
В Правило Маделунга предсказывает, что внутренний d орбиталь заполняется после валентной оболочки s орбитальный. Типичный электронная структура атомов переходного металла записывается как (благородный газ) нс2(п − 1)dм. Однако это правило является лишь приблизительным - оно справедливо только для некоторых переходных элементов и только тогда в основных нейтральных состояниях.
В d sub-shell - предпоследняя подоболочка, обозначается как суб-оболочка. Число s-электронов во внешней s-подоболочке обычно составляет один или два, за исключением палладия (Pd), в котором нет электронов. s субоболочка в основном состоянии. В s суб-оболочка в валентной оболочке представлена как нс суб-оболочка, например 4с. В периодической таблице переходные металлы представлены в восьми группах (от 4 до 11), некоторые авторы включают некоторые элементы в группы 3 или 12.
Элементы в группе 3 имеют нс2(п − 1)d1 конфигурация. Первая серия переходов присутствует в 4-м периоде и начинается после Ca (Z = 20) группы 2 с конфигурацией [Ar] 4s2, или же скандий (Sc), первый элемент группы 3 с атомным номером Z = 21 и конфигурация [Ar] 4s23d1, в зависимости от используемого определения. При перемещении слева направо электроны добавляются к одному и тому же d суб-оболочка, пока она не будет завершена. Элемент группы 11 в первой переходной серии - это медь (Cu) нетипичной конфигурации [Ar] 4s13d10. Несмотря на заполненную подоболочку d в металлической меди, она, тем не менее, образует стабильный ион с неполной подоболочкой d. Поскольку добавленные электроны заполняют орбитали, свойства d-элементы блока сильно отличаются от элементов s и п блочные элементы, в которых заливка происходит либо в s или в п-орбитали валентной оболочки. Электронная конфигурация отдельных элементов, присутствующих во всех сериях d-блоков, представлена ниже:[16]
| Группа | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
|---|---|---|---|---|---|---|---|---|---|---|
| Атомный номер | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| Элемент | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn |
| Электрон конфигурация | 3d14s2 | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 | 3d104s2 |
| Атомный номер | 39 | 40 | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 |
|---|---|---|---|---|---|---|---|---|---|---|
| Элемент | Y | Zr | Nb | Пн | Tc | RU | Rh | Pd | Ag | CD |
| Электрон конфигурация | 4d15s2 | 4d25s2 | 4d45s1 | 4d55s1 | 4d55s2 | 4d75s1 | 4d85s1 | 4d10 | 4d105s1 | 4d105s2 |
| Атомный номер | 57 | 72 | 73 | 74 | 75 | 76 | 77 | 78 | 79 | 80 |
|---|---|---|---|---|---|---|---|---|---|---|
| Элемент | Ла | Hf | Та | W | Re | Операционные системы | Ir | Pt | Au | Hg |
| Электрон конфигурация | 5d16s2 | 5d26s2 | 5d36s2 | 5d46s2 | 5d56s2 | 5d66s2 | 5d76s2 | 5d96s1 | 5d106s1 | 5d106s2 |
| Атомный номер | 89 | 104 | 105 | 106 | 107 | 108 | 109 | 110 | 111 | 112 |
|---|---|---|---|---|---|---|---|---|---|---|
| Элемент | Ac | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn |
| Электрон конфигурация | 6d17s2 | 6d27s2 | 6d37s2 | 6d47s2 | 6d57s2 | 6d67s2 | 6d77s2 | 6d87s2 | 6d97s2 | 6d107s2 |
Внимательный взгляд на электронную конфигурацию элементов показывает, что есть определенные исключения из правила Маделунга. Для Cr в качестве примера правило предсказывает конфигурацию 3d44s2, но наблюдаемые атомные спектры показывают, что реальное основное состояние равно 3d54s1. Чтобы объяснить такие исключения, необходимо рассмотреть влияние увеличения заряда ядра на орбитальные энергии, а также электрон-электронные взаимодействия, включая оба кулоновское отталкивание и обменять энергию.[16]
В орбитали, которые участвуют в переходных металлах, очень важны, потому что они влияют на такие свойства, как магнитный характер, переменные степени окисления, образование окрашенных соединений и т. д. и орбитали имеют очень небольшой вклад в этом отношении, поскольку они почти не изменяются при движении слева направо в переходной серии. В переходных металлах наблюдается большее горизонтальное сходство в свойствах элементов в периоде по сравнению с периодами в который d-орбитали не задействованы. Это связано с тем, что в серии переходов электронная конфигурация валентной оболочки элементов не изменяется. Однако есть и некоторые групповые сходства.
Характерные свойства
Есть ряд свойств, общих для переходных элементов, которых нет в других элементах, что является результатом частично заполненного d ракушка. К ним относятся
- образование соединений, цвет которых обусловлен d–d электронные переходы
- образование соединений во многих степенях окисления из-за относительно небольшого энергетического зазора между различными возможными степенями окисления[17]
- формирование многих парамагнитный соединения из-за наличия непарных d электроны. Некоторые соединения элементов основной группы также являются парамагнитными (например, оксид азота, кислород )
Большинство переходных металлов могут быть связаны с различными лиганды, что позволяет получить широкий спектр комплексов переходных металлов.[18]
Цветные соединения
Цвет в соединениях металлов переходного ряда обычно обусловлен электронными переходами двух основных типов.
- перенос заряда переходы. Электрон может выпрыгнуть из преимущественно лиганд орбитальный к преимущественно металлической орбитали, вызывая переход с переносом заряда лиганд-металл (LMCT). Это наиболее легко может произойти, когда металл находится в высокой степени окисления. Например, цвет хромат, дихромат и перманганат ионов происходит за счет LMCT-переходов. Другой пример: йодид ртути, HgI2, красный из-за перехода LMCT.
Переход с переносом заряда металл-лиганд (MLCT) наиболее вероятен, когда металл находится в низкой степени окисления и лиганд легко восстанавливается.
Обычно переходы с переносом заряда дают более интенсивные цвета, чем переходы d-d.
- d-d переходы. Электрон прыгает с одного d-орбитальный другому. В комплексах переходных металлов d не все орбитали имеют одинаковую энергию. Схема расщепления d орбитали можно рассчитать, используя кристаллическое поле теория. Степень расщепления зависит от конкретного металла, его степени окисления и природы лигандов. Фактические уровни энергии показаны на Диаграммы Танабэ – Сугано.
В центросимметричный комплексы, такие как октаэдрические комплексы, d-d переходы запрещены Правило Лапорта и происходит только из-за вибронная муфта в котором молекулярная вибрация происходит вместе с д-д переход. Тетраэдрические комплексы имеют несколько более интенсивную окраску из-за смешения d и п орбитали возможны, когда нет центра симметрии, поэтому переходы не чистые д-д переходы. В молярная поглощающая способность (ε) полос, вызванных д-д переходы относительно низкие, примерно в пределах 5-500 М−1см−1 (куда M = моль дм−3).[19] Немного d-d переходы вращение запрещено. Пример встречается в октаэдрических высокоспиновых комплексах марганец (II), который имеет d5 конфигурация, в которой все пять электронов имеют параллельные спины; окраска таких комплексов намного слабее, чем у комплексов со спин-разрешенными переходами. Многие соединения марганца (II) кажутся почти бесцветными. В спектр [Mn (H
2O)
6]2+
показывает максимальную молярную поглощающую способность около 0,04 M−1см−1 в видимый спектр.
Состояния окисления
Характерной чертой переходных металлов является то, что они проявляют два или более состояния окисления, обычно отличающиеся на единицу. Например, соединения ванадий известны во всех степенях окисления от -1, например [V (CO)
6]−
, и +5, например VO3−
4.
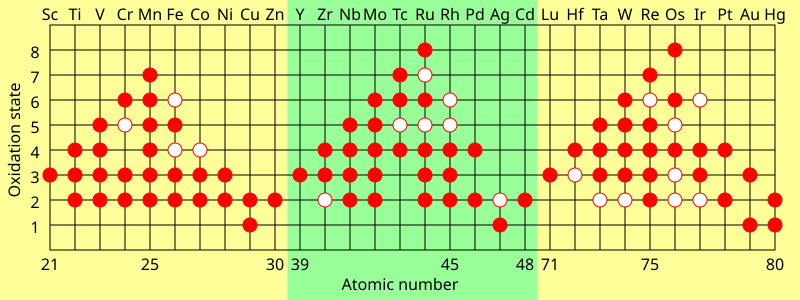
Элементы основной группы в группах с 13 по 18 также проявляются множественные степени окисления. «Обычные» степени окисления этих элементов обычно различаются на два, а не на один. Например, соединения галлий в степенях окисления +1 и +3 существуют, в которых есть единственный атом галлия. Соединение Ga (II) не известно: любое такое соединение будет иметь неспаренный электрон и вести себя как свободный радикал и быть уничтоженным быстро. Единственные соединения, в которых галлий имеет формальную степень окисления +2, - это димерные соединения, такие как [Ga
2Cl
6]2−
, которые содержат связь Ga-Ga, образованную неспаренным электроном на каждом атоме Ga.[20] Таким образом, основное различие в степенях окисления между переходными элементами и другими элементами состоит в том, что известны степени окисления, в которых имеется один атом элемента и один или несколько неспаренных электронов.
Максимальная степень окисления в переходных металлах первого ряда равна количеству валентных электронов от титан (+4) до марганец (+7), но уменьшается в более поздних элементах. Во второй строке максимум приходится на рутений (+8), а в третьей строке максимум приходится на иридий (+9). В таких соединениях, как [MnO
4]−
и OsO
4, элементы достигают стабильной конфигурации за счет ковалентная связь.
Самые низкие степени окисления проявляются в карбонил металла комплексы, такие как Cr (CO)
6 (нулевая степень окисления) и [Fe (CO)
4]2−
(степень окисления -2), в которой 18-электронное правило подчиняется. Эти комплексы также ковалентны.
Ионные соединения в основном образуются со степенями окисления +2 и +3. В водном растворе ионы гидратируются (обычно) шестью молекулами воды, расположенными октаэдрически.
Магнетизм
Соединения переходных металлов парамагнитный когда у них есть один или несколько непарных d электроны.[21] В октаэдрических комплексах от четырех до семи d электроны оба высокое вращение и низкое вращение состояния возможны. Тетраэдрические комплексы переходных металлов, такие как [FeCl
4]2−
находятся высокое вращение потому что расщепление кристаллического поля невелико, так что энергия, которая может быть получена за счет того, что электроны находятся на более низких орбиталях энергии, всегда меньше энергии, необходимой для образования пары спинов. Некоторые соединения диамагнитный. К ним относятся октаэдрические, низкоспиновые, d6 и квадратно-плоские d8 комплексы. В этих случаях, кристаллическое поле расщепление таково, что все электроны спарены.
Ферромагнетизм происходит, когда отдельные атомы парамагнитны, а векторы спина выровнены параллельно друг другу в кристаллическом материале. Металлическое железо и сплав алнико являются примерами ферромагнитных материалов, содержащих переходные металлы. Антиферромагнетизм - еще один пример магнитного свойства, возникающего из-за определенного выравнивания отдельных спинов в твердом состоянии.
Каталитические свойства
Переходные металлы и их соединения известны своими гомогенными и гетерогенными каталитический Мероприятия. Эта активность приписывается их способности принимать различные состояния окисления и образовывать комплексы. Ванадий (V) оксид (в контактный процесс ), мелко разделенный утюг (в Процесс Габера ), и никель (в каталитическое гидрирование ) являются некоторыми из примеров. Катализаторы на твердой поверхности (катализаторы на основе наноматериалов ) связаны с образованием связей между молекулами реагента и атомами поверхности катализатора (переходные металлы первого ряда используют 3d- и 4s-электроны для связывания). Это приводит к увеличению концентрации реагентов на поверхности катализатора, а также к ослаблению связей в реагирующих молекулах (снижается энергия активации). Кроме того, поскольку ионы переходных металлов могут изменять свою степень окисления, они становятся более эффективными, если катализаторы.
Интересный тип катализа происходит, когда продукты реакции катализируют реакцию с образованием большего количества катализатора (автокатализ ). Одним из примеров является реакция Щавелевая кислота с подкисленным перманганат калия (или манганат (VII)).[22] Однажды немного Mn2+ был произведен, он может реагировать с MnO4− формирование Mn3+. Затем он реагирует с C2О4− ионы, образующие Mn2+ опять таки.
Физические свойства
Как следует из названия, все переходные металлы являются металлы и таким образом проводники электричества.
В целом переходные металлы обладают высокой плотность и высокий точки плавления и точки кипения. Эти свойства обусловлены металлическое соединение делокализованными d-электронами, что приводит к сплоченность который увеличивается с количеством общих электронов. Однако металлы группы 12 имеют гораздо более низкие температуры плавления и кипения, так как их полные d-подоболочки предотвращают d – d-связывание, что опять же имеет тенденцию отличать их от принятых переходных металлов. Ртуть имеет температуру плавления -38,83 ° C (-37,89 ° F) и является жидкостью при комнатной температуре.
Смотрите также
| Scholia имеет профиль для переходный металл (Q19588). |
- Внутренний переходный элемент, имя, данное любому члену f-блок
- Элемент основной группы, элемент, отличный от переходного металла
- Теория поля лигандов развитие теории кристаллического поля с учетом ковалентности
- Теория кристаллического поля модель, описывающая нарушение вырождение электронных орбитальных состояний
- Постпереходный металл, металлический элемент справа от переходных металлов в периодической таблице
Рекомендации
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "переходный элемент ". Дои:10.1351 / goldbook.T06456
- ^ Petrucci, Ralph H .; Харвуд, Уильям S .; Херринг, Ф. Джеффри (2002). Общая химия: принципы и современные приложения (8-е изд.). Река Аппер Сэдл, штат Нью-Джерси: Prentice Hall. стр.341–342. ISBN 978-0-13-014329-7. LCCN 2001032331. OCLC 46872308.CS1 maint: ref = harv (связь)
- ^ Хаукрофт, К. Э. и Шарп, А. Г. (2005) Неорганическая химия, 2-е изд., Пирсон Прентис-Холл, стр. 20–21.
- ^ а б Коттон, Ф. А. и Уилкинсон, Г. (1988) Неорганическая химия, 5-е изд., Wiley, стр. 625–627. ISBN 978-0-471-84997-1.
- ^ а б c Дженсен, Уильям Б. (2003). «Место цинка, кадмия и ртути в Периодической таблице» (PDF). Журнал химического образования. 80 (8): 952–961. Bibcode:2003JChEd..80..952J. Дои:10.1021 / ed080p952.
- ^ Бери, К. Р. (1921). «Теория Ленгмюра о расположении электронов в атомах и молекулах». Варенье. Chem. Soc. 43 (7): 1602–1609. Дои:10.1021 / ja01440a023.
- ^ Бери, Чарльз Рагли. Encyclopedia.com Полный словарь научной биографии (2008).
- ^ Петруччи, Харвуд и Херринг, 2002 г. С. 49–50, 951.
- ^ Мисслер, Г. Л. и Тарр, Д. А. (1999) Неорганическая химия, 2-е изд., Прентис-Холл, стр. 16. ISBN 978-0-13-841891-5.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Хаукрофт, К. Э. и Шарп, А. Г. (2005) Неорганическая химия, 2-е изд., Пирсон Прентис-Холл, стр. 741.
- ^ Шерри, Э. Р. (2011) Очень краткое введение в Периодическую таблицу, Oxford University Press.
- ^ Коттон, Ф. Альберт; Wilkinson, G .; Мурильо, К. А. (1999). Продвинутая неорганическая химия (6-е изд.). Нью-Йорк: Уайли, ISBN 978-0-471-19957-1.
- ^ Ван, Сюэфан; Эндрюс, Лестер; Ридель, Себастьян; Каупп, Мартин (2007). «Ртуть - это переходный металл: первые экспериментальные доказательства наличия HgF.4". Энгью. Chem. Int. Эд. 46 (44): 8371–8375. Дои:10.1002 / anie.200703710. PMID 17899620.
- ^ Дженсен, Уильям Б. (2008). «Является ли Меркурий переходным элементом?». J. Chem. Образовательный. 85 (9): 1182–1183. Bibcode:2008JChEd..85.1182J. Дои:10.1021 / ed085p1182.
- ^ а б Мисслер, Г. Л. и Тарр, Д. А. (1999) Неорганическая химия, 2-е изд., Прентис-Холл, стр. 38–39 ISBN 978-0-13-841891-5
- ^ Мацумото, Пол S (2005). «Тенденции в области энергии ионизации элементов переходных металлов». Журнал химического образования. 82 (11): 1660. Bibcode:2005JChEd..82.1660M. Дои:10.1021 / ed082p1660.
- ^ Хоган, К. Майкл (2010). "Тяжелый металл" в Энциклопедия Земли. Национальный совет по науке и окружающей среде. Э. Моноссон и К. Кливленд (ред.) Вашингтон, округ Колумбия.
- ^ Оргель, Л. (1966). Введение в химию переходных металлов, теорию поля лигандов (2-е изд.). Лондон: Метуэн.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8. п. 240
- ^ Figgis, B.N .; Льюис, Дж. (1960). Lewis, J .; Уилкинс, Р. (ред.). Магнитохимия сложных соединений.. Современная координационная химия. Нью-Йорк: Wiley Interscience. С. 400–454.
- ^ Ковач К.А., Гроф П., Бурай Л., Ридель М. (2004). «Пересмотр механизма реакции перманганат / оксалат». J. Phys. Chem. А. 108 (50): 11026–11031. Bibcode:2004JPCA..10811026K. Дои:10.1021 / jp047061u.




