Электронная оболочка - Electron shell
В химия и атомная физика, электронная оболочка можно рассматривать как орбита с последующим электроны вокруг атом с ядро. Ближайшая к ядру оболочка называется "1 оболочка »(также называемая« оболочкой K »), за которой следует«2 shell "(или" L shell "), затем"3 оболочка »(или« М-оболочка ») и т. д. все дальше и дальше от ядра. Оболочки соответствуют главные квантовые числа (п = 1, 2, 3, 4 ...) или обозначены в алфавитном порядке буквами, используемыми в Рентгеновское обозначение (K, L, M,…).
Каждая оболочка может содержать только фиксированное количество электронов: первая оболочка может содержать до двух электронов, вторая оболочка может содержать до восьми (2 + 6) электронов, третья оболочка может содержать до 18 (2 + 6 + 10 ) и так далее. Общая формула такова: п-я оболочка в принципе может вместить до 2 (п2 ) электроны.[1] Для объяснения того, почему электроны существуют в этих оболочках, см. электронная конфигурация.[2]
Каждая оболочка состоит из одного или нескольких подоболочки, и каждая подоболочка состоит из одного или нескольких атомные орбитали.
История
Терминология оболочки взята из Арнольд Зоммерфельд модификация Модель Бора. Зоммерфельд сохранил планетную модель Бора, но добавил слегка эллиптические орбиты (характеризующиеся дополнительными квантовые числа ℓ и м) чтобы объяснить штраф спектроскопическая структура некоторых элементов.[3] Несколько электронов с одинаковым главным квантовым числом (п) имели близкие орбиты, которые образовывали «оболочку» положительной толщины вместо бесконечно тонкой круговой орбиты модели Бора.
Существование электронных оболочек было впервые экспериментально обнаружено в Чарльз Баркла 'песок Генри Мозли с рентгеновский снимок абсорбционные исследования.[неосновной источник необходим ] Баркла обозначил их буквами K, L, M, N, O, P и Q.[4] Происхождение этой терминологии было алфавитным. Предполагалась также серия "J", хотя более поздние эксперименты показали, что линии поглощения K создаются самыми внутренними электронами. Позднее выяснилось, что эти буквы соответствуют п значения 1, 2, 3 и т. Д. Они используются в спектроскопической Обозначение Зигбана.
Подоболочки

Каждая оболочка состоит из одной или нескольких подоболочек, которые сами состоят из атомные орбитали. Например, первая (K) оболочка имеет одну подоболочку, называемую 1 с; вторая (L) оболочка имеет две подоболочки, называемые 2 с и 2p; третья оболочка 3 с, 3p, и 3D; четвертая оболочка 4 с, 4p, 4d и 4f; пятая оболочка 5 с, 5p, 5d, и 5f и теоретически может удерживать больше в 5 г подоболочка, которая не занята в основной электронной конфигурации любого известного элемента.[2] Различные возможные подоболочки показаны в следующей таблице:
| Ярлык субоболочки | ℓ | Макс электронов | Снаряды, содержащие его | Историческое название |
|---|---|---|---|---|
| s | 0 | 2 | Каждая оболочка | sарфа |
| п | 1 | 6 | 2-я оболочка и выше | пглавный |
| d | 2 | 10 | 3-я оболочка и выше | dпредохранитель |
| ж | 3 | 14 | 4-я оболочка и выше | жнеобоснованный |
| грамм | 4 | 18 | 5-я оболочка и выше (теоретически) | (следующий по алфавиту после ж, без учета я)[5] |
- Первый столбец - это «метка подоболочки», метка из строчных букв для типа подоболочки. Например, "4 с подоболочка »- подоболочка четвертой (N) оболочки с типом (s) описан в первом ряду.
- Второй столбец - это азимутальное квантовое число (ℓ) подоболочки. Точное определение включает квантовая механика, но это число, которое характеризует подоболочку.
- Третий столбец - это максимальное количество электронов, которое можно поместить в подоболочку этого типа. Например, в верхнем ряду указано, что каждый s-тип подоболочки (1 с, 2 си т. д.) может иметь не более двух электронов. В каждом случае цифра на 4 больше, чем предыдущая.
- В четвертом столбце указано, какие оболочки имеют подоболочку этого типа. Например, если посмотреть на два верхних ряда, у каждой оболочки есть s подоболочка, в то время как только вторая оболочка и выше имеет п подоболочка (т.е. подоболочки "1p" не существует).
- В последнем столбце указано историческое происхождение этикеток. s, п, d, и ж. Они пришли из ранних исследований атомные спектральные линии. Остальные ярлыки, а именно грамм, час и я, являются алфавитным продолжением последнего исторически возникшего ярлыка ж.
Количество электронов в каждой оболочке
Каждая подоболочка должна содержать 4ℓ + 2 электронов самое большее, а именно:
- Каждый s подоболочка содержит не более 2 электронов
- Каждый п подоболочка содержит не более 6 электронов
- Каждый d подоболочка содержит не более 10 электронов
- Каждый ж подоболочка содержит не более 14 электронов
- Каждый грамм подоболочка вмещает не более 18 электронов
Следовательно, K-оболочка, содержащая только s подоболочка, вмещает до 2-х электронов; оболочка L, содержащая s и п, может содержать до 2 + 6 = 8 электронов и так далее; в целом п-й снаряд может вместить до 2п2 электроны.[1]
| Ракушка имя | Subshell имя | Subshell Максимум электроны | Ракушка Максимум электроны |
|---|---|---|---|
| K | 1 с | 2 | 2 |
| L | 2 с | 2 | 2 + 6 = 8 |
| 2p | 6 | ||
| M | 3 с | 2 | 2 + 6 + 10 = 18 |
| 3p | 6 | ||
| 3D | 10 | ||
| N | 4 с | 2 | 2 + 6 + 10 + 14 = 32 |
| 4p | 6 | ||
| 4d | 10 | ||
| 4f | 14 | ||
| О | 5 с | 2 | 2 + 6 + 10 + 14 + 18 = 50 |
| 5p | 6 | ||
| 5d | 10 | ||
| 5f | 14 | ||
| 5 г | 18 |
Хотя эта формула в принципе дает максимум, на самом деле он составляет только достигнуто (по известным элементам) для первых четырех оболочек (K, L, M, N). Ни один из известных элементов не имеет более 32 электронов в одной оболочке.[6][7] Это потому, что подоболочки заполняются в соответствии с Принцип Ауфбау. Первые элементы, содержащие более 32 электронов в одной оболочке, будут принадлежать g-блок из период 8 из периодическая таблица. В этих элементах будет несколько электронов. 5 г подоболочки и, таким образом, имеют более 32 электронов в О-оболочке (пятая основная оболочка).
Энергии подоболочки и порядок заполнения

Хотя иногда говорят, что все электроны в оболочке имеют одинаковую энергию, это лишь приближение. Однако электроны в одном подоболочка имеют точно такой же уровень энергии, причем более поздние подоболочки имеют больше энергии на электрон, чем более ранние. Этот эффект настолько велик, что диапазоны энергии, связанные с оболочками, могут перекрываться.
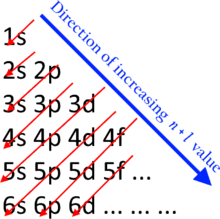
Заполнение оболочек и подоболочек электронами происходит от подоболочек с меньшей энергией к подоболочкам с более высокой энергией. Это следует за n + ℓ правило которое также широко известно как правило Маделунга. Корпуса с нижним п + ℓ значения заполняются перед теми, у которых больше п + ℓ значения. В случае равных п + ℓ значения, подоболочка с нижним п значение заполняется первым.
Список элементов с электронами на оболочку
В приведенном ниже списке перечислены элементы, упорядоченные по возрастанию атомного номера, и показано количество электронов на оболочку. На первый взгляд, подмножества списка демонстрируют очевидные закономерности. В частности, каждый набор из пяти элементов (в электрик) перед каждым благородный газ (группа 18, в желтый) тяжелее гелия, имеют последовательное число электронов на внешней оболочке, а именно от трех до семи. (Однако этот шаблон может нарушиться в седьмой период из-за релятивистские эффекты.)
Сортировка таблицы по химическому составу группа показывает дополнительные шаблоны, особенно в отношении двух последних крайних оболочек. (Элементы с 57 по 71 принадлежат лантаноиды, а от 89 до 103 - актиниды.)
Приведенный ниже список в первую очередь соответствует Принцип Ауфбау. Однако из правила есть ряд исключений; Например палладий (атомный номер 46) не имеет электронов в пятой оболочке, в отличие от других атомов с ниже атомный номер. Некоторые записи в таблице недостоверны, когда экспериментальные данные недоступны. (Например, элементы после 108 имеют такой короткий период полураспада что их электронные конфигурации еще не были измерены.)
| Z | Элемент | Количество электронов / оболочка | Группа |
|---|---|---|---|
| 1 | Водород | 1 | 1 |
| 2 | Гелий | 2 | 18 |
| 3 | Литий | 2, 1 | 1 |
| 4 | Бериллий | 2, 2 | 2 |
| 5 | Бор | 2, 3 | 13 |
| 6 | Углерод | 2, 4 | 14 |
| 7 | Азот | 2, 5 | 15 |
| 8 | Кислород | 2, 6 | 16 |
| 9 | Фтор | 2, 7 | 17 |
| 10 | Неон | 2, 8 | 18 |
| 11 | Натрий | 2, 8, 1 | 1 |
| 12 | Магний | 2, 8, 2 | 2 |
| 13 | Алюминий | 2, 8, 3 | 13 |
| 14 | Кремний | 2, 8, 4 | 14 |
| 15 | Фосфор | 2, 8, 5 | 15 |
| 16 | Сера | 2, 8, 6 | 16 |
| 17 | Хлор | 2, 8, 7 | 17 |
| 18 | Аргон | 2, 8, 8 | 18 |
| 19 | Калий | 2, 8, 8, 1 | 1 |
| 20 | Кальций | 2, 8, 8, 2 | 2 |
| 21 | Скандий | 2, 8, 9, 2 | 3 |
| 22 | Титана | 2, 8, 10, 2 | 4 |
| 23 | Ванадий | 2, 8, 11, 2 | 5 |
| 24 | Хром | 2, 8, 13, 1 | 6 |
| 25 | Марганец | 2, 8, 13, 2 | 7 |
| 26 | Утюг | 2, 8, 14, 2 | 8 |
| 27 | Кобальт | 2, 8, 15, 2 | 9 |
| 28 | Никель | 2, 8, 16, 2 | 10 |
| 29 | Медь | 2, 8, 18, 1 | 11 |
| 30 | Цинк | 2, 8, 18, 2 | 12 |
| 31 | Галлий | 2, 8, 18, 3 | 13 |
| 32 | Германий | 2, 8, 18, 4 | 14 |
| 33 | Мышьяк | 2, 8, 18, 5 | 15 |
| 34 | Селен | 2, 8, 18, 6 | 16 |
| 35 | Бром | 2, 8, 18, 7 | 17 |
| 36 | Криптон | 2, 8, 18, 8 | 18 |
| 37 | Рубидий | 2, 8, 18, 8, 1 | 1 |
| 38 | Стронций | 2, 8, 18, 8, 2 | 2 |
| 39 | Иттрий | 2, 8, 18, 9, 2 | 3 |
| 40 | Цирконий | 2, 8, 18, 10, 2 | 4 |
| 41 | Ниобий | 2, 8, 18, 12, 1 | 5 |
| 42 | Молибден | 2, 8, 18, 13, 1 | 6 |
| 43 | Технеций | 2, 8, 18, 13, 2 | 7 |
| 44 | Рутений | 2, 8, 18, 15, 1 | 8 |
| 45 | Родий | 2, 8, 18, 16, 1 | 9 |
| 46 | Палладий | 2, 8, 18, 18 | 10 |
| 47 | Серебро | 2, 8, 18, 18, 1 | 11 |
| 48 | Кадмий | 2, 8, 18, 18, 2 | 12 |
| 49 | Индий | 2, 8, 18, 18, 3 | 13 |
| 50 | Банка | 2, 8, 18, 18, 4 | 14 |
| 51 | Сурьма | 2, 8, 18, 18, 5 | 15 |
| 52 | Теллур | 2, 8, 18, 18, 6 | 16 |
| 53 | Йод | 2, 8, 18, 18, 7 | 17 |
| 54 | Ксенон | 2, 8, 18, 18, 8 | 18 |
| 55 | Цезий | 2, 8, 18, 18, 8, 1 | 1 |
| 56 | Барий | 2, 8, 18, 18, 8, 2 | 2 |
| 57 | Лантан | 2, 8, 18, 18, 9, 2 | 3 |
| 58 | Церий | 2, 8, 18, 19, 9, 2 | |
| 59 | Празеодим | 2, 8, 18, 21, 8, 2 | |
| 60 | Неодим | 2, 8, 18, 22, 8, 2 | |
| 61 | Прометий | 2, 8, 18, 23, 8, 2 | |
| 62 | Самарий | 2, 8, 18, 24, 8, 2 | |
| 63 | Европий | 2, 8, 18, 25, 8, 2 | |
| 64 | Гадолиний | 2, 8, 18, 25, 9, 2 | |
| 65 | Тербий | 2, 8, 18, 27, 8, 2 | |
| 66 | Диспрозий | 2, 8, 18, 28, 8, 2 | |
| 67 | Гольмий | 2, 8, 18, 29, 8, 2 | |
| 68 | Эрбий | 2, 8, 18, 30, 8, 2 | |
| 69 | Тулий | 2, 8, 18, 31, 8, 2 | |
| 70 | Иттербий | 2, 8, 18, 32, 8, 2 | |
| 71 | Лютеций | 2, 8, 18, 32, 9, 2 | |
| 72 | Гафний | 2, 8, 18, 32, 10, 2 | 4 |
| 73 | Тантал | 2, 8, 18, 32, 11, 2 | 5 |
| 74 | Вольфрам | 2, 8, 18, 32, 12, 2 | 6 |
| 75 | Рений | 2, 8, 18, 32, 13, 2 | 7 |
| 76 | Осмий | 2, 8, 18, 32, 14, 2 | 8 |
| 77 | Иридий | 2, 8, 18, 32, 15, 2 | 9 |
| 78 | Платина | 2, 8, 18, 32, 17, 1 | 10 |
| 79 | Золото | 2, 8, 18, 32, 18, 1 | 11 |
| 80 | Меркурий | 2, 8, 18, 32, 18, 2 | 12 |
| 81 | Таллий | 2, 8, 18, 32, 18, 3 | 13 |
| 82 | Свинец | 2, 8, 18, 32, 18, 4 | 14 |
| 83 | Висмут | 2, 8, 18, 32, 18, 5 | 15 |
| 84 | Полоний | 2, 8, 18, 32, 18, 6 | 16 |
| 85 | Астатин | 2, 8, 18, 32, 18, 7 | 17 |
| 86 | Радон | 2, 8, 18, 32, 18, 8 | 18 |
| 87 | Франций | 2, 8, 18, 32, 18, 8, 1 | 1 |
| 88 | Радий | 2, 8, 18, 32, 18, 8, 2 | 2 |
| 89 | Актиний | 2, 8, 18, 32, 18, 9, 2 | 3 |
| 90 | Торий | 2, 8, 18, 32, 18, 10, 2 | |
| 91 | Протактиний | 2, 8, 18, 32, 20, 9, 2 | |
| 92 | Уран | 2, 8, 18, 32, 21, 9, 2 | |
| 93 | Нептуний | 2, 8, 18, 32, 22, 9, 2 | |
| 94 | Плутоний | 2, 8, 18, 32, 24, 8, 2 | |
| 95 | Америций | 2, 8, 18, 32, 25, 8, 2 | |
| 96 | Кюрий | 2, 8, 18, 32, 25, 9, 2 | |
| 97 | Берклиум | 2, 8, 18, 32, 27, 8, 2 | |
| 98 | Калифорний | 2, 8, 18, 32, 28, 8, 2 | |
| 99 | Эйнштейний | 2, 8, 18, 32, 29, 8, 2 | |
| 100 | Фермий | 2, 8, 18, 32, 30, 8, 2 | |
| 101 | Менделевий | 2, 8, 18, 32, 31, 8, 2 | |
| 102 | Нобелий | 2, 8, 18, 32, 32, 8, 2 | |
| 103 | Лоуренсий | 2, 8, 18, 32, 32, 8, 3 | |
| 104 | Резерфордий | 2, 8, 18, 32, 32, 10, 2 | 4 |
| 105 | Дубний | 2, 8, 18, 32, 32, 11, 2 | 5 |
| 106 | Сиборгий | 2, 8, 18, 32, 32, 12, 2 | 6 |
| 107 | Бориум | 2, 8, 18, 32, 32, 13, 2 | 7 |
| 108 | Калий | 2, 8, 18, 32, 32, 14, 2 | 8 |
| 109 | Мейтнерий | 2, 8, 18, 32, 32, 15, 2 (?) | 9 |
| 110 | Дармштадтиум | 2, 8, 18, 32, 32, 16, 2 (?) | 10 |
| 111 | Рентгений | 2, 8, 18, 32, 32, 17, 2 (?) | 11 |
| 112 | Копернициум | 2, 8, 18, 32, 32, 18, 2 (?) | 12 |
| 113 | Nihonium | 2, 8, 18, 32, 32, 18, 3 (?) | 13 |
| 114 | Флеровий | 2, 8, 18, 32, 32, 18, 4 (?) | 14 |
| 115 | Московиум | 2, 8, 18, 32, 32, 18, 5 (?) | 15 |
| 116 | Ливерморий | 2, 8, 18, 32, 32, 18, 6 (?) | 16 |
| 117 | Tennessine | 2, 8, 18, 32, 32, 18, 7 (?) | 17 |
| 118 | Оганессон | 2, 8, 18, 32, 32, 18, 8 (?) | 18 |
Смотрите также
Рекомендации
- ^ а б Re: Почему электронные оболочки имеют ограничения? madsci.org, 17 марта 1999 г., Дэн Бергер, факультет химии / естественных наук, колледж Блаффтон
- ^ а б Электронные подоболочки. Источник коррозии.
- ^ Дональд Садовей, Введение в химию твердого тела, Лекция 5
- ^ Баркла, Чарльз Г. (1911). «XXXIX. Спектры флуоресцентного рентгеновского излучения» (PDF). Философский журнал. 6 серия. 22 (129): 396–412. Дои:10.1080/14786440908637137.
Ранее обозначается буквами B и A (...). Буквы K и L, однако, предпочтительны, так как весьма вероятно, что существуют серии излучений, как более поглощаемых, так и более проникающих.
- ^ Цзюэ, Т. (2009). "Квантовая механика, основы биофизических методов". Фундаментальные концепции биофизики. Берлин: Springer. п. 33. ISBN 978-1-58829-973-4.
- ^ Орбитали. Chem4Kids. Проверено 1 декабря 2011 г.
- ^ Электронная конфигурация и конфигурация оболочки В архиве 28 декабря 2018 в Wayback Machine. Chemistry.patent-invent.com. Проверено 1 декабря 2011 г.

