Куриум - Википедия - Curium
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кюрий | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /ˈkjʊərяəм/ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешность | серебристый металлик, в темноте светится пурпурным | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Массовое число | [247] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кюрий в периодическая таблица | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер (Z) | 96 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа н / д | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | f-блок | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Категория элемента | Актинид | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [Rn ] 5f7 6d1 7 с2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 32, 25, 9, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза вSTP | твердый | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 1613 K (1340 ° С, 2444 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 3383 К (3110 ° С, 5630 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | 13,51 г / см3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 13.85 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Давление газа
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Состояния окисления | +3, +4, +5,[1] +6[2] (анамфотерный окись) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус атома | эмпирические: 174вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 169 ± 15:00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | синтетический | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристальная структура | двойной шестиугольный плотно упакованный (dhcp) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 1,25 мкОм · м[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | антиферромагнитно-парамагнитный переход при 52 К[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Количество CAS | 7440-51-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Именование | названный в честь Мария Склодовская-Кюри и Пьер Кюри | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие | Гленн Т. Сиборг, Ральф А. Джеймс, Альберт Гиорсо (1944) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Главный изотопы кюрия | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Кюрий это трансурановый радиоактивный химический элемент с символ См и атомный номер 96. Этот элемент актинид сериал был назван в честь Мари и Пьер Кюри, оба известны своими исследованиями радиоактивность. Кюрий был впервые намеренно произведен и идентифицирован в июле 1944 г. Гленн Т. Сиборг на Калифорнийский университет в Беркли. Открытие держалось в секрете и обнародовано только в ноябре 1947 года. Большая часть кюрия производится путем бомбардировки. уран или же плутоний с нейтроны в ядерные реакторы - один тонна потраченных ядерное топливо содержит около 20 граммов кюрия.
Кюрий - твердый, плотный, серебристый металл с относительно высокой температурой плавления и кипения актинида. Тогда как это парамагнитный в условия окружающей среды, это становится антиферромагнитный при охлаждении и другие магнитные переходы наблюдаются также для многих соединений кюрия. В соединениях кюрий обычно проявляет валентность +3, а иногда и +4, причем в растворах преобладает валентность +3. Кюрий легко окисляется, и его оксиды являются доминирующей формой этого элемента. Образует сильно флуоресцентный комплексы с различными органическими соединениями, но нет данных о его включении в бактерии и археи. При попадании в организм человека кюрий накапливается в костях, легких и печени, где способствует рак.
Все известные изотопы кюрия радиоактивны и имеют небольшой критическая масса для устойчивого ядерная цепная реакция. Они преимущественно излучают α-частицы, а выделяющееся при этом тепло может служить источником тепла в радиоизотопные термоэлектрические генераторы, но этому применению мешает нехватка и высокая стоимость изотопов кюрия. Кюрий используется в производстве более тяжелых актинидов и 238Пу радионуклид для источников энергии в искусственные кардиостимуляторы и РИТЭГи для космического корабля. Он служил α-источник в рентгеновские спектрометры альфа-частиц установлен на нескольких космических зондах, включая Соджорнер, Дух, Возможность и Любопытство Марс вездеходы и Посадочный модуль Philae на комета 67P / Чурюмов – Герасименко, чтобы проанализировать состав и структуру поверхности.
История

Хотя кюрий, вероятно, был произведен в предыдущих ядерных экспериментах, он был первый намеренно синтезированный, выделенный и идентифицированный в 1944 г. Калифорнийский университет в Беркли, к Гленн Т. Сиборг, Ральф А. Джеймс, и Альберт Гиорсо. В своих экспериментах они использовали 60-дюймовый (150 см) циклотрон.[4]
Кюрий был химически идентифицирован в Металлургической лаборатории (ныне Аргоннская национальная лаборатория ) на Чикагский университет. Это был третий трансурановый элемент быть обнаруженным, хотя это четвертый в серии - более легкий элемент америций был неизвестен в то время.[5][6]
Образец готовился следующим образом: сначала плутоний раствор нитрата был нанесен на платина фольга около 0,5 см2 области раствор упаривали и остаток превращали в оксид плутония (IV) (PuO2) к отжиг. После циклотронного облучения оксида покрытие растворялось азотная кислота и затем осаждали в виде гидроксида с использованием концентрированной водной раствор аммиака. Остаток растворяли в хлорная кислота, а дальнейшее разделение проводилось ионный обмен чтобы получить определенный изотоп кюрия. Разделение кюрия и америция было настолько сложным, что группа Беркли первоначально назвала эти элементы столпотворение (с греческого для все демоны или же ад) и бред (от латинского для безумие).[7][8]
Изотоп кюрий-242 был получен в июле – августе 1944 г. путем бомбардировки. 239Пу с α-частицы производить кюрий с выделением нейтрон:
Кюрий-242 был однозначно идентифицирован по характерной энергии испускаемых при распаде α-частиц:
В период полураспада этого альфа-распад сначала было измерено как 150 дней, а затем было исправлено до 162,8 дня.[9]
Другой изотоп 240См был произведен аналогичной реакцией в марте 1945 г .:
Период полураспада 240Cm α-распад был правильно определен как 26,7 дня.[9]
Открытие кюрия, а также америция в 1944 году было тесно связано с Манхэттенский проект, поэтому результаты были конфиденциальными и рассекречены только в 1945 году. Сиборг просочил синтез элементов 95 и 96 в американское радио-шоу для детей. Дети викторины, за пять дней до официальной презентации на Американское химическое общество встреча 11 ноября 1945 г., когда один из слушателей спросил, есть ли какой-либо новый трансурановый элемент, кроме плутония и нептуний был обнаружен во время войны.[7] Открытие кюрия (242См и 240Cm), его производство и его соединения были позже запатентованы, указав только Сиборга в качестве изобретателя.[10]
Новый элемент был назван в честь Мария Склодовская-Кюри и ее муж Пьер Кюри кто известен открытием радий и за их работу в радиоактивность. Он последовал примеру гадолиний, а лантаноид элемент над кюрием в периодической таблице, названной в честь исследователя редкоземельные элементы Йохан Гадолин:[11]
- «В качестве названия элемента с атомным номером 96 мы хотели бы предложить« кюрий »с символом Cm. Свидетельства показывают, что элемент 96 содержит семь 5f-электронов и, таким образом, аналогичен элементу гадолинию с его семью 4f-электронами в регулярном ряд редкоземельных элементов. На этом основном элементе 96 назван в честь Кюри аналогично названию гадолиния, которым был удостоен чести химик Гадолин ».[5]
Первые образцы кюрия были едва видны и были идентифицированы по их радиоактивности. Луи Вернер и Исадор Перлман создал первый существенный образец 30 мкг гидроксида кюрия-242 в Калифорнийском университете в Беркли в 1947 году путем бомбардировки америций -241 с нейтронами.[12][13][14] Макроскопические количества фторид кюрия (III) были получены в 1950 году У. Т. Крейном, Дж. К. Валлманном и Б. Б. Каннингемом. Его магнитная восприимчивость была очень близка к GdF.3 предоставление первых экспериментальных доказательств +3 валентности кюрия в его соединениях.[12] Металлический кюрий был получен только в 1951 году путем восстановления CmF.3 с барий.[15][16]
Характеристики
Физический


Синтетический радиоактивный элемент, кюрий - твердый, плотный металл с серебристо-белым внешним видом и физико-химическими свойствами, напоминающими свойства гадолиний. Его температура плавления 1344 ° C значительно выше, чем у предыдущих трансурановых элементов нептуния (637 ° C), плутония (639 ° C) и америция (1173 ° C). Для сравнения, гадолиний плавится при 1312 ° C. Температура кипения кюрия - 3556 ° C. Плотностью 13,52 г / см3, кюрий значительно легче нептуния (20,45 г / см3) и плутоний (19,8 г / см3), но тяжелее большинства других металлов. Между двумя кристаллическими формами кюрия α-Cm более стабилен в условиях окружающей среды. Имеет гексагональную симметрию, космическая группа P63/ mmc, параметры решетки а = 365 вечера и c = 1182 вечера, а четыре формульные единицы на ячейка.[17] Кристалл состоит из двойногогексагональная плотная упаковка с последовательностью слоев ABAC и поэтому изотипен α-лантану. При давлении выше 23 ГПа, при комнатной температуре α-Cm превращается в β-Cm, который имеет гранецентрированная кубическая симметрия, пространственная группа Fm3m и постоянная решетки а = 493 вечера.[17] При дальнейшем сжатии до 43 ГПа кюрий переходит в ромбический Структура γ-Cm аналогична структуре α-урана, без дальнейших переходов до 52 ГПа. Эти три фазы кюрия также называются Cm I, II и III.[18][19]
Кюрий обладает особыми магнитными свойствами. В то время как его соседний элемент америций не показывает отклонений от Кюри-Вайс парамагнетизм во всем диапазоне температур α-Cm переходит в антиферромагнитный состояние при охлаждении до 65–52 К,[20][21] и β-Cm проявляет ферримагнитный переход примерно при 205 К. Между тем, пниктиды кюрия показывают ферромагнитный переходы при охлаждении: 244CmN и 244CmAs при 109 К, 248CmP при 73 К и 248CmSb при 162 К. Лантаноидный аналог кюрия, гадолиний, а также его пниктиды также демонстрируют магнитные переходы при охлаждении, но характер перехода несколько иной: Gd и GdN становятся ферромагнитными, а GdP, GdAs и GdSb обнаруживают антиферромагнитное упорядочение.[22]
Согласно магнитным данным, удельное сопротивление кюрия увеличивается с температурой - примерно в два раза между 4 и 60 К - и затем остается почти постоянным до комнатной температуры. С течением времени наблюдается значительное увеличение удельного сопротивления (около 10 мкОм · см / ч) из-за саморазрушения кристаллической решетки альфа-излучением. Это делает неопределенным абсолютное значение удельного сопротивления для кюрия (около 125 мкОм · см). Удельное сопротивление кюрия такое же, как у гадолиния и актинидов плутония и нептуния, но значительно выше, чем у америция, урана, полоний и торий.[3][23]
Под ультрафиолетовым освещением ионы кюрия (III) проявляют сильный и стабильный желто-оранжевый цвет. флуоресценция с максимумом в диапазоне 590–640 нм в зависимости от окружающей среды.[24] Флуоресценция возникает при переходах из первого возбужденного состояния 6D7/2 и основное состояние 8S7/2. Анализ этой флуоресценции позволяет отслеживать взаимодействия между ионами Cm (III) в органических и неорганических комплексах.[25]
Химическая
Ионы кюрия в растворе почти исключительно принимают степень окисления +3, что является наиболее стабильной степенью окисления кюрия.[26] Степень окисления +4 наблюдается в основном в нескольких твердых фазах, таких как CmO2 и CmF4.[27][28] Водный кюрий (IV) известен только в присутствии сильных окислителей, таких как персульфат калия, и легко восстанавливается до кюрия (III) радиолиз и даже самой водой.[29] Химическое поведение кюрия отличается от актинидов тория и урана и похоже на поведение америция и многих других веществ. лантаноиды. В водном растворе Cm3+ ион от бесцветного до бледно-зеленого,[30] и см4+ ион бледно-желтый.[31] Оптическое поглощение Cm3+ Ионы содержат три острых пика при 375,4, 381,2 и 396,5 нм, и их сила может быть напрямую преобразована в концентрацию ионов.[32] О степени окисления +6 сообщалось только один раз в растворе в 1978 г., как ион курил (СмО2+
2): это было приготовлено из бета-распад из америций-242 в ионе америция (V) 242
AmO+
2.[2] Неспособность получить Cm (VI) в результате окисления Cm (III) и Cm (IV) может быть связано с высоким Cm4+/См3+ потенциал ионизации и неустойчивость Cm (V).[29]
Ионы кюрия являются жесткие кислоты Льюиса и таким образом образуют наиболее прочные комплексы с твердыми основаниями.[33] Связь в основном ионная с небольшой ковалентной составляющей.[34] Кюрий в его комплексах обычно проявляет 9-кратную координационную среду в пределах трехшпиндельной тригонально-призматическая геометрия.[35]
Изотопы
Около 19 радиоизотопы и 7 ядерные изомеры между 233См и 251Cm известны кюрий, ни один из которых стабильный. Самый длинный период полураспада был зарегистрирован для 247См (15,6 млн лет) и 248См (348000 лет). Другие долгоживущие изотопы: 245См (период полураспада 8500 лет), 250См (8300 лет) и 246См (4760 лет). Кюрий-250 необычен тем, что он преимущественно (около 86%) распадается через спонтанное деление. Наиболее часто используемые изотопы кюрия: 242См и 244См с периодом полураспада 162,8 суток и 18,1 года соответственно.[9]
| Тепловые нейтроны поперечные сечения (сараи )[36] | ||||||
|---|---|---|---|---|---|---|
| 242См | 243См | 244См | 245См | 246См | 247См | |
| Деление | 5 | 617 | 1.04 | 2145 | 0.14 | 81.90 |
| Захватывать | 16 | 130 | 15.20 | 369 | 1.22 | 57 |
| Соотношение C / F | 3.20 | 0.21 | 14.62 | 0.17 | 8.71 | 0.70 |
| ЛЕЯ отработанное топливо 20 лет после 53 МВт · сут / кг сжечь[37] | ||||||
| 3 распространенных изотопа | 51 | 3700 | 390 | |||
| Быстрый реактор МОКС-топливо (в среднем 5 образцов, сжечь 66–120 ГВт-сут / т)[38] | ||||||
| Кюрий общий 3,09×10−3% | 27.64% | 70.16% | 2.166% | 0.0376% | 0.000928% | |
| Изотоп | 242См | 243См | 244См | 245См | 246См | 247См | 248См | 250См |
| Критическая масса, кг | 25 | 7.5 | 33 | 6.8 | 39 | 7 | 40.4 | 23.5 |
Все изотопы между 242См и 248См, а также 250См, пройти хозрасчет ядерная цепная реакция и, таким образом, в принципе может действовать как ядерное топливо в реакторе. Как и в большинстве трансурановых элементов, ядерное деление сечение особенно велико для изотопов кюрия нечетной массы 243См, 245См и 247См. Их можно использовать в реакторы на тепловых нейтронах, тогда как смесь изотопов кюрия подходит только для быстрые реакторы-размножители поскольку изотопы с четной массой не расщепляются в тепловом реакторе и накапливаются по мере увеличения выгорания.[39] Смешанное оксидное топливо (МОКС), которое будет использоваться в энергетических реакторах, должно содержать мало кюрия или не содержать его, поскольку нейтронная активация из 248См создам калифорний. Калифорний - сильный нейтрон излучатель, и это приведет к загрязнению конечной части топливного цикла и увеличению дозы для персонала реактора. Следовательно, если второстепенные актиниды Для использования в качестве топлива в реакторе на тепловых нейтронах, кюрий следует исключить из топлива или поместить в специальные топливные стержни, где он является единственным присутствующим актинидом.[40]
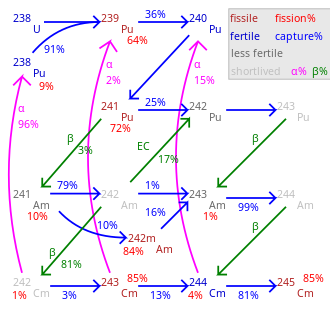
Процент деления составляет 100 минус указанные проценты.
Общая скорость трансмутации сильно зависит от нуклида.
245См-248См являются долгоживущими с незначительным распадом.
В соседней таблице перечислены критические массы для изотопов кюрия для шара без замедлителя и отражателя. С металлическим отражателем (30 см из стали) критические массы нечетных изотопов составляют около 3–4 кг. При использовании воды (толщиной ~ 20–30 см) в качестве отражателя критическая масса может составлять всего 59 грамм для 245См, 155 грамм для 243См и 1550 грамм для 247См. Эти значения критической массы содержат значительную неопределенность. Хотя обычно он составляет порядка 20%, значения для 242См и 246Некоторые исследовательские группы указали, что Cm составляет 371 кг и 70,1 кг соответственно.[39][42]
Кюрий в настоящее время не используется в качестве ядерного топлива из-за его низкой доступности и высокой цены.[43] 245См и 247Cm имеют очень маленькие критические массы и поэтому могут использоваться в тактическое ядерное оружие, но ни один из них не был произведен. Кюрий-243 не подходит для этой цели из-за его короткого периода полураспада и сильного α-излучения, которое может привести к чрезмерному нагреванию.[44] Кюрий-247 был бы очень подходящим из-за его длительного периода полураспада, который в 647 раз дольше, чем плутоний-239 (используется во многих существующих ядерное оружие ).
Вхождение

Самый долгоживущий изотоп кюрия, 247См, имеет период полураспада 15,6 миллиона лет. Поэтому любой изначальный кюрий, то есть кюрий, присутствовавший на Земле во время ее образования, к настоящему времени должен был распасться, хотя некоторые его количества можно было бы обнаружить как потухший радионуклид как избыток своей изначальной долгоживущей дочери 235U. Следы кюрия, возможно, встречаются в урановых минералах в естественных условиях в результате последовательностей захвата нейтронов и бета-распада, хотя это не подтверждено.[45][46]
Кюрий производится искусственно в небольших количествах для исследовательских целей. Кроме того, это происходит в потраченных ядерное топливо. Кюрий присутствует в природе в определенных областях, используемых для испытания ядерного оружия.[47] Анализ обломков на полигоне первых американских водородная бомба, Айви Майк, (1 ноября 1952 г., Атолл Эниветак ), Помимо эйнштейний, фермий, плутоний и америций также выявлены изотопы берклия, калифорния и кюрия, в частности 245См, 246См и меньшие количества 247См, 248См и 249См.[48]
Атмосферные соединения кюрия плохо растворяются в обычных растворителях и в основном прилипают к частицам почвы. Анализ почвы показал, что концентрация кюрия в песчаных частицах почвы примерно в 4000 раз выше, чем в воде, присутствующей в порах почвы. Еще более высокий коэффициент, около 18000, был измерен в суглинок почвы.[49]
В трансурановые элементы от америция до фермия, включая кюрий, естественным образом происходил в естественный ядерный реактор деления в Окло, но больше не делайте этого.[50]
Синтез
Подготовка изотопов
Кюрий производится в небольших количествах в ядерные реакторы, и к настоящему времени накоплены лишь килограммы. 242См и 244См и граммы или даже миллиграммы для более тяжелых изотопов. Этим объясняется высокая цена на кюрий, котируемая на уровне 160–185. доллар США на миллиграмм,[12] с более поздней оценкой в 2000 долларов США / г для 242См и 170 долларов США / г для 244См.[51] В ядерных реакторах кюрий образуется из 238U в серии ядерных реакций. В первой цепочке 238U захватывает нейтрон и превращается в 239U, который через β− разлагаться превращается в 239Np и 239Пу.
- (время период полураспада ).
(1)
Дальнейший захват нейтронов с последующим β−-распад производит 241Am изотоп америций который в дальнейшем преобразуется в 242См:
- .
(2)
В исследовательских целях кюрий получают путем облучения не урана, а плутония, который в больших количествах содержится в отработавшем ядерном топливе. Для облучения используется гораздо более высокий нейтронный поток, что приводит к другой цепочке реакций и образованию 244См:[6]
(3)
Кюрий-244 распадается на 240Pu путем испускания альфа-частиц, но он также поглощает нейтроны, что приводит к образованию небольшого количества более тяжелых изотопов кюрия. Среди тех, 247См и 248См являются популярными в научных исследованиях из-за их длительного периода полураспада. Однако производительность 247Cm в реакторах на тепловых нейтронах относительно низка, поскольку она склонна к делению под действием тепловых нейтронов.[52] Синтез 250См через поглощение нейтронов также маловероятно из-за короткого периода полураспада промежуточного продукта. 249Cm (64 мин), которое преобразуется β− распад на берклий изотоп 249Кн.[52]
(4)
Вышеупомянутый каскад (n, γ) реакций дает смесь различных изотопов кюрия. Их разделение после синтеза является обременительным, и поэтому желателен селективный синтез. Кюрий-248 является предпочтительным для исследовательских целей из-за его длительного периода полураспада. Наиболее эффективный метод получения этого изотопа - через α-распад калифорний изотоп 252Cf, который доступен в относительно больших количествах из-за его длительного периода полураспада (2,65 года). Около 35–50 мг 248Cm производится этим методом каждый год. Связанная реакция производит 248См с изотопной чистотой 97%.[52]
(5)
Еще один интересный для исследования изотоп 245Cm можно получить из α-распада 249Cf, и последний изотоп производится в ничтожных количествах из β−-распад берклий изотоп 249Кн.
(6)
Подготовка металла

Большинство программ синтеза дают смесь различных изотопов актинидов в виде оксиды, от которого необходимо отделить определенный изотоп кюрия. Примером процедуры может быть растворение отработавшего топлива реактора (например, МОКС-топливо ) в азотная кислота, и удалите основную часть урана и плутония с помощью PUREX (плутоний - URAnium БЫВШИЙтяга) типа вытяжной с трибутилфосфат в углеводороде. Затем лантаноиды и оставшиеся актиноиды отделяют от водного остатка (рафинат ) экстракцией на основе диамида с получением после отгонки смеси трехвалентных актинидов и лантаноидов. Затем соединение кюрия селективно экстрагируется с использованием многоступенчатой хроматографический и методы центрифугирования с подходящим реагентом.[53] Бис-триазинил бипиридин Комплекс недавно был предложен в качестве такого реагента, который обладает высокой селективностью к кюрию.[54] Отделение кюрия от очень похожего америция также может быть достигнуто путем обработки суспензии их гидроксидов в водной среде. бикарбонат натрия с озон при повышенной температуре. И америций, и кюрий присутствуют в растворах в основном в состоянии валентности +3; в то время как америций окисляется до растворимых комплексов Am (IV), кюрий остается неизменным и, таким образом, может быть выделен повторным центрифугированием.[55]
Металлический кюрий получают снижение его соединений. Первоначально для этой цели использовался фторид кюрия (III). Реакцию проводили в среде, свободной от воды и кислорода, в аппарате из тантал и вольфрам, используя элементаль барий или же литий как восстановители.[6][15][56][57][58]
Другая возможность - восстановление оксида кюрия (IV) с использованием сплава магния с цинком в расплаве хлорид магния и фторид магния.[59]
Соединения и реакции
Оксиды
Кюрий легко реагирует с кислородом, образуя в основном Cm2О3 и CmO2 оксиды,[47] но также известен двухвалентный оксид CmO.[60] Черный CmO2 можно получить сжиганием кюрия оксалат (См
2(C
2О
4)
3), нитрат (См (НЕТ
3)
3), или гидроксид в чистом кислороде.[28][61] При нагревании до 600–650 ° С в вакууме (около 0,01 Па ) он переходит в белесый цвет Cm2О3:[28][62]
- .
В качестве альтернативы Cm2О3 можно получить, уменьшив CmO2 с молекулярным водород:[63]
Кроме того, ряд тройных оксидов типа M (II) CmO3 известны, где М обозначает двухвалентный металл, такой как барий.[64]
Термическое окисление следовых количеств гидрида кюрия (CmH2–3), как сообщалось, производит летучую форму CmO2 и летучий триоксид CmO3, один из двух известных примеров очень редкого состояния +6 для кюрия.[2] Сообщалось, что другой наблюдаемый вид ведет себя аналогично предполагаемому четырехокиси плутония и предварительно охарактеризован как CmO4, с кюрием в крайне редком состоянии +8;[65] однако новые эксперименты, кажется, указывают на то, что CmO4 не существует, и поставили под сомнение существование PuO4 также.[66]
Галогениды
Бесцветный фторид кюрия (III) (CmF3) можно получить, вводя фторид-ионы в растворы, содержащие кюрий (III). Коричневый фторид четырехвалентного кюрия (IV) (CmF4) с другой стороны, получается только при взаимодействии фторида кюрия (III) с молекулярными фтор:[6]
Известен ряд тройных фторидов формы A7См6F31, где A означает щелочной металл.[67]
Бесцветный хлорид кюрия (III) (CmCl3) образуется в реакции гидроксид кюрия (III) (См (ОН)3) с безводным хлористый водород газ. Кроме того, он может быть преобразован в другие галогениды, такие как бромид кюрия (III) (от бесцветного до светло-зеленого) и иодид кюрия (III) (бесцветный), путем взаимодействия с аммиак соль соответствующего галогенида при повышенной температуре около 400–450 ° C:[68]
Альтернативной процедурой является нагревание оксида кюрия до примерно 600 ° C с соответствующей кислотой (такой как бромистоводородный для бромида кюрия).[69][70] Паровая фаза гидролиз хлорида кюрия (III) приводит к оксихлориду кюрия:[71]
Халькогениды и пниктиды
Сульфиды, селениды и теллуриды кюрия были получены обработкой кюрия газообразным сера, селен или же теллур в вакууме при повышенной температуре.[72][73] В пниктиды кюрия типа CmX известны элементами азот, фосфор, мышьяк и сурьма.[6] Их можно получить реакцией либо гидрида кюрия (III) (CmH3) или металлический кюрий с этими элементами при повышенных температурах.[74]
Органикоорганические соединения и биологические аспекты
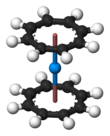
Металлоорганические комплексы, аналогичные ураноцен известны также другими актинидами, такими как торий, протактиний, нептуний, плутоний и америций. Молекулярная орбитальная теория предсказывает стабильный «куроценовый» комплекс (η8-C8ЧАС8)2См, но экспериментально пока не зарегистрировано.[75][76]
Формирование комплексов типа См (н-с
3ЧАС
7-BTP)
3, где BTP обозначает 2,6-ди (1,2,4-триазин-3-ил) пиридин, в растворах, содержащих n-C3ЧАС7-BTP и Cm3+ ионов подтверждено EXAFS. Некоторые из этих комплексов BTP-типа селективно взаимодействуют с кюрием и поэтому полезны для его селективного отделения от лантаноидов и других актинидов.[24][77] Растворенный см3+ ионы связываются со многими органическими соединениями, такими как гидроксамовая кислота,[78] мочевина,[79] флуоресцеин[80] и аденозинтрифосфат.[81] Многие из этих соединений связаны с биологической активностью различных микроорганизмы. Полученные комплексы демонстрируют сильную желто-оранжевую эмиссию при возбуждении УФ-светом, что удобно не только для их обнаружения, но и для изучения взаимодействия между Cm3+ ион и лиганды через изменение периода полураспада (порядка ~ 0,1 мс) и спектра флуоресценции.[25][78][79][80][81]
Кюрий не имеет биологического значения.[82] Есть несколько отчетов по биосорбция см3+ к бактерии и археи, однако нет доказательств включения в них кюрия.[83][84]
Приложения
Радионуклиды

Кюрий - один из самых радиоактивных изолируемых элементов. Два его самых распространенных изотопа 242См и 244См - сильные альфа-излучатели (энергия 6 МэВ); они имеют относительно короткий период полураспада, составляющий 162,8 дня и 18,1 года, и производят до 120 Вт / г и 3 Вт / г тепловой энергии, соответственно.[12][85][86] Таким образом, кюрий может использоваться в его обычной оксидной форме в радиоизотопные термоэлектрические генераторы как в космическом корабле. Это приложение было изучено на 244См изотоп, а 242От Cm отказались из-за его непомерно высокой цены около 2000 долларов США за грамм. 243См с периодом полураспада ~ 30 лет и хорошим выходом энергии ~ 1,6 Вт / г может быть подходящим топливом, но он производит значительное количество вредных веществ. гамма и бета излучение от продуктов радиоактивного распада. Хотя как α-излучатель, 244Для Cm требуется гораздо более тонкая радиационная защита, он имеет высокую скорость спонтанного деления, и, следовательно, интенсивность нейтронного и гамма-излучения относительно высока. По сравнению с конкурирующим изотопом термоэлектрического генератора, таким как 238Пу, 244Cm излучает в 500 раз больший флюенс нейтронов, а его более высокое гамма-излучение требует экрана, который в 20 раз толще - около 2 дюймов свинца для источника мощностью 1 кВт по сравнению с 0,1 дюйма для 238Пу. Поэтому такое применение кюрия в настоящее время считается непрактичным.[51]
Более перспективное применение 242См производить 238Pu, более подходящий радиоизотоп для термоэлектрических генераторов, таких как кардиостимуляторы. Альтернативные маршруты к 238Pu используют (n, γ) реакцию 237Np, или дейтрон бомбардировка урана, которые всегда производят 236Pu как нежелательный побочный продукт, поскольку последний распадается на 232U с сильным гамма-излучением.[87] Кюрий также является обычным исходным материалом для производства более высоких трансурановые элементы и трансактиниды. Таким образом, бомбардировка 248См с неоном (22Ne), магний (26Mg) или кальций (48Ca) дали определенные изотопы сиборгий (265Sg), хасиум (269Hs и 270Hs), и ливерморий (292Lv, 293Lv и, возможно, 294Lv).[88] Калифорний был открыт, когда мишень из кюрия-242 размером в микрограмм была облучена с энергией 35 МэВ. альфа-частицы с помощью 60-дюймового (150 см) циклотрона в Беркли:
- 242
96См
+ 4
2Он
→ 245
98Cf
+ 1
0п
В этом эксперименте было произведено всего около 5000 атомов калифорния.[89]

Рентгеновский спектрометр
Наиболее практическое применение 244См - хотя и довольно ограниченный в общем объеме - является источником α-частиц в рентгеновские спектрометры альфа-частиц (APXS). Эти инструменты были установлены на Соджорнер, Марс, Марс 96, Марсоходы и Посадочный модуль кометы Philae,[90] так же хорошо как Марсианская научная лаборатория анализировать состав и структуру горных пород на поверхности планеты Марс.[91] APXS также использовался в Сюрвейер 5–7 лунные зонды, но с 242См исходник.[49][92][93]
Разработанная установка APXS оснащена сенсорной головкой, содержащей шесть источников кюрия, суммарная скорость радиоактивного распада которых составляет несколько десятков милликюри (примерно гигабеккерель ). Источники коллимируются на образце, и анализируются энергетические спектры рассеянных от образца альфа-частиц и протонов (протонный анализ реализован только в некоторых спектрометрах). Эти спектры содержат количественную информацию обо всех основных элементах в образцах, кроме водорода, гелия и лития.[94]
Безопасность
Из-за его высокой радиоактивности с кюрием и его соединениями следует обращаться в соответствующих лабораториях с соблюдением специальных мер. В то время как сам кюрий в основном испускает α-частицы, которые поглощаются тонкими слоями обычных материалов, некоторые из продуктов его распада испускают значительные доли бета- и гамма-излучения, которые требуют более сложной защиты.[47] При употреблении кюрий выводится в течение нескольких дней, и только 0,05% всасывается с кровью. Оттуда около 45% идет в печень, 45% к костям, а оставшиеся 10% выводятся из организма. В кости кюрий накапливается на внутренней стороне интерфейсов с Костный мозг и со временем существенно не перераспределяется; его излучение разрушает Костный мозг и таким образом останавливается эритроцит творчество. В биологический период полураспада Кюрия составляет около 20 лет в печени и 50 лет в костях.[47][49] Кюрий всасывается в организме намного сильнее при вдыхании, и допустимая общая доза составляет 244См в растворимой форме составляет 0,3 мкм.C.[12] Внутривенное введение 242См и 244Cm-содержащие растворы для крыс увеличивали частоту костная опухоль, и ингаляции способствовали легочный и рак печени.[47]
Изотопы кюрия неизбежно присутствуют в отработавшем ядерном топливе с концентрацией около 20 г / т.[95] Среди них 245См-248Время распада изотопов Cm составляет тысячи лет, и их необходимо удалить, чтобы нейтрализовать топливо для утилизации.[96] Соответствующая процедура включает несколько этапов, на которых кюрий сначала отделяется, а затем превращается нейтронной бомбардировкой в специальных реакторах в короткоживущие нуклиды. Эта процедура, ядерная трансмутация хотя и хорошо документированы для других элементов, для кюрия все еще разрабатывается.[24]
Рекомендации
- ^ Ковач, Аттила; Dau, Phuong D .; Марсало, Жоаким; Гибсон, Джон К. (2018). «Пятивалентный кюрий, берклий и калифорний в нитратных комплексах: расширение химии актинидов и состояния окисления». Неорг. Chem. Американское химическое общество. 57 (15): 9453–9467. Дои:10.1021 / acs.inorgchem.8b01450. PMID 30040397.
- ^ а б c Доманов, В. П .; Лобанов, Ю. В. (октябрь 2011 г.). «Образование летучего триоксида кюрия (VI) CmO3". Радиохимия. ИП МАИК Наука / Интерпериодика. 53 (5): 453–6. Дои:10.1134 / S1066362211050018. S2CID 98052484.
- ^ а б c Шенкель Р. (1977). «Удельное электрическое сопротивление металла 244 см». Твердотельные коммуникации. 23 (6): 389. Bibcode:1977SSCom..23..389S. Дои:10.1016/0038-1098(77)90239-3.
- ^ Холл, Нина (2000). Новая химия: пример современной химии и ее приложений. Издательство Кембриджского университета. стр.8 –9. ISBN 978-0-521-45224-3.
- ^ а б Сиборг, Гленн Т .; Джеймс, Р. А .; Гиорсо, А. (1949). «Новый элемент кюрий (атомный номер 96)» (PDF). NNES PPR (Национальная серия по ядерной энергии, рекорд плутониевого проекта). Трансурановые элементы: научные статьи, доклад № 22.2. 14 млрд. OSTI http://www.osti.gov/cgi-bin/rd_accomplishments/display_biblio.cgi?id=ACC0049&numPages=13&fp=N.
- ^ а б c d е Morss, L.R .; Эдельштейн, Н. М. и Фугере, Дж. (Ред.): Химия актинидных элементов и трансактинидов, том 3, Springer-Verlag, Dordrecht 2006, ISBN 1-4020-3555-1.
- ^ а б Пеплинг, Рэйчел Шеремета (2003). "Новости химии и техники: это элементарно: Периодическая таблица - Америций". Получено 2008-12-07.
- ^ Кребс, Роберт Э. История и использование химических элементов нашей Земли: справочное руководство, Greenwood Publishing Group, 2006 г., ISBN 0-313-33438-2 п. 322
- ^ а б c Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (1997). "ТогдаUBASE оценка ядерных и распадных свойств » (PDF). Ядерная физика A. 624 (1): 1–124. Bibcode:1997НуФА.624 .... 1А. Дои:10.1016 / S0375-9474 (97) 00482-X. Архивировано из оригинал (PDF) на 2008-09-23.
- ^ Сиборг, Г. Т. Патент США 3,161,462 «Элемент», дата подачи: 7 февраля 1949 г., дата выдачи: декабрь 1964 г.
- ^ Гринвуд, стр. 1252
- ^ а б c d е Хаммонд С. Р. "Элементы" в Лиде, Д. Р., изд. (2005). CRC Справочник по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5.
- ^ Л. Б. Вернер, И. Перлман: «Выделение кюрия», ННЭС ППР (Национальная серия по атомной энергии, Рекорд плутониевого проекта), Т. 14 Б, Трансурановые элементы: исследовательские работы, Бумага № 22.5, McGraw-Hill Book Co., Inc., Нью-Йорк, 1949.
- ^ "Национальная академия наук. Исадор Перлман 1915–1991". Nap.edu. Получено 2011-03-25.
- ^ а б Wallmann, J.C .; Crane, W. W. T .; Каннингем, Б. Б. (1951). «Получение и некоторые свойства металлического кюрия» (PDF). Журнал Американского химического общества. 73 (1): 493–494. Дои:10.1021 / ja01145a537. HDL:2027 / mdp.39015086479790.
- ^ Werner, L.B .; Перлман И. (1951). «Первое выделение кюрия». Журнал Американского химического общества. 73 (1): 5215–5217. Дои:10.1021 / ja01155a063.
- ^ а б Мильман, В .; Винклер, Б .; Пикард, К. Дж. (2003). «Кристаллические структуры соединений кюрия: исследование ab initio». Журнал ядерных материалов. 322 (2–3): 165. Bibcode:2003JNuM..322..165M. Дои:10.1016 / S0022-3115 (03) 00321-0.
- ^ Янг, Д.А. Фазовые диаграммы элементов, Калифорнийский университет Press, 1991, ISBN 0-520-07483-1, п. 227
- ^ Haire, R .; Peterson, J .; Benedict, U .; Dufour, C .; Ити, Дж. (1985). «Рентгеновская дифракция металла кюрий-248 при давлениях до 52 ГПа». Журнал менее распространенных металлов. 109 (1): 71. Дои:10.1016/0022-5088(85)90108-0.
- ^ Kanellakopulos, B .; Blaise, A .; Fournier, J.M .; Мюллер, В. (1975). «Магнитная восприимчивость америция и металлического кюрия». Твердотельные коммуникации. 17 (6): 713. Bibcode:1975SSCom..17..713K. Дои:10.1016/0038-1098(75)90392-0.
- ^ Fournier, J .; Blaise, A .; Muller, W .; Спирлет, Ж.-К. (1977). «Кюрий: новый магнитный элемент». Физика B + C. 86–88: 30. Bibcode:1977PhyBC..86 ... 30F. Дои:10.1016/0378-4363(77)90214-5.
- ^ Nave, S. E .; Huray, P.G .; Петерсон, Дж. Р. и Дэмиен, Д. А. Магнитная восприимчивость пниктидов кюрия, Национальная лаборатория Ок-Ридж
- ^ Шенкель Р. (1977). «Удельное электрическое сопротивление металла 244 см». Твердотельные коммуникации. 23 (6): 389. Bibcode:1977SSCom..23..389S. Дои:10.1016/0038-1098(77)90239-3.
- ^ а б c Денеке, Мелисса А .; Россберг, Андре; Panak, Petra J .; Weigl, Майкл; Шиммельпфенниг, Бернд; Гейст, Андреас (2005). «Характеристика и сравнение Cm (III) и Eu (III) в комплексе с 2,6-ди (5,6-дипропил-1,2,4-триазин-3-ил) пиридином с использованием EXAFS, TRFLS и Quantum-Chemical Методы ». Неорганическая химия. 44 (23): 8418–8425. Дои:10.1021 / ic0511726. PMID 16270980.
- ^ а б Bünzli, J.-C. Г. и Чоппин, Г. Р. Зонды на лантаноиды в биологии, химии и науках о Земле: теория и практика, Эльзевир, Амстердам, 1989 ISBN 0-444-88199-9
- ^ Пеннеман, стр. 24
- ^ Кинан, Томас К. (1961). «Первое наблюдение за водным четырехвалентным кюрием». Журнал Американского химического общества. 83 (17): 3719. Дои:10.1021 / ja01478a039.
- ^ а б c Asprey, L.B .; Ellinger, F.H .; Fried, S .; Захариасен, В. Х. (1955). «Доказательства для четырехвалентного кюрия: данные рентгеновского излучения на оксидах кюрия1». Журнал Американского химического общества. 77 (6): 1707. Дои:10.1021 / ja01611a108.
- ^ а б Грегг Дж., Люметта; Томпсон, майор К .; Пеннеман, Роберт А .; Эллер, П. Гэри (2006). «Кюриум». In Morss, Lester R .; Эдельштейн, Норман М .; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (PDF). 3 (3-е изд.). Дордрехт, Нидерланды: Springer. С. 1397–1443. Дои:10.1007/1-4020-3598-5_9. ISBN 978-1-4020-3555-5.
- ^ Гринвуд, стр. 1265
- ^ Холлеман, стр. 1956 г.
- ^ Пеннеман, стр. 25–26.
- ^ Дженсен, Марк П .; Бонд, Эндрю Х. (2002). «Сравнение ковалентности комплексов трехвалентных актинидов и катионов лантанидов». Журнал Американского химического общества. 124 (33): 9870–9877. Дои:10.1021 / ja0178620. PMID 12175247.
- ^ Сиборг, Гленн Т. (1993). "Обзор актинидов и лантанидов ( ж) Элементы ». Radiochimica Acta. 61 (3–4): 115–122. Дои:10.1524/ract.1993.61.34.115. S2CID 99634366.
- ^ Гринвуд, стр. 1267
- ^ Pfennig, G.; Klewe-Nebenius, H. and Seelmann Eggebert, W. (Eds.): Karlsruhe нуклид, 6-е изд. 1998 г.
- ^ Kang, Jungmin; Von Hippel, Frank (2005). "Limited Proliferation-Resistance Benefits from Recycling Unseparated Transuranics and Lanthanides from Light-Water Reactor Spent Fuel" (PDF). Science and Global Security. 13 (3): 169. Bibcode:2005S&GS...13..169K. Дои:10.1080/08929880500357682. S2CID 123552796.
- ^ Osaka, M.; и другие. (2001). "Analysis of Curium Isotopes in Mixed Oxide Fuel Irradiated in Fast Reactor" (PDF). Журнал ядерной науки и технологий. 38 (10): 912–914. Дои:10.3327/jnst.38.912. Архивировано из оригинал (PDF) 3 июля 2007 г.
- ^ а б Institut de Radioprotection et de Sûreté Nucléaire: "Evaluation of nuclear criticality safety. data and limits for actinides in transport" В архиве May 19, 2011, at the Wayback Machine, п. 16
- ^ Национальный исследовательский совет (США). Committee on Separations Technology and Transmutation Systems (1996). Nuclear wastes: technologies for separations and transmutation. Национальная академия прессы. стр. 231–. ISBN 978-0-309-05226-9. Получено 19 апреля 2011.
- ^ Sasahara, Akihiro; Matsumura, Tetsuo; Nicolaou, Giorgos; Papaioannou, Dimitri (2004). "Neutron and Gamma Ray Source Evaluation of LWR High Burn-up UO2 and MOX Spent Fuels" (PDF). Журнал ядерной науки и технологий. 41 (4): 448–456. Дои:10.3327/jnst.41.448.
- ^ Okundo, H. & Kawasaki, H. (2002). "Critical and Subcritical Mass Calculations of Curium-243 to −247 Based on JENDL-3.2 for Revision of ANSI/ANS-8.15". Журнал ядерной науки и технологий. 39 (10): 1072–1085. Дои:10.3327/jnst.39.1072.
- ^ § 2 Begriffsbestimmungen (Atomic Energy Act) (на немецком)
- ^ Jukka Lehto; Xiaolin Hou (2 February 2011). Chemistry and Analysis of Radionuclides: Laboratory Techniques and Methodology. Wiley-VCH. С. 303–. ISBN 978-3-527-32658-7. Получено 19 апреля 2011.
- ^ Earth, Live Science Staff 2013-09-24T21:44:13Z Planet. "Facts About Curium". livescience.com. Получено 2019-08-10.
- ^ "Curium - Element information, properties and uses | Periodic Table". www.rsc.org. Получено 2019-08-10.
- ^ а б c d е Кюрий (на немецком)
- ^ Fields, P. R.; Studier, M. H.; Diamond, H.; и другие. (1956). "Transplutonium Elements in Thermonuclear Test Debris". Физический обзор. 102 (1): 180–182. Bibcode:1956PhRv..102..180F. Дои:10.1103/PhysRev.102.180.
- ^ а б c Human Health Fact Sheet on Curium В архиве 2006-02-18 в Wayback Machine, Лос-Аламосская национальная лаборатория
- ^ Emsley, John (2011). Строительные блоки природы: руководство по элементам от А до Я (New ed.). Нью-Йорк, Нью-Йорк: Издательство Оксфордского университета. ISBN 978-0-19-960563-7.
- ^ а б Basic elements of static RTGs, G.L. Kulcinski, NEEP 602 Course Notes (Spring 2000), Nuclear Power in Space, University of Wisconsin Fusion Technology Institute (see last page)
- ^ а б c Lumetta, Gregg J.; Thompson, Major C.; Penneman, Robert A.; Eller, P. Gary (2006). "Curium" (PDF). In Morss; Edelstein, Norman M.; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (3-е изд.). Dordrecht, The Netherlands: Springer Science + Business Media. п. 1401. ISBN 978-1-4020-3555-5. Архивировано из оригинал (PDF) on 2010-07-17.
- ^ Penneman, pp. 34–48
- ^ Magnusson D; Christiansen B; Foreman MRS; Geist A; Glatz JP; Malmbeck R; Modolo G; Serrano-Purroy D & Sorel C (2009). "Demonstration of a SANEX Process in Centrifugal Contactors using the CyMe4-BTBP Molecule on a Genuine Fuel Solution". Экстракция растворителем и ионный обмен. 27 (2): 97. Дои:10.1080/07366290802672204. S2CID 94720457.
- ^ Penneman, p. 25
- ^ Cunningham, B. B.; Wallmann, J. C. (1964). "Crystal structure and melting point of curium metal". Журнал неорганической и ядерной химии. 26 (2): 271. Дои:10.1016/0022-1902(64)80069-5. OSTI 4667421.
- ^ Stevenson, J.; Peterson, J. (1979). "Preparation and structural studies of elemental curium-248 and the nitrides of curium-248 and berkelium-249". Журнал менее распространенных металлов. 66 (2): 201. Дои:10.1016/0022-5088(79)90229-7.
- ^ Gmelin Handbook of Inorganic Chemistry, System No. 71, Volume 7 a, transuranics, Part B 1, pp. 67–68.
- ^ Eubanks, I.; Thompson, M. C. (1969). "Preparation of curium metal". Письма по неорганической и ядерной химии. 5 (3): 187. Дои:10.1016/0020-1650(69)80221-7.
- ^ Holleman, p. 1972 г.
- ^ Гринвуд, стр. 1268
- ^ Noe, M.; Fuger, J. (1971). "Self-radiation effects on the lattice parameter of 244CmO2". Письма по неорганической и ядерной химии. 7 (5): 421. Дои:10.1016/0020-1650(71)80177-0.
- ^ Haug, H. (1967). "Curium sesquioxide Cm2O3". Журнал неорганической и ядерной химии. 29 (11): 2753. Дои:10.1016/0022-1902(67)80014-9.
- ^ Fuger, J.; Haire, R.; Peterson, J. (1993). "Molar enthalpies of formation of BaCmO3 and BaCfO3". Журнал сплавов и соединений. 200 (1–2): 181. Дои:10.1016/0925-8388(93)90491-5.
- ^ Domanov, V. P. (January 2013). "Possibility of generation of octavalent curium in the gas phase in the form of volatile tetraoxide CmO4". Радиохимия. 55 (1): 46–51. Дои:10.1134/S1066362213010098. S2CID 98076989.
- ^ Zaitsevskii, Andréi; Schwarz, W. H. Eugen (April 2014). "Structures and stability of AnO4 isomers, An = Pu, Am, and Cm: a relativistic density functional study". Физическая химия Химическая физика. 2014 (16): 8997–9001. Bibcode:2014PCCP...16.8997Z. Дои:10.1039/c4cp00235k. PMID 24695756.
- ^ Keenan, T. (1967). "Lattice constants of K7Cm6F31 trends in the 1:1 and 7:6 alkali metal-actinide(IV) series". Письма по неорганической и ядерной химии. 3 (10): 391. Дои:10.1016/0020-1650(67)80092-8.
- ^ Asprey, L.B .; Keenan, T. K.; Kruse, F. H. (1965). "Crystal Structures of the Trifluorides, Trichlorides, Tribromides, and Triiodides of Americium and Curium". Неорганическая химия. 4 (7): 985. Дои:10.1021/ic50029a013.
- ^ Burns, J .; Peterson, J. R .; Stevenson, J. N. (1975). "Crystallographic studies of some transuranic trihalides: 239PuCl3, 244CmBr3, 249BkBr3 and 249CfBr3". Журнал неорганической и ядерной химии. 37 (3): 743. Дои:10.1016/0022-1902(75)80532-X.
- ^ Wallmann, J.; Fuger, J.; Peterson, J. R .; Green, J. L. (1967). "Crystal structure and lattice parameters of curium trichloride". Журнал неорганической и ядерной химии. 29 (11): 2745. Дои:10.1016/0022-1902(67)80013-7.
- ^ Weigel, F .; Wishnevsky, V.; Hauske, H. (1977). "The vapor phase hydrolysis of PuCl3 and CmCl3: heats of formation of PuOC1 and CmOCl". Журнал менее распространенных металлов. 56 (1): 113. Дои:10.1016/0022-5088(77)90224-7.
- ^ Troc, R. Actinide Monochalcogenides, Volume 27, Springer, 2009 ISBN 3-540-29177-6, п. 4
- ^ Damien, D.; Charvillat, J. P.; Müller, W. (1975). "Preparation and lattice parameters of curium sulfides and selenides". Письма по неорганической и ядерной химии. 11 (7–8): 451. Дои:10.1016/0020-1650(75)80017-1.
- ^ Lumetta, G. J.; Thompson, M. C.; Penneman, R. A.; Eller, P. G. Кюрий В архиве 2010-07-17 на Wayback Machine, Chapter Nine in Radioanalytical Chemistry, Springer, 2004, pp. 1420–1421. ISBN 0387341226, ISBN 978-0387 341224
- ^ Elschenbroich, Ch. Organometallic Chemistry, 6th edition, Wiesbaden 2008, ISBN 978-3-8351-0167-8, п. 589
- ^ Kerridge, Andrew; Kaltsoyannis, Nikolas (2009). "Are the Ground States of the Later Actinocenes Multiconfigurational? All-Electron Spin−Orbit Coupled CASPT2 Calculations on An(η8-C8H8)2(An = Th, U, Pu, Cm)". Журнал физической химии A. 113 (30): 8737–8745. Bibcode:2009JPCA..113.8737K. Дои:10.1021/jp903912q. PMID 19719318.
- ^ Girnt, Denise; Roesky, Peter W.; Гейст, Андреас; Ruff, Christian M.; Panak, Petra J.; Denecke, Melissa A. (2010). "6-(3,5-Dimethyl-1H-pyrazol-1-yl)-2,2′-bipyridine as Ligand for Actinide(III)/Lanthanide(III) Separation". Неорганическая химия. 49 (20): 9627–9635. Дои:10.1021/ic101309j. PMID 20849125. S2CID 978265.
- ^ а б Glorius, M.; Moll, H.; Bernhard, G. (2008). "Complexation of curium(III) with hydroxamic acids investigated by time-resolved laser-induced fluorescence spectroscopy". Многогранник. 27 (9–10): 2113. Дои:10.1016/j.poly.2008.04.002.
- ^ а б Heller, Anne; Barkleit, Astrid; Bernhard, Gert; Ackermann, Jörg-Uwe (2009). "Complexation study of europium(III) and curium(III) with urea in aqueous solution investigated by time-resolved laser-induced fluorescence spectroscopy". Неорганика Chimica Acta. 362 (4): 1215. Дои:10.1016/j.ica.2008.06.016.
- ^ а б Moll, Henry; Johnsson, Anna; Schäfer, Mathias; Pedersen, Karsten; Budzikiewicz, Herbert; Bernhard, Gert (2007). "Curium(III) complexation with pyoverdins secreted by a groundwater strain of Pseudomonas fluorescens". БиоМеталлы. 21 (2): 219–228. Дои:10.1007/s10534-007-9111-x. PMID 17653625. S2CID 24565144.
- ^ а б Moll, Henry; Geipel, Gerhard; Bernhard, Gert (2005). "Complexation of curium(III) by adenosine 5′-triphosphate (ATP): A time-resolved laser-induced fluorescence spectroscopy (TRLFS) study". Неорганика Chimica Acta. 358 (7): 2275. Дои:10.1016/j.ica.2004.12.055.
- ^ "Biochemical Periodic Table – Curium". UMBBD. 2007-06-08. Получено 2011-03-25.
- ^ Moll, H.; Stumpf, T.; Merroun, M.; Rossberg, A.; Selenska-Pobell, S.; Bernhard, G. (2004). "Time-resolved laser fluorescence spectroscopy study on the interaction of curium(III) with Desulfovibrio äspöensis DSM 10631T". Экологические науки и технологии. 38 (5): 1455–1459. Bibcode:2004EnST...38.1455M. Дои:10.1021/es0301166. PMID 15046347.
- ^ Ozaki, T .; и другие. (2002). "Association of Eu(III) and Cm(III) with Bacillus subtilis and Halobacterium salinarium". Журнал ядерной науки и технологий. Дополнение 3: 950–953. Дои:10.1080/00223131.2002.10875626. S2CID 98319565. Архивировано из оригинал 25 февраля 2009 г.
- ^ Binder, Harry H.: Lexikon der chemischen Elemente, S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3С. 174–178.
- ^ Gmelin Handbook of Inorganic Chemistry, System No. 71, Volume 7a, transuranics, Part A2, p. 289
- ^ Kronenberg, Andreas, Plutonium-Batterien В архиве 2013-12-26 в Wayback Machine (на немецком) «Архивная копия». Archived from the original on February 21, 2011. Получено 28 апреля, 2011.CS1 maint: заархивированная копия как заголовок (связь) CS1 maint: BOT: статус исходного URL-адреса неизвестен (связь)
- ^ Holleman, pp. 1980–1981.
- ^ Seaborg, Glenn T. (1996). Adloff, J. P. (ed.). One Hundred Years after the Discovery of Radioactivity. Oldenbourg Wissenschaftsverlag. п. 82. ISBN 978-3-486-64252-0.
- ^ "Der Rosetta Lander Philae". Bernd-leitenberger.de. 2003-07-01. Получено 2011-03-25.
- ^ Rieder, R.; Wanke, H.; Economou, T. (September 1996). "An Alpha Proton X-Ray Spectrometer for Mars-96 and Mars Pathfinder". Бюллетень Американского астрономического общества. 28: 1062. Bibcode:1996DPS....28.0221R.
- ^ Leitenberger, Bernd Die Surveyor Raumsonden (на немецком)
- ^ Nicks, Oran (1985). "Ch. 9. Essentials for Surveyor". SP-480 Far Travelers: The Exploring Machines. НАСА.
- ^ Alpha Particle X-Ray Spectrometer (APXS), Корнелл Университет
- ^ Hoffmann, K. Kann man Gold machen? Gauner, Gaukler und Gelehrte. Aus der Geschichte der chemischen Elemente (Can you make gold? Crooks, clowns and scholars. From the history of the chemical elements), Urania-Verlag, Leipzig, Jena, Berlin 1979, no ISBN, p. 233
- ^ Baetslé, L. H. Application of Partitioning/Transmutation of Radioactive Materials in Radioactive Waste Management В архиве 2005-04-26 на Wayback Machine, Nuclear Research Centre of Belgium Sck/Cen, Mol, Belgium, September 2001.
Библиография
- Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- Holleman, Arnold F. and Wiberg, Nils Lehrbuch der Anorganischen Chemie, 102 Edition, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Penneman, R. A. and Keenan T. K. The radiochemistry of americium and curium, University of California, Los Alamos, California, 1960
внешняя ссылка
- Кюрий в Периодическая таблица видео (Ноттингемский университет)
- NLM Hazardous Substances Databank – Curium, Radioactive






![{ displaystyle { ce {^ {238} _ {92} U -> [{ ce {(n, gamma)}}] {^ {239} _ {92} U} -> [ beta ^ { -}] [23.5 { ce {мин}}] _ {93} ^ {239} Np -> [ beta ^ {-}] [2.3565 { ce {d}}] _ {94} ^ { 239} Пу}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c30c60d3b829e92822267f24b94337ce0d267d38)
![{ displaystyle { ce {^ {239} _ {94} Pu -> [{ ce {2 (n, gamma)}}] _ {94} ^ {241} Pu -> [ beta ^ {- }] [14.35 { ce {yr}}] {^ {241} _ {95} Am} -> [{ ce {(n, gamma)}}] _ {95} ^ {242} Am- > [ beta ^ {-}] [16.02 { ce {h}}] _ {96} ^ {242} Cm}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ee8c743c87eab605b6f80f80388eeb9f462b4086)
![{ displaystyle { ce {^ {239} _ {94} Pu -> [{ ce {4 (n, gamma)}}] _ {94} ^ {243} Pu -> [ beta ^ {- }] [4.956 { ce {h}}] _ {95} ^ {243} Am -> [({ ce {n}}, gamma)] _ {95} ^ {244} Am -> [ beta ^ {-}] [10.1 { ce {h}}] _ {96} ^ {244} Cm -> [ alpha] [18.11 { ce {yr}}] _ {94} ^ {240 } Pu}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e202c162172b717f887b5f0bd06d3e01057ae924)

![{ displaystyle { begin {matrix} {} { ce {^ {252} _ {98} Cf -> [ alpha] [2.645 { ce {yr}}] ^ {248} _ {96 } Cm}} {} end {matrix}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c6cc4394eb604706a66a7112cda30cf38f857380)
![{ displaystyle { ce {^ {249} _ {97} Bk -> [ beta ^ -] [330 { ce {d}}] ^ {249} _ {98} Cf -> [ alpha] [351 { ce {yr}}] ^ {245} _ {96} Cm}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7ccddd548852fda4a6af794bec61eda1293ebdd8)

![{ Displaystyle { ce {4CmO2 -> [ Delta T] 2Cm2O3 + O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d347ad5669ad313e0453be3c15f15e400c2d5ef8)



