Нептуний - Neptunium
 | ||||||||||||||||||||||||||||||||
| Нептуний | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /пɛпˈtjuпяəм/ | |||||||||||||||||||||||||||||||
| Внешность | серебристый металлик | |||||||||||||||||||||||||||||||
| Массовое число | [237] | |||||||||||||||||||||||||||||||
| Нептуний в периодическая таблица | ||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||
| Атомный номер (Z) | 93 | |||||||||||||||||||||||||||||||
| Группа | группа н / д | |||||||||||||||||||||||||||||||
| Период | период 7 | |||||||||||||||||||||||||||||||
| Блокировать | f-блок | |||||||||||||||||||||||||||||||
| Категория элемента | Актинид | |||||||||||||||||||||||||||||||
| Электронная конфигурация | [Rn ] 5f4 6d1 7 с2 | |||||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 32, 22, 9, 2 | |||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||
| Фаза вSTP | твердый | |||||||||||||||||||||||||||||||
| Температура плавления | 912±3 K (639 ± 3 ° C, 1182 ± 5 ° F) | |||||||||||||||||||||||||||||||
| Точка кипения | 4447 К (4174 ° С, 7545 ° F) (экстраполировано) | |||||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | альфа: 20,45 г / см3[1] принятое нормативное значение: 19,38 г / см3 | |||||||||||||||||||||||||||||||
| Теплота плавления | 5.19 кДж / моль | |||||||||||||||||||||||||||||||
| Теплота испарения | 336 кДж / моль | |||||||||||||||||||||||||||||||
| Молярная теплоемкость | 29,46 Дж / (моль · К) | |||||||||||||||||||||||||||||||
Давление газа
| ||||||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||||||
| Состояния окисления | +2, +3, +4,[2] +5, +6, +7 (анамфотерный окись) | |||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,36 | |||||||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||||||
| Радиус атома | эмпирические: 155вечера | |||||||||||||||||||||||||||||||
| Ковалентный радиус | 190 ± 13 часов | |||||||||||||||||||||||||||||||
| Другие свойства | ||||||||||||||||||||||||||||||||
| Естественное явление | от разложения | |||||||||||||||||||||||||||||||
| Кристальная структура | ромбический | |||||||||||||||||||||||||||||||
| Теплопроводность | 6,3 Вт / (м · К) | |||||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 1,220 мкОм · м (при 22 ° C) | |||||||||||||||||||||||||||||||
| Магнитный заказ | парамагнитный[3] | |||||||||||||||||||||||||||||||
| Количество CAS | 7439-99-8 | |||||||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||||||
| Именование | после планеты Нептун, названный в честь римского бога моря Нептун | |||||||||||||||||||||||||||||||
| Открытие | Эдвин Макмиллан и Филип Х. Абельсон (1940) | |||||||||||||||||||||||||||||||
| Главный изотопы нептуния | ||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||
Нептуний это химический элемент с символ Np и атомный номер 93. А радиоактивный актинид металл, нептуний - первый трансурановый элемент. Его положение в периодическая таблица только после уран, названный в честь планеты Уран, привело к тому, что он был назван в честь Нептун, следующая планета за Ураном. В атоме нептуния 93 протоны и 93 электрона, из которых семь являются валентные электроны. Металлический нептуний серебристый и тускнеет при контакте с воздухом. Элемент встречается в трех аллотропный формы и обычно показывает пять состояния окисления от +3 до +7. это радиоактивный, ядовитый, пирофорный, и способна накапливаться в кости, что делает опасным обращение с нептунием.
Хотя на протяжении многих лет было сделано много ложных заявлений о его открытии, этот элемент был впервые синтезирован Эдвин Макмиллан и Филип Х. Абельсон на Радиационная лаборатория Беркли в 1940 г.[4] С тех пор большая часть нептуния производилась и до сих пор производится нейтронное облучение урана в ядерных реакторах. Подавляющее большинство генерируется как побочный продукт в обычных атомная энергия реакторы. Хотя сам нептуний в настоящее время не имеет коммерческого использования, он используется в качестве прекурсора для образования плутоний-238, используется в радиоизотопные термогенераторы обеспечить электричеством космический корабль. Нептуний также использовался в детекторы высокоэнергетических нейтроны.
Самый долгоживущий изотоп нептуния, нептуний-237, является побочным продуктом ядерные реакторы и плутоний производство. Он и изотоп нептуний-239 также в следовых количествах содержатся в уран руды из-за реакции захвата нейтронов и бета-распад.[5]
Характеристики
Физический
Нептуний - это жесткий, серебристый, пластичный, радиоактивный актинид металл. в периодическая таблица, он расположен справа от актинида уран, слева от актинида плутоний и ниже лантаноид прометий.[6] Нептуний - твердый металл, имеющий модуль объемной упругости 118ГПа, сравнимо с марганец.[7] Металлический нептуний похож на уран с точки зрения физической обрабатываемости. При воздействии воздуха при нормальной температуре образует тонкий оксидный слой. Эта реакция протекает быстрее при повышении температуры.[6] Было установлено, что нептуний плавится при температуре 639 ± 3 ° C: эта низкая температура плавления, свойство металла разделяет с соседним элементом плутонием (который имеет точку плавления 639,4 ° C), благодаря гибридизация 5f и 6d орбиталей и образование направленных связей в металле.[8] Температура кипения нептуния эмпирически не известна, и обычно данное значение 4174 ° C экстраполируется из давление газа элемента. Если быть точным, это дало бы нептунию самый большой диапазон жидких веществ из всех элементов (3535 К проходит между его точками плавления и кипения).[6][9]
Нептуний встречается как минимум в трех аллотропы.[5] Были сделаны некоторые утверждения о четвертом аллотропе, но они пока не доказаны.[6] Такая множественность аллотропов обычна среди актинидов. В кристаллические структуры нептуния, протактиний, уран и плутоний не имеют четких аналогов среди лантаноидов и больше похожи на аналогии 3-гопереходные металлы.[8]
| Аллотроп нептуний | α | β (измерено при 313 ° C) | γ (измерено при 600 ° C) |
|---|---|---|---|
| Температура перехода | (α → β) 282 ° С | (β → γ) 583 ° С | (γ → жидкость) 639 ° C |
| Симметрия | Орторомбический | Тетрагональный | Телоцентрированный кубический |
| Плотность (г / см3, 237Np)[11] | 20.45 | 19.36 | 18.0 |
| Космическая группа | ПНМА | P42[сомнительный ] | Im3m |
| Параметры решетки (вечера ) | а = 666.3 б = 472.3 c = 488.7 | а = 489.7 c = 338.8 | а = 351.8 |

α-нептуний приобретает ромбический структура, напоминающая сильно искаженную объемно-центрированную кубическую структуру.[11][12] Каждый атом нептуния координирован с четырьмя другими, а длина связи Np – Np составляет 260 пм.[13] Он является самым плотным из всех актинидов и пятым по плотности из всех природных элементов, уступая только рений, платина, иридий, и осмий.[9] α-нептуний имеет полуметаллический свойства, такие как сильные ковалентная связь и высокий удельное электрическое сопротивление, а его металлические физические свойства ближе к свойствам металлоиды чем настоящий металл. Некоторые аллотропы других актинидов также демонстрируют подобное поведение, хотя и в меньшей степени.[14][15] Ожидается, что плотности различных изотопов нептуния в альфа-фазе будут заметно различаться:235Нп должен иметь плотность 20,303 г / см.3; α-236Np, плотность 20,389 г / см3; α-237Np, плотность 20,476 г / см3.[16]
β-нептуний приобретает искаженную тетрагональную плотноупакованную структуру. Четыре атома нептуния составляют элементарную ячейку, а длина связи Np – Np составляет 276 пм.[13] γ-нептуний имеет объемно-центрированный кубический структура и имеет длину связи Np – Np 297 пм. Γ-форма становится менее стабильной с повышением давления, хотя точка плавления нептуния также увеличивается с повышением давления.[13] Β-Np / γ-Np / жидкость тройная точка происходит при 725 ° C и 3200МПа.[13][17]
Сплавы
Из-за наличия валентных 5f-электронов нептуний и его сплавы, как и многие другие актиниды, демонстрируют очень интересное магнитное поведение. Они могут варьироваться от странствующего полосообразного характера, характерного для переходные металлы к локальному моменту поведения, типичному для скандий, иттрий, а лантаноиды. Это связано с гибридизацией 5f-орбиталей с орбиталями металла. лиганды, и тот факт, что орбиталь 5f релятивистски дестабилизируется и распространяется наружу.[18] Например, чистый нептуний - это парамагнитный, NpAl3 является ферромагнитный, NpGe3 не имеет магнитного упорядочения, а NpSn3 ведет себя фермионно.[18] Ведутся исследования сплавов нептуния с ураном, америций, плутоний, цирконий, и утюг, чтобы перерабатывать долгоживущие изотопы отходов, такие как нептуний-237, в более короткоживущие изотопы, более полезные в качестве ядерного топлива.[18]
Один на основе нептуния сверхпроводник сплав был обнаружен с формулой NpPd5Al2. Это явление в соединениях нептуния несколько неожиданно, поскольку они часто обладают сильным магнетизмом, который обычно разрушает сверхпроводимость. Сплав имеет тетрагональную структуру с температурой перехода в сверхпроводимость −268,3 ° C (4,9 K).[19][20]
Химическая
Нептуний имеет пять ионных состояния окисления от +3 до +7 при образовании химических соединений, которые одновременно могут наблюдаться в растворах. Это самый тяжелый актинид, который может потерять все свои валентные электроны в стабильном соединении. Наиболее стабильное состояние в растворе +5, но валентность +4 предпочтительна для твердых соединений нептуния. Металлический нептуний очень реактивен. Ионы нептуния склонны к гидролизу и образованию координационные соединения.[21]
Атомный
Атом нептуния имеет 93 электрона, расположенных в конфигурация [Rn ] 5f46d17 с2. Это отличается от конфигурации, ожидаемой Принцип Ауфбау в этом один электрон находится в подоболочке 6d, а не в подоболочке 5f, как ожидалось. Это происходит из-за схожести энергий электронов подоболочек 5f, 6d и 7s. При образовании соединений и ионов все валентные электроны могут быть потеряны, оставив после себя инертное ядро из внутренних электронов с электронной конфигурацией благородный газ радон;[22] чаще всего теряется только часть валентных электронов. Электронная конфигурация триположительного иона Np3+ равно [Rn] 5f4, причем первыми теряются внешние 7s и 6d электроны: это в точности аналогично прометию, гомологу лантанида нептуния, и соответствует тенденции, заданной другими актинидами с их [Rn] 5fп электронные конфигурации в триположительном состоянии. Первый потенциал ионизации нептуния не превышало 6.19±0.12 эВ в 1974 г., исходя из предположения, что электроны 7s ионизируются раньше, чем 5f и 6d;[23] более поздние измерения уточнили это значение до 6,2657 эВ.[24]
Изотопы

24 нептуний радиоизотопы были охарактеризованы как наиболее стабильные 237Np с период полураспада 2,14 миллиона лет, 236Np с периодом полураспада 154000 лет, и 235Np с периодом полураспада 396,1 суток. Все остальные радиоактивный изотопы имеют период полураспада менее 4,5 дней, и у большинства из них период полураспада составляет менее 50 минут. Этот элемент также имеет не менее четырех мета состояния, с наиболее устойчивым существом 236 кв.м.Np с периодом полураспада 22,5 часа.[25]
Изотопы нептуния в диапазоне атомный вес из 219.032 ты (219Np) до 244,068 u (244Np), хотя 221Np и 222Np пока не сообщается.[25] Большинство изотопов легче, чем самый стабильный, 237Np, разлагаться в первую очередь захват электронов хотя и значительное число, особенно 229Np и 230Np, также демонстрируют различные уровни распада через альфа-излучение стать протактиний. 237Сам Np, будучи бета-стабильная изобара массового числа 237, распадается почти исключительно за счет альфа-излучения в 233Па, с очень редкими (встречается только один раз из триллионов распадов) спонтанное деление и кластерный распад (выброс 30Mg для образования 207Тл). Все известные изотопы, кроме одного тяжелее этого распада, распадаются исключительно через бета-излучение.[25][26] Единственное исключение, 240 мNp, имеет редкий (> 0,12%) распад на изомерный переход в дополнение к бета-излучению.[25] 237Np в конечном итоге распадается с образованием висмут -209 и таллий -205, в отличие от большинства других обычных тяжелых ядер, которые распадаются на изотопы свинца. Этот цепочка распада известен как нептуний ряд.[19][27] Эта цепочка распада давно исчезла на Земле из-за короткого периода полураспада всех ее изотопов выше висмута-209, но теперь возрождается благодаря искусственному производству нептуния в тоннах.[28]
Изотопы нептуний-235, -236 и -237, по прогнозам, будут делящийся;[16] экспериментально показана только расщепляемость нептуния-237, причем критическая масса около 60 кг, всего на 10 кг больше, чем у обычно используемых уран-235.[29] Расчетные значения критических масс нептуния-235, -236 и -237 соответственно составляют 66,2 кг, 6,79 кг и 63,6 кг: значение нептуния-236 даже ниже, чем у нептуния-236. плутоний-239. Особенно 236Np также имеет низкую нейтронную поперечное сечение.[16] Несмотря на это, нептуний Атомная бомба никогда не строился:[29] уран и плутоний имеют более низкие критические массы, чем 235Np и 237Np и 236Np трудно очистить, так как он не содержится в количестве в отработанное ядерное топливо[26] и практически невозможно отделить в каких-либо значительных количествах от родительского 237Np.[30]
Вхождение
Поскольку все изотопы нептуния имеют период полураспада во много раз короче, чем возраст Земли, любой изначальный нептуний к настоящему времени должен был распасться. Спустя всего около 80 миллионов лет концентрация даже самого долгоживущего изотопа, 237Np, сократилась бы до менее одной триллионной (10−12) от первоначальной суммы;[31] и даже если бы вся Земля изначально была сделана из чистого 237Np (и игнорируя, что это было бы намного критическая масса 60 кг), 2100 периодов полураспада прошло бы с момента формирование Солнечной системы, и поэтому все это распалось бы. Таким образом, нептуний присутствует в природе только в незначительных количествах и образуется как промежуточные продукты распада других изотопов.[21]
След количества изотопов нептуния нептуний-237 и -239 встречаются в природе как продукты распада из трансмутация реакции в урановые руды.[5][32] Особенно, 239Np и 237Np - самые распространенные из этих изотопов; они непосредственно сформированы из захват нейтронов атомами урана-238. Эти нейтроны приходят из спонтанное деление урана-238, естественное нейтронно-индуцированное деление урана-235, расщепление космических лучей ядер и легких элементов, поглощающих альфа-частицы и испускает нейтрон.[31] Период полураспада 239Np очень короткий, хотя обнаружение его гораздо более долгоживущих дочь 239Pu в природе в 1951 г. окончательно установил его естественное распространение.[31] В 1952 г. 237Np был идентифицирован и выделен из концентратов урановой руды месторождения. Бельгийское Конго: в этих минералах отношение нептуния-237 к урану меньше или равно примерно 10−12 к 1.[31][33][34]
Большая часть нептуния (и плутония), встречающегося в настоящее время в окружающей среде, связана с ядерными взрывами в атмосфере, которые произошли между взрывом первая атомная бомба в 1945 г. и ратификация Договор о частичном запрещении ядерных испытаний в 1963 году. Общее количество нептуния, выделившегося в результате этих взрывов и нескольких атмосферных испытаний, проведенных с 1963 года, оценивается примерно в 2500 кг. Подавляющее большинство из них состоит из долгоживущих изотопов. 236Np и 237Нп так как даже умеренно долгоживущие 235Np (период полураспада 396 дней) распался бы до менее одной миллиардной (10−9) его первоначальная концентрация за прошедшие десятилетия. Дополнительное очень небольшое количество нептуния, образовавшееся при нейтронном облучении природного урана в охлаждающей воде ядерного реактора, выделяется, когда вода сбрасывается в реки или озера.[31][33][35] Концентрация 237Np в морской воде составляет примерно 6,5 × 10−5 миллибеккерели на литр: эта концентрация составляет от 0,1% до 1% от концентрации плутония.[31]
Попадая в окружающую среду, нептуний обычно окисляет довольно быстро, обычно до состояния +4 или +5. Независимо от степени окисления элемент демонстрирует гораздо большую подвижность, чем другие актиниды, в основном из-за его способности легко образовывать водные растворы с различными другими элементами. В одном исследовании, сравнивающем скорость диффузии нептуния (V), плутония (IV) и америция (III) в песчанике и известняке, нептуний проникал более чем в десять раз, как и другие элементы. Np (V) также будет эффективно реагировать при уровнях pH выше 5,5, если нет карбонаты присутствует, и в этих условиях также было замечено, что он легко связывается с кварц. Также было замечено хорошее сцепление с гетит, оксид железа коллоиды и несколько глин, включая каолинит и смектит. Np (V) не так легко связывается с частицами почвы в умеренно кислых условиях, как его собратья актиниды америций и кюрий почти на порядок величины. Такое поведение позволяет ему быстро перемещаться через почву, находясь в растворе, не закрепляясь на месте, что еще больше способствует его подвижности.[33][36] Np (V) также легко поглощается бетоном, что из-за радиоактивности элемента является фактором, который необходимо учитывать при строительстве. ядерные отходы складское хозяйство. При впитывании в бетон он уменьшенный к Np (IV) за относительно короткий период времени. Np (V) также уменьшается на гуминовая кислота если он присутствует на поверхности гетита, гематит, и магнетит. Np (IV) эффективно поглощается туф, гранодиорит, и бентонит; хотя поглощение последним наиболее выражено в умеренно кислых условиях. Он также проявляет сильную тенденцию связываться с коллоидные частицы, эффект, который усиливается при использовании почвы с высоким содержанием глины. Такое поведение обеспечивает дополнительную помощь в наблюдаемой высокой подвижности элемента.[33][36][37][38]
История
Предпосылки и ранние претензии
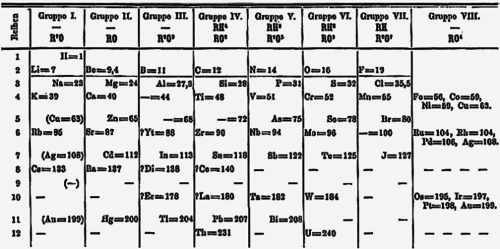
Когда первый периодическая таблица элементов был опубликован Дмитрий Менделеев в начале 1870-х годов на месте урана был отмечен знак «-», как и в некоторых других местах для еще не открытых элементов. Другие последующие таблицы известных элементов, включая публикацию известных радиоактивных изотопов 1913 г. Казимир Фаянс, также показывают пустое место после урана, элемента 92.[39]
До и после открытия последнего компонента атомного ядра нейтрон в 1932 году большинство ученых не рассматривали всерьез возможность элементов тяжелее урана. Хотя ядерная теория в то время явно не запрещала их существование, было мало свидетельств, позволяющих предположить, что они действительно существуют. Однако открытие наведенная радиоактивность к Ирен и Фредерик Жолио-Кюри в конце 1933 г. открыл совершенно новый метод исследования элементов и вдохновил небольшую группу итальянских ученых во главе с Энрико Ферми начать серию экспериментов по нейтронной бомбардировке. Хотя эксперимент Жолио-Кюри включал бомбардировку образца 27Al с альфа-частицы производить радиоактивный 30п Ферми понял, что использование нейтронов, не имеющих электрического заряда, скорее всего, даст даже лучшие результаты, чем положительно заряженные альфа-частицы. Соответственно, в марте 1934 года он начал систематически подвергать все известные в то время элементы бомбардировке нейтронами, чтобы определить, могут ли другие элементы также быть индуцированы радиоактивностью.[40][41]
После нескольких месяцев работы группа Ферми предварительно определила, что более легкие элементы будут рассеивать энергию захваченного нейтрона, испуская протон или же альфа-частица и более тяжелые элементы обычно достигают того же, испуская гамма-луч. Это последнее поведение позже приведет к бета-распад нейтрона в протон, таким образом перемещая полученный изотоп на одно место в периодической таблице. Когда группа Ферми бомбила уран, они также наблюдали это поведение, что убедительно свидетельствовало о том, что полученный изотоп имел атомный номер из 93. Ферми изначально не хотел оглашать такое заявление, но после того, как его команда обнаружила несколько неизвестных периодов полураспада продуктов бомбардировки урана, которые не совпадали с периодами полураспада какого-либо известного изотопа, он опубликовал статью, озаглавленную Возможное образование элементов с атомным номером выше 92 в июне 1934 года. В нем он предложил название аусоний (атомный символ Ao) для элемента 93 после греческого названия Ausonia (Италия).[42]
Вскоре возникло несколько теоретических возражений против утверждений статьи Ферми; в частности, точный процесс, который имел место, когда атом захватил нейтрон в то время не был хорошо понят. Это и случайное открытие Ферми тремя месяцами позже того, что ядерные реакции могут быть вызваны медленными нейтронами, вызывают дальнейшие сомнения в умах многих ученых, особенно Аристид фон Гросс и Ида Ноддак, что эксперимент создавал элемент 93. В то время как утверждение фон Гроссе, что Ферми на самом деле производил протактиний (элемент 91) был быстро протестирован и опровергнут, предложение Ноддака о том, что уран был разбит на два или более гораздо меньших осколка, было просто проигнорировано большинством, потому что существующая ядерная теория не предусматривала способ сделать это возможным. Ферми и его команда утверждали, что они фактически синтезировали новый элемент, но вопрос оставался нерешенным в течение нескольких лет.[43][44][45]

Хотя множество различных и неизвестных периодов полураспада радиоактивных веществ в результатах эксперимента показали, что происходило несколько ядерных реакций, группа Ферми не могла доказать, что элемент 93 создается, если они не могли изолировать его химически. Они и многие другие ученые пытались добиться этого, в том числе Отто Хан и Лиз Мейтнер которые были одними из лучших радиохимиков в мире в то время и сторонниками утверждения Ферми, но все они потерпели неудачу. Намного позже было установлено, что основная причина этой неудачи заключалась в том, что предсказания химических свойств элемента 93 были основаны на периодической таблице, в которой отсутствовали актинидный ряд. Это расположение помещало протактиний ниже тантала, уран ниже вольфрама, а также предполагало, что элемент 93, в этой точке называемый экарением, должен быть похож на группа 7 элементов, в том числе марганец и рений. Торий, протактиний и уран с их преобладающими степенями окисления +4, +5 и +6 соответственно обманули ученых, заставив думать, что они принадлежат ниже гафния, тантала и вольфрама, а не ниже ряда лантанидов, который был в то время рассматривается как случайность, и все члены которой имеют доминирующие +3 состояния; Нептуний, с другой стороны, имеет гораздо более редкое, более нестабильное состояние +7, причем +4 и +5 являются наиболее стабильными. Обнаружив, что плутоний и другие трансурановые элементы также имеют доминирующие состояния +3 и +4, наряду с открытием f-блок, серия актинидов была прочно установлена.[46][47]
Хотя вопрос о том, произвел ли эксперимент Ферми элемент 93, зашел в тупик, появились два дополнительных заявления об открытии этого элемента, хотя, в отличие от Ферми, оба они утверждали, что наблюдали его в природе. Первое заявление было сделано чешским инженером. Одолен Коблич в 1934 году, когда он извлек небольшое количество материала из промывочной воды нагретой уран. Он предложил название богемий для элемента, но после анализа выяснилось, что образец представляет собой смесь вольфрам и ванадий.[48][49][50] Другое утверждение, сделанное в 1938 году румынским физиком Хория Хулубей и французский химик Иветт Кошуа, заявил, что обнаружил новый элемент через спектроскопия в минералах. Они назвали свой элемент секванум, но это утверждение было отклонено, потому что в то время преобладала теория, согласно которой, если бы он вообще существовал, элемент 93 не существовал бы естественным образом. Однако, поскольку нептуний действительно встречается в природе в следовых количествах, как было продемонстрировано, когда он был обнаружен в урановой руде в 1952 году, возможно, что Хулубей и Кошуа действительно наблюдали нептуний.[32][51][52][53]
Хотя к 1938 г. некоторые ученые, в том числе Нильс Бор, все еще неохотно признавали, что Ферми действительно произвел новый элемент, тем не менее он был награжден Нобелевская премия по физике в ноябре 1938 г. "за демонстрацию существования новых радиоактивных элементов, образующихся при нейтронном облучении, и за связанное с ним открытие ядерных реакций, вызываемых медленными нейтронами.". Спустя месяц почти совершенно неожиданное открытие ядерное деление Ханом, Мейтнер и Отто Фриш положить конец возможности того, что Ферми открыл элемент 93, потому что большинство неизвестных периодов полураспада, которые наблюдались командой Ферми, были быстро идентифицированы как периоды полураспада продукты деления.[54][55][56][57][58]
Возможно, самой близкой из всех попыток создать недостающий элемент 93 была попытка японского физика. Ёсио Нишина работа с химиком Кендзиро Кимура в 1940 году, незадолго до начала Тихоокеанская война в 1941: бомбили 238U с быстрыми нейтронами. Однако, в то время как медленные нейтроны имеют тенденцию вызывать захват нейтронов посредством реакции (n, γ), быстрые нейтроны имеют тенденцию вызывать реакцию «выбивания» (n, 2n), когда один нейтрон добавляется, а еще два удаляются, что приводит к чистая потеря нейтрона. Нишина и Кимура, протестировав эту технику на 232Чт и успешно произвел известные 231Th и его долгоживущая дочь бета-распада 231Па (оба происходят в естественной цепочке распада 235U ), поэтому правильно отнесли новый период полураспада 6,75 дня, который они наблюдали, новому изотопу 237У. Они подтвердили, что этот изотоп также был бета-излучателем и, следовательно, должен распадаться до неизвестного нуклида. 23793. Они попытались изолировать этот нуклид, неся его с предполагаемым более легким родственным ему рением, но бета- или альфа-распад ренийсодержащей фракции не наблюдался: таким образом, Нишина и Кимура правильно предположили, что период полураспада 23793, как у 231Pa, был очень длинным, и, следовательно, его активность была бы настолько слабой, что ее невозможно было бы измерить с помощью их оборудования, что завершило последний и самый близкий безуспешный поиск трансурановых элементов.[59]
Открытие

По мере развития исследований ядерного деления в начале 1939 г. Эдвин Макмиллан на Радиационная лаборатория Беркли из Калифорнийский университет в Беркли решил провести эксперимент по бомбардировке ураном мощным 60-дюймовым (1,52 м) циклотрон недавно построенный в университете. Цель состояла в том, чтобы разделить различные продукты деления, произведенные бомбардировкой, используя огромную силу, которую осколки получают от их взаимного электрического отталкивания после деления. Хотя он не обнаружил из этого ничего примечательного, Макмиллан действительно наблюдал два новых периода полураспада бета-распада в самой мишени из триоксида урана, а это означало, что все, что производило радиоактивность, не отталкивало друг друга так сильно, как обычные продукты деления. Он быстро понял, что один из периодов полураспада близко соответствует известному 23-минутному периоду распада урана-239, но другой период полураспада в 2,3 дня неизвестен. Макмиллан рассказал о результатах своего эксперимента химику и коллеге-профессору из Беркли. Эмилио Сегре попытаться изолировать источник радиоактивности. Оба ученых начали свою работу, используя преобладающую теорию о том, что химический элемент 93 должен иметь схожий химический состав с рением, но Сегре быстро определил, что образец Макмиллана совсем не похож на рений. Вместо этого, когда он отреагировал на это фтороводород (ВЧ) с сильным окислитель в настоящее время он вел себя так же, как члены редкие земли. Поскольку эти элементы составляют большой процент продуктов деления, Сегре и Макмиллан решили, что период полураспада, должно быть, был просто еще одним продуктом деления, озаглавив статью «Неудачный поиск трансурановых элементов».[60][61][62]

Однако по мере того, как стало доступно больше информации о делении, возможность того, что осколки ядерного деления все еще могли присутствовать в мишени, стала более маловероятной. Макмиллан и несколько ученых, в том числе Филип Х. Абельсон, снова попытался определить, что дает неизвестный период полураспада. В начале 1940 года Макмиллан понял, что его эксперимент 1939 года с Сегре не смог с достаточной тщательностью проверить химические реакции радиоактивного источника. В новом эксперименте Макмиллан попытался подвергнуть неизвестное вещество воздействию HF в присутствии Восстановитель, чего он раньше не делал. Эта реакция привела к тому, что образец осаждающий с HF, действие, которое окончательно исключило возможность того, что неизвестное вещество было редкоземельным элементом. Вскоре после этого Абельсон, получивший высшее образование из университета, посетил Беркли на короткий отпуск, и Макмиллан попросил более способного химика помочь с разделением результатов эксперимента. Абельсон очень быстро заметил, что все, что производит 2,3-дневный период полураспада, не имеет химического состава, как любой известный элемент, и на самом деле больше похоже на уран, чем на редкоземельный элемент. Это открытие, наконец, позволило изолировать источник, а позже, в 1945 году, привело к классификации актинидный ряд. В качестве последнего шага Макмиллан и Абельсон приготовили гораздо больший образец бомбардируемого урана, у которого был заметный период полураспада 23 минуты от 239U и убедительно продемонстрировали, что неизвестный 2,3-дневный период полувыведения увеличивается в силе вместе с уменьшением 23-минутной активности в результате следующей реакции:[63]
- (Время период полураспада.)
Это доказало, что неизвестный радиоактивный источник возник в результате распада урана, и в сочетании с предыдущим наблюдением о том, что источник химически отличался от всех известных элементов, вне всяких сомнений доказало, что был открыт новый элемент. Макмиллан и Абельсон опубликовали свои результаты в статье под названием Радиоактивный элемент 93 в Физический обзор 27 мая 1940 г.[63] Они не предложили название для элемента в документе, но вскоре они выбрали название. нептуний поскольку Нептун следующая планета за пределами Уран в нашей солнечной системе.[19][64][65][66] Успех Макмиллана и Абельсона по сравнению с промахом Нишины и Кимуры можно отнести к благоприятному периоду полураспада 239Np для радиохимического анализа и быстрого распада 239U, в отличие от более медленного распада 237U и чрезвычайно длительный период полураспада 237Np.[59]
Последующие события

Также было установлено, что бета-распад 239Np должен производить изотоп элемента 94 (теперь называемый плутоний ), но количества, использованные в первоначальном эксперименте Макмиллана и Абельсона, были слишком малы, чтобы изолировать и идентифицировать плутоний вместе с нептунием.[67] Открытие плутония пришлось отложить до конца 1940 г., когда Гленн Т. Сиборг и его команда определила изотоп плутоний-238.[68]
Уникальные радиоактивные характеристики нептуния позволили проследить его прохождение через различные соединения в химических реакциях. Сначала это был единственный доступный метод, чтобы доказать, что его химический состав отличается от других элементов. Поскольку первый обнаруженный изотоп нептуния имеет такой короткий период полураспада, Макмиллан и Абельсон не смогли подготовить образец, который был бы достаточно большим для проведения химического анализа нового элемента с использованием технологии, которая была тогда доступна. Однако после открытия долгоживущих 237Изотоп Np в 1942 г. Гленн Сиборг и Артур Валь создание весовых количеств нептуния стало реальной задачей.[19][69] Его период полураспада был первоначально определен как около 3 миллионов лет (позже пересмотрен на 2,144 миллиона лет), что подтверждает предсказания Нишины и Кимуры об очень долгом периоде полураспада.[59]
Ранние исследования этого элемента были несколько ограничены, потому что большинство ядерных физиков и химиков в Соединенных Штатах в то время были сосредоточены на огромных усилиях по исследованию свойств плутония как части Манхэттенский проект. Исследования этого элемента продолжались как второстепенная часть проекта, и первый объемный образец нептуния был выделен в 1944 году.[19][69][70]
С тех пор большая часть исследований свойств нептуния была сосредоточена на понимании того, как удержать его в составе ядерных отходов. Поскольку в нем есть изотопы с очень длительным периодом полураспада, он вызывает особую озабоченность в контексте проектирования установок для локализации, которые могут прослужить тысячи лет. Он нашел ограниченное применение в качестве радиоактивного индикатора и прекурсора для различных ядерных реакций с целью получения полезных изотопов плутония. Однако большая часть нептуния, который образуется в качестве побочного продукта реакции на атомных электростанциях, считается отходами.[19][69]
Производство
Синтез
Подавляющее большинство нептуния, существующего в настоящее время на Земле, было произведено искусственно в ядерных реакциях. Нептуний-237 является наиболее часто синтезируемым изотопом, так как это единственный изотоп, который можно создать с помощью захват нейтронов а также имеет достаточно длительный период полураспада, чтобы можно было легко изолировать взвешиваемые количества. Таким образом, это наиболее распространенный изотоп, который используется в химических исследованиях элемента.[26]
- Когда 235U атом захватывает нейтрон, он переходит в возбужденное состояние 236U. Около 81% возбужденных 236Ядра U делятся, а остальные распадаются до основного состояния 236U, испуская гамма-излучение. Дальнейший захват нейтронов создает 237U с периодом полураспада 7 дней и быстро распадается до 237Np через бета-распад. Во время бета-распада возбужденные 237U излучает электрон, а атомный слабое взаимодействие преобразует нейтрон к протон, таким образом создавая 237Np.[26]
- 237U также производится через (п, 2n) реакция с 238U. Это происходит только с очень энергичными нейтронами.[26]
- 237Np является продуктом альфа-распад из 241Являюсь, который образуется при нейтронном облучении уран-238.[26]
Более тяжелые изотопы нептуния быстро распадаются, а более легкие изотопы нептуния не могут быть произведены путем захвата нейтронов, поэтому химическое отделение нептуния от охлажденного отработанное ядерное топливо дает почти чистый 237Np.[26] Короткоживущие тяжелые изотопы 238Np и 239Np, полезен как радиоактивные индикаторы, образуются при нейтронном облучении 237Np и 238U соответственно, а более долгоживущие легкие изотопы 235Np и 236Np образуются при облучении 235U с протоны и дейтроны в циклотрон.[26]
Искусственный 237Металл Np обычно выделяется в результате реакции 237NpF3 с жидкостью барий или же литий около 1200 °C и чаще всего извлекается из потраченных стержни ядерного топлива в килограммах как побочный продукт в плутоний производство.[32]
- 2 нпФ3 + 3 Ba → 2 Np + 3 BaF2
По весу выбросы нептуния-237 составляют примерно 5% от выбросов плутония и примерно 0,05% отработанное ядерное топливо разряды.[72] Однако даже эта доля по-прежнему составляет более пятидесяти тонн в год во всем мире.[73]
Методы очистки
Восстановление урана и плутония из отработавшего ядерного топлива для повторного использования является одним из основных процессов ядерный топливный цикл. Поскольку его период полураспада составляет чуть более 2 миллионов лет, альфа-излучатель 237Np - один из основных изотопов второстепенные актиниды отделено от отработавшего ядерного топлива.[74] Для отделения нептуния использовались многие методы разделения, работающие в малых и больших масштабах. Операции по очистке в небольшом масштабе имеют целью получение чистого нептуния в качестве предшественник металлического нептуния и его соединений, а также для выделения и предварительного концентрирования нептуния в пробах для анализа.[74]
Большинство методов, разделяющих ионы нептуния, используют различное химическое поведение различных степеней окисления нептуния (от +3 до +6 или иногда даже +7) в растворе.[74] Среди методов, которые используются или использовались: растворитель добыча (используя различные экстрагенты, обычно многозубый производные β-дикетона, фосфорорганические соединения, и амин соединения), хроматография используя различные ионный обмен или же хелатирующий смолы, соосаждение (возможный матрицы включают LaF3, БиПО4, BaSO4, Fe (ОН)3, и MnO2 ), электроосаждение, и биотехнологический методы.[75] В настоящее время коммерческие перерабатывающие предприятия используют процесс Purex, включающий экстракцию урана и плутония растворителем с трибутилфосфат.[71]
Химия и соединения
Химия раствора

Когда он находится в водном растворе, нептуний может существовать в любом из пяти возможных состояний окисления (от +3 до +7), и каждая из них имеет характерный цвет. Стабильность каждой степени окисления сильно зависит от различных факторов, таких как присутствие окисляющий или же восстановители, pH раствора, наличие координационный комплекс -формирование лиганды, и даже концентрацию нептуния в растворе.[76]
В кислый В растворах нептуний (III) и ионы нептуния (VII) существуют в виде Np3+, Np4+, Нпо+
2, Нпо2+
2, и Нпо+
3. В базовый растворов, они существуют в виде оксидов и гидроксидов Np (OH)3, NpO2, NpO2OH, NpO2(ОЙ)2, и Нпо3−
5. Для характеристики нептуния в основных растворах было проведено не так много работы.[76] Np3+ и Np4+ легко восстанавливаются и окисляются друг в друга, как и Нпо+
2 и Нпо2+
2.[77]
- Нептуний (III)
Np (III) или Np3+ существует в виде гидратированных комплексов в кислых растворах, Np (H
2O)3+
п.[19] Это темно-сине-фиолетовый цвет, аналог его более светлого цвета. конгенер, розовый редкоземельный ион Вечера3+.[19][78] В присутствии кислород, он быстро окисляется до Np (IV), если также не присутствуют сильные восстановители. Тем не менее, это второй по сложности гидролизованный ион нептуния в воде, образуя NpOH2+ ион.[79] Np3+ является преобладающим ионом нептуния в растворах с pH 4–5.[79]
- Нептуний (IV)
Np (IV) или Np4+ бледно-желто-зеленый в кислых растворах,[19] где он существует в виде гидратированных комплексов (Np (H
2O)4+
п). Он довольно нестабилен к гидролизу в кислых водных растворах при pH 1 и выше с образованием NpOH.3+.[79] В базовых решениях Np4+ имеет тенденцию гидролизоваться с образованием нейтрального гидроксида нептуния (IV) (Np (OH)4) и оксид нептуния (IV) (NpO2).[79]
- Нептуний (V)
Np (V) или Нпо+
2 зелено-синий в водном растворе,[19] в котором он ведет себя как сильный Кислота Льюиса.[76] Это стабильный ион[76] и является наиболее распространенной формой нептуния в водных растворах. В отличие от соседних гомологов UO+
2 и PuO+
2, Нпо+
2 не спонтанно непропорционально за исключением очень низкого pH и высокой концентрации:[77]
- 2 Нпо+
2 + 4 часа+ ⇌ Np4+ + Нпо2+
2 + 2 часа2О
Гидролизуется в основных растворах с образованием NpO2ОН и Нпо
2(ОЙ)−
2.[79]
- Нептуний (VI)
Np (VI) или Нпо2+
2, ион нептунила, имеет светло-розовый или красноватый цвет в кислом растворе и желто-зеленый в противном случае.[19] Это сильная кислота Льюиса.[76] и является основным ионом нептуния, встречающимся в растворах с pH 3–4.[79] Хотя он стабилен в кислых растворах, он довольно легко восстанавливается до иона Np (V),[76] и он не так стабилен, как гомологические шестивалентные ионы своих соседей урана и плутония ( уранил и ионы плутонила). Гидролизуется в основных растворах с образованием оксо- и гидроксо-ионов NpO.2ОЙ+, (NpO
2)
2(ОЙ)2+
2, и (NpO
2)
3(ОЙ)+
5.[79]
- Нептуний (VII)
Np (VII) темно-зеленый в сильно базовый решение. Хотя его химическая формула в основном решении часто цитируется как Нпо3−
5, это упрощение, и реальная структура, вероятно, ближе к гидроксо-видам, таким как [NpO
4(ОЙ)
2]3−
.[19][78] Впервые Np (VII) был получен в щелочном растворе в 1967 г.[76] В сильно кислый решения, Np (VII) находится как Нпо+
3; вода быстро снижает его до Np (VI).[76] Продукты его гидролиза не охарактеризованы.[79]
Гидроксиды
Оксиды и гидроксиды нептуния тесно связаны с его ионами. В общем, гидроксиды Np на различных уровнях окисления менее стабильны, чем актиниды до него в периодической таблице, такие как торий и уран, и более стабильный, чем те, что после него, такие как плутоний и америций. Это явление связано с тем, что стабильность иона увеличивается с увеличением отношения атомного номера к радиусу иона. Таким образом, актиниды, расположенные выше в таблице Менделеева, будут легче подвергаться гидролиз.[76][79]
Гидроксид нептуния (III) довольно стабилен в кислых растворах и в среде, в которой отсутствует кислород, но он быстро окисляется до состояния IV в присутствии воздуха. Не растворяется в воде.[69] Гидроксиды Np (IV) существуют в основном в виде электрически нейтрального Np (OH)4 и его умеренная растворимость в воде совсем не зависит от pH раствора. Это предполагает, что другой гидроксид Np (IV), Np (OH)−
5, не имеет значительного присутствия.[79][80]
Поскольку ион Np (V) Нпо+
2 очень стабилен, он может образовывать гидроксид только при высоких уровнях кислотности. При размещении в 0,1M перхлорат натрия раствор, он не вступает в значительную реакцию в течение нескольких месяцев, хотя более высокая молярная концентрация 3,0 M приведет к его реакции с твердым гидроксидом NpO2ОН почти сразу. Гидроксид Np (VI) более реакционноспособен, но все еще достаточно стабилен в кислых растворах. Он образует соединение NpO3· H2O при наличии озон под различными углекислый газ давления. Np (VII) изучен недостаточно, и о нейтральных гидроксидах не сообщалось. Вероятно, он существует в основном как [NpO
4(ОЙ)
2]3−
.[79][81][82][83]
Оксиды
Сообщалось о трех безводных оксидах нептуния, Нпо2, Np2О5, а Np5О8, хотя некоторые исследования[84] заявили, что существуют только первые два из них, предполагая, что претензии Np5О8 на самом деле являются результатом ошибочного анализа Np2О5. Однако, поскольку полный объем реакций, происходящих между нептунием и кислородом, еще не исследован, неясно, какое из этих утверждений является точным. Хотя оксиды нептуния не были произведены с нептунием в настолько высоких степенях окисления, сколько возможно с соседним актинидом ураном, оксиды нептуния более стабильны при более низких степенях окисления. Такое поведение иллюстрируется тем фактом, что NpO2 может быть получен простым сжиганием нептуниевых солей оксикислот на воздухе.[19][85][86][87]
Зеленовато-коричневый NpO2 очень стабилен в большом диапазоне давлений и температур и не претерпевает фазовых переходов при низких температурах. Он действительно показывает фазовый переход от гранецентрированного куба к орторомбическому при около 33-37 ГПа, хотя он возвращается к исходной фазе, когда давление сбрасывается. Он остается стабильным при давлении кислорода до 2,84 МПа и температуре до 400 ° C. Np2О5 имеет черно-коричневый цвет и моноклинический с размером решетки 418 × 658 × 409 пикометров. Он относительно нестабилен и разлагается до NpO.2 и O2 при 420-695 ° С. Хотя Np2О5 изначально был предметом нескольких исследований, в которых утверждалось, что он получен взаимно противоречивыми методами, в конечном итоге он был успешно получен путем нагревания нептуния. перекись до 300-350 ° C в течение 2–3 часов или нагреванием под слоем воды в ампула при 180 ° С.[85][87][88][89]
Нептуний также образует большое количество оксидных соединений с большим разнообразием элементов, хотя оксиды нептуната, образованные с щелочных металлов и щелочноземельные металлы были, безусловно, наиболее изученными. Тройные оксиды нептуния обычно образуются при взаимодействии NpO2 с оксидом другого элемента или осаждением из щелочного раствора. Ли5Нпо6 был подготовлен реакцией Li2O и NpO2 при 400 ° C в течение 16 часов или реагируя на Li2О2 с NpO3 · H2O при 400 ° C в течение 16 часов в кварцевой трубке и пропускании кислорода. Щелочные нептунатные соединения K3Нпо5, CS3Нпо5, и Руб.3Нпо5 все создаются аналогичной реакцией:
- Нпо2 + 3 мес.2 → M3Нпо5 (M = K, Cs, Rb)
Оксидные соединения KNpO4, CsNpO4, и RbNpO4 образуются при реакции Np (VII) ([NpO
4(ОЙ)
2]3−
) с соединением щелочного металла нитрат и озон. Дополнительные соединения были произведены реакцией NpO3 и вода с твердой щелочью и щелочью перекиси при температуре 400–600 ° С в течение 15–30 часов. Некоторые из них включают Ba3(NpO5)2, Ba2Na Нпо6, а Ba2LiNpO6. Кроме того, значительное количество шестигранных оксидов нептуния образуется при взаимодействии твердотельного NpO2 с различными оксидами щелочных или щелочноземельных металлов в среде проточного кислорода. Многие из полученных соединений также имеют эквивалентное соединение, которое заменяет уран нептуний. Некоторые охарактеризованные соединения включают Na2Np2О7, Na4Нпо5, Na6Нпо6, а Na2Нпо4. Их можно получить, нагревая различные комбинации NpO.2 и Na2O до различных температурных порогов и дальнейшее нагревание также вызовет у этих соединений разные аллотропы нептуния. Оксиды нептуната лития Li6Нпо6 и Ли4Нпо5 можно получить с помощью аналогичных реакций NpO2 и Ли2О.[90][91][92][93][94][95][96][97]
Большое количество дополнительных щелочных и щелочных соединений оксида нептуния, таких как Cs4Np5О17 и Cs2Np3О10 были охарактеризованы различными методами производства. Также было обнаружено, что нептуний образует тройные оксиды со многими дополнительными элементами в группы С 3 по 7, хотя эти соединения изучены гораздо хуже.[90][98][99]
Галогениды
Хотя нептуний галогенид соединения не были изучены так хорошо, как его оксиды, довольно большое количество успешно охарактеризовано. Из них нептуний фториды были исследованы наиболее широко, в основном из-за их потенциального использования для отделения элемента от ядерных отходов. Четыре бинарных соединения фторида нептуния, NpF3, NpF4, NpF5, и NpF6, были зарегистрированы. Первые два достаточно стабильны и были впервые получены в 1947 году в результате следующих реакций:
- Нпо2 + 1⁄2 ЧАС2 + 3 ВЧ → NpF3 + 2 часа2О (400 ° С)
- NpF3 + 1⁄2 О2 + HF → NpF4 + 1⁄2 ЧАС2О (400 ° С)
Позже NpF4 был получен непосредственно нагреванием NpO2 до различных температур в смесях фтороводород или чистый газообразный фтор. NpF5 намного сложнее создать, и большинство известных методов приготовления включают реакцию NpF4 или NpF6 соединения с различными другими фторидными соединениями. NpF5 разложится на NpF4 и NpF6 при нагревании примерно до 320 ° C.[100][101][102][103]
NpF6 или же гексафторид нептуния чрезвычайно летуч, как и соседние с ним актинидные соединения гексафторид урана (УФ6) и гексафторид плутония (PuF6). Эта летучесть вызвала большой интерес к этому соединению в попытке разработать простой метод извлечения нептуния из отработавших топливных стержней атомной электростанции. NpF6 был впервые приготовлен в 1943 году путем реакции NpF3 и газообразный фтор при очень высоких температурах, и первые объемные количества были получены в 1958 году путем нагревания NpF4 и закапывая на нее чистый фтор в специально подготовленном аппарате. Дополнительные методы, которые позволили успешно получить гексафторид нептуния, включают реакцию BrF3 и BrF5 с NpF4 и взаимодействием нескольких различных соединений оксида и фторида нептуния с безводными фторидами водорода.[101][104][105][106]
Четыре нептуниума оксифторид соединения, NpO2F, NpOF3, NpO2F2, и NpOF4, были зарегистрированы, хотя ни один из них не был тщательно изучен. Нпо2F2 представляет собой твердое вещество розоватого цвета и может быть получено путем реакции NpO3 · H2O и Np2F5 с чистым фтором при температуре около 330 ° C. NpOF3 и NpOF4 могут быть получены реакцией оксидов нептуния с безводным фтористым водородом при различных температурах. Нептуний также образует большое количество фторидных соединений с различными элементами. Некоторые из них, которые были охарактеризованы, включают CsNpF6, Руб.2NpF7, Na3NpF8, а K3Нпо2F5.[101][103][107][108][109][110][111]
Два нептуниума хлориды, NpCl3 и NpCl4, были охарактеризованы. Хотя несколько попыток создать NpCl5 были сделаны, они не увенчались успехом. NpCl3 создается путем восстановления диоксида нептуния водородом и четыреххлористый углерод (C Cl4) и NpCl4 реакцией оксида нептуния с CCl4 при температуре около 500 ° C. Сообщалось также о других соединениях хлорида нептуния, включая NpOCl.2, Cs2NpCl6, Cs3Нпо2Cl4, а Cs2NaNpCl6. Нептуний бромиды NpBr3 и NpBr4 также были созданы; последний, реагируя бромид алюминия с NpO2 при 350 ° C и первом почти идентичной процедуре, но с цинк настоящее время. Нептуний йодид Npя3 также был приготовлен тем же методом, что и NpBr3.[112][113][114]
Халькогениды, пниктиды и карбиды
Нептуний халькоген и пниктоген соединения были хорошо изучены, прежде всего, в рамках исследований их электронных и магнитных свойств и их взаимодействия в естественной среде. Пниктид и карбид Соединения также вызвали интерес из-за их присутствия в топливе нескольких усовершенствованных конструкций ядерных реакторов, хотя последняя группа не провела почти таких исследований, как первая.[115]
- Халькогениды
Широкое разнообразие нептуний сульфид охарактеризованы соединения, в том числе чистые сульфидные соединения NpS, NpS3, Np2S5, Np3S5, Np2S3, а Np3S4. Из них Np2S3, приготовленный реакцией NpO2 с сероводород и сероуглерод при температуре около 1000 ° C является наиболее хорошо изученной и известны три аллотропные формы. Форма α существует примерно до 1230 ° C, β до 1530 ° C, а форма γ, которая также может существовать как Np3S4, при более высоких температурах. NpS можно создать, реагируя на Np2S3 и металлический нептуний при 1600 ° C и Np3S5 может быть получен разложением Np2S3 при 500 ° C или взаимодействием серы и гидрида нептуния при 650 ° C. Np2S5 производится нагреванием смеси Np3S5 и чистая сера до 500 ° С.Все сульфиды нептуния, кроме β- и γ-форм Np2S3 находятся изоструктурный с эквивалентным сульфидом урана и несколькими, включая NpS, α − Np2S3, а β − Np2S3 также изоструктурны эквивалентному сульфиду плутония. Оксисульфиды NpOS, Np4О4S и Np2О2S также были созданы, хотя последние три изучены недостаточно. NpOS был впервые приготовлен в 1985 году путем вакуумной герметизации NpO.2, Np3S5, и чистую серу в кварцевой трубке и нагревают до 900 ° C в течение одной недели.[115][116][117][118][119][120][121]
Нептуний селенид соединения, о которых сообщалось, включают NpSe, NpSe3, Np2Se3, Np2Se5, Np3Se4, а Np3Se5. Все они были получены только путем нагревания гидрида нептуния и металлического селена до различных температур в вакууме в течение длительного периода времени и Np2Se3 известно только о существовании в γ-аллотропе при относительно высоких температурах. Два нептуниума оксиселенид соединения известны, NpOSe и Np2О2Se, образуются аналогичными методами путем замены гидрида нептуния диоксидом нептуния. Известный нептуний теллурид соединения NpTe, NpTe3, Np3Te4, Np2Te3, а Np2О2Те образуются аналогичными процедурами для селенидов и Np2О2Te изоструктурен эквивалентным соединениям урана и плутония. Нет нептуния -полоний о соединениях не сообщалось.[115][121][122][123][124]
- Пниктиды и карбиды
Нептуний нитрид (NpN ) был впервые получен в 1953 году путем взаимодействия гидрида нептуния и аммиак газ при температуре около 750 ° C в кварцевой капиллярной трубке. Позже он был получен путем взаимодействия различных смесей азота и водорода с металлическим нептунием при различных температурах. Он также был создан восстановлением диоксида нептуния с двухатомный газообразный азот при 1550 ° C. NpN - это изоморфный с мононитрид урана (ООН) и мононитрид плутония (PuN) и имеет температуру плавления 2830 ° C при давлении азота около 1 МПа. Два нептуниума фосфид соединений, Npп и Np3п4. Первый имеет гранецентрированную кубическую структуру и готовится преобразованием металлического нептуния в порошок с последующим его взаимодействием с фосфин газ при 350 ° C. Np3п4 могут быть созданы путем реакции металлического нептуния с красный фосфор при 740 ° C в вакууме, а затем позволяя лишнему фосфору сублимировать прочь. Соединение не реагирует с водой, но будет реагировать с азотная кислота для получения раствора Np (IV).[125][126][127]
Три нептуниума арсенид соединений, NpВ качестве, NpAs2, а Np3В качестве4. Первые два были впервые созданы путем нагревания мышьяка и гидрида нептуния в герметичной трубке в течение примерно недели. Позже, NpAs также был получен путем заключения металлического нептуния и мышьяка в вакуумную трубку, разделения их кварцевой мембраной и нагревания их до температуры чуть ниже температуры плавления нептуния 639 ° C, что немного выше, чем температура сублимации мышьяка 615 ° C. С. Np3В качестве4 готовится аналогичным способом с использованием йода в качестве транспортный агент. NpAs2 кристаллы коричневато-золотые и Np3В качестве4 черный. Нептуний антимонид соединение NpSb был создан в 1971 году путем помещения равных количеств обоих элементов в вакуумную трубку, нагревания их до температуры плавления сурьмы и последующего нагрева до 1000 ° C в течение шестнадцати дней. Эта процедура также создала следовые количества дополнительного соединения антимонида Np.3Sb4. Один нептуний-висмут также сообщалось о соединении NpBi.[125][126][128][129][130][131]
Нептуний карбиды NpC, Np2C3, и NpC2 (предварительно) сообщалось, но не было дано подробное описание, несмотря на высокую важность и полезность карбидов актинидов в качестве топлива для современных ядерных реакторов. NpC - это нестехиометрическое соединение, и его лучше обозначить как NpCИкс (0.82 ≤ Икс ≤ 0,96). Его можно получить реакцией гидрида нептуния с графит при 1400 ° C или путем нагревания составляющих элементов вместе в электродуговая печь используя вольфрам электрод. Он реагирует с избытком углерода с образованием чистого Np.2C3. NpC2 образуется при нагревании NpO2 в графитовом тигле при 2660–2800 ° С.[125][126][132][133]
Прочие неорганические
- Гидриды
Нептуний реагирует с водород аналогично своему соседнему плутонию, образуя гидриды NpH2+Икс (гранецентрированная кубическая ) и NpH3 (шестиугольник ). Это изоструктурный с соответствующими гидридами плутония, хотя в отличие от PuH2+Икс, то параметры решетки NpH2+Икс тем больше, чем больше содержание водорода (Икс) увеличивается. Гидриды требуют особой осторожности при обращении, поскольку они разлагаются в вакууме при 300 ° C с образованием тонкодисперсного металлического нептуния, который является пирофорный.[134]
- Фосфаты, сульфаты и карбонаты
Будучи химически стабильным, нептуний фосфаты были исследованы на предмет потенциального использования при иммобилизации ядерных отходов. Пирофосфат нептуния (α-NpP2О7), зеленое твердое вещество, образовалось в реакции между диоксидом нептуния и фосфат бора при 1100 ° C, хотя фосфат нептуния (IV) до сих пор остается неуловимым. Серия соединений NpM2(PO4)3, где M - щелочной металл (Ли, Na, K, Руб., или же CS ), все известны. Некоторый нептуний сульфаты были охарактеризованы как водные, так и твердые и при различных степенях окисления нептуния (наблюдались с IV по VI). Дополнительно нептуний карбонаты были исследованы, чтобы лучше понять поведение нептуния в геологические хранилища и окружающая среда, где он может контактировать с карбонатами и бикарбонат водные растворы и образуют растворимые комплексы.[135][136]
Металлорганический

Некоторые органические соединения птуния известны и химически охарактеризованы, хотя и не так много, как уран из-за дефицита и радиоактивности нептуния. Наиболее известными органическими соединениями птуния являются циклопентадиенил и циклооктатетраенил соединения и их производные.[137] Трехвалентное циклопентадиенильное соединение Np (C5ЧАС5)3·THF был получен в 1972 г. в результате реакции Np (C5ЧАС5)3Cl с натрий, хотя более простой Np (C5ЧАС5) получить не удалось.[137] Тетравалентный циклопентадиенил нептуния, красновато-коричневый комплекс, был синтезирован в 1968 году путем взаимодействия хлорида нептуния (IV) с циклопентадиенидом калия:[137]
- NpCl4 + 4 KC5ЧАС5 → Np (C5ЧАС5)4 + 4 KCl
Растворим в бензол и THF, и менее чувствителен к кислород и вода, чем Пу (C5ЧАС5)3 и Являюсь (C5ЧАС5)3.[137] Другие циклопентадиенильные соединения Np (IV) известны многим лиганды: они имеют общую формулу (C5ЧАС5)3NpL, где L представляет собой лиганд.[137]Нептуноцен, Np (C8ЧАС8)2, был синтезирован в 1970 году реакцией хлорида нептуния (IV) с K2(C8ЧАС8). это изоморфный к ураноцен и плутоноцен, и они ведут себя химически идентично: все три соединения нечувствительны к воде или разбавленным основаниям, но чувствительны к воздуху, быстро реагируют с образованием оксидов и лишь слабо растворимы в бензоле и толуол.[137] Другие известные циклооктатетраенильные производные нептуния включают Np (RC8ЧАС7)2 (R = этиловый спирт, бутанол ) и KNp (C8ЧАС8) · 2ТГФ, изоструктурный соответствующему соединению плутония.[137] Кроме того, нептуний гидрокарбилы были получены, и сольватированные трииодидные комплексы нептуния являются предшественниками многих нептунийорганических и неорганических соединений нептуния.[137]
Координационные комплексы
Большой интерес вызывает координационная химия нептуния, потому что все его пять степеней окисления демонстрируют свое собственное химическое поведение, а координационная химия актинидов находится под сильным влиянием сокращение актинидов (большее, чем ожидалось, снижение ионные радиусы по ряду актинидов, аналогично сокращение лантаноидов ).[138]
Твердое состояние
Известно мало координационных соединений нептуния (III), поскольку Np (III) легко окисляется кислородом воздуха, находясь в водном растворе. Тем не мение, формальдегид сульфоксилат натрия может восстанавливать Np (IV) до Np (III), стабилизируя более низкую степень окисления и образуя различные труднорастворимые координационные комплексы Np (III), такие как Np
2(C
2О
4)
3· 11H2О, Np
2(C
6ЧАС
5AsO
3)
3·ЧАС2O и Np
2[C
6ЧАС
4(OH) COO]
3.[138]
Сообщалось о многих координационных соединениях нептуния (IV), первым из которых является (Et
4N) Np (NCS)
8, который изоструктурен аналогичному координационному соединению урана (IV).[138] Известны и другие координационные соединения Np (IV), некоторые из которых включают другие металлы, такие как кобальт (CoNp
2F
10· 8H2O, образовавшийся при 400 К) и медь (CuNp
2F
10· 6H2O, сформированный при 600 К).[138] Известны также сложные нитратные соединения: экспериментаторы, которые получили их в 1986 и 1987 годах, получили монокристаллы путем медленного испарения раствора Np (IV) при температуре окружающей среды в концентрированной среде. азотная кислота и избыток 2,2′-пиримидин.[138]
Координационная химия нептуния (V) широко исследовалась из-за присутствия катион-катионное взаимодействие в твердом состоянии, что уже было известно актинил ионы.[138] Некоторые известные такие соединения включают нептунил димер Na
4(NpO
4)
2C
12О
12· 8H2О и гликолят нептуния, оба из которых образуют зеленые кристаллы.[138]
Соединения нептуния (VI) варьируются от простого оксалата Нпо
2C
2О
4 (который нестабилен, обычно превращается в Np (IV)) к таким сложным соединениям, как зеленый (NH
4)
4Нпо
2(CO
3)
3.[138] Были проведены обширные исследования соединений формы M
4AnO
2(CO
3)
3, где M представляет собой одновалентный катион, а An представляет собой уран, нептуний или плутоний.[138]
С 1967 г., когда был открыт нептуний (VII), были получены и исследованы некоторые координационные соединения с нептунием в степени окисления +7. Первое сообщение о таком соединении первоначально было охарактеризовано как Co (NH
3)
6Нпо
5·пЧАС2O в 1968 году, но в 1973 году было предложено иметь формулу [Co (NH
3)
6] [NpO
4(ОЙ)
2]· 2H2O на основании того, что Np (VII) имеет вид [NpO
4(ОЙ)
2]3−
в водном растворе.[138] Это соединение образует темно-зеленые призматические кристаллы с максимальной длиной ребра 0,15–0,4.мм.[138]
В водном растворе
Самый нептуний координационные комплексы Известно, что в растворах присутствуют элементы в степенях окисления +4, +5 и +6: лишь несколько исследований были проведены по координационным комплексам нептуния (III) и (VII).[139] Для первых NpX2+ и NpX+
2 (X = Cl, Br ) были получены в 1966 г. LiCl и LiBr решений соответственно: для последнего эксперименты 1970 г. обнаружили, что Нпо3+
2 ион мог образовывать сульфат комплексы в кислых растворах, таких как Нпо
2ТАК+
4 и Нпо
2(ТАК
4)−
2; у них было обнаружено более высокое константы устойчивости чем нептунил-ион (Нпо2+
2).[139] Известно очень много комплексов для других состояний окисления нептуния: участвующие неорганические лиганды представляют собой галогениды, йодат, азид, нитрид, нитрат, тиоцианат, сульфат, карбонат, хромат, и фосфат. Известно, что многие органические лиганды могут использоваться в координационных комплексах нептуния: они включают ацетат, пропионат, гликолят, лактат, оксалат, малонатный, фталат, мелодировать, и цитрат.[139]
Аналогично своим соседям, урану и плутонию, порядок ионов нептуния с точки зрения способности к комплексообразованию равен Np4+ > Нпо2+
2 ≥ Np3+ > Нпо+
2. (Относительный порядок двух средних ионов нептуния зависит от лиганды и использованные растворители.)[139] Последовательность стабильности для комплексов Np (IV), Np (V) и Np (VI) с одновалентными неорганическими лигандами: F− > ЧАС
2PO−
4 > SCN− > НЕТ−
3 > Cl− > ClO−
4; порядок двухвалентных неорганических лигандов CO2−
3 > HPO2−
4 > ТАК2−
4. Они соответствуют сильным сторонам соответствующих кислоты. Двухвалентные лиганды образуют более сложные комплексы, чем одновалентные.[139] Нпо+
2 может также образовывать комплексные ионы [Нпо+
2M3+
] (M = Al, Ga, Sc, В, Fe, Cr, Rh ) в хлорная кислота Решение: сила взаимодействия между двумя катионами соответствует порядку Fe> In> Sc> Ga> Al.[139] Ионы нептунила и уранила также могут вместе образовывать комплекс.[139]
Приложения
Прекурсор в производстве плутония
Важное использование 237Np используется в качестве прекурсора при производстве плутония, где его облучают нейтронами для создания 238Пу, альфа-излучатель за радиоизотопные термогенераторы для космических кораблей и военного назначения. 237Np захватит нейтрон с образованием 238Np и бета-распад с периодом полураспада чуть более двух дней до 238Пу.[140]
238Pu также присутствует в значительных количествах в отработанное ядерное топливо но должно быть отделено от других изотопы плутония.[141] Облучение нептуния-237 электронными пучками, провоцирующих тормозное излучение, также производит довольно чистые образцы изотопа плутоний-236, полезен как индикатор для определения концентрации плутония в окружающей среде.[141]
Оружие
Нептуний - это расщепляющийся, и теоретически может использоваться в качестве топлива в реактор на быстрых нейтронах или ядерное оружие, с критическая масса около 60 кг.[73] В 1992 г. Министерство энергетики США рассекретили заявление о том, что нептуний-237 «может быть использован для создания ядерного взрывного устройства».[142] Не предполагается, что настоящее оружие когда-либо было построено с использованием нептуния. По состоянию на 2009 год мировое производство нептуния-237 в промышленных энергетических реакторах превышало 1000 критических масс в год, но извлечение изотопа из облученных топливных элементов было бы крупным промышленным предприятием.[143]
В сентябре 2002 г. исследователи Лос-Аламосская национальная лаборатория кратко создал первую известную ядерную критическая масса используя нептуний в сочетании с раковинами обогащенный уран (уран-235 ), обнаружив, что критическая масса голой сферы из нептуния-237 «колеблется от килограммов в диапазоне от пятидесяти до шестидесятых»,[1] показывая, что это «примерно такой же хороший материал для бомбы, как [уран-235]».[29] Федеральное правительство Соединенных Штатов в марте 2004 г. разработало планы по перемещению запасов выделенного нептуния из Америки на полигон для захоронения ядерных отходов в г. Невада.[143]
Физика
237Np используется в устройствах для регистрации нейтронов высоких энергий (МэВ).[144]
Роль в ядерных отходах
Нептуний накапливается в коммерческой бытовой ионизационной камере детекторы дыма от распада (обычно) 0,2 микрограмм америция-241, изначально присутствовавшего в качестве источника ионизирующего излучения. С периодом полураспада 432 года америций-241 в ионизационный детектор дыма включает около 3% нептуния через 20 лет и около 15% через 100 лет.
Нептуний-237 - самый мобильный актинид в глубокое геологическое хранилище среда.[145] Это делает его и его предшественников, таких как америций-241 кандидатов на уничтожение ядерная трансмутация.[146] Из-за своего длительного периода полураспада нептуний станет основным источником общего радиотоксичность через 10000 лет. Поскольку неясно, что происходит с защитной оболочкой в течение этого длительного периода времени, извлечение нептуния свело бы к минимуму загрязнение окружающей среды, если бы ядерные отходы могли быть перемещены через несколько тысяч лет.[143][147]
Биологическая роль и меры предосторожности
Нептуний не играет биологической роли, так как имеет короткий период полураспада и в естественных условиях встречается только в небольших количествах. Тесты на животных показали, что он не всасывается через пищеварительный тракт. При введении он концентрируется в костях, из которых медленно высвобождается.[32]
Мелкодисперсный металлический нептуний представляет опасность пожара, поскольку нептуний пирофорный; мелкие зерна самовозгораются на воздухе при комнатной температуре.[85]
Рекомендации
- ^ а б Санчес, Рене Дж .; Loaiza, Дэвид Дж .; Kimpland, Роберт H .; Hayes, Дэвид К .; Cappiello, Charlene C .; Майерс, Уильям Л .; Jaegers, Питер Дж .; Клемент, Стивен Д .; Баттерфилд, Кеннет Б. "Критичность 237Np Sphere " (PDF). Японское агентство по атомной энергии. Получено 2014-08-06.
- ^ Np (II), (III) и (IV) наблюдались, см. Дуткевич, Михал С .; Апостолидис, Христос; Уолтер, Олаф; Арнольд, Полли Л. (2017). «Восстановительная химия циклопентадиенидных комплексов нептуния: от структуры к пониманию». Chem. Наука. 8 (4): 2553–2561. Дои:10.1039 / C7SC00034K. ЧВК 5431675. PMID 28553487.
- ^ Магнитная восприимчивость элементов и неорганических соединений, в Справочнике по химии и физике, 81-е издание, CRC press.
- ^ Макмиллан, Эдвин; Абельсон, Филип Хауге (1940-06-15). «Радиоактивный элемент 93». Физический обзор. 57 (12): 1185–1186. Bibcode:1940ПхРв ... 57.1185М. Дои:10.1103 / PhysRev.57.1185.2.
- ^ а б c К. Р. Хаммонд (2004). Элементы, в Справочнике химии и физики (81-е изд.). CRC Press. ISBN 978-0-8493-0485-9.
- ^ а б c d е Йошида и др., Стр. 718.
- ^ Dabos, S .; Dufour, C .; Benedict, U .; Пажес, М. (1987). «Объемный модуль и зависимость P – V до 52 ГПа металлического нептуния при комнатной температуре». Журнал магнетизма и магнитных материалов. 63–64: 661–3. Bibcode:1987JMMM ... 63..661D. Дои:10.1016/0304-8853(87)90697-4.
- ^ а б Ю. Д. Третьяков, изд. (2007). Неорганическая химия в трех томах. Химия переходных элементов. 3. Москва: Академия. ISBN 978-5-7695-2533-9.
- ^ а б Теодор Грей. Элементы. Стр. 215.
- ^ Lee, J .; Mardon, P .; Pearce, J .; Холл, Р. (1959). «Некоторые физические свойства металлического нептуния II: исследование аллотропных превращений в нептунии». Журнал физики и химии твердого тела. 11 (3–4): 177–181. Bibcode:1959JPCS ... 11..177L. Дои:10.1016/0022-3697(59)90211-2.
- ^ а б Лемир, Р. Дж. И др.,Химическая термодинамика нептуния и плутония., Эльзевир, Амстердам, 2001.
- ^ «Структуры кристаллической решетки: структура αNp (Ac)». Лаборатория военно-морских исследований США Центр вычислительного материаловедения. Архивировано из оригинал на 2012-10-02. Получено 2013-10-16.
- ^ а б c d Йошида и др., Стр. 719.
- ^ Хиндман Дж. К. 1968, «Нептуниум», в К. А. Хэмпеле (ред.), Энциклопедия химических элементов, Рейнхольд, Нью-Йорк, стр. 434.
- ^ Dunlap, B.D .; Бродский, М.Б .; Шеной, Г. К .; Кальвиус, Г. М. (1970). «Сверхтонкие взаимодействия и анизотропные колебания решетки 237Np в металле α-Np ». Физический обзор B. 1 (1): 44–46. Bibcode:1970ПхРвБ ... 1 ... 44Д. Дои:10.1103 / PhysRevB.1.44.
- ^ а б c «Оценка данных по безопасности ядерной критичности и пределов для актинидов на транспорте» (PDF). Institut de Radioprotection et de Sûreté Nucléaire. п. 15. Получено 2010-12-20.
- ^ Стивенс, Д. Р. (1966). «Фазовая диаграмма и сжимаемость нептуния». Журнал физики. 27 (8): 1201–4. Bibcode:1966JPCS ... 27.1201S. Дои:10.1016/0022-3697(66)90002-3.
- ^ а б c Йошида и др., Стр. 719–20.
- ^ а б c d е ж грамм час я j k л м "Периодическая таблица элементов: LANL - Нептуний". Лос-Аламосская национальная лаборатория. Получено 2013-10-13.
- ^ Т. Д. Мацуда; Ю. Хагал; Д. Аоки; Х. Сакаи; Y. Homma; Н. Татейва; Э. Ямамото; Ю. Онуки (2009). «Транспортные свойства нептуниевого сверхпроводника NpPd.5Al2". Journal of Physics: Серия конференций. 150 (4): 042119. Bibcode:2009JPhCS.150d2119M. Дои:10.1088/1742-6596/150/4/042119.
- ^ а б Михайлов В.А. / Под ред. (1971). Аналитическая химия нептуния. Москва: Наука.
- ^ Голуб, А. М. (1971). Общая и неорганическая химия (Общая и неорганическая химия). 2. С. 222–7.
- ^ Martin, W. C .; Хэган, Люси; Читатель, Джозеф; Суган, Джек (1974). «Уровни земли и потенциал ионизации для атомов и ионов лантанидов и актинидов» (PDF). J. Phys. Chem. Ref. Данные. 3 (3): 771–9. Bibcode:1974JPCRD ... 3..771M. Дои:10.1063/1.3253147. Получено 2013-10-19.
- ^ Дэвид Р. Лид (редактор), CRC Справочник по химии и физике, 84-е издание. CRC Press. Бока-Ратон, Флорида, 2003 год; Секция 10 «Атомная, молекулярная и оптическая физика»; Ионизационные потенциалы атомов и атомных ионов.
- ^ а б c d Nucleonica (2007–2013). «Универсальная карта нуклидов». Nucleonica: веб-ядерная наука. Получено 2013-10-15. (требуется регистрация).
- ^ а б c d е ж грамм час Йошида и др., Стр. 700–2.
- ^ К. М. Ледерер; Дж. М. Холландер; И. Перлман (1968). Таблица изотопов (6-е изд.). Нью-Йорк: Джон Уайли и сыновья.
- ^ Кох, Лотар (2000). «Трансурановые элементы». Трансурановые элементы в Энциклопедии промышленной химии Ульмана. Вайли. Дои:10.1002 / 14356007.a27_167. ISBN 978-3527306732.
- ^ а б c Вайс, Питер (2 июля 2009 г.). «Neptunium nukes? Малоизученный металл становится критическим». Новости науки. 162 (17): 259. Дои:10.2307/4014034. JSTOR 4014034.
- ^ Юкка Лехто; Сяолинь Хоу (2011). «15.15: Нептуний». Химия и анализ радионуклидов (1-е изд.). Джон Уайли и сыновья. 231. ISBN 978-3527633029.
- ^ а б c d е ж Йошида и др., Стр. 703–4.
- ^ а б c d Эмсли, стр. 345–347.
- ^ а б c d Томпсон, Рой С. (1982). «Нептуний: забытый актинид: обзор биологической и экологической литературы». Радиационные исследования. 90 (1): 1–32. Bibcode:1982РадР ... 90 .... 1Т. Дои:10.2307/3575792. JSTOR 3575792. PMID 7038752.
- ^ Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (2003), "ТогдаUBASE оценка ядерных и распадных свойств », Ядерная физика A, 729: 3–128, Bibcode:2003НуФА.729 .... 3А, Дои:10.1016 / j.nuclphysa.2003.11.001
- ^ Фостер, Р. Ф. (1963). Поведение хрома и нептуния в окружающей среде в Радиоэкология. Нью-Йорк: Рейнхольд. С. 569–576.
- ^ а б Этвуд, раздел 4.
- ^ Этвуд, раздел 1.
- ^ "Информационный бюллетень о здоровье человека - Нептуниум" (PDF). Общество физиков здоровья. 2001 г.. Получено 2013-10-15.
- ^ Фаяс, Казимир (1913). "Die radioaktiven Umwandlungen und das periodische System der Elemente (Радиоактивные превращения и Периодическая таблица элементов)". Berichte der Deutschen Chemischen Gesellschaft (отчеты Немецкого химического общества). 46: 422–439. Дои:10.1002 / cber.19130460162.
- ^ Родс, стр. 201–202.
- ^ Родс, стр. 209–210.
- ^ Ферми, Э. (1934). «Возможное образование элементов с атомным номером выше 92». Природа. 133 (3372): 898–899. Bibcode:1934Натура.133..898F. Дои:10.1038 / 133898a0.
- ^ Хоффман, стр. 120–123.
- ^ Ида Ноддак (1934). "Убер дас Элемент 93". Zeitschrift für Angewandte Chemie. 47 (37): 653–655. Дои:10.1002 / ange.19340473707.
- ^ Родс, стр. 210–220.
- ^ Родс, стр. 221–222.
- ^ Родос, стр. 349.
- ^ Коблич, Одолен (1934). «Новый радиоактивный элемент помимо урана». Природа. 134 (3376): 55. Bibcode:1934Натура.134Р..55.. Дои:10.1038 / 134055b0.
- ^ Хоффман, стр. 118.
- ^ Спетер, М. (1934). «Богемий - некролог». Наука. 80 (2086): 588–9. Bibcode:1934Sci .... 80..588S. Дои:10.1126 / science.80.2086.588-а. PMID 17798409.
- ^ Фонтани, Марко (2005). «Сумерки естественных элементов: Молдавий (Ml), Sequanium (Sq) и Дор (Do)». Международная конференция по истории химии. Лиссабон. С. 1–8. Архивировано из оригинал на 2006-02-24. Получено 2013-10-13.
- ^ Hulubei, H .; Кошуа, Ю. (1939). "Nouvelles recherches sur l'élément 93 naturel". Comptes Rendus. 209: 476–479.
- ^ Пеппард, Д. Ф .; Mason, G.W .; Gray, P.R .; Мех, Дж. Ф. (1952). «Возникновение серии (4n + 1) в природе». Журнал Американского химического общества. 74 (23): 6081–6084. Дои:10.1021 / ja01143a074.
- ^ Родс, стр. 264–267.
- ^ Родос, стр. 346.
- ^ "Нобелевская премия по физике 1938 г.". Нобелевский фонд. Получено 2013-10-13.
- ^ Мейтнер, Лиза; Фриш, О. Р. (1939). «Распад урана нейтронами: новый тип ядерной реакции». Природа. 143 (3615): 239–240. Bibcode:1939Натура.143..239М. Дои:10.1038 / 143239a0. S2CID 4113262.
- ^ Отто Хан (1958). «Открытие деления». Scientific American. Архивировано из оригинал 24 декабря 2010 г.
- ^ а б c Икеда, Нагао (25 июля 2011 г.). «Открытия урана-237 и симметричного деления - Из архивных документов Нишины и Кимуры». Труды Японской академии, серия B: Физические и биологические науки. 87 (7): 371–6. Bibcode:2011PJAB ... 87..371I. Дои:10.2183 / pjab.87.371. ЧВК 3171289. PMID 21785255.
- ^ Сегре, Эмилио (1939). «Неудачный поиск трансурановых элементов». Физический обзор. 55 (11): 1104–5. Bibcode:1939ПхРв ... 55.1104С. Дои:10.1103 / PhysRev.55.1104.
- ^ Родс, стр. 346–350.
- ^ Йошида и др., Стр. 699–700.
- ^ а б Макмиллан, Эдвин; Абельсон, Филипп (1940). «Радиоактивный элемент 93». Физический обзор. 57 (12): 1185–1186. Bibcode:1940ПхРв ... 57.1185М. Дои:10.1103 / PhysRev.57.1185.2.
- ^ Сиборг, Г. Т. (1994). «Гл. 118. Происхождение концепции актинидов». В K. A. Gschneidner, Jr .; L, Айринг; Г. Р. Чоппин; Г. Х. Ланде (ред.). Справочник по физике и химии редких земель. 18 - Лантаноиды / Актиниды: Химия. Эльзевир. С. 4–6, 10–14.
- ^ Родос, стр. 348–350.
- ^ Йошида и др., Стр. 700.
- ^ Кларк, Дэвид Л .; Hecker, Siegfried S .; Ярвинен, Гордон Д .; Neu, Мэри П. (2006). «Нептуниум». In Morss, Lester R .; Эдельштейн, Норман М .; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (PDF). 3 (3-е изд.). Дордрехт, Нидерланды: Springer. п. 814. Дои:10.1007/1-4020-3598-5_7. ISBN 978-1-4020-3555-5.
- ^ Гленн Т. Сиборг (сентябрь 1981 г.). "Плутониевая история". Лаборатория Лоуренса Беркли, Калифорнийский университет.LBL-13492, DE82 004551. Цитировать журнал требует
| журнал =(помощь) - ^ а б c d Берни, Г. А; Харбор, Р. М; Подкомитет по радиохимии, Национальный исследовательский совет (США); Центр технической информации, Комиссия по атомной энергии США (1974). Радиохимия нептуния.
- ^ Нильссон, Карен (1989). Миграционная химия нептуния. ISBN 978-87-550-1535-7.
- ^ а б Йошида и др., Стр. 710.
- ^ «Разделенные Нептуний 237 и Америций» (PDF). Получено 2009-06-06.
- ^ а б «Новости химии, исследования и мнения».
- ^ а б c Йодшида и др., Стр. 704–5.
- ^ Йошида и др., Стр. 705–17.
- ^ а б c d е ж грамм час я Йошида и др., Стр. 752–4.
- ^ а б Йошида и др., Стр. 759.
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. п. 1265. ISBN 978-0-08-037941-8.
- ^ а б c d е ж грамм час я j k Йошида и др., Стр. 766–70.
- ^ Трюгве Эриксен; Пьер Ндаламба; Дацин Цуй; Хорди Бруно; и другие. (1993). «Растворимость редокс-чувствительных радионуклидов 99Tc и 237Np в восстановительных условиях от нейтральных до щелочных растворов » (PDF). Технический отчет SKB. 93-18: 1–32.
- ^ Шея, V .; Kim, J. I .; Канеллакопулос Б. (1992). «Растворимость и гидролизное поведение нептуния (V)». Радиохим. Acta. 56: 25–30. Дои:10.1524 / ract.1992.56.1.25. S2CID 99239460.
- ^ Kato, Y .; Kimura, T .; Yoshida, Z .; Нитани, Н. (1996). "Фазовое равновесие твердое тело-жидкость Np (VI) и U (VI) под контролируемым CO2 Частичное давление ». Радиохим. Acta. 74: 21–25. Дои:10.1524 / ract.1996.74.special-issue.21. S2CID 100097624.
- ^ Никонов, М. В .; Бессонов, А. А .; Krot, N. N .; Перминов, В. П. (1994). «Синтез и характеристика соединения смешанной валентности Np (VI, VII)». Радиохимия. 36: 237–8.
- ^ Fahey, J. A .; Turcotte, R.P .; Чикалла Т. Д. (1976). «Состав, стехиометрия и структура оксидов нептуния». Журнал неорганической и ядерной химии. 38 (3): 495–500. Дои:10.1016/0022-1902(76)80291-6.
- ^ а б c Йошида и др., 724–726.
- ^ Шарма, Б. К. Ядерная и радиационная химия - трансурановые элементы. Кришна Пракашан СМИ. С. 128–9. ISBN 9788185842639.
- ^ а б Рихтер К .; Сари К. (1987). «Фазовые соотношения в системе нептуний-кислород». Журнал ядерных материалов. 148 (3): 266–71. Bibcode:1987JNuM..148..266R. Дои:10.1016/0022-3115(87)90019-5.
- ^ Benedict, U .; Dabos, S .; Dufour, C .; Спирелет, Дж. К. (1986). «Соединения нептуния под высоким давлением». Журнал менее распространенных металлов. 121: 461–68. Дои:10.1016/0022-5088(86)90563-1.
- ^ Фэи, Дж. А. (1986). «Нептуниум». В Katz, J. J .; Сиборг, Г. Т .; Морсс, Л. Р. (ред.). Химия элементов актинидов. 1. Нью-Йорк: Чепмен и Холл. п. 456.
- ^ а б Йошида и др., Стр. 728–730.
- ^ Keller, C .; Kock, L .; Уолтер, К. Х. (1965). «Die reaktion der oxid der transurane mit alkalioxiden — I: Ternäre oxid der sechswertigen transurane mit lithium und natrium». Журнал неорганической и ядерной химии. 27 (6): 1205–23. Дои:10.1016/0022-1902(65)80083-5.
- ^ Carnall, W. T .; Neufeldt, S.J .; Уокер, А. (1965). «Реакции в растворах расплавленных солей. I. Образование уранатов и нептунатов в расплавленном нитрате лития-нитрате натрия». Неорганическая химия. 4 (12): 1808–13. Дои:10.1021 / ic50034a034.
- ^ Morss, L.R .; Appelman, E.H .; Gerz, R. R .; Мартин-Ровет, Д. (1994). «Структурные исследования Ли5ReO6, Ли4Нпо5 и Ли5Нпо6 методом нейтронной и порошковой дифракции рентгеновских лучей ». Журнал сплавов и соединений. 203: 289–95. Дои:10.1016 / 0925-8388 (94) 90748-х.
- ^ Keller, C .; Зайфферт, Х. (1969). "Ли5Нпо6, die erste kristalline verbindung mit siebenwertigem neptunium; zur frage der existenz von siebenwertigem plutonium und americium ". Письма по неорганической и ядерной химии. 5: 51–7. Дои:10.1016/0020-1650(69)80236-9.
- ^ Awasthi, S.K .; Martinot, L .; Fuger, J .; Duyckaerts, Г. (1971). «Получение и характеристика некоторых соединений Np (VII)». Письма по неорганической и ядерной химии. 7 (2): 145–51. Дои:10.1016/0020-1650(71)80143-5.
- ^ Pagès, M .; Nectoux, F .; Фрейндлих, В. (1971). Радиохимические и радиоаналитические письма. 7: 155–62. Отсутствует или пусто
| название =(помощь) - ^ Мефодьева, М. П .; Krot, N. N .; Смирнова, Т. В .; Гельман, А. Д. (1969). «Оксалатные соединения шестивалентного нептуния». Радиохимия (на русском). 11: 193–200.
- ^ Hoekstra, H.R .; Геберт, Э. (1977). «Некоторые тройные оксиды нептуния и плутония со щелочными металлами». Журнал неорганической и ядерной химии. 39 (12): 2219–21. Дои:10.1016/0022-1902(77)80399-0.
- ^ Tabuteau, A .; Пажес, М. (1985). «Нептуниум». В Freeman, A. J .; Келлер, К. (ред.). Справочник по физике и химии актинидов. 3. Амстердам: Северная Голландия. С. 184–241.
- ^ С. Фрид, Н. Р. Дэвидсон: Основы сухой химии нептуния, (1947) Отчет MDDC-1332, Комиссия по атомной энергии США - Аргоннская национальная лаборатория, рассекречено: 18 июля 1947 года.
- ^ а б c Йошида и др., Стр. 730–736.
- ^ Kleinschmidt, P.D .; Lau, K. H .; Хильденбранд, Д. Л. (1992). «Сублимационные исследования NpF4". Журнал химической физики. 97 (3): 1950–3. Bibcode:1992ЖЧФ..97.1950К. Дои:10.1063/1.463131.
- ^ а б Дробышевский, Ю.В. Серик, В. Ф .; Соколов В.Б .; Тульский М. Н. (1978). «Синтез и некоторые свойства тетрафторида нептуния и пентафторида нептуния». Радиохимия (на русском). 20: 238–243.
- ^ Сиборг, Г. Т. и Браун, Х. С. (1961) Патент США № 2,982,604..
- ^ Флорин, А. Э. (1943) Отчет MUC-GTS-2165, рассекреченный: 23 января 1946 г.
- ^ Malm, J.G .; Weinstock, B .; Уивер, Э. (1958). «Приготовление и свойства NpF6; Сравнение с PuF6". Журнал физической химии. 62 (12): 1506–8. Дои:10.1021 / j150570a009.
- ^ Фрид, С. (1954). «Нептуниум». В Сиборге, Г. Т .; Кац, Дж. Дж. (Ред.). Элементы актинидов. Нью-Йорк: Макгроу-Хилл. п. 471.
- ^ Eller, P. G .; Asprey, L.B .; Kinkead, S.A .; Swanson, B.I .; и другие. (1998). «Реакция дифторида кислорода с оксидами и фторидами нептуния». Журнал сплавов и соединений. 269 (1–2): 63–6. Дои:10.1016 / s0925-8388 (98) 00005-х.
- ^ Kleinschmidt, P.D .; Lau, K. H .; Хильденбранд, Д. Л. (1992). «Сублимационные исследования NpO2F2". Журнал физической химии. 97 (4): 2417–21. Bibcode:1992ЖЧФ..97.2417К. Дои:10.1063/1.463080.
- ^ Peacock, R.D .; Эдельштейн, Н. (1976). «Некоторые реакции гексафторида нептуния». Журнал неорганической и ядерной химии. 38 (4): 771–3. Дои:10.1016/0022-1902(76)80353-3.
- ^ Браун, Д. (1972). «Трансуран». Gmelin Handbuck der Anorganischen Chemie, Suppl. Работа. 4. Вайнхайм, Германия: Verlag Chemie.
- ^ Йошида и др., Стр. 736–738.
- ^ Фрид С. и Дэвидсон Н. Р. (1951) Патент США № 2,578,416..
- ^ Лемир, стр. 143–155.
- ^ а б c Йошида и др., Стр. 739–742.
- ^ Marcon, J. P. (1967) C. R. Acad. Sci. Париж 265 Серия C 235.
- ^ Fried, S .; Дэвидсон, Н. Р. (1948). «Получение твердых соединений нептуния». Журнал Американского химического общества. 70 (11): 3539–47. Дои:10.1021 / ja01191a003. PMID 18102891.
- ^ Захариасен, В. Х. (1949). «Кристаллохимические исследования tf-ряда элементов. X. Сульфиды и окс-сульфиды». Acta Crystallographica. 2 (5): 291–6. Дои:10.1107 / s0365110x49000758.
- ^ Charvillat, J.P .; Benedict, U .; Damien, D .; Новион, Д .; и другие. (1976). «Нептуниум». В Muller, W .; Линдер Р. (ред.). Транплутониевые элементы. Амстердам: Северная Голландия. п. 79.
- ^ Peacock, R.D .; Эдельштейн, Н. (1997). «Эксперименты по дифракции рентгеновских лучей высокого давления на NpS и PuS до 60 ГПа». Исследование высокого давления. 15 (6): 387–92. Bibcode:1997HPR .... 15..387B. Дои:10.1080/08957959708240482.
- ^ а б Thevenin, T .; Jove, J .; Пейджерс, М. (1985). «Кристаллохимия и 237Мёссбауэровские исследования Np на халькогенидах оксида нептуния NpOS и NpOSe ». Бюллетень материаловедения. 20 (6): 723–30. Дои:10.1016/0025-5408(85)90151-5.
- ^ Damien, D .; Бергер, Р. (1976). Спицын, В. И .; Кац, Дж. Дж. (Ред.). Приложение к Журналу неорганической и ядерной химии - Московский симпозиум - По химии трансурановых элементов. Оксфорд: Pergamon Press. С. 109–16.
- ^ Thevenin, T .; Пейджс, М. (1982). «Кристаллографические и магнитные исследования нового селенида нептуния: Np2Se5". Журнал менее распространенных металлов. 84: 133–7. Дои:10.1016/0022-5088(82)90138-2.
- ^ Damien, D .; Вояковский, А. (1975). «Приготовление и параметры почтовых моноселенюров и монотонных рисунков нептуния и америки». Радиохимические и радиоаналитические письма (На французском). 23: 145–54.
- ^ а б c Йошида и др., Стр. 742–744.
- ^ а б c Шефт, I .; Фрид, С. (1953). «Соединения нептуния». Журнал Американского химического общества. 75 (5): 1236–7. Дои:10.1021 / ja01101a067.
- ^ Olson, W. M .; Малфорд Р. Н. Р. (1966). «Температура плавления и давление разложения мононитрида нептуния». Журнал физической химии. 70 (9): 2932–2934. Дои:10.1021 / j100881a035.
- ^ Blaise, A .; Damien, D .; Suski, W. (1981). «Удельное электрическое сопротивление моно и диарсенида нептуния». Твердотельные коммуникации. 37 (8): 659–62. Bibcode:1981SSCom..37..659B. Дои:10.1016/0038-1098(81)90543-3.
- ^ Dabos, S .; Dufour, C .; Benedict, U .; Spirlet, J.C .; и другие. (1986). «Дифракция рентгеновских лучей под высоким давлением на соединениях нептуния: последние результаты для NpAs». Physica B. 144 (1): 79–83. Bibcode:1986PhyBC.144 ... 79D. Дои:10.1016/0378-4363(86)90296-2.
- ^ Aldred, A. T .; Dunlap, B.D .; Харви, А. Р .; Lam, D. J .; и другие. (1974). «Магнитные свойства монопниктидов нептуния». Физический обзор B. 9 (9): 3766–78. Bibcode:1974PhRvB ... 9.3766A. Дои:10.1103 / PhysRevB.9.3766.
- ^ Burlet, P .; Bourdarot, F .; Rossat-Mignod, J .; Sanchez, J. P .; и другие. (1992). «Нейтронографическое исследование магнитного упорядочения в NpBi». Physica B. 180: 131–2. Bibcode:1992PhyB..180..131B. Дои:10.1016 / 0921-4526 (92) 90683-J.
- ^ De Novion, C.H .; Лоренцелли, Р. (1968). "Proprietes electroniciques du monocarbure et du mononitrure de neptunium". Журнал физики и химии твердого тела. 29 (10): 1901–5. Bibcode:1968JPCS ... 29.1901D. Дои:10.1016/0022-3697(68)90174-1.
- ^ Holley, C. E. Jr .; Rand, M. H .; Штормы, Э. К. (1984). Химическая термодинамика элементов и соединений актинидов, часть 6. Карбиды актинидов.. Вена: Международное агентство по атомной энергии. С. 49–51.
- ^ Йошида и др., Стр. 722–4.
- ^ Лемир и др., Стр. 177–180.
- ^ Йошида и др., Стр. 744–5.
- ^ а б c d е ж грамм час Йошида и др., Стр. 750–2.
- ^ а б c d е ж грамм час я j k Йошида и др., Стр. 745–750.
- ^ а б c d е ж грамм Йошида и др., Стр. 771–82.
- ^ Lange, R; Кэрролл, В. (2008). «Обзор последних достижений радиоизотопных энергосистем». Преобразование энергии и управление. 49 (3): 393–401. Дои:10.1016 / j.enconman.2007.10.028.
- ^ а б Йошида и др., Стр. 702–3.
- ^ «Решения об ограничении рассекречивания данных с 1946 года по настоящее время», по состоянию на 23 сентября 2006 г.
- ^ а б c Яррис, Линн (2005-11-29). «Получение нептуния из ядерных отходов». Лаборатория Беркли, Министерство энергетики США. Получено 2014-07-26.
- ^ Дорин Н. Поэнару; Вальтер Грейнер (1997). Экспериментальная техника в ядерной физике. Вальтер де Грюйтер. п. 236. ISBN 978-3-11-014467-3.
- ^ "Юкка Маунтин" (PDF). Получено 2009-06-06.
- ^ Родригес, К; Baxter, A .; McEachern, D .; Fikani, M .; и другие. (2003). «Глубокое сжигание: практическое применение трансмутации ядерных отходов». Ядерная инженерия и дизайн. 222 (2–3): 299–317. Дои:10.1016 / S0029-5493 (03) 00034-7.
- ^ J. I. Friese; Э. К. Бак; Б. К. Макнамара; Б. Д. Хэнсон; и другие. (2003-01-06). "Существующие доказательства судьбы Нептуния в хранилище горы Юкка" (PDF). Национальная лаборатория северо-западной части Тихого океана, Министерство энергетики США. Получено 2014-07-26.
Библиография
- Этвуд, Дэвид А. (2013). Радионуклиды в окружающей среде. Джон Уайли и сыновья. ISBN 9781118632697.
- Эмсли, Джон (2011). Строительные блоки природы: руководство по элементам от А до Я. Нью-Йорк: Издательство Оксфордского университета, США. ISBN 978-0-199-60563-7.
- Хоффман, Клаус (2001). Отто Хан: достижения и ответственность. Springer. Bibcode:2002ohar.book ..... H. ISBN 978-0-387-95057-0.
- Лемир, Роберт Дж. (2001). Химическая термодинамика нептуния и плутония.. Амстердам: Эльзевир. ISBN 978-0-444-50379-4.
- Родос, Ричард (2012). Создание атомной бомбы (25-летие изд.). Нью-Йорк: Саймон и Шустер. ISBN 978-1-451-67761-4.
- Ёсида, Зенко; Джонсон, Стивен Дж .; Кимура, Такауми; Крсул, Джон Р. (2006). «Нептуниум». In Morss, Lester R .; Эдельштейн, Норман М .; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (PDF). 3 (3-е изд.). Дордрехт, Нидерланды: Springer. С. 699–812. Дои:10.1007/1-4020-3598-5_6. ISBN 978-1-4020-3555-5. Архивировано из оригинал (PDF) 17 января 2018 г.
Литература
- Путеводитель по элементам - переработанное издание, Альберт Ствертка, (Oxford University Press; 1998) ISBN 0-19-508083-1
- Лестер Р. Морсс, Норман М. Эдельштейн, Жан Фугер (Hrsg.): Химия актинидных и трансактинидных элементов, Springer-Verlag, Dordrecht 2006, ISBN 1-4020-3555-1.
- Ида Ноддак (1934). "Убер дас Элемент 93". Zeitschrift für Angewandte Chemie. 47 (37): 653–655. Дои:10.1002 / ange.19340473707.
- Эрик Шерри, Очень краткое введение в периодическую таблицу, Oxford University Press, Оксфорд, 2011 г., ISBN 978-0-19-958249-5.
внешняя ссылка
- Нептуний в Периодическая таблица видео (Ноттингемский университет)
- Лаборатория построила первую в мире нептуниевую сферу, Министерство энергетики США Новости исследований
- Банк данных по опасным веществам NLM - Нептуний, радиоактивный
- Нептуний: информационный бюллетень о здоровье человека
- C&EN: It's Elemental: The Periodic Table - Neptunium

![{displaystyle {ce {{^ {238} _ {92} U} + {^ {1} _ {0} n} -> {^ {239} _ {92} U} -> [eta ^ {-}] [23 {ce {min}}] {^ {239} _ {93} Np} -> [eta ^ {-}] [2.355 {ce {days}}] {^ {239} _ {94} Pu}} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/93b95114fe8847dcf5cd481fc8c5d755b4a1b823)

![{displaystyle {egin {case} {ce {^ {235} _ {92} U + ^ {1} _ {0} n -> ^ {236m} _ {92} U -> [] [120 {ce {ns] }}] ^ {236} _ {92} U + гамма}} {ce {^ {236} _ {92} U + ^ {1} _ {0} n -> ^ {237} _ {92} U -> [eta ^ -] [6.75 {ce {d}}] ^ {237} _ {93} Np}} конец {случаи}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/200d66a55c52bc1210e970e37646a4d81842aa34)
![{displaystyle {ce {^ {237} _ {93} Np + ^ {1} _ {0} n -> ^ {238} _ {93} Np -> [eta ^ -] [2.117 {ce {d}} ] ^ {238} _ {94} Пу}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/18a4a99dfdd1831d6e5ba84881bc0c24d9985cc8)