Фосфид - Википедия - Phosphide

В химии фосфид представляет собой соединение, содержащее P3− ion или его аналог. Известно много различных фосфидов с сильно различающейся структурой.[1] Чаще всего встречается на двойных фосфидах, т.е. тех материалах, которые состоят только из фосфора и менее электроотрицательного элемента. Многочисленны полифосфиды, которые представляют собой твердые вещества, состоящие из анионных цепей или кластеров фосфора. Фосфиды известны с большинством менее электроотрицательных элементов, за исключением Hg, Pb, Sb, Би, Te, и По.[2] Наконец, некоторые фосфиды являются молекулярными.
Бинарные фосфиды
Бинарные фосфиды включают фосфор и еще один элемент. Примером фосфида группы 1 является фосфид натрия (Na3П). Другие известные примеры включают фосфид алюминия (AlP) и фосфид кальция (Ca3п2), которые используются в качестве пестицидов, используя их склонность выделять токсичные вещества. фосфин при гидролизе. Фосфид магния (Mg3п2) также чувствителен к влаге. Фосфид индия (InP) и Зазор используются как полупроводники, часто в сочетании с родственными арсениды.[3] Фосфид меди (Cu3P) иллюстрирует редкую стехиометрию для фосфида. Эти частицы нерастворимы во всех растворителях - это трехмерные твердотельные полимеры. В случае с электроположительными металлами материалы гидролизуются:
- Ca3п2 + 6 часов2О → 3 Са (ОН)2 + 2 PH3

Полифосфиды
Полифосфиды содержат связи P-P. Простейшие полифосфиды содержат п4−
2 ионы ;. Другие содержат кластер п3−
11 ионы и анионы полимерных цепей (например, спиральные (П−
)
п ion) и комплексные листовые или 3-D анионы.[4] Ассортимент конструкций обширен. Калий имеет девять фосфидов: K3P, K4п3, К5п4, КП, К4п6, К3п7, К3п11, КП10.3, КП15. Восемь моно- и полифосфидов никель также существуют: (Ni3P, Ni5п2, Ni12п5, Ni2P, Ni5п4, NiP, NiP2, NiP3).[2]
Два полифосфид-иона, п4−
3 нашел в K
4п
3 и п5−
4 найдено в K5п4, находятся радикальные анионы с нечетным числом валентные электроны делая оба соединения парамагнитный.[2]
Получение фосфидных и полифосфидных материалов
Есть много способов приготовления фосфидных соединений. Один из распространенных способов заключается в нагревании металла и красный фосфор (P) в инертных атмосферных условиях или в вакууме. В принципе, все фосфиды и полифосфиды металлов могут быть синтезированы из элементарного фосфора и соответствующего металлического элемента в стехиометрических формах. Однако синтез затруднен из-за нескольких проблем. В экзотермические реакции часто взрывоопасны из-за местного перегрева. Окисленные металлы или даже просто окисленный слой на внешней стороне металла вызывают экстремально и недопустимо высокие температуры для начала фосфорирования.[5] Гидротермальные реакции с образованием фосфидов никеля дали чистые и хорошо кристаллизованные соединения фосфида никеля, Ni2P и Ni12п5. Эти соединения были синтезированы в результате реакции твердое тело-жидкость между NiCl2∙ 12H2O и красный фосфор при 200 ° C в течение 24 и 48 часов соответственно.[6]
Фосфиды металлов также производятся реакцией трис (триметилсилил) фосфин с галогенидами металлов. В этом методе галогенид выделяется в виде летучих триметилсилилхлорид.
Способ приготовления К2п16 из красного фосфора и этоксид калия было сообщено.[7]
Молекулярные фосфиды
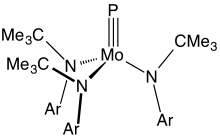
Соединения с тройными связями между металлом и фосфором встречаются редко. Основные примеры имеют формулу Mo (P) (NR2)3, где R - объемный органический заместитель.[8]
Органические фосфиды
Известно много органофосфидов. Общие примеры имеют формуляр R2PM, где R - органический заместитель, а M - металл. Одним из примеров является дифенилфосфид лития. В Zintl кластер п3−
7 получается с различными производными щелочных металлов.
Природные примеры
Минерал Шрайберсит (Fe, Ni)3P часто встречается в некоторых метеоритах.
Рекомендации
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б c Фон Шнеринг, Х.Г. и Хенле, В. (1994) "Фосфиды - химия твердого тела" в Энциклопедия неорганической химии. Р. Брюс Кинг (ред.). Джон Уайли и сыновья ISBN 0-471-93620-0
- ^ Blackman, C. S .; Carmalt, C.J .; O'Neill, S.A .; Паркин, И. П .; Molloy, K. C .; Апостолико, Л. (2003). «Химическое осаждение из газовой фазы тонких пленок фосфидов металлов Vb группы» (PDF). Журнал химии материалов. 13 (8): 1930. Дои:10.1039 / b304084b.
- ^ Jeitschko, W .; Мёллер, М. Х. (1987). «Фосфиды и полифосфиды переходных металлов». Фосфор, сера и родственные элементы. 30 (1–2): 413–416. Дои:10.1080/03086648708080608.
- ^ фон Шнеринг, Ханс-Георг; Хенле, Вольфганг (1988). «Преодоление пропастей с помощью фосфидов». Chem. Rev. 88: 243–273. Дои:10.1021 / cr00083a012.
- ^ Лю, Цзунъи; Хуанг, Сян; Жу, Жибин; Дай, Цзиньхуэй (2010). «Простой умеренный гидротермальный способ синтеза порошков фосфида никеля». Керамика Интернэшнл. 36 (3): 1155–1158. Дои:10.1016 / j.ceramint.2009.12.015.
- ^ Легкое превращение красного фосфора в растворимые полифосфид-анионы путем реакции с этоксидом калия А. Драгулеску-Андраси, Л. З. Миллер, Б. Чен, Д. Т. Маккуэйд, М. Шатрук, Angew. Chem. Int. Эд. 2016, 55, 3904.Дои:10.1002 / anie.201511186
- ^ Cossairt, B.M .; Пиро, Н. А .; Камминс, К. С. (2010). «Активация и трансформация белого фосфора, опосредованная ранними переходными металлами». Химические обзоры. 110 (7): 4164–77. CiteSeerX 10.1.1.666.8019. Дои:10.1021 / cr9003709. PMID 20175534.
