Оксогалогенид - Oxohalide
Молекулярные оксогалогениды (оксигалогениды) являются группой химические соединения в котором оба кислород и галоген атомы прикреплены к другому химический элемент А в сингле молекула. У них есть общая формула АОмИксп, X = F, Cl, Br, я. Элемент A может быть основная группа элемент, a переходный элемент или актинид. Термин оксогалогенид или оксигалогенид может также относиться к минералам и другим кристаллическим веществам с той же общей химической формулой, но имеющим ионный структура.
Синтез

Оксогалогениды можно рассматривать как промежуточные соединения между оксиды и галогениды. Есть три основных метода синтеза:[1]
- Частичное окисление галогенида: 2 ПКл.3 + O2 → 2 POCl3. В этом примере степень окисления увеличивается на два, а электрический заряд не изменяется.
- Частичное галогенирование оксида: 2 В2О5 + 6 Cl2 + 3 C → 4 VOCl3 + 3 СО2
- Замещение оксида: [CrO4]2− + 2 кл− + 4 часа+ → CrO2Cl2 + 4 часа2О
Кроме того, различные оксогалогениды могут быть получены реакциями обмена галогенов, и эта реакция также может привести к образованию смешанных оксогалогенидов, таких как POFCl.2 и CrO2FCl.
Характеристики
По отношению к оксиду или галогениду для данной степени окисления элемента A, если два атома галогена заменяют один атом кислорода, или наоборот, общий заряд молекулы не изменится и координационный номер центрального атома уменьшается на единицу. Например, оба оксихлорид фосфора, POCl3 и пентахлорид фосфора, PCl5 нейтральны ковалентный соединения фосфор в +5 степень окисления. Если атом кислорода просто заменить атомом галогена, заряд увеличивается на +1, но координационное число не изменяется. Это иллюстрируется реакцией смеси хромат или дихромат соль и хлорид калия с концентрированным серная кислота.
- [Cr2О7]2− + 4 кл− + 6 часов+ → 2 CrO2Cl2 + 3 часа2О
В хромилхлорид произведенный не имеет электрического заряда и представляет собой летучую ковалентную молекулу, которая может быть удалена из реакционной смеси.[2]
Оксогалогениды элементов в высоких степенях окисления сильны окислители с окислительной способностью, аналогичной окислительной способности соответствующего оксида или галогенида. Большинство оксогалогенидов легко гидролизованный. Например, хромилхлорид гидролизуют до хромата в обратной реакции синтеза, описанной выше. Движущей силой этой реакции является образование связей A-O, которые сильнее, чем связи A-Cl. Это дает благоприятный энтальпия вклад в Свободная энергия Гиббса изменение для реакции[3]
Многие оксогалогениды могут действовать как Кислоты Льюиса. Это особенно верно для оксогалогенидов координационный номер 3 или 4, которые при приеме одной или нескольких электронных пар от База Льюиса, становятся 5- или 6-координатными. Оксогалогенидные анионы, такие как [VOCl4]2− можно рассматривать как кислотно-основные комплексы оксогалогенида (VOCl2) с большим количеством галогенид-ионов, действующих как основания Льюиса. Другой пример - VOCl.2 который формирует тригонально-бипирамидный комплекс VOCl2(N (CH3)3)2 с основанием триметиламин.[4]
В колебательные спектры многих оксогалогенидов описаны подробно. Они дают полезную информацию об относительной прочности сцепления. Например, в CrO2F2валентные колебания Cr – O находятся при 1006 см−1 и 1016 см−1 валентные колебания Cr – F находятся на 727 см−1 и 789 см−1. Разница слишком велика, чтобы быть вызванной разной массой атомов O и F. Скорее, это показывает, что связь Cr – O намного прочнее, чем связь Cr – F. Связи M – O обычно считаются двойные связи и это подтверждается измерениями длин связей M – O. Отсюда следует, что элементы A и O являются химически связанный вместе с помощью σ-связи и π-связи.[5]
Оксогалогениды элементов в высоких степенях окисления сильно окрашены из-за лиганда металла перенос заряда (LMCT) переходы.[6]

Элементы основной группы

- Группа углерода: Углерод образует оксогалогениды COX.2, X = F, Br, и очень токсичный фосген (X = Cl), который производят в промышленных масштабах путем катализируемой углеродом реакции монооксид углерода с хлор. Это полезный реагент в органическая химия для формирования карбонильные соединения.[7] Например,
- COCl2 + 2 ROH → CO (ИЛИ)2 + 2 HCl
- Пниктогены: Азот образует две серии оксогалогенидов с азотом в степени окисления 3, NOX, X = F, Cl, Br и 5, НЕТ2Х, Х = F, Кл. Их получают галогенированием оксидов азота. Обратите внимание, что НЕТ2F - это изоэлектронный с нитрат ион, NO3−. Только оксогалогениды фосфор (V) известны.[8]
- Халькогены: Сера образует оксогалогениды[9] в степени окисления +4, например тионилхлорид, SOCl2 и степень окисления +6, например сульфурилфторид, ТАК2F2, сульфурилхлорид, ТАК2Cl2, и тионилтетрафторид, СОФ4. Все легко гидролизуются. Действительно, тионилхлорид можно использовать в качестве агента дегидратации, поскольку молекулы воды превращаются в газообразные продукты, оставляя после себя безводный твердый хлорид.[10]
- MgCl2· 6H2O + 6 SOCl2 → MgCl2 + 6 СО2 + 12 HCl
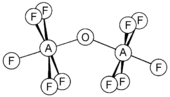
Селен и теллур образуют аналогичные соединения, а также оксо-мостиковые соединения F5AOAF5 (А = S, Se, Te). Они нелинейны с углом A-O-A 142,5, 142,4 и 145,5 ° для S, Se и Te соответственно.[11] Анион теллура [TeOF5]−, известный как тефлировать, представляет собой большой и довольно стабильный анион, пригодный для образования стабильных солей с большими катионами.[10]
- Галогены: Галогены образуют различные оксофториды с формулами XO2F, XO3F и XOF3 с X = Cl, Br и I. IO2F3 и ИОФ5 также известны.[12]
- благородные газы: XeOF4
Переходные металлы и актиниды

Ряд известных оксогалогенидов переходные металлы показан ниже, а более подробные списки доступны в литературе.[14] X обозначает различные галогениды, чаще всего F и Cl.
| Состояние окисления | оксогалогениды |
|---|---|
| 3 | VOCl, VOBr,[15] FeOCl |
| 4 | [TiOCl4]2−, Cl3TiOTiCl3, VOCl2, [VOCl4]2− |
| 5 | VOX3, В.О.2X, [CrOF4]−, [CrOF5]2−, MnOCl3, TcOCl3, VOF3, VOCl3, NbOCl3 |
| 6 | CrO2Cl2, [CrO3Cl]−, ReOX4, ReO2F2, OsOF4, CrO2F2, MoOCl4 МоО2Cl2, WO2Cl2, WOCl4 |
| 7 | MnO3Cl, РеОФ5, ReO2F3, ReO3Cl, OsOF5 |
| 8 | OsO2F4, OsO3F2 |

Высокая степень окисления металла продиктована тем, что кислород сильный окислитель, как есть фтор. Бром и йод являются относительно слабыми окислителями, поэтому известно меньше оксобромидов и оксоиодидов. Структуры для соединений с d0 конфигурация предсказывается Теория VSEPR. Таким образом, CrO2Cl2 является четырехгранный, OsO3F2 является тригонально-бипирамидный, XeOF4 является квадратно-пирамидальный и OsOF5 является восьмигранный.[17] D1 комплекс ReOCl4 квадратно-пирамидальный.
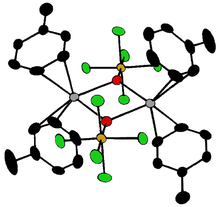
Соединения [Ta2OX10]2− И м2OCl10]4− (M = W, Ru, Os) имеют два MX5 группы, соединенные мостиковым атомом кислорода.[18] Каждый металл имеет октаэдрическое окружение. Необычная линейная структура M — O — M может быть объяснена в терминах молекулярная орбиталь теория, указывающая на наличие dπ - пπ связь между атомами металла и кислорода.[19] Кислородные мостики присутствуют в более сложных конфигурациях, таких как M (cp)2(OTeF5)2 (M = Ti, Zr, Hf, Mo или W; cp = η5−C5ЧАС5 )[20] или [AgOTeF5−(C6ЧАС5CH3)2]2.[16]
в актинид серии, уранил такие соединения, как UO2Cl2 и [UO2Cl4]2− хорошо известны и содержат линейные UO2 часть. Подобные виды существуют для нептуний и плутоний.
Минералы и ионные соединения

Оксохлорид висмута (BiOCl, бисмоклит ) является редким примером минерального оксогалогенида. В Кристальная структура имеет четырехугольный симметрии и может рассматриваться как состоящий из слоев Cl−, Би3+ и O2− ионы в порядке Cl-Bi-O-Bi-Cl-Cl-Bi-O-Bi-Cl. Эта слоистая графитоподобная структура обеспечивает относительно низкую твердость бисмоклита (Моос 2–2,5) и большинство других оксогалогенидных минералов.[21] Эти другие минералы включают терлингваит Hg2OCl, образующийся при выветривании ртутьсодержащих минералов.[22] Мендипит, Pb3О2Cl2, сформированный из первоначального месторождения сульфид свинца в ряде стадий является еще одним примером вторичного оксогалогенидного минерала.
Элементы утюг, сурьма, висмут и лантан образуют оксохлориды общей формулы MOCl. MOBr и MOI также известны для Sb и Bi. Определены многие из их кристаллических структур.[23]
Смотрите также
Рекомендации
- ^ Синтез отдельных соединений можно найти в Housecroft & Sharpe и Greenwood & Earnshaw в разделах, относящихся к конкретному элементу, A
- ^ Сислер, Х. Х. «Хромилхлорид» Неорганический синтез Макгроу-Хилл: Нью-Йорк, 1946; Vol. 2. С. 205–207.
- ^ Гринвуд и Эрншоу, стр. 1023
- ^ Гринвуд и Эрншоу, стр. 996.
- ^ К. Накамото Инфракрасные и рамановские спектры неорганических и координационных соединений, 5-й. издание, Часть A, Wiley, 1997 ISBN 0-471-19406-9, Таблицы II-4c, II-6g, II-6h, II-7b, II-8c
- ^ Шрайвер и Аткинс, рис. 13.8, стр. 447
- ^ Шрайвер и Аткинс, стр. 358
- ^ Housecroft & Sharpe, стр. 329–330.
- ^ Housecroft & Sharpe, стр. 365–367.
- ^ а б Шрайвер и Аткинс, стр. 397
- ^ Оберхаммер, Хайнц; Сеппельт, Конрад (1978). «Молекулярная структура F5SOSF5, F5SeOSeF5, а F5TeOTeF5: d-Orbital Участие в связях между основными элементами группы ». Angewandte Chemie International Edition. 17 (1): 69–70. Дои:10.1002 / anie.197800691.
- ^ Housecroft & Sharpe, стр. 395
- ^ Фурати, Мохиеддин; Чаабуни, Монсеф; Белин, Клод Анри; Шарбоннель, Моник; Паскаль, Жан Луи; Потье, Жаклин (1986). "Сильно хелатирующий бидентатный CLO4. Новый маршрут синтеза и определение кристаллической структуры Ti (CLO4)4". Неорг. Chem. 25 (9): 1386–1390. Дои:10.1021 / ic00229a019.
- ^ Greenwood & Earnshaw, главы 22–25, раздел галогениды и оксогалогениды
- ^ Гринвуд и Эрншоу, стр. 993.
- ^ а б Штраус, Стивен Х .; Нуаро, Марк Д .; Андерсон, Орен П. (1985). «Получение и характеристика тефлатных комплексов серебра (I): мостиковый OTeF5 группы в твердом состоянии и в растворе ». Неорг. Chem. 24 (25): 4307–4311. Дои:10.1021 / ic00219a022.
- ^ Housectroft & Sharpe, главы 21 и 22 иллюстрируют многие структуры, в том числе длины связей M-O и M-Cl.
- ^ Деван, Джон. C .; Эдвардс, Энтони Дж .; Телята, Жан Й .; Герше, Жак Э. (1997). «Кристаллические структуры фторида. Часть 28. Бис (тетраэтиламмоний) µ-оксо-бис [пентафтортанталат (V)]». J. Chem. Soc., Dalton Trans. (10): 978–980. Дои:10.1039 / DT9770000978.CS1 maint: несколько имен: список авторов (связь). Структура проиллюстрирована Housectroft & Sharpe, рис. 22.5.
- ^ Housectroft & Sharpe, рисунок 22.15.
- ^ Кроссман, Мартин С .; Надежда, Эрик Дж .; Сондерс, Грэм С. (1996). «Циклопентадиенил тефлат металла (OTeF5) комплексы ». J. Chem. Soc., Dalton Trans. (4): 509–511. Дои:10.1039 / DT9960000509.
- ^ Энтони, Джон В .; Бидо, Ричард А .; Bladh, Kenneth W .; Николс, Монте К. (ред.). «Бисмоклит». Справочник по минералогии (PDF). III (галогениды, гидроксиды, оксиды). Шантильи, Вирджиния: Минералогическое общество Америки. ISBN 0-9622097-2-4. Получено 5 декабря, 2011.
- ^ Hillebrand, W. F .; У. Т. Шаллер (1907). "Статья XXVI. Минералы ртути из Терлингуа, штат Техас: клейнит, терлингваит, эглстонит, монройдит, каломель, ртуть.". Американский журнал науки (139): 259–274. Получено 2009-05-21.
- ^ Уэллс, стр. 390–392.
Библиография
- Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- Хаускрофт, К. Э. и Шарп, А. Г. Неорганическая химия, 2-е изд., Pearson Prentice-Hall 2005. ISBN 0-582-31080-6
- Шривр, Д. Ф. и Аткинс, П. В. Неорганическая химия, 3-е изд. Издательство Оксфордского университета, 1999. ISBN 0-19-850330-X
- Уэллс, А. Ф. (1962). Структурная неорганическая химия (3-е изд.). Оксфорд: Clarendon Press. С. 384–392. ISBN 0-19-855125-8..
