Тионил хлорид - Thionyl chloride
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Дихлорид серы | |
Другие имена
| |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.028.863 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1836 |
| |
| |
| Свойства | |
| SOCl2 | |
| Молярная масса | 118.97 г / моль |
| Внешность | Бесцветная жидкость (желтеет при старении) |
| Запах | Острый и неприятный |
| Плотность | 1.638 г / см3, жидкость |
| Температура плавления | -104,5 ° С (-156,1 ° F, 168,7 К) |
| Точка кипения | 74,6 ° С (166,3 ° F, 347,8 К) |
| Реагирует | |
| Растворимость | Растворим в большинстве апротонных растворителей: толуол, хлороформ, диэтиловый эфир. Реагирует с протонными растворителями, такими как спирты. |
| Давление газа |
|
| 1.517 (20 ° C)[2] | |
| Вязкость | 0.6 cP |
| Структура | |
| пирамидальный | |
| 1.44 D | |
| Термохимия | |
Теплоемкость (C) | 121.0 Дж / моль (жидкость)[3] |
Стандартный моляр энтропия (S | 309.8 кДж / моль (газ)[3] |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −245.6 кДж / моль (жидкость)[3] |
| Опасности | |
| Основной опасности |
|
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H302, H314, H331 | |
| P261, P280, P305 + 351 + 338, P310 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | Никто[4] |
REL (Рекомендуемые) | C 1 частей на миллион (5 мг / м3)[4] |
IDLH (Непосредственная опасность) | N.D.[4] |
| Родственные соединения | |
Родственные тионилгалогениды | |
Родственные соединения | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тионил хлорид является неорганическое соединение с химическая формула SОCl
2. Это умеренно летучая бесцветная жидкость с неприятным едким запахом. Тионилхлорид в основном используется в качестве хлорирующего реагента, при этом в начале 1990-х годов производилось примерно 45 000 тонн (50 000 коротких тонн) в год.[5] Он токсичен, реагирует с водой, а также перечисленные под Конвенция о химическом оружии поскольку он может быть использован для производства химическое оружие.
Тионилхлорид иногда путают с сульфурилхлорид, ТАК2Cl2, но свойства этих соединений существенно различаются. Сульфурилхлорид является источником хлор тогда как тионилхлорид является источником хлористый ионы.
Производство
Основной промышленный синтез включает реакцию триоксид серы и дихлорид серы:[6]
- ТАК3 + SCl2 → SOCl2 + ТАК2
Другие методы включают синтез из пентахлорид фосфора, хлор и дихлорид серы, или фосген:
- ТАК2 + PCl5 → SOCl2 + POCl3
- ТАК2 + Cl2 + SCl2 → 2 SOCl2
- ТАК3 + Cl2 + 2 ст.2 → 3 SOCl2
- ТАК2 + COCl2 → SOCl2 + CO2
Первая из четырех вышеупомянутых реакций также дает оксихлорид фосфора (фосфорилхлорид), который во многих своих реакциях напоминает тионилхлорид.
Свойства и структура

SOCl2 принимает треугольная пирамидальная геометрия молекул с Cs молекулярная симметрия. Эта геометрия объясняется влиянием одинокая пара на центральном серном (IV) центре.
В твердотельном SOCl2 формы моноклинический кристаллы с космическая группа P21/ c.[7]
Стабильность
Тионилхлорид имеет длительный срок хранения, однако "выдержанные" образцы приобретают желтый оттенок, возможно, из-за образования дихлорид дисеры. Это медленно разлагается к S2Cl2, ТАК2 и Cl2 чуть выше точки кипения.[6][8] Тионилхлорид подвержен фотолизу, который в основном протекает по радикальному механизму.[9] Образцы, показывающие признаки старения, можно очистить перегонкой при пониженном давлении, чтобы получить бесцветную жидкость.[10]
Реакции
Тионилхлорид в основном используется в промышленном производстве хлорорганические соединения, которые часто являются промежуточными продуктами в фармацевтике и агрохимии. Обычно он предпочтительнее других реагентов, таких как пентахлорид фосфора, в качестве побочных продуктов (HCl и SO2) являются газообразными, что упрощает очистку продукта.
Многие из продуктов тионилхлорида сами по себе обладают высокой реакционной способностью и, как таковые, участвуют в широком диапазоне реакций.
С водой и спиртами
Тионилхлорид экзотермически реагирует с водой с образованием диоксид серы и соляная кислота:
- SOCl2 + H2О → 2 HCl + SO2
Подобным образом он также реагирует с спирты формировать алкилхлориды. Если алкоголь хиральный реакция обычно протекает через SNя механизм с сохранением стереохимии;[11] однако, в зависимости от точных используемых условий, также может быть достигнута стереоинверсия. Исторически использование SOCl2 в сочетании с третичным амином, таким как пиридин был назван Галогенирование Дарценса, но это название редко используется современными химиками.

Реакции с избытком алкоголя производят сульфитные эфиры, который может быть мощным метилирование, алкилирование и реагенты гидроксиалкилирования.[12]
- SOCl2 + 2 ROH → (RO)2SO + 2 HCl
Например, добавление SOCl2 к аминокислоты в метаноле селективно дает соответствующие метиловые эфиры.[13]
С карбоновыми кислотами
Классически он преобразует карбоновые кислоты к ацилхлориды:[14][15][16]
- SOCl2 + RCO2H → RCOCl + SO2 + HCl
Был исследован механизм реакции:[17]
С азотными видами
С первичными аминами тионилхлорид дает сульфиниламин производные (RNSO), одним из примеров является N-сульфиниланилин. Тионилхлорид реагирует с первичными формамиды формировать изоцианиды[18] и вторичными формамидами с образованием хлороиминий ионы; как такая реакция с диметилформамид сформирует Реагент Вильсмайера.[19]Аналогичным способом первичный амиды будет реагировать с тионилхлоридом с образованием имидоилхлориды, с вторичными амидами, также дающими хлороиминий ионы. Эти частицы обладают высокой реакционной способностью и могут быть использованы для катализирования превращения карбоновых кислот в ацилхлориды, они также используются в Реакция Бишлера – Наперальского как средство формирования изохинолины.
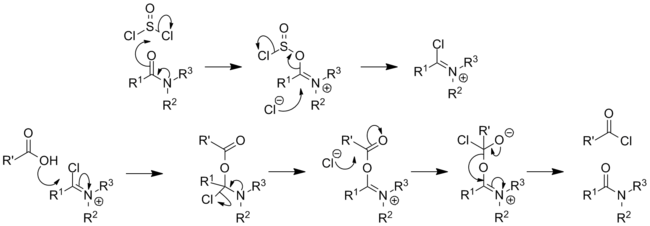
Первичные амиды продолжат образование нитрилы при нагревании (Разложение амида фон Брауна ).[20]Тионилхлорид также использовался для стимулирования Перестановка Бекмана из оксимы.
С разновидностями серы
- Тионилхлорид преобразует сульфиновые кислоты в сульфинилхлориды[21][22]
- Сульфоновые кислоты реакция с тионилхлоридом с образованием сульфонилхлориды.[23][24] Сульфонилхлориды также были получены прямой реакцией соответствующих диазоний соль с тионилхлоридом.[25]
- Тионилхлорид можно использовать в различных вариантах Перестановка молотка.

С видами фосфора
Тионилхлорид превращает фосфоновые кислоты и фосфонаты в фосфорилхлориды. Именно для этого типа реакции тионилхлорид указан как График 3 соединение, так как оно может быть использовано в методе "ди-ди" производства серии G нервно-паралитические вещества. Например, тионилхлорид превращает диметилметилфосфонат в дихлорид метилфосфоновой кислоты, который может быть использован при производстве зарин и зоман.
Металлами
Как SOCl2 реагирует с водой, его можно использовать для обезвоживания различных гидратов хлоридов металлов, таких как MgCl2· 6H2О, AlCl3· 6H2О, и FeCl3· 6H2О.[6] Это преобразование включает обработку кипящим тионилхлоридом и следует следующему общему уравнению:[26]
- MClп·ИксЧАС2O + Икс SOCl2 → MClп + Икс ТАК2 + 2Икс HCl
Другие реакции
- Тионилхлорид может вступать в ряд различных реакций электрофильного присоединения. Добавляет к алкенам в присутствии AlCl3 с образованием комплекса алюминия, который может быть гидролизован с образованием сульфиновой кислоты. И арилсульфинилхлориды, и диарилсульфоксиды могут быть получены из аренов посредством реакции с тионилхлоридом в трифликовая кислота[27] или наличие катализаторов, таких как BiCl3, Bi (OTf)3, LiClO4 или NaClO4.[28][29]
- В лаборатории реакция между тионилхлоридом и избытком безводный спирт может быть использован для производства безводных спиртовых растворов HCl.
- Тионилхлорид претерпевает реакции обмена галогенов с образованием таких соединений, как тионил бромид и тионил фторид
Аккумуляторы

Тионилхлорид входит в состав литий-тионилхлорида. батареи, где он действует как положительный электрод (катод ) с участием литий формирование отрицательного электрода (анод ); то электролит обычно тетрахлоралюминат лития. Общая реакция разряда следующая:
- 4 Li + 2 SOCl2 → 4 LiCl + S + SO2
Эти неперезаряжаемые батареи имеют много преимуществ по сравнению с другими формами литиевых батарей, таких как высокая плотность энергии, широкий диапазон рабочих температур и длительный срок хранения и эксплуатации. Однако их высокая стоимость и соображения безопасности ограничили их использование. Содержимое батарей очень токсично и требует специальных процедур утилизации; кроме того, они могут взорваться при коротком замыкании.
Безопасность
SOCl2 представляет собой реактивное соединение, которое может сильно выделять опасные газы при контакте с водой и другими реагентами. Он также контролируется Конвенция о химическом оружии и внесен в список График 3 вещество, так как оно используется в методе "ди-ди" производства серии G нервно-паралитические вещества.[нужна цитата ]
История
В 1849 г. французские химики Жан-Франсуа Персоз и Блох, и немецкий химик Петер Кремерс (1827-?) независимо впервые синтезировали тионилхлорид путем реакции пентахлорид фосфора с участием диоксид серы.[30][31] Однако их продукты были нечистыми: и Персоз, и Кремерс утверждали, что тионилхлорид содержит фосфор,[32] и Кремерс зафиксировали его точку кипения как 100 ° C (вместо 74,6 ° C). В 1857 г. немецко-итальянский химик Хьюго Шифф подвергал неочищенный тионилхлорид многократной фракционной перегонке и получил жидкость, которая кипела при 82 ° C и которую он назвал Тионилхлорид.[33] В 1859 г. немецкий химик Георг Людвиг Кариус отметил, что тионилхлорид может использоваться для производства ангидриды кислот и ацилхлориды от карбоновые кислоты и сделать алкилхлориды от спирты.[34]
Смотрите также
использованная литература
- ^ Тионил хлорид в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69, Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (Проверено 11 мая 2014 г.)
- ^ Патнаик, Прадёт (2003). Справочник неорганических химикатов. Нью-Йорк, штат Нью-Йорк: Макгроу-Хилл. ISBN 0-07-049439-8.
- ^ а б c Лиде, Дэвид Р .; и др., ред. (1996). CRC Справочник по химии и физике (76-е изд.). Бока-Ратон, Флорида: CRC Press. С. 5–10. ISBN 0-8493-0476-8.
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0611". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Lauss, H.-D .; Стеффенс, В. "Галогениды серы". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a25_623.
- ^ а б c Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. п. 694. ISBN 978-0-08-037941-8.
- ^ Mootz, D .; Мершенц-Кряк, А. (15 мая 1988 г.). «Структуры тионилгалогенидов: SOCl2 и СОБР2" (PDF). Acta Crystallographica Раздел C. 44 (5): 926–927. Дои:10.1107 / S010827018800085X.
- ^ Брауэр, Георг, изд. (1963). Справочник по препаративной неорганической химии. 1. Перевод Scripta Technica; Рид, Ф. (2-е изд.). Нью-Йорк, Нью-Йорк: Academic Press. п. 383. ISBN 978-0121266011.
- ^ Донован, Р. Дж .; Husain, D .; Джексон, П. Т. (1969). «Спектроскопические и кинетические исследования радикала SO и фотолиза тионилхлорида». Труды общества Фарадея. 65: 2930. Дои:10.1039 / TF9696502930.
- ^ Фридман, Л .; Веттер, У. П. (1967). «Очистка тионилхлорида». Журнал химического общества A: неорганический, физический, теоретический: 36. Дои:10.1039 / J19670000036.
- ^ Смит, Майкл Б .; Марш, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 469, г. ISBN 978-0-471-72091-1
- ^ Ван Верден, Х. Ф. (1963). «Органические сульфиты». Химические обзоры. 63 (6): 557–571. Дои:10.1021 / cr60226a001.
- ^ Brenner, M .; Хубер, В. (1953). "Herstellung von α-Aminosäureestern durch Alkoholyse der Methylester" [Производство сложных эфиров α-аминокислот путем алкоголиза метиловых эфиров]. Helvetica Chimica Acta (на немецком). 36 (5): 1109–1115. Дои:10.1002 / hlca.19530360522.
- ^ Клейден, Джонатан; Гривс, Ник; Уоррен, Стюарт; Уотерс, Питер (2001). Органическая химия (1-е изд.). Издательство Оксфордского университета. п. 295. ISBN 978-0-19-850346-0.
- ^ Allen, C.F.H .; Байерс, Дж. Р., младший; Хамфлетт, У. Дж. (1963). «Олеоилхлорид». Органический синтез.; Коллективный объем, 4, п. 739
- ^ Рутенберг, М. З .; Хорнинг, Э. К. (1963). «1-Метил-3-этилоксиндол». Органический синтез.; Коллективный объем, 4, п. 620
- ^ Ошибка цитирования: указанная ссылка
клейденбыл вызван, но не определен (см. страница помощи). - ^ Низник, Г. Э .; Моррисон, В. Х., III; Валборский, Х. М. (1988). "1-d-Альдегиды из металлоорганических реагентов: 2-метилбутаналь-1-d". Органический синтез.; Коллективный объем, 6, п. 751
- ^ Arrieta, A .; Aizpurua, J.M .; Паломо, К. (1984). "N,N-Диметилхлорсульфитметанинийхлорид (SOCl2-ДМФ) универсальный дегидратирующий реагент ». Буквы Тетраэдра. 25 (31): 3365–3368. Дои:10.1016 / S0040-4039 (01) 81386-1.
- ^ Крыницкий, Дж. А .; Кархарт, Х. В. (1963). «2-Этилгексанонитрил». Органический синтез.; Коллективный объем, 4, п. 436
- ^ Hulce, M .; Mallomo, J. P .; Frye, L. L .; Коган, Т. П .; Познер, Г. Х. (1990). "(S)-(+)-2-(п-толуолсульфинил) -2-циклопентенон: предшественник для энантиоселективного синтеза 3-замещенных циклопентанонов ». Органический синтез.; Коллективный объем, 7, п. 495
- ^ Курцер, Ф. (1963). "п-Толуолсульфинилхлорид ". Органический синтез.; Коллективный объем, 4, п. 937
- ^ Weinreb, S.M .; Chase, C.E .; Wipf, P .; Венкатраман, С. (2004). «2-Триметилсилилэтансульфонилхлорид (SES-Cl)». Органический синтез.; Коллективный объем, 10, п. 707
- ^ Hazen, G.G .; Bollinger, F.W .; Робертс, Ф. Э .; Russ, W. K .; Seman, J. J .; Стаскевич, С. (1998). «4-Додецилбензолсульфонилазиды». Органический синтез.; Коллективный объем, 9, п. 400
- ^ Hogan, P.J .; Кокс, Б. Г. (2009). «Химия водных процессов: получение арилсульфонилхлоридов». Исследования и разработки в области органических процессов. 13 (5): 875–879. Дои:10.1021 / op9000862.
- ^ Молитесь, A.R .; Heitmiller, R. F .; Страйкер, С .; Афтандилиан, В. Д .; Muniyappan, T .; Choudhury, D .; Тамрес, М. (1990). Безводные хлориды металлов. Неорганические синтезы. 28. С. 321–323. Дои:10.1002 / 9780470132593.ch80. ISBN 978-0-470-13259-3.
- ^ Смит, Майкл Б .; Марш, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 697, г. ISBN 978-0-471-72091-1
- ^ Peyronneau, M .; Roques, N .; Mazières, S .; Ле Ру, К. (2003). «Каталитическая активация тионилхлорида кислотой Льюиса: применение к синтезу арилсульфинилхлоридов, катализируемых солями висмута (III)». Synlett (5): 0631–0634. Дои:10.1055 / с-2003-38358.
- ^ Bandgar, B.P .; Маконе, С. С. (2004). «Катализируемый литием / перхлоратом натрия синтез симметричных диарилсульфоксидов». Синтетические коммуникации. 34 (4): 743–750. Дои:10.1081 / SCC-120027723.
- ^ Увидеть:
- Персоз; Блох (1849). "Des composés binaires formés par les métalloïdes, et, en speulier, de l'action du chlor phosphorique sur les acides sulfureux, sulfureique, phosphorique, chromique, и т. Д." [Бинарные соединения, образованные металлоидами, и в частности действие пентахлорида фосфора на сернистую кислоту, серную кислоту, фосфорную кислоту, хромовую кислоту и т. Д.]. Comptes rendus (На французском). 28: 86–88.
- Персоз; Блох (1849). "Добавление примечания к статье, касающейся комбинаций фосфорного хлорида с фосфорными, серными и сульфатными кислотами" [Дополнение к предыдущему примечанию относительно соединений пентахлорида фосфора с фосфорной кислотой, серной кислотой и сернистой кислотой]. Comptes rendus (На французском). 28: 389.
- ^ Кремерс, П. (1849). "Ueber schwefligsaures Phosphorchlorid" [О сернистом пентахлориде фосфора]. Annalen der Chemie und Pharmacie (на немецком). 70 (3): 297–300. Дои:10.1002 / jlac.18490700311.
- ^ Немецкий химик Георг Людвиг Кариус отметил, что, когда реакционная смесь, которая произвела тионилхлорид, была дистиллирована, сырая смесь первоначально выделяла значительные количества газа, так что фосфорилхлорид (POCl3) был перенесен в ствольную коробку. Кариус, Л. (1859 г.). "Ueber die Chloride des Schwefels und deren Derivate" [О хлориде серы и ее производных]. Annalen der Chemie und Pharmacie (на немецком). 111: 93–113. Дои:10.1002 / jlac.18591110111. С п. 94: «… Dabei ist jedoch die Vorsicht zu gebrauchen,… und nie reines Chlorthionyl erhalten wird». (… Однако во время этой [то есть фракционной перегонки] следует соблюдать осторожность, [чтобы] тщательно избегать концентрации хлористого водорода или избытка серной кислоты в жидкости, которая должна быть перегоняема, в противном случае, путем эволюции газа, который возникает в начале перегонки, переносится много фосфорилхлорида и чистый тионилхлорид никогда не получается.)
- ^ Шифф, Гюго (1857). "Ueber die Einwirkung des Phosphorsuperchlorids auf einige anorganische Säuren" [О реакции пентахлорида фосфора с некоторыми неорганическими кислотами]. Annalen der Chemie und Pharmacie (на немецком). 102: 111–118. Дои:10.1002 / jlac.18571020116. Температура кипения тионилхлорида, которую наблюдал Шифф, указана на стр. 112. Имя Тионилхлорид придуман на стр. 113.
- ^ Кариус, Л. (1859 г.). "Ueber die Chloride des Schwefels und deren Derivate" [О хлориде серы и ее производных]. Annalen der Chemie und Pharmacie (на немецком). 111: 93–113. Дои:10.1002 / jlac.18591110111. На стр. 94 Кариус отмечает, что тионилхлорид может быть «… Mit Vortheil zur Darstellung wasserfreier Säuren verwenden». (… Преимущественно используется для получения ангидридов кислот.) Также на стр. 94 Кариус показывает химические уравнения, в которых тионилхлорид используется для преобразования бензойная кислота (OC7ЧАС5OH) в бензоилхлорид (ClC7ЧАС5O) и преобразовать бензоат натрия в бензойный ангидрид. На стр. 96, он упоминает, что тионилхлорид преобразует метанол в метилхлорид (Хлорметил). Тионилхлорид ведет себя как фосфорилхлорид: с. 94-95: «Die Einwirkung des Chlorthionyls… die Reaction des Chlorthionyls weit heftiger statt». (Реакция тионилхлорида с [органическими] веществами, содержащими кислород, в целом протекает параллельно реакции фосфорилхлорида; там, где последний оказывает влияние, обычно действует и тионилхлорид, только почти во всех случаях реакция протекает гораздо более интенсивно.)


