Хлорид алюминия - Aluminium chloride
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК хлорид алюминия | |
| Другие имена хлорид алюминия (III) трихлорид алюминия | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.028.371 |
| Номер ЕС |
|
| 1876 | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| Характеристики | |
| AlCl3 | |
| Молярная масса | 133,341 г / моль (безводный) 241,432 г / моль (гексагидрат)[1] |
| Внешность | белое или бледно-желтое твердое вещество, гигроскопичный |
| Плотность | 2,48 г / см3 (безводный) 2,398 г / см3 (гексагидрат)[1] |
| Температура плавления | 192,6 ° С (378,7 ° F, 465,8 К) (безводный)[1] 100 ° С (212 ° F, 373 К) (гексагидрат, разл.)[1] |
| Точка кипения | 180 ° С (356 ° F, 453 К) (сублимированные)[1] |
| 439 г / л (0 ° С) 449 г / л (10 ° С) 458 г / л (20 ° С) 466 г / л (30 ° С) 473 г / л (40 ° С) 481 г / л (60 ° С) 486 г / л (80 ° С) 490 г / л (100 ° С) | |
| Растворимость | растворим в хлористом водороде, этаноле, хлороформе, четыреххлористом углероде слабо растворяется в бензоле |
| Давление газа | 133,3 Па (99 ° C) 13,3 кПа (151 ° C)[2] |
| Вязкость | 0,35 сП (197 ° C) 0,26 сП (237 ° С)[2] |
| Структура | |
| Моноклиника, mS16 | |
| С12 / м1, №12[3] | |
а = 0,591 нм, б = 0,591 нм, c = 1,752 нм[3] | |
Объем решетки (V) | 0,52996 нм3 |
Формула единиц (Z) | 6 |
| Октаэдрический (сплошной) Тетраэдр (жидкость) | |
| Тригональный планарный (мономерный пар) | |
| Термохимия | |
Теплоемкость (C) | 91,1 Дж / моль · К[4] |
Стандартный моляр энтропия (S | 109,3 Дж / моль · К[4] |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -704,2 кДж / моль[4] |
Свободная энергия Гиббса (Δжграмм˚) | -628,8 кДж / моль[4] |
| Фармакология | |
| D10AX01 (ВОЗ) | |
| Опасности | |
| Паспорт безопасности | Видеть: страница данных |
| Пиктограммы GHS |  [5] [5] |
| Сигнальное слово GHS | Опасность |
| H314[5] | |
| P280, P310, P305 + 351 + 338[5] | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | безводный: 380 мг / кг, крыса (перорально) гексагидрат: 3311 мг / кг, крыса (перорально) |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | никто[6] |
REL (Рекомендуемые) | 2 мг / м3[6] |
IDLH (Непосредственная опасность) | N.D.[6] |
| Родственные соединения | |
Другой анионы | Фторид алюминия Бромид алюминия Иодид алюминия |
Другой катионы | Трихлорид бора Трихлорид галлия Хлорид индия (III) Хлорид магния |
Связанный Кислоты Льюиса | Хлорид железа (III) Трифторид бора |
| Страница дополнительных данных | |
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ |
| УФ, ИК, ЯМР, РС | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорид алюминия (AlCl3), также известный как трихлорид алюминия, описать соединения с формулой AlCl3(ЧАС2O)п (n = 0 или 6). Они состоят из алюминий и хлор атомов в соотношении 1: 3, и одна форма также содержит шесть воды гидратации. Оба являются твердыми веществами белого цвета, но образцы часто загрязнены хлорид железа (III), давая желтый цвет.
Безводный материал имеет важное коммерческое значение. Он имеет низкие температуры плавления и кипения. В основном он производится и потребляется при производстве металлического алюминия, но в больших количествах он также используется в других областях химической промышленности.[7] Это соединение часто называют Кислота Льюиса. Это пример неорганическое соединение который обратимо меняется с полимер к мономер при умеренной температуре.
Использует
Алкилирование и ацилирование аренов
AlCl3 обычная кислота Льюиса катализатор за Реакции Фриделя – Крафтса, как ацилирование, так и алкилирование.[8] Важные продукты моющие средства и этилбензол. Эти типы реакций являются основным применением хлорида алюминия, например, при получении антрахинон (используется в красители промышленность) из бензол и фосген.[9] В общей реакции Фриделя – Крафтса ацилхлорид или же алкилгалогенид реагирует с ароматный система, как показано:[8]
В алкилирование реакция используется более широко, чем ацилирование реакция, хотя ее практика более сложна с технической точки зрения. Для обеих реакций хлорид алюминия, а также другие материалы и оборудование должны быть сухими, хотя для протекания реакции необходимо присутствие влаги.[нужна цитата ] Доступны подробные процедуры алкилирования.[10] и ацилирование[11][12] арен.
Общая проблема с реакцией Фриделя – Крафтса заключается в том, что катализатор хлорид алюминия иногда требуется полностью. стехиометрический количества, потому что это комплексы сильно с продуктами. Это осложнение иногда приводит к возникновению большого количества разъедающий напрасно тратить. По этим и подобным причинам хлорид алюминия часто заменяют цеолиты.[7]
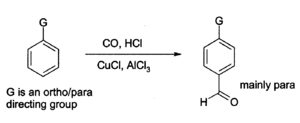
Хлорид алюминия также можно использовать для введения альдегид группы на ароматный кольца, например, через Реакция Гаттермана-Коха который использует монооксид углерода, хлористый водород и хлорид меди (I) сокатализатор.[13]
Другие применения в органическом и металлоорганическом синтезе
Хлорид алюминия находит множество других применений в органическая химия.[14] Например, он может катализировать "ее реакция ", например добавление 3-бутен-2-он (метилвинилкетон) в Carvone:[15]
Он используется для индукции различных углеводородных взаимодействий и перегруппировок.[16][17]
Хлорид алюминия в сочетании с алюминием в присутствии арена можно использовать для синтеза бис (арен) комплексов металлов, например бис (бензол) хром, из некоторых галогенидов металлов через так называемые Фишер -Синтез Хафнера. Дихлорфенилфосфин готовится по реакции бензол и трихлорид фосфора катализируется хлоридом алюминия.[18]
Структура
Безводный
AlCl3 принимает три структуры, в зависимости от температура и государственный (твердое, жидкое, газовое). Твердый AlCl3 представляет собой пластинчато-слоистые кубические плотноупакованные слои. В этом контексте центры Al демонстрируют октаэдрическая координационная геометрия.[19] Когда трихлорид алюминия находится в расплавленном состоянии, он существует в виде димер Al2Cl6, с четырехкоординатный алюминий. Это изменение структуры связано с более низкой плотностью жидкой фазы (1,78 г / см3) по сравнению с твердым трихлоридом алюминия (2,48 г / см3). Al2Cl6 димеры также встречаются в паровая фаза. При более высоких температурах Al2Cl6 димеры диссоциировать в тригонально плоский AlCl3, который структурно аналогичен BF3. Расплав проводит электричество плохо,[9] в отличие от более-ионный галогениды Такие как хлорид натрия.
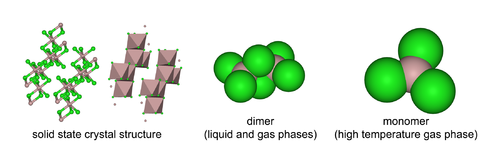
Мономер хлорида алюминия относится к точечной группе D3ч в мономерной форме и D2ч в димерной форме.
Гексагидрат
Гексагидрат состоит из восьмигранный [Al (H2O)6]3+ центры и хлорид противоионы. Водородные связи связать катион и анионы.[20]Гидратированная форма хлорида алюминия имеет октаэдрическую молекулярную геометрию с центральным ионом алюминия, окруженным шестью водный лиганд молекулы. Будучи координационно насыщенным, гидрат не представляет особой ценности в качестве катализатор в Алкилирование Фриделя-Крафтса и родственные реакции.
Реакции
Безводный хлорид алюминия - мощный Кислота Льюиса, способный образовывать кислотно-основную аддукты с даже слабым Базы Льюиса Такие как бензофенон и мезитилен.[8] Он образует тетрахлоралюминат (AlCl4−) в присутствии хлористый ионы.
Хлорид алюминия реагирует с кальций и гидриды магния в тетрагидрофуран с образованием тетрагидроалюминатов.
Реакции с водой
Безводный хлорид алюминия гигроскопичный, имеющий очень выраженное сродство к воде. Он дымится во влажном воздухе и шипит при смешивании с жидкой водой, поскольку Cl− лиганды замещаются H2Молекулы O с образованием гексагидрата [Al (H2O)6] Cl3 . Безводная фаза не может быть восстановлена при нагревании гексагидрата. Вместо этого HCl теряется, оставляя гидроксид алюминия или оксид алюминия (оксид алюминия):
- Al (H2O)6Cl3 → Al (OH)3 + 3 HCl + 3 H2О
Нравиться металлические акво комплексы, водный AlCl3 кислая из-за ионизации акво-лиганды:
- [Al (H2O)6]3+ ⇌ [Al (OH) (H2O)5]2+ + H+
Водные растворы ведут себя аналогично другим алюминий соли содержащий гидратированный Al3+ ионы, давая студенистую осадок из гидроксид алюминия при реакции с разбавленным едкий натр:
- AlCl3 + 3 NaOH → [Al (OH)3] + 3 NaCl
Синтез
Хлорид алюминия в больших объемах производится экзотермический реакция алюминий металл с хлором или хлористый водород при температуре от 650 до 750 ° C (от 1202 до 1382 ° F).[9]
- 2 Al + 3 Cl2 → 2 AlCl3
- 2 Al + 6 HCl → 2 AlCl3 + 3 часа2
Хлорид алюминия может быть образован реакция одиночного вытеснения между хлорид меди и алюминиевый металл.
- 2 Al + 3 CuCl2 → 2 AlCl3 + 3 Cu
В США в 1993 году было произведено около 21000 тонн, не считая количества, потребленного при производстве алюминия.[7]
Гидратированный трихлорид алюминия получают растворением оксидов алюминия в соляная кислота. Металлический алюминий также легко растворяется в соляной кислоте, выделяя газообразный водород и выделяя значительное количество тепла. При нагревании этого твердого вещества безводный трихлорид алюминия не образуется, гексагидрат разлагается на гидроксид алюминия при нагревании:
- Al (H2O)6Cl3 → Al (ОН)3 + 3 HCl + 3 H2О
Алюминий также образует нижний хлористый, хлорид алюминия (I) (AlCl), но это очень нестабильно и известно только в паровой фазе.[9]
Естественное явление
Безводное соединение сейчас среди минералов неизвестно. Однако гексагидрат известен как редкий минерал хлоралюминит.[21] Более сложный, основной и гидратированный минерал - кадваладерит.[22][21]
Безопасность
Безводный AlCl3 активно реагирует с базы, поэтому необходимы соответствующие меры предосторожности. Он может вызвать раздражение глаз, кожи и дыхательной системы при вдыхании или контакте.[23]
Смотрите также
Рекомендации
- ^ а б c d е Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 4.45. ISBN 1439855110.
- ^ а б Хлорид алюминия В архиве 2014-05-05 в Wayback Machine. Chemister.ru (19 марта 2007 г.). Проверено 17 марта 2017.
- ^ а б Кетелаар, Дж. А. А. (1935). "Die Kristallstruktur der Aluminiumhalogenide II". Zeitschrift für Kristallographie - Кристаллические материалы. 90 (1–6). Дои:10.1524 / zkri.1935.90.1.237. S2CID 100796636.
- ^ а б c d Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 5.5. ISBN 1439855110.
- ^ а б c Сигма-Олдрич Ко., Хлорид алюминия. Проверено 5 мая 2014.
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0024". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б c Гельмбольдт, Отто; Кейт Хадсон, L .; Мишра, Чанакья; Wefers, Карл; Черт возьми, Вольфганг; Старк, Ганс; Даннер, Макс; Рёш, Норберт (2007). «Соединения алюминия неорганические». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a01_527.pub2.
- ^ а б c Олах, Г.А., изд. (1963). Фриделя-Крафтса и родственные реакции. 1. Нью-Йорк: Interscience.
- ^ а б c d Гринвуд, Норман Н.; Эрншоу, Алан (1984). Химия элементов. Оксфорд: Pergamon Press. ISBN 978-0-08-022057-4.
- ^ Джонатан Т. Ривз1, Жулин Тан, Дэниел Р. Фандрик, Джинхуа Дж. Сон, Натан К. Йи, Крис Х. Сенанаяке (2012). «Синтез трифторметилкетонов из карбоновых кислот: 4- (3,4-дибромфенил) -1,1,1-трифтор-4-метилпентан-2-он». Органический синтез. 89: 210. Дои:10.15227 / orgsyn.089.0210.CS1 maint: несколько имен: список авторов (связь)
- ^ Камил Паруч; Libor Vyklicky; Томас Дж. Кац (2003). «Получение 9,10-диметоксифенантрена и 3,6-диацетил-9,10-диметоксифенантрена». Органический синтез. 80: 227. Дои:10.15227 / orgsyn.080.0227.
- ^ Александр Дж. Сид; Вайшали Сонпатки; Марк Р. Герберт (2002). «3- (4-Бромбензоил) пропановая кислота». Органический синтез. 79: 204. Дои:10.15227 / orgsyn.079.0204.
- ^ Уэйд, Л. Г. (2003) Органическая химия, 5-е издание, Prentice Hall, Река Аппер Сэдл, Нью-Джерси, Соединенные Штаты. ISBN 013033832X.
- ^ Галацис, П. (1999) Справочник реагентов для органического синтеза: кислотные и основные реагенты, Х. Дж. Райх, Дж. Х. Ригби (ред.) Wiley, Нью-Йорк. С. 12–15. ISBN 978-0-471-97925-8.
- ^ Снайдер, Б. Б. (1980). «Катализируемые кислотой Льюиса еновые реакции». Соотв. Chem. Res. 13 (11): 426. Дои:10.1021 / ar50155a007.
- ^ Рубен Д. Рике; Стивен Э. Бейлз; Филип М. Хадналл; Тимоти П. Бернс; Грэм С. Пойндекстер (1979). «Высокоактивный магний для приготовления реактивов Гриньяра: 1-норборнанкарбоновая кислота». Органический синтез. 59: 85. Дои:10.15227 / orgsyn.059.0085.
- ^ Сами А. Шама; Карл К. Вамсер (1983). «Гексаметил-бензол Дьюара». Органический синтез. 61: 62. Дои:10.15227 / orgsyn.061.0062.
- ^ Б. Бюхнер; Л. Б. Локхарт младший (1951). «Фенилдихлорфосфин». Органический синтез. 31: 88. Дои:10.15227 / orgsyn.031.0088.
- ^ Напротив, AlBr3 имеет более молекулярную структуру, с Al3+ центры, занимающие соседние тетраэдрические отверстия плотноупакованного каркаса Br− ионы. Уэллс, А. Ф. (1984) Структурная неорганическая химия, Oxford Press, Оксфорд, Объединенное Королевство. ISBN 0198553706.
- ^ Андресс, К.Р .; Карпентер, К. (1934). "Кристаллгидрат II. Die Struktur von Chromchlorid- und Aluminiumchloridhexahydrat". Zeitschrift für Kristallographie - Кристаллические материалы. 87. Дои:10.1524 / zkri.1934.87.1.446.
- ^ а б https://www.ima-mineralogy.org/Minlist.htm
- ^ https://www.mindat.org/min-845.html
- ^ Хлорид алюминия. solvaychemicals.us
внешняя ссылка
- Международная карта химической безопасности 1125
- Указатель процедур органического синтеза, в которых используется AlCl3
- Период 3 хлоридов
- MSDS
- Информационные бюллетени правительства Канады и часто задаваемые вопросы: соли алюминия