Гидрид диизобутилалюминия - Diisobutylaluminium hydride
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Диизобутилалюминий гидрид | |
| Другие имена ДИБАХ; ДИБАЛ; DiBAlH; ДИБАЛ-Н; ДИБАЛХ | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.391 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C8ЧАС19Al (мономер) C16ЧАС38Al2 (димер) | |
| Молярная масса | 142,22 г / моль (мономер) 284,44 г / моль (димер) |
| Внешность | Бесцветная жидкость |
| Плотность | 0,798 г / см3 |
| Температура плавления | -80 ° С (-112 ° F, 193 К) |
| Точка кипения | От 116 до 118 ° C (от 241 до 244 ° F, от 389 до 391 K) при 1 мм рт. |
| Бурно реагирует с водой | |
| Растворимость в углеводородных растворителях | Растворимый |
| Опасности | |
| Главный опасности | воспламеняется в воздухе |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| H220, H225, H250, H260, H314, H318 | |
| P210, P222, P223, P231 + 232, P233, P240, P241, P242, P243, P260, P264, P280, P301 + 330 + 331, P302 + 334, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P335 + 334, P363, P370 + 378, P377, P381, P402 + 404 | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
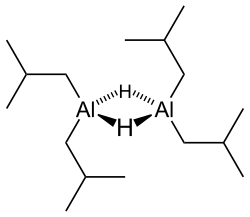
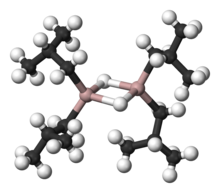
Гидрид диизобутилалюминия (ДИБАЛХ, ДИБАЛ, ДИБАЛ-Н или же ДИБА, /ˈdаɪбæл/ DY-бал ) это Восстановитель с формула (я-Bu2AlH)2, куда я-Bu представляет изобутил (-CH2CH (CH3)2). Этот алюминийорганическое соединение первоначально исследовалась как сокатализатор для полимеризация из алкены.[1]
Характеристики
Как и большинство алюминийорганических соединений, структура соединения, скорее всего, больше, чем предполагаемая его эмпирическая формула. Разнообразные техники, не считая Рентгеновская кристаллография, предполагаем, что соединение существует как димер и тример, состоящий из тетраэдрических центров алюминия, разделяющих мостиковую гидрид лиганды.[2] Гидриды малы и для производных алюминия очень базовый, поэтому они предпочитают мост алкил группы.
DIBAL можно приготовить путем нагревания триизобутилалюминий (сам по себе димер), чтобы вызвать устранение бета-гидрида:[3]
- (я-Bu3Al)2 → (я-Bu2AlH)2 + 2 (CH3)2C = CH2
Хотя DIBAL можно приобрести в коммерческих целях в виде бесцветной жидкости, его чаще всего покупают и отпускают в виде раствора в органическом растворителе, таком как толуол или же гексан.
Использование в органическом синтезе
DIBAL полезен в органический синтез для различных скидок, включая конвертацию карбоновые кислоты, их производные и нитрилы к альдегиды. DIBAL эффективно восстанавливает α-β ненасыщенные сложные эфиры до соответствующего аллилового спирта.[4] Напротив, LiAlH4 восстанавливает сложные эфиры и ацилхлориды к первичному спирты, и нитрилы к первичному амины [с использованием процедуры исследования Физера]. DIBAL медленно реагирует с соединениями, бедными электронами, и быстрее - с соединениями, богатыми электронами. Таким образом, это электрофильный восстановитель, тогда как LiAlH4 можно рассматривать как нуклеофильный Восстановитель.
Хотя DIBAL надежно восстанавливает нитрилы до альдегидов, восстановление сложных эфиров до одной и той же функциональной группы является печально известной реакцией, которая выглядит полезной на бумаге, но на практике часто приводит к смесям спирта и альдегида. Эта проблема была решена путем тщательного контроля условий реакции с использованием химии непрерывного потока.[5]
Безопасность
DIBAL, как и большинство соединений алкилалюминия, бурно реагирует с воздухом и водой, что может привести к пожару.
Рекомендации
- ^ Циглер, К.; Martin, H .; Крупп, Ф. (1960). "Metallorganische Verbindungen, XXVII Aluminiumtrialkyle und Dialkyl-Aluminiumhydride aus Aluminiumisobutyl-Verbindungen". Юстус Либигс Аннален дер Хеми. 629 (1): 14–19. Дои:10.1002 / jlac.19606290103.
- ^ Self, M. F .; Pennington, W. T .; Робинсон, Г. Х. (1990). «Реакция диизобутилалюминийгидрида с макроциклическим тетрадентатным вторичным амином. Синтез и молекулярная структура [Al (изо-Bu)]2[C10ЧАС20N4] [Al (изо-Bu)3]2: Свидетельства необычного диспропорционирования (изо-Bu)2AlH ». Неорганика Chimica Acta. 175 (2): 151–153. Дои:10.1016 / S0020-1693 (00) 84819-7.
- ^ Эйш, Дж. Дж. (1981). Металлоорганические синтезы. 2. Нью-Йорк: Academic Press. ISBN 0-12-234950-4.
- ^ Галацис, П. (2001). «Гидрид диизобутилалюминия». Энциклопедия реагентов для органического синтеза. Нью-Йорк: Джон Вили и сыновья. Дои:10.1002 / 047084289X.rd245. ISBN 0471936235.
- ^ Уэбб, Дэмиен; Джеймисон, Тимоти Ф. (20 января 2012 г.). «Восстановленное восстановление диизобутилалюминийгидрида: быстрая, надежная и селективная система непрерывного потока для синтеза альдегида». Органические буквы. 14 (2): 568–571. Дои:10.1021 / ol2031872. HDL:1721.1/76286. ISSN 1523-7060. PMID 22206502.
внешняя ссылка
- Штокман, Р. (2001). «Дибал-восстановление метилового эфира, производного от аминокислоты; альдегид Гарнера». Синтетические страницы ChemSpider. Дои:10.1039 / SP161. Synthetic Страница 161.[постоянная мертвая ссылка ]
- «Реакции окисления и восстановления в органической химии». Университет Южного Мэна, факультет химии. Архивировано из оригинал 11 июня 2011 г.
- «Диизобутилалюминийгидрид (DIBAL-H) и другие изобутилалюминиевые алкилы (DIBAL-BOT, TIBAL) в качестве специальных реагентов для органического синтеза» (PDF). Акзо-Нобель. Архивировано из оригинал (PDF) на 2011-04-08. Получено 2011-02-23.
