Литий-алюминиевый гидрид - Lithium aluminium hydride
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Тетрагидридоалюминат лития (III) | |||
| Систематическое название ИЮПАК Литий алюмогидрат | |||
| Другие имена Литий-алюминиевый гидрид Литал | |||
| Идентификаторы | |||
| |||
3D модель (JSmol ) | |||
| Сокращения | LAH | ||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.037.146 | ||
| Номер ЕС |
| ||
| 13167 | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| LiAlH4 | |||
| Молярная масса | 37,95 г / моль | ||
| Внешность | белые кристаллы (чистые образцы) серый порошок (товарный материал) гигроскопичный | ||
| Запах | без запаха | ||
| Плотность | 0,917 г / см3, твердый | ||
| Температура плавления | 150 ° С (302 ° F, 423 К) (разлагается) | ||
| Реагирует | |||
| Растворимость в тетрагидрофуран | 112,332 г / л | ||
| Растворимость в диэтиловый эфир | 39,5 г / 100 мл | ||
| Структура | |||
| моноклинический | |||
| п21/c | |||
| Термохимия | |||
Теплоемкость (C) | 86,4 Дж / моль К | ||
Стандартный моляр энтропия (S | 87,9 Дж / моль К | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -117 кДж / моль | ||
Свободная энергия Гиббса (Δжграмм˚) | -48,4 кДж / моль | ||
| Опасности[2] | |||
| Паспорт безопасности | Литий-алюминиевый гидрид | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H260, H314 | |||
| P223, P231 + 232, P280, P305 + 351 + 338, P370 + 378, P422[1] | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 125 ° С (257 ° F, 398 К) | ||
| Родственные соединения | |||
Связанный гидрид | гидрид алюминия борогидрид натрия гидрид натрия Алюминий гидрид натрия | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Литий-алюминиевый гидрид, обычно сокращенно LAH, является неорганическое соединение с химическая формула ЛиAlЧАС4. Это серое твердое вещество. Его обнаружили Финхольт, Бонд и Шлезингер в 1947 году.[4] Это соединение используется как Восстановитель в органический синтез, особенно для уменьшения сложные эфиры, карбоновые кислоты, и амиды. Твердое вещество опасно реагирует с водой, выделяя газообразные водород (ЧАС2). Некоторые родственные производные обсуждались для хранение водорода.
Свойства, состав, подготовка

LAH - бесцветное твердое вещество, но коммерческие образцы обычно имеют серый цвет из-за загрязнения.[5] Этот материал можно очистить перекристаллизацией из диэтиловый эфир. В крупномасштабных очистках используется Экстрактор Сокслета. Обычно нечистый серый материал используется в синтезе, поскольку примеси безвредны и могут быть легко отделены от органических продуктов. Чистый порошкообразный материал пирофорный, но не его крупные кристаллы.[6] Некоторые коммерческие материалы содержат минеральное масло для подавления реакций с атмосферной влагой, но чаще его упаковывают во влагонепроницаемые пластиковые мешки.[7]
LAH бурно реагирует с водой, в том числе с атмосферной влагой. Реакция протекает по следующему идеализированному уравнению:[5]
- LiAlH4 + 4 часа2О → LiOH + Al (ОН)3 + 4 часа2
Эта реакция представляет собой полезный метод получения водорода в лаборатории. Старые образцы, подвергшиеся воздействию воздуха, часто кажутся белыми, потому что они впитали достаточно влаги для образования смеси белых соединений. гидроксид лития и гидроксид алюминия.[8]
Структура
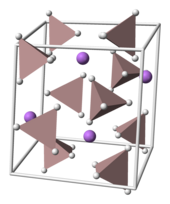
ЛАГ кристаллизуется в моноклинический космическая группа п21/c. В ячейка имеет размеры: а = 4.82, б = 7,81 и c = 7,92 Å, α = γ = 90 ° и β = 112 °. В структуре Ли+ центры окружены пятью AlH−
4 тетраэдры. Ли+ центры связаны с одним водород атом от каждого из окружающих тетраэдров, создавая бипирамида расположение. При высоких давлениях (> 2,2 ГПа) может происходить фазовый переход с образованием β-LAH.[9]
Подготовка
LiAlH4 был впервые приготовлен из реакции между гидрид лития (LiH) и хлорид алюминия:[4][5]
- 4 LiH + AlCl3 → LiAlH4 + 3 LiCl
Помимо этого метода, промышленный синтез включает в себя первоначальную подготовку алюмогидрид натрия от элементов, находящихся под высоким давлением и температурой:[10]
- Na + Al + 2 H2 → NaAlH4
LiAlH4 затем готовится реакция метатезиса солей в соответствии с:
- NaAlH4 + LiCl → LiAlH4 + NaCl
который идет с высокой доходностью. LiCl удаляется фильтрация из эфирный раствор LAH с последующим осаждением LiAlH4 чтобы получить продукт, содержащий около 1% ш/ш LiCl.[10]
Альтернативное получение начинается с LiH, а металлический Al вместо AlCl.3. Катализируется небольшим количеством TiCl3 (0,2%) реакция идет хорошо при использовании диметиловый эфир как растворитель. Этот метод позволяет избежать образования соли.[11]
Данные о растворимости
| Растворитель | Температура (° C) | ||||
|---|---|---|---|---|---|
| 0 | 25 | 50 | 75 | 100 | |
| Диэтиловый эфир | – | 5.92 | – | – | – |
| THF | – | 2.96 | – | – | – |
| Моноглим | 1.29 | 1.80 | 2.57 | 3.09 | 3.34 |
| Диглим | 0.26 | 1.29 | 1.54 | 2.06 | 2.06 |
| Триглим | 0.56 | 0.77 | 1.29 | 1.80 | 2.06 |
| Тетраглим | 0.77 | 1.54 | 2.06 | 2.06 | 1.54 |
| Диоксан | – | 0.03 | – | – | – |
| Дибутиловый эфир | – | 0.56 | – | – | – |
ЛАГ растворим во многих эфирный решения. Однако он может самопроизвольно разлагаться из-за присутствия каталитических примесей, хотя, по-видимому, он более стабилен в тетрагидрофуран (THF). Таким образом, ТГФ предпочтительнее, например, диэтиловый эфир, несмотря на меньшую растворимость.[12]
Термодинамические данные
В таблице приведены термодинамический данные для LAH и реакций с участием LAH,[13][14] в виде стандарт энтальпия, энтропия, и Свободная энергия Гиббса поменять соответственно.
| Реакция | ΔH ° (кДж / моль) | ΔS ° (Дж / (моль · К)) | ΔG ° (кДж / моль) | Комментарий |
|---|---|---|---|---|
| Li (s) + Al (s) + 2 H2(г) → LiAlH4 (s) | −116.3 | −240.1 | −44.7 | Стандартное формирование из элементов. |
| LiH (s) + Al (s) +3⁄2 ЧАС2 (г) → LiAlH4 (s) | −95.6 | −180.2 | 237.6 | Используя ΔH °ж(LiH) = -90,579865, ΔS °ж(LiH) = -679,9, а ΔG °ж(LiH) = -67,31235744. |
| LiAlH4 (т) → LiAlH4 (l) | 22 | – | – | Теплота плавления. Стоимость может быть ненадежной. |
| LiAlH4 (l) →1⁄3 Ли3AlH6 (s) +2⁄3 Al (s) + H2 (грамм) | 3.46 | 104.5 | −27.68 | ΔS ° рассчитывается на основе заявленных значений ΔH ° и ΔG °. |
Термическое разложение
LAH - это метастабильный при комнатной температуре. При длительном хранении медленно разлагается до Li.3AlH6 и LiH.[15] Этот процесс может быть ускорен наличием каталитический элементы, такие как титан, утюг или же ванадий.

При нагревании ЛАГ разлагается в три этапа. механизм реакции:[15][16][17]
- 3 LiAlH4 → Ли3AlH6 + 2 Al + 3 H2
(R1)
- 2 Ли3AlH6 → 6 LiH + 2 Al + 3 H2
(R2)
- 2 LiH + 2 Al → 2 LiAl + H2
(R3)
R1 обычно инициируется таяние ЛАГ в диапазоне температур 150–170 ° С,[18][19][20] сразу с последующим распадом на твердый Li3AlH6, несмотря на то что R1 как известно, происходит ниже точки плавления LiAlH4 также.[21] Примерно при 200 ° C Li3AlH6 распадается на LiH (R2)[15][17][20] и Al, которые впоследствии превращаются в LiAl при температуре выше 400 ° C (R3).[17] Реакция R1 фактически необратима. R3 является обратимым при равновесном давлении около 0,25 бар при 500 ° C. R1 и R2 может происходить при комнатной температуре с подходящими катализаторами.[22]
Приложения
Использование в органической химии
Литийалюминийгидрид широко используется в органической химии в качестве Восстановитель.[5] Он более мощный, чем родственный реагент борогидрид натрия из-за более слабой связи Al-H по сравнению со связью B-H.[23] Часто как решение в диэтиловый эфир и после кислотной обработки он преобразует сложные эфиры, карбоновые кислоты, ацилхлориды, альдегиды, и кетоны в соответствующий спирты (видеть: восстановление карбонила ). Точно так же он преобразует амид,[24][25] нитро, нитрил, я добываю, оксим,[26] и азид соединения в амины (видеть: восстановление амида ). Это уменьшает катионы четвертичного аммония в соответствующие третичные амины. Реактивность можно регулировать путем замены гидридных групп. алкоксигруппами. В связи с его пирофорной природой, нестабильностью, токсичностью, малым сроком хранения и проблемами обращения, связанными с его реакционной способностью, в последнее десятилетие он был заменен как в мелком промышленном масштабе, так и для крупномасштабного восстановления более удобным соответствующим реагентом. бис (2-метоксиэтокси) алюминия гидрид натрия, который демонстрирует аналогичную реактивность, но с более высокой безопасностью, более простым обращением и лучшей экономичностью.[27]
LAH чаще всего используется для уменьшения сложные эфиры[28][29] и карбоновые кислоты[30] к первичным спиртам; до появления LiAlH4 это было трудное преобразование с участием натрий металл в кипении этиловый спирт (в Редукция Буво-Блана ). Альдегиды и кетоны[31] также может быть восстановлен до спиртов с помощью LAH, но обычно это делается с использованием более мягких реагентов, таких как NaBH4; α, β-ненасыщенные кетоны восстанавливаются до аллиловых спиртов.[32] Когда эпоксиды уменьшаются при использовании LAH, реагент атакует меньше затрудненный конец эпоксида, обычно производящий вторичный или третичный спирт. Эпоксициклогексаны восстанавливаются с образованием предпочтительно аксиальных спиртов.[33]
Частичное сокращение хлорангидриды с образованием соответствующего альдегидного продукта не может происходить через LAH, поскольку последний полностью восстанавливается до первичного спирта. Вместо этого более мягкий литийалюминий три (трет-бутокси) гидрид, который вступает в реакцию с хлорангидридом значительно быстрее, чем с альдегидом. Например, когда изовалериановая кислота лечится с тионилхлорид чтобы получить изовалероилхлорид, его затем можно восстановить с помощью три (трет-бутокси) гидрида лития-алюминия с получением изовалеральдегида с выходом 65%.[34]

Литийалюминийгидрид также снижает алкилгалогениды к алканы.[35][36] Быстрее всего реагируют алкилйодиды, затем идут алкилбромиды и затем алкилхлориды. Первичные галогениды являются наиболее реактивными, за ними следуют вторичные галогениды. Третичные галогениды реагируют только в определенных случаях.[37]
Литийалюминийгидрид не восстанавливает простой алкены или же арены. Алкины уменьшаются только в том случае, если рядом находится алкогольная группа.[38]Было обнаружено, что LiAlH4 восстанавливает двойную связь в N-аллиламидах.[39]
Неорганическая химия
LAH широко используется для подготовки основной группы и перехода гидриды металлов из соответствующего металла галогениды. Например, гидрид натрия (NaH) можно получить из хлорид натрия (NaCl) через следующую реакцию:[13]
- LiAlH4 + 4 NaCl → 4 NaH + LiCl + AlCl3
LAH также реагирует со многими неорганическими лигандами с образованием координированных комплексов оксида алюминия, связанных с ионами лития.[13]
- LiAlH4 + 4NH3 → Li [Al (NH2)4] + 4H2
Хранение водорода

LiAlH4 содержит 10,6 мас.% водорода, что делает ЛАГ потенциальным хранение водорода среда для будущего топливная ячейка -приведенный автомобили. Высокое содержание водорода, а также открытие обратимого накопления водорода в NaAlH, легированном титаном.4,[40] вызвали возобновление исследований LiAlH4 в течение последнего десятилетия. Значительные исследовательские усилия были посвящены ускорению кинетики разложения каталитическим легированием и шаровая мельница.[41]Чтобы воспользоваться преимуществом общей водородной емкости, промежуточное соединение LiH также должны быть дегидрированы. Из-за его высокой термодинамической стабильности для этого требуются температуры выше 400 ° C, что считается неприемлемым для транспортных целей. Принимая LiH + Al в качестве конечного продукта, емкость хранения водорода снижается до 7,96 мас.%. Еще одна проблема, связанная с хранением водорода, - это возврат в LiAlH.4 который из-за его относительно низкой стабильности требует чрезвычайно высокого давления водорода, превышающего 10000 бар.[41] Цикл только реакции R2, то есть с использованием Li3AlH6 в качестве исходного материала - будет хранить 5,6 мас.% водорода за одну стадию (по сравнению с двумя стадиями для NaAlH4 в котором хранится примерно такое же количество водорода). Однако попытки этого процесса пока не увенчались успехом.[нужна цитата ]
Другие тетрагидридоалюминийаты
Известно множество солей, аналогичных LAH. Неа можно использовать для эффективного производства алюмогидрид натрия (NaAlH4) к метатезис в THF:
- LiAlH4 + NaH → NaAlH4 + LiH
Гидрид алюминия калия (KAlH4) можно получить аналогично в диглим в качестве растворителя:[42]
- LiAlH4 + KH → KAlH4 + LiH
Обратное, т.е. получение ЛАГ из алюмогидрида натрия или алюмогидрида калия может быть достигнуто путем реакции с LiCl или гидрид лития в диэтиловый эфир или же THF:[42]
- NaAlH4 + LiCl → LiAlH4 + NaCl
- KAlH4 + LiCl → LiAlH4 + KCl
«Аланат магния» (Mg (AlH4)2) возникает аналогично при использовании MgBr2:[43]
- 2 LiAlH4 + MgBr2 → Mg (AlH4)2 + 2 LiBr
Red-Al (или SMEAH, NaAlH2(OC2ЧАС4ОСН3)2) синтезируется реакцией тетрагидрида алюминия натрия (NaAlH4) и 2-метоксиэтанол:[44]
Смотрите также
Рекомендации
- ^ Сигма-Олдрич Ко., Литий-алюминиевый гидрид. Проверено 1 июня 2018.
- ^ Индекс № 001-002-00-4 Приложения VI, Часть 3, к Регламент (ЕС) № 1272/2008 Европейского парламента и Совета от 16 декабря 2008 г. о классификации, маркировке и упаковке веществ и смесей, изменяющий и отменяющий Директивы 67/548 / EEC и 1999/45 / EC, и изменяющий Регламент (ЕС) № 1907/2006. OJEU L353, 31.12.2008, стр. 1–1355, стр. 472.
- ^ Литий-алюминиевый гидрид
- ^ а б Finholt, A.E .; Bond, A.C .; Шлезингер, Х. И. (1947). «Литий-алюминиевый гидрид, алюминиевый гидрид и литий-галлий гидрид и некоторые их применения в органической и неорганической химии». Журнал Американского химического общества. 69 (5): 1199–1203. Дои:10.1021 / ja01197a061.
- ^ а б c d Gerrans, G.C .; Хартманн-Петерсен, П. (2007). «Литий-алюминиевый гидрид». Энциклопедия науки и технологий Sasol. Новые книги Африки. п. 143. ISBN 978-1-86928-384-1.
- ^ Keese, R .; Brändle, M .; Тубе, Т. П. (2006). Практический органический синтез: руководство для студентов. Джон Уайли и сыновья. п.134. ISBN 0-470-02966-8.
- ^ Андреасен, А .; Vegge, T .; Педерсен, А. С. (2005). «Кинетика дегидрирования LiAlH как полученного, так и измельченного в шаровой мельнице.4" (PDF). Журнал химии твердого тела. 178 (12): 3672–3678. Bibcode:2005JSSCh.178.3672A. Дои:10.1016 / j.jssc.2005.09.027. Архивировано из оригинал (PDF) на 2016-03-03. Получено 2010-05-07.
- ^ Поханиш, Р. П. (2008). Справочник Ситтига по токсичным и опасным химическим веществам и канцерогенам (5-е изд.). Издательство Уильям Эндрю. п. 1540. ISBN 978-0-8155-1553-1.
- ^ Løvvik, O.M .; Опалка, С. М .; Brinks, H.W .; Хаубак, Б. С. (2004). «Кристаллическая структура и термодинамическая стабильность аланатов лития LiAlH.4 и Ли3AlH6". Физический обзор B. 69 (13): 134117. Bibcode:2004ПхРвБ..69м4117Л. Дои:10.1103 / PhysRevB.69.134117.
- ^ а б Холлеман, А. Ф., Виберг, Э., Виберг, Н. (2007). Lehrbuch der Anorganischen Chemie (102-е изд.). де Грюйтер. ISBN 978-3-11-017770-1.CS1 maint: несколько имен: список авторов (связь)
- ^ Сянфэн, Лю; Langmi, Henrietta W .; Макгрэйди, Дж. Шон; Крейг, М. Дженсен; Битти, Шейн Д .; Азенви, Феликс Ф. (2011). "Ti-легированный LiAlH4 для хранения водорода: синтез, загрузка катализатора и циклические характеристики ». Варенье. Chem. Soc. 133 (39): 15593–15597. Дои:10.1021 / ja204976z. PMID 21863886.
- ^ а б Михеева, В. И .; Трояновская, Е. А. (1971). «Растворимость литийалюминийгидрида и боргидрида лития в диэтиловом эфире». Вестник АН СССР. Отделение химических наук.. 20 (12): 2497–2500. Дои:10.1007 / BF00853610.
- ^ а б c Патнаик, П. (2003). Справочник неорганических химикатов. Макгроу-Хилл. п.492. ISBN 978-0-07-049439-8.
- ^ Smith, M. B .; Басс, Г. Э. (1963). «Теплота и свободная энергия образования щелочных гидридов алюминия и гидрида цезия». Журнал химических и технических данных. 8 (3): 342–346. Дои:10.1021 / je60018a020.
- ^ а б c Дымова Т. Н .; Александров, Д.П .; Коноплев, В. Н .; Силина, Т. А .; Сизарева; А.С. (1994). Российский журнал координационной химии. 20: 279. Отсутствует или пусто
| название =(помощь) - ^ Дилтс, Дж. А .; Эшби, Э. С. (1972). «Термическое разложение сложных гидридов металлов». Неорганическая химия. 11 (6): 1230–1236. Дои:10.1021 / ic50112a015.
- ^ а б c Blanchard, D .; Brinks, H .; Hauback, B .; Норби, П. (2004). «Десорбция LiAlH4 с добавками на основе Ti и V ». Материаловедение и инженерия B. 108 (1–2): 54–59. Дои:10.1016 / j.mseb.2003.10.114.
- ^ Chen, J .; Курияма, Н .; Xu, Q .; Takeshita, H.T .; Сакаи, Т. (2001). «Обратимое хранение водорода с помощью LiAlH, катализируемого титаном.4 и Ли3AlH6". Журнал физической химии B. 105 (45): 11214–11220. Дои:10.1021 / jp012127w.
- ^ Balema, V .; Печарский, В. К .; Деннис, К. В. (2000). «Твердотельные фазовые превращения в LiAlH.4 при высокоэнергетическом фрезеровании шаров ". Журнал сплавов и соединений. 313 (1–2): 69–74. Дои:10.1016 / S0925-8388 (00) 01201-9.
- ^ а б Андреасен, А. (2006). «Влияние легирования титаном на кинетические параметры дегидрирования алюмогидрида лития». Журнал сплавов и соединений. 419 (1–2): 40–44. Дои:10.1016 / j.jallcom.2005.09.067.
- ^ Андреасен, А .; Педерсен, А. С .; Вегге, Т. (2005). «Кинетика дегидрирования LiAlH как полученного, так и измельченного в шаровой мельнице.4". Журнал химии твердого тела. 178 (12): 3672–3678. Bibcode:2005JSSCh.178.3672A. Дои:10.1016 / j.jssc.2005.09.027.
- ^ Balema, V .; Wiench, J. W .; Деннис, К. В .; Пруски, М .; Печарский, В. К. (2001). «Твердотельные превращения, катализируемые титаном в LiAlH.4 Во время высокоэнергетического фрезерования шаров ". Журнал сплавов и соединений. 329 (1–2): 108–114. Дои:10.1016 / S0925-8388 (01) 01570-5.
- ^ Браун, Х.С. (1951). «Восстановления алюмогидридом лития». Органические реакции. 6: 469. Дои:10.1002 / 0471264180.or006.10. ISBN 0471264180.
- ^ Seebach, D .; Калиновский, Х.-О .; Langer, W .; Crass, G .; Вилька, Э.-М. (1991). «Хиральная среда для асимметричной индукции растворителем. (S, S) - (+) -1,4-бис (диметиламино) -2,3-диметоксибутан из (R, R) - (+) -диэтилтартрата». Органический синтез.; Коллективный объем, 7, п. 41 год
- ^ Park, C.H .; Симмонс, Х. Э. (1974). «Макроциклические диимины: 1,10-диазациклооктадекан». Органический синтез. 54: 88.; Коллективный объем, 6, п. 382
- ^ Chen, Y.K .; Jeon, S.J .; Уолш, П. Дж .; Наджент, В. А. (2005). «(2S) - (-) - 3-экзо- (морфолино) изоборнеол». Органический синтез. 82: 87.
- ^ "Red-Al, бис (2-метоксиэтокси) алюмогидрид натрия". Портал органической химии.
- ^ Reetz, M. T .; Drewes, M. W .; Швикарди, Р. (1999). «Получение энантиомерно чистых α-N, N-дибензиламиноальдегидов: S-2- (N, N-дибензиламино) -3-фенилпропаналя». Органический синтез. 76: 110.; Коллективный объем, 10, п. 256
- ^ Oi, R .; Шарплесс, К. Б. (1996). «3 - [(1S) -1,2-дигидроксиэтил] -1,5-дигидро-3H-2,4-бензодиоксепин». Органический синтез. 73: 1.; Коллективный объем, 9, п. 251
- ^ Koppenhoefer, B .; Шуриг В. (1988). «(R) -Алкилоксираны высокой энантиомерной чистоты из (S) -2-хлоралкановой кислоты через (S) -2-хлор-1-алканолы: (R) -метилоксиран». Органический синтез. 66: 160.; Коллективный объем, 8, п. 434
- ^ Barnier, J. P .; Чемпион, J .; Кониа, Дж. М. (1981). «Циклопропанкарбоксальдегид». Органический синтез. 60: 25.; Коллективный объем, 7, п. 129
- ^ Эльфимофф-Фелкин, И .; Сарда, П. (1977). «Восстановительное расщепление аллиловых спиртов, простых эфиров или ацетатов до олефинов: 3-метилциклогексен». Органический синтез. 56: 101.; Коллективный объем, 6, п. 769
- ^ Rickborn, B .; Куартуччи, Дж. (1964). «Стереохимия и механизм восстановления алюмогидрида лития и смешанного гидрида 4-т-Бутилциклогексеноксид ». Журнал органической химии. 29 (11): 3185–3188. Дои:10.1021 / jo01034a015.
- ^ Уэйд, Л. Г. младший (2006). Органическая химия (6-е изд.). Пирсон Прентис Холл. ISBN 0-13-147871-0.
- ^ Johnson, J. E .; Blizzard, R.H .; Кархарт, Х. В. (1948). «Гидрогенолиз алкилгалогенидов алюмогидридом лития». Журнал Американского химического общества. 70 (11): 3664–3665. Дои:10.1021 / ja01191a035. PMID 18121883.
- ^ Krishnamurthy, S .; Браун, Х.С. (1982). «Селективное восстановление. 28. Быстрая реакция литийалюминийгидрида с алкилгалогенидами в ТГФ. Переоценка объема реакции». Журнал органической химии. 47 (2): 276–280. Дои:10.1021 / jo00341a018.
- ^ Каррутерс, В. (2004). Некоторые современные методы органического синтеза. Издательство Кембриджского университета. п. 470. ISBN 0-521-31117-9.
- ^ Wender, P.A .; Холт, Д. А .; Зибурт, С. Мак Н. (1986). «2-Алкенилкарбинолы из 2-галогенкетонов: 2-Е-пропенилциклогексанол». Органический синтез. 64: 10.; Коллективный объем, 7, п. 456
- ^ Thiedemann, B .; Schmitz, C.M .; Стаубиц А. (2014). «Восстановление N-аллиламидов с помощью LiAlH4: неожиданная атака двойной связи с механистическими исследованиями образования продуктов и побочных продуктов». Журнал органической химии. 79 (21): 10284–95. Дои:10.1021 / jo501907v. PMID 25347383.
- ^ Богданович, Б .; Швикарди, М. (1997). «Легированные титаном алюминиевые гидриды щелочных металлов как потенциальные новые материалы для обратимого хранения водорода». Журнал сплавов и соединений. 253–254: 1–9. Дои:10.1016 / S0925-8388 (96) 03049-6.
- ^ а б Варин, Р.А.; Czujko, T .; Вронски, З. С. (2009). Наноматериалы для твердотельного хранения водорода (5-е изд.). Springer. п. 338. ISBN 978-0-387-77711-5.
- ^ а б Santhanam, R .; Макгрэйди, Г.С. (2008). «Синтез гексагидроалюминатных комплексов щелочных металлов с использованием диметилового эфира в качестве реакционной среды». Неорганика Chimica Acta. 361 (2): 473–478. Дои:10.1016 / j.ica.2007.04.044.
- ^ Wiberg, E .; Wiberg, N .; Холлеман, А. Ф. (2001). Неорганическая химия. Академическая пресса. п. 1056. ISBN 0-12-352651-5.
- ^ Казенский, Б .; Machacek, J .; Абрахам, К. (1971). «Химия гидридов алкоксиалюминия натрия. I. Синтез бис (2-метоксиэтокси) алюмогидрида натрия». Сборник чехословацких химических сообщений. 36 (7): 2648–2657. Дои:10.1135 / cccc19712648.
дальнейшее чтение
- Wiberg, E .; Амбергер, Э. (1971). Гидриды элементов I-IV основных групп.. Эльзевир. ISBN 0-444-40807-X.
- Хаджос, А. (1979). Комплексные гидриды и родственные восстановители в органическом синтезе. Эльзевир. ISBN 0-444-99791-1.
- Лиде, Д. Р., изд. (1997). Справочник по химии и физике. CRC Press. ISBN 0-8493-0478-4.
- Кэри, Ф.А. (2002). Органическая химия с онлайн-центром обучения и обучение с помощью модельного компакт-диска. Макгроу-Хилл. ISBN 0-07-252170-8.
- Андреасен, А. (2005). «Глава 5: Комплексные гидриды» (PDF). Материалы для хранения водорода с акцентом на элементы основных групп I-II. Национальная лаборатория Рисё. ISBN 87-550-3498-5. Архивировано из оригинал (PDF) на 19.08.2012.
внешняя ссылка
- "Использование LiAlH4". Органический синтез.
- «Тетрагидридоалюминат лития - Резюме соединений (CID 28112)». PubChem.
- «Тетрагидридоалюминат лития». Интернет-книга. NIST.
- «Паспорт безопасности материалов». Корнелл Университет. Архивировано из оригинал 8 марта 2006 г.
- «Гидридный информационный центр». Сандийская национальная лаборатория. Архивировано из оригинал 7 мая 2005 г.
- «Реакции восстановления» (PDF). Учебные ресурсы - 4-й год. Бирмингемский университет. Архивировано из оригинал (PDF) 23 мая 2016 года.



