Механизм реакции - Reaction mechanism
В химия, а механизм реакции шаг за шагом последовательность из элементарные реакции по которому в целом химический происходит изменение.[1]
Химический механизм - это теоретическая гипотеза, которая пытается подробно описать, что происходит на каждой стадии общей химической реакции. Подробные шаги реакции в большинстве случаев не наблюдаются. Предполагаемый механизм выбран потому, что он термодинамически осуществим и имеет экспериментальное подтверждение в виде изолированных промежуточных продуктов (см. Следующий раздел) или других количественных и качественных характеристик реакции. Он также описывает каждый реактивный промежуточный продукт, активированный комплекс, и переходное состояние, и какие связи разорваны (и в каком порядке), и какие связи образуются (и в каком порядке). Полный механизм должен также объяснить причину реагенты и катализатор использованный, стереохимия наблюдается в реагентах и продуктах, все товары сформировано и количество каждого.

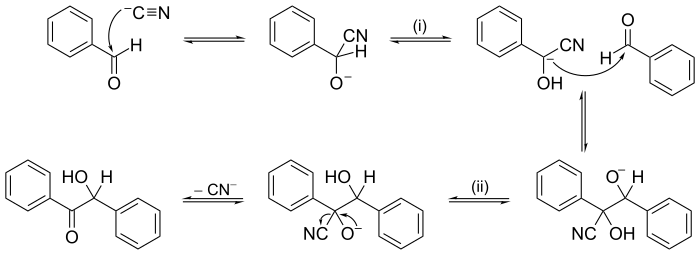
В электрон или стрелка метод часто используется для иллюстрации механизма реакции; например, см. иллюстрацию механизма для бензоиновая конденсация в следующем разделе примеров.
Механизм реакции также должен учитывать порядок, в котором реагируют молекулы. Часто то, что кажется одностадийным превращением, на самом деле является многоступенчатой реакцией.
Промежуточные продукты реакции
Промежуточные продукты реакции представляют собой химические соединения, часто нестабильные и недолговечные (однако иногда их можно выделить), которые не являются реагентами или продуктами общей химической реакции, а являются временными продуктами и / или реагентами на стадиях реакции механизма. Промежуточные продукты реакции часто свободные радикалы или же ионы.
Кинетика (относительные скорости стадий реакции и уравнение скорости для реакции в целом) объясняются с точки зрения энергии, необходимой для превращения реагентов в предложенные переходные состояния (молекулярные состояния, которые соответствуют максимумам на координаты реакции, и чтобы седловые точки на поверхность потенциальной энергии для реакции).
Химическая кинетика
Информация о механизме реакции часто предоставляется с помощью химическая кинетика определить уравнение скорости и порядок реакции в каждом реагенте.[2]
Рассмотрим, например, следующую реакцию:
- CO + NO2 → CO2 + НЕТ
В этом случае эксперименты определили, что эта реакция протекает согласно тарифный закон . Эта форма предполагает, что этап определения ставки реакция между двумя молекулами NO2. Возможный механизм общей реакции, объясняющий закон скорости:
- 2 НЕТ2 → НЕТ3 + НЕТ (медленно)
- НЕТ3 + CO → НЕТ2 + CO2 (быстрый)
Каждый шаг называется элементарным, и у каждого свой тарифный закон и молекулярность. Элементарные шаги должны составлять исходную реакцию. (Это означает, что если бы мы отменили все молекулы, которые появляются по обе стороны от реакции, мы остались бы с исходной реакцией.)
При определении общего закона скорости реакции самым медленным шагом является шаг, определяющий скорость реакции. Поскольку первый шаг (в приведенной выше реакции) самый медленный, это этап определения ставки. Потому что это столкновение двух НЕТ2 молекул, это бимолекулярная реакция со скоростью который подчиняется закону скорости .
Другие реакции могут иметь механизмы из нескольких последовательных этапов. В органическая химия, механизм реакции для бензоиновая конденсация, выдвинутый в 1903 г. А. Дж. Лэпворт, был одним из первых предложенных механизмов реакции.
А цепная реакция является примером сложного механизма, в котором распространение шаги образуют замкнутый цикл.
Другие экспериментальные методы определения механизма
Много эксперименты которые предполагают возможную последовательность шагов в механизме реакции, были разработаны, включая:
- измерение влияния температуры (Уравнение Аррениуса ) для определения энергия активации[3]
- спектроскопический наблюдение за промежуточные продукты реакции
- определение стереохимия продуктов, например в нуклеофильное замещение реакции[4]
- измерение эффекта изотопное замещение от скорости реакции[5]
- для реакций в растворе: измерение влияния давления на скорость реакции для определения изменения объема при образовании активированного комплекса.[6][7]
- для реакций с ионами в растворе, измерение влияния ионная сила от скорости реакции[8][9]
- прямое наблюдение за активированный комплекс к спектроскопия зондирования накачки[10]
- инфракрасный хемилюминесценция для обнаружения вибрационного возбуждения в изделиях[11][12]
- масс-спектрометрия с ионизацией электрораспылением.[13]
- кроссоверные эксперименты.[14]
Теоретическое моделирование
Правильный механизм реакции - важная часть точного прогнозное моделирование. Для многих систем горения и плазмы подробные механизмы недоступны или требуют разработки.
Даже когда информация доступна, идентификация и сбор соответствующих данных из различных источников, согласование несовпадающих значений и экстраполяция на различные условия могут оказаться трудным процессом без помощи экспертов. Константы скорости или термохимические данные часто отсутствуют в литературе, поэтому вычислительная химия методы или методы групповой аддитивности необходимо использовать для получения требуемых параметров.
Методы вычислительной химии также могут использоваться для расчета поверхности потенциальной энергии для реакций и определения возможных механизмов.[15]
Молекулярность
Молекулярность в химия это количество столкновений молекулярные объекты которые участвуют в одном стадия реакции.
- Стадия реакции с участием одного молекулярного объекта называется мономолекулярной.
- Стадия реакции с участием двух молекулярных объектов называется бимолекулярной.
- Стадия реакции с участием трех молекулярных единиц называется тримолекулярной или термолекулярной.
В общем, стадии реакции с участием более чем трех молекулярных объектов не происходят, потому что с точки зрения распределения Максвелла найти такое переходное состояние статистически невозможно.
Смотрите также
- Органические реакции по механизму под Органическая реакция
- Нуклеофильное ацильное замещение
- Участие в соседней группе
- Реакция Финкельштейна
- Механизм Линдеманна
- Механизм электрохимической реакции
- Нуклеофильная абстракция
Рекомендации
- ^ Марш, Джерри (1985), Продвинутая органическая химия: реакции, механизмы и структура (3-е изд.), Нью-Йорк: Wiley, ISBN 0-471-85472-7
- ^ Эспенсон, Джеймс Х. Химическая кинетика и механизмы реакций (2-е изд., McGraw-Hill, 2002), глава 6, Вывод механизмов реакции ISBN 0-07-288362-6
- ^ Эспенсон стр.156-160
- ^ Моррисон Р. и Бойд Р. Органическая химия (4-е изд., Аллин и Бэкон, 1983 г.), стр. 216-9 и стр. 228-231, ISBN 0-205-05838-8
- ^ Аткинс П. и де Паула Дж., Физическая химия (8-е изд., W.H. Freeman, 2006) с. 816-8. ISBN 0-7167-8759-8
- ^ Мур Дж. В. и Пирсон Р.Г. Кинетика и механизм (3-е изд., Джон Вили, 1981) с.276-8. ISBN 0-471-03558-0
- ^ Лайдлер К.Дж. и Мейзер Дж. Х., Физическая химия (Бенджамин / Каммингс 1982) стр.389-392 ISBN 0-8053-5682-7
- ^ Аткинс и де Паула с.884-5
- ^ Лайдлер и Мейзер с.388-9
- ^ Аткинс и де Паула с.892-3
- ^ Аткинс и де Паула с.886
- ^ Лайдлер и Мейзер с.396-7
- ^ Исследование химических реакций в растворе с использованием API-MSЛеонардо Сильва Сантос, Лариса Кнаак, Юрген О. Мецгер Int. J. Mass Spectrom.; 2005; 246 с. 84 - 104; (Рассмотрение) Дои:10.1016 / j.ijms.2005.08.016
- ^ Эспенсон стр.112
- ^ Аткинс и де Паула с.887-891
Л. Г. УЭЙД, ОРГАНИЧЕСКАЯ ХИМИЯ, 7-е ИЗД., 2010 г.

![r = k [NO_ {2}] ^ {2}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7c34576960b3342cceed6c0b51b1764beb2dfcf4)

![{ Displaystyle г = к [NO_ {2} (т)] ^ {2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/581dd3ba310fe8d53ab10b6a2ed319f4d67ed40a)