Этиловый спирт - Ethanol
| |||
| |||
| Имена | |||
|---|---|---|---|
| Произношение | /ˈɛθəпɒл/ | ||
| Предпочтительное название IUPAC Этиловый спирт[1] | |||
| Другие имена абсолютный алкоголь алкоголь одеколон употребление алкоголя этиловый спирт EtOH этиловый спирт этилгидрат этилгидроксид этилол зерновой спирт гидроксиэтан метилкарбинол | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 3DMet | |||
| 1718733 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.526 | ||
| Номер E | E1510 (дополнительные химикаты) | ||
| 787 | |||
PubChem CID | |||
| UNII | |||
| Номер ООН | ООН 1170 | ||
| |||
| |||
| Характеристики | |||
| C2ЧАС6О | |||
| Молярная масса | 46.069 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Метанолоподобный[2] | ||
| Плотность | 0,78945 г / см3 (при 20 ° C)[3] | ||
| Температура плавления | −114.14 ± 0.03[3] ° С (-173,45 ± 0,05 ° F, 159,01 ± 0,03 К) | ||
| Точка кипения | 78.23 ± 0.09[3] ° С (172,81 ± 0,16 ° F, 351,38 ± 0,09 К) | ||
| Смешиваемый | |||
| бревно п | −0.18 | ||
| Давление газа | 5,95 кПа (при 20 ° C) | ||
| Кислотность (пKа) | 15,9 (В2O), 29,8 (ДМСО)[4][5] | ||
| −33.60·10−6 см3/ моль | |||
| 1.3611[3] | |||
| Вязкость | 1,2 мПа · с (при 20 ° C), 1,074 мПа · с (при 25 ° C)[6] | ||
| 1,69 D[7] | |||
| Опасности | |||
| Паспорт безопасности | Видеть: страница данных [8] | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H225, H319 | |||
| P210, P280, P305 + 351 + 338 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 14 ° C (абсолютный)[нужна цитата ] | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 7340 мг / кг (перорально, крыса) 7300 мг / кг (мышь) | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 1000 частей на миллион (1900 мг / м3) [9] | ||
REL (Рекомендуемые) | TWA 1000 частей на миллион (1900 мг / м3) [9] | ||
IDLH (Непосредственная опасность) | N.D.[9] | ||
| Родственные соединения | |||
Родственные соединения | Этан Метанол | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
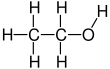
Этиловый спирт (также называемый этиловый спирт, зерновой спирт, употребление алкоголя, духи, или просто алкоголь) является органическим химическое соединение. Это простой алкоголь с химическая формула C
2ЧАС
6О. Его формулу также можно записать как CH
3−CH
2−ОЙ или же C
2ЧАС
5ОЙ (ан этильная группа связан с гидроксил группа), и часто сокращенный в качестве EtOH. Этанол - это летучий, легковоспламеняющийся, бесцветная жидкость со слабым характерным запахом. Это психоактивное вещество, рекреационный наркотик, и активный ингредиент в алкогольные напитки.
Этанол естественным образом производится ферментация из сахара к дрожжи или через нефтехимический такие процессы, как гидратация этилена. Он имеет медицинские применения в качестве антисептик и дезинфицирующее средство. Он используется как химический растворитель и в синтез из органические соединения. Этанол - альтернатива источник топлива.
Этимология
Этиловый спирт это систематическое название определяется Международный союз чистой и прикладной химии (IUPAC) для соединения, состоящего из алкильная группа с двумя углеродными атомы (приставка «eth-»), имеющая одинарную связь между ними (инфикс «-an-»), прилагается функциональная группа -OH группа (суффикс «-ol»).[10]
Префикс «eth-» и определитель «этил» в слове «этиловый спирт» первоначально произошли от названия «этил», присвоенного группе в 1834 г. C
2ЧАС
5- по Юстус Либих. Он придумал это слово из Немецкий имя Эфир соединения C
2ЧАС
5−O−C
2ЧАС
5 (обычно называемый «эфиром» в английский, более конкретно называемый "диэтиловый эфир ”).[11] Согласно Оксфордский словарь английского языка, Этил сокращение от древнегреческого αἰθήρ (aithḗr, «Верхний воздух») и греческое слово ὕλη (привет, «Вещество»).[12]
Название этиловый спирт был придуман в результате резолюции, принятой на Международной конференции по химической номенклатуре, которая состоялась в апреле 1892 года в Женеве, Швейцария.[13]
Период, термин "алкоголь «Теперь относится к более широкому классу веществ в химической номенклатуре, но в просторечии остается названием этанола. В Оксфордский словарь английского языка утверждает, что это средневековый заем от арабский аль-куḥл, порошкообразная руда сурьмы, которая использовалась с древних времен как косметическое средство, и сохранила это значение в Средняя латынь.[14] Использование «алкоголя» для этанола (в полной мере, «спирт вина») является современным, впервые зарегистрировано в 1753 году, а к концу 18 века относилось к «любому сублимированному веществу»; «дистиллированный спирт "Используется для" спиртного напитка "(сокращенно от полного выражения дух алкоголь вина). Систематическое использование в химии датируется 1850 годом.
Использует
Медицинское
Антисептик
Этанол используется в медицинских салфетках и чаще всего в антибактериальных средствах. дезинфицирующее средство для рук гели как антисептик за его бактерицидное и противогрибковое действие.[15] Этанол убивает микроорганизмы растворяя их мембрану липидный бислой и денатурирующий их белки, и эффективен против большинства бактерии и грибы и вирусы. Однако он неэффективен против бактериального споры, но это можно уменьшить, используя пероксид водорода.[16] Раствор 70% этанола более эффективен, чем чистый этанол, потому что этанол полагается на молекулы воды для оптимальной антимикробной активности. Абсолютный этанол может инактивировать микробы, не уничтожая их, потому что спирт не может полностью проникнуть через мембрану микроба.[17][18] Этанол также можно использовать в качестве дезинфицирующего и антисептического средства, поскольку он вызывает обезвоживание клеток, нарушая осмотический баланс клеточной мембраны, поэтому вода покидает клетку, что приводит к ее гибели.[19]
Противоядие
Этанол можно вводить как противоядие к отравление этиленгликолем[20] и отравление метанолом.[21]
Лекарственный растворитель
Этанол, часто в высоких концентрациях, используется для растворения многих нерастворимых в воде лекарств и родственных соединений. Жидкие препараты обезболивающие, лекарства от кашля и простуды, и жидкости для полоскания рта, например, могут содержать до 25% этанола.[22] и, возможно, следует избегать у людей с побочными реакциями на этанол, такими как респираторные реакции, вызванные алкоголем.[23] Этанол присутствует в основном в качестве противомикробного консерванта в более чем 700 жидких лекарственных препаратах, включая ацетаминофен, добавки железа, ранитидин, фуросемид, маннитол, фенобарбитал, триметоприм / сульфаметоксазол и без рецепта лекарства от кашля.[24]
Фармакология
При пероральном приеме этанол интенсивно метаболизируется в печени, особенно через фермент CYP450.[25] Этиловый спирт увеличивает секрецию кислот в желудке.[25] Метаболит ацетальдегид отвечает за большую часть краткосрочных и долгосрочных последствий токсичности этилового спирта.[26]
Рекреационный
Как Центральная нервная система депрессант, этанол - один из наиболее часто потребляемых психоактивные препараты.[27]
Несмотря на то, что алкоголь обладает психоактивными свойствами, он легко доступен и легален для продажи в большинстве стран. Однако существуют законы, регулирующие продажу, экспорт / импорт, налогообложение, производство, потребление и хранение алкогольных напитков. Самым распространенным правилом является запрет для несовершеннолетних.
Топливо
Топливо двигателя
| Тип топлива | МДж / л | МДж / кг | Исследование октан номер |
|---|---|---|---|
| Сухая древесина (влажность 20%) | ~19.5 | ||
| Метанол | 17.9 | 19.9 | 108.7[29] |
| Этиловый спирт | 21.2[30] | 26.8[30] | 108.6[29] |
| E85 (85% этанол, 15% бензин) | 25.2 | 33.2 | 105 |
| Сжиженный природный газ | 25.3 | ~55 | |
| Автогаз (СУГ ) (60% пропан + 40% бутан ) | 26.8 | 50 | |
| Авиационный бензин (высокооктановый бензин, а не авиакеросин) | 33.5 | 46.8 | 100/130 (постное / богатое) |
| Газохол (90% бензина + 10% этанола) | 33.7 | 47.1 | 93/94 |
| Обычный бензин / бензин | 34.8 | 44.4[31] | мин. 91 |
| Премиум бензин / бензин | Максимум. 104 | ||
| Дизель | 38.6 | 45.4 | 25 |
| Уголь, экструдированный | 50 | 23 |
Наиболее часто этанол используется в качестве двигателя. топливо и топливная добавка. Бразилия в частности, в значительной степени полагается на использование этанола в качестве моторного топлива, отчасти из-за его роли в качестве одного из ведущих производителей этанола в мире.[32] Бензин продается в Бразилии, содержит не менее 25% безводный этиловый спирт. Водный этанол (около 95% этанола и 5% воды) может использоваться в качестве топлива более чем в 90% новых бензиновых автомобилей, продаваемых в стране. Бразильский этанол производится из сахарный тростник и отмечен высоким связывание углерода.[33] США и многие другие страны в основном используют смеси этанола и бензина E10 (10% этанол, иногда называемый бензином) и E85 (85% этанол).

Этанол использовался как ракетное горючие и в настоящее время в легкий гоночный самолет с ракетным двигателем.[34]
Австралийский закон ограничивает использование чистого этанола из отходов сахарного тростника до 10% в автомобилях. В старых автомобилях (и старинных автомобилях, рассчитанных на использование более медленно горящего топлива) необходимо обновить или заменить клапаны двигателя.[35]
Согласно отрасли группа адвокатов, этанол в качестве топлива снижает вредные выхлопные газы оксида углерода, твердых частиц, оксиды азота, и другие озонообразующие загрязнители.[36] Аргоннская национальная лаборатория проанализировали выбросы парниковых газов от множества различных двигателей и комбинаций топлива и обнаружили, что биодизель / нефтедизельная смесь (B20 ) показал снижение на 8%, обычное E85 смесь этанола сокращение на 17% и целлюлозный этанол 64% по сравнению с чистым бензином.[37] У этанола гораздо большее октановое число (RON), чем у бензина, что означает, что он менее подвержен преждевременному воспламенению, что обеспечивает более оптимальное опережение зажигания, что означает больший крутящий момент и эффективность в дополнение к более низким выбросам углерода.[38]
Сгорание этанола в двигателе внутреннего сгорания дает многие продукты неполного сгорания, производимые бензином, и значительно большие количества формальдегид и родственные виды, такие как ацетальдегид.[39] Это приводит к значительно большей фотохимической реактивности и большему количеству озон на уровне земли.[40] Эти данные были собраны в отчете о чистом топливе, где сравниваются выбросы топлива.[41] и показывают, что выхлопные газы этанола генерируют в 2,14 раза больше озона, чем выхлопные газы бензина.[42] Когда это добавляется в кастом Индекс локального загрязнения (LPI) В Докладе о чистом топливе местное загрязнение этанолом (загрязнение, способствующее образованию смога) имеет рейтинг 1,7, где бензин - 1,0, а более высокие значения означают большее загрязнение.[43] В Калифорнийский совет по воздушным ресурсам формализовала этот вопрос в 2008 году, признав стандарты контроля для формальдегидов в качестве группы контроля выбросов, во многом аналогично традиционной NOx и реактивные органические газы (ROG).[44]
Мировое производство этанола в 2006 г. составило 51 гигалитр (1,3×1010 Галлоны США), при этом 69% мировых поставок приходится на Бразилию и США.[45] Более 20% бразильских автомобилей могут использовать 100% этанол в качестве топлива, в том числе двигатели, работающие только на этаноле, и гибкое топливо двигатели.[46] Двигатели с гибким топливом в Бразилии могут работать со всем этанолом, любым бензином или любой их смесью. В США автомобили с гибким топливом могут работать на этаноле от 0% до 85% (15% бензина), поскольку смеси с более высоким содержанием этанола еще не разрешены или неэффективны. Бразилия поддерживает этот парк автомобилей, работающих на этаноле, с большой национальной инфраструктурой, которая производит этанол из выращенных внутри страны. сахарный тростник. Сахарный тростник не только имеет более высокую концентрацию сахарозы, чем кукуруза (примерно на 30%), но также намного легче извлекается. В жмых произведенные в процессе не тратятся впустую, а используются на электростанциях для производства электроэнергии.[нужна цитата ]
В Соединенных Штатах топливная промышленность этанола основана в основном на кукуруза. По данным Ассоциации возобновляемых источников топлива, по состоянию на 30 октября 2007 года 131 завод по переработке этанола из 131 зерна в Соединенных Штатах имеют мощность для производства 7,0 млрд галлонов США (26000000 м3).3) этанола в год. Дополнительные 72 строительных проекта в стадии реализации (в США) могут добавить 6,4 млрд галлонов США (24000000 м3) новой мощности в ближайшие 18 месяцев. Со временем считается, что материальная часть ≈150 миллиардов галлонов США (570 000 000 м3) в год рынок бензина начнет заменяться топливным этанолом.[47]
Сладкое сорго является еще одним потенциальным источником этанола и подходит для выращивания в условиях засушливых земель. В Международный научно-исследовательский институт сельскохозяйственных культур полузасушливых тропиков (ИКРИСАТ ) изучает возможность выращивания сорго в качестве источника топлива, пищи и корма для животных в засушливых районах Азия и Африка.[48] Сладкое сорго имеет одну треть потребности в воде сахарного тростника за тот же период времени. Он также требует примерно на 22% меньше воды, чем кукуруза (также известная как кукуруза). Первый в мире завод по производству сладкого сорго этанола начал коммерческое производство в 2007 году в Андхра-Прадеше, Индия.[49]
Этанол высокий смешиваемость с водой делает его непригодным для транспортировки по современным трубопроводы как жидкие углеводороды.[50] Механики видели увеличение случаев повреждения двигателей малого объема (в частности, карбюратор ) и объясняют повреждение повышенным удержанием воды этанолом в топливе.[51]
Ракетное горючие
Этанол обычно использовался в качестве топлива в начале двухкомпонентное топливо ракета (жидкостных) транспортных средств в сочетании с окислитель например жидкий кислород. Немецкая баллистическая ракета А-4, более известная под пропагандистским названием Ракета Фау-2 из Вторая Мировая Война,[52] приписывают начало космической эры, использовали этанол в качестве основного компонента B-Stoff. При такой номенклатуре этанол смешивали с 25% воды для снижения температуры камеры сгорания.[53][54] Команда разработчиков V-2 помогла разработать американские ракеты после Второй мировой войны, в том числе работающие на этаноле. Ракета из красного камня который запустил первый спутник США.[55] Спирты вышли из употребления, поскольку были разработаны более энергоемкие ракетные топлива.[54]
Топливные элементы
Коммерческие топливные элементы работают на реформированном природном газе, водород или же метанол. Этанол является привлекательной альтернативой из-за его широкой доступности, низкой стоимости, высокой чистоты и низкой токсичности. Существует широкий спектр концепций топливных элементов, которые прошли испытания, включая топливные элементы с прямым этанолом, системы автотермического риформинга и термически интегрированные системы. Большая часть работы ведется на исследовательском уровне, хотя ряд организаций находится в начале коммерциализации этанольных топливных элементов.[56]
Домашнее отопление
Камины на этаноле можно использовать для отопления дома или для украшения.[57]
Сырье
Этанол - важный промышленный ингредиент. Он широко используется в качестве прекурсора для других органических соединений, таких как этил. галогениды, этил сложные эфиры, диэтиловый эфир, уксусная кислота и этил амины.
Растворитель
Этанол считается универсальным растворитель, поскольку его молекулярный структура позволяет растворять как полярный, гидрофильный и неполярный, гидрофобный соединения. Поскольку этанол также имеет низкую точка кипения, его легко удалить из раствора, который использовался для растворения других соединений, что делает его популярным экстрагирующим агентом для растительных масел. Каннабис методы экстракции масла часто используют этанол в качестве экстракции растворитель,[58] а также в качестве растворителя для последующей обработки для удаления масел, восков и хлорофилл из раствора в процессе, известном как подготовка к зиме.
Этанол содержится в краски, настойки, маркеры и средства личной гигиены, такие как жидкости для полоскания рта, духи и дезодоранты. Тем не мение, полисахариды осадок из водного раствора в присутствии спирта, и осаждение этанолом используется по этой причине при очистке ДНК и РНК.
Низкотемпературная жидкость
Из-за низкой точки замерзания -173,20 ° F (-114,14 ° C) и низкой токсичности этанол иногда используется в лабораториях (с сухой лед или другие охлаждающие жидкости) в качестве охлаждающая ванна хранить сосуды при температуре ниже точки замерзания воды. По той же причине он также используется в качестве активной жидкости в спиртовые термометры.
Химия
Химическая формула
Этанол - это двухуглеродный спирт. Его молекулярная формула это CH3CH2ОЙ. Альтернативное обозначение - CH3-CH2−OH, что указывает на то, что углерод метильная группа (CH3-) прикреплен к углероду метиленовая группа (-CH2-), который присоединен к кислороду гидроксильная группа (-OH). Это конституционный изомер из диметиловый эфир. Этанол иногда сокращенно обозначают как EtOH, используя общепринятые обозначения органической химии, представляющие этильную группу (C2ЧАС5-) с Et.
Физические свойства

Этанол - летучая бесцветная жидкость с легким запахом. Он горит бездымным голубым пламенем, которое не всегда видно при обычном освещении. Физические свойства этанола в первую очередь связаны с наличием в нем гидроксил группа и короткость ее углеродной цепи. Гидроксильная группа этанола способна участвовать в образовании водородных связей, делая его более вязким и менее летучим, чем менее полярные органические соединения аналогичной молекулярной массы, такие как пропан.
Этанол немного более преломлен, чем вода, имея показатель преломления 1,36242 (при λ = 589,3 нм и 18,35 ° C или 65,03 ° F).[59] В тройная точка для этанола 150 K под давлением 4.3 × 10−4 Па.[60]
Свойства растворителя
Этанол - универсальный растворитель, смешивающийся с водой и со многими органическими растворителями, в том числе уксусная кислота, ацетон, бензол, четыреххлористый углерод, хлороформ, диэтиловый эфир, этиленгликоль, глицерин, нитрометан, пиридин, и толуол. Его основное применение в качестве растворителя - приготовление настойки йода, сиропов от кашля и т. Д.[59][61] Он также смешивается с легкими алифатическими углеводородами, такими как пентан и гексан и с алифатическими хлоридами, такими как трихлорэтан и тетрахлорэтилен.[61]
Смешиваемость этанола с водой контрастирует с несмешиваемостью длинноцепочечных спиртов (пять или более атомов углерода), смешиваемость которых с водой резко снижается с увеличением количества атомов углерода.[62] Смешиваемость этанола с алканы ограничивается алканами до ундекан: смеси с додекан и высшие алканы показывают разрыв в смешиваемости ниже определенной температуры (около 13 ° C для додекана[63]). Разрыв в смешиваемости имеет тенденцию к увеличению с более высоким содержанием алканов, и температура для полной смешиваемости увеличивается.
Смеси этанол-вода имеют меньший объем, чем сумма их отдельных компонентов в данных фракциях. При смешивании равных объемов этанола и воды получается всего 1,92 объема смеси.[59][64] Смешивание этанола и воды экзотермический, с до 777 Дж / моль[65] выпускается при 298 К.
Смеси этанола и воды образуют азеотроп примерно при 89 мол.% этанола и 11 мол.% воды[66] или смесь 95,6% этанола по массе (или около 97% спирт по объему ) при нормальном давлении, который закипает при 351K (78 ° C). Этот азеотропный состав сильно зависит от температуры и давления и исчезает при температурах ниже 303 К.[67]

Водородная связь вызывает образование чистого этанола. гигроскопичный в той степени, в которой он легко впитывает воду из воздуха. Полярная природа гидроксильной группы заставляет этанол растворять многие ионные соединения, особенно натрий и гидроксиды калия, хлорид магния, хлорид кальция, хлорид аммония, бромид аммония, и бромид натрия.[61] Натрий и хлориды калия слабо растворимы в этаноле.[61] Поскольку молекула этанола также имеет неполярный конец, она также растворяет неполярные вещества, в том числе большинство эфирные масла[68] и многочисленные ароматизаторы, красители и лекарственные средства.
Добавление к воде даже нескольких процентов этанола резко снижает поверхностное натяжение воды. Это свойство частично объясняет "слезы вина "явление. Когда вино взбалтывается в бокале, этанол быстро испаряется из тонкой пленки вина на стенке бокала. По мере того, как содержание этанола в вине уменьшается, его поверхностное натяжение увеличивается, и тонкая пленка" поднимается вверх "и стекает вниз по поверхности. стекло в каналах, а не в виде гладкого листа.
Воспламеняемость
Раствор этанол-вода загорится, если его нагреть выше температуры, называемой его точка возгорания и затем к нему прикладывают источник воспламенения.[69] Для 20% спирта по массе (около 25% по объему) это происходит при температуре около 25 ° C (77 ° F). Температура вспышки чистого этанола составляет 13 ° C (55 ° F),[70] но на него может очень незначительно влиять состав атмосферы, например давление и влажность. Смеси этанола могут воспламениться при температуре ниже средней комнатной. Этанол считается легковоспламеняющейся жидкостью (опасный материал класса 3) в концентрациях выше 2,35% по массе (3,0% по объему; 6 доказательство ).[71][72][73]
Температуры вспышки смесей этанол – вода[74][72][75] Этиловый спирт
массовая доля, %Температура ° C ° F 1 84.5 184.1[72] 2 64 147[72] 2.35 60 140[72][71] 3 51.5 124.7[72] 5 43 109[74] 6 39.5 103.1[72] 10 31 88[74] 20 25 77[72] 30 24 75[74] 40 21.9 71.4[нужна цитата ][74] 50 20 68[74][72] 60 17.9 64.2[нужна цитата ][74] 70 16 61[74] 80 15.8 60.4[72] 90 14 57[74] 100 12.5 54.5[74][72][70]
Блюда с использованием горячего спирта для кулинарного воздействия называются фламбе.
Естественное явление
Этанол является побочным продуктом метаболический процесс дрожжей. Таким образом, этанол будет присутствовать в любой среде обитания дрожжей. Этанол обычно содержится в перезрелых фруктах.[76] Этанол, производимый симбиотическими дрожжами, можно найти в Bertam Palm цветет. Хотя некоторые виды животных, такие как шестигранные деревья, проявляют стремление к этанолу, большинство не проявляют интереса к источникам пищи, содержащим этанол, и не избегают их.[77] Этанол также производится при прорастании многих растений в результате естественного анаэробиоз.[78] Этанол обнаружен в космическое пространство, образуя ледяной покров вокруг пылинок в межзвездные облака.[79]Суммы минутного количества (в среднем 196 ppb ) эндогенного этанола и ацетальдегида были обнаружены в выдыхаемом воздухе здоровых добровольцев.[80] Синдром автопивоварни, также известный как синдром кишечной ферментации, является редким заболеванием, при котором опьяняющий количество этанола производится за счет эндогенный ферментация в пределах пищеварительная система.[81]
Производство

Этанол производится как в нефтехимический за счет гидратации этилена и за счет биологических процессов брожение сахара с дрожжи.[82] Какой процесс более экономичный, зависит от преобладающих цен на нефть и зерновое сырье. В 1970-х годах большая часть промышленного этанола в Соединенных Штатах производилась в нефтехимической промышленности, но в 1980-х годах Соединенные Штаты ввели субсидии на этанол на основе кукурузы, и сегодня почти весь этанол производится из этого источника.[83]
Гидратация этилена
Этанол для использования в качестве промышленного сырья или растворителя (иногда называемый синтетическим этанолом) производится из нефтехимический сырье, в первую очередь кислота -катализированный гидратация этилена:
- C
2ЧАС
4 + ЧАС
2О → CH
3CH
2ОЙ
Катализатор чаще всего фосфорная кислота,[84][85] адсорбированный на пористую основу, такую как силикагель или же диатомовая земля. Этот катализатор впервые был использован для крупномасштабного производства этанола Shell Oil Company в 1947 г.[86] Реакцию проводят в присутствии пара под высоким давлением при 300 ° C (572 ° F), где поддерживается соотношение этилена и пара 5: 3.[87][88] Этот процесс был использован в промышленных масштабах Union Carbide Corporation и другие в США, но только сейчас LyondellBasell использует его в коммерческих целях.
В более старом процессе, впервые примененном в промышленных масштабах в 1930 году компанией Union Carbide,[89] но теперь почти полностью устаревший, этилен гидратировался косвенно путем его реакции с концентрированным серная кислота производить этилсульфат, который был гидролизованный для получения этанола и регенерации серной кислоты:[90]
- C
2ЧАС
4 + ЧАС
2ТАК
4 → CH
3CH
2ТАК
4ЧАС - CH
3CЧАС
2ТАК
4ЧАС + ЧАС
2О → CH
3CЧАС
2ОH + ЧАС
2ТАК
4
Из CO2
CO2 также может использоваться как сырье.
CO2 может быть восстановлен водородом с образованием этанола, уксусная кислота, и меньшее количество 2,3-бутандиол и молочная кислота с помощью Clostridium ljungdahlii, Clostridium autoethanogenum или же Мурелла sp. HUC22-1.[91][92]
CO2 можно преобразовать с помощью электрохимический реакции при комнатной температуре и давлении.[93][94] В системе, разработанной в Делфтский технологический университет, медь нанопроволока Массив, используемый в качестве катода, адсорбирует молекулы диоксида углерода и восстановленных промежуточных частиц, таких как CO и COH. Однако даже при самых лучших результатах около половины тока шло на производство водорода и было произведено лишь небольшое количество этанола. Остальные товары, произведенные в больших количествах, были (в порядке убывания) муравьиная кислота, этилен, CO и н-пропанол.[95]
Из липидов
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Ноябрь 2019) |
Липиды также можно использовать для производства этанола, и их можно найти в таком сырье, как водоросли.[96]
Ферментация
Этанол в Алкогольные напитки и топливо производится путем ферментации. Некоторые виды дрожжи (например., Saccharomyces cerevisiae ) метаболизировать сахар, производящие этанол и диоксид углерода. Приведенные ниже химические уравнения резюмируют преобразование:
- C
6ЧАС
12О
6 → 2 CH
3CH
2ОH + 2 CO2 - C
12ЧАС
22О
11 + ЧАС
2О → 4 CH
3CH
2ОH + 4 CO2
Ферментация - это процесс выращивания дрожжей в благоприятных тепловых условиях для производства спирта. Этот процесс выполняется при температуре около 35–40 ° C (95–104 ° F). Токсичность этанола для дрожжей ограничивает концентрацию этанола, которую можно получить при пивоварении; более высокие концентрации, следовательно, получаются фортификация или же дистилляция. Наиболее устойчивые к этанолу штаммы дрожжей могут выжить при содержании этанола примерно до 18% по объему.
Для производства этанола из крахмалистых материалов, таких как хлопья, то крахмал сначала необходимо преобразовать в сахар. В пивоварении пиво, это традиционно достигается путем прорастания зерна, или солод, что дает фермент амилаза. Когда солодовое зерно пюре, амилаза превращает оставшиеся крахмалы в сахара.
Celtic Renewables производит этанол, используя отходы производства виски, и низкосортный картофель, через ABE ферментация.
Целлюлоза
Сахара для ферментация этанола можно получить из целлюлоза. Внедрение этой технологии может привести к появлению целлюлозосодержащих побочных продуктов сельского хозяйства, таких как початки кукурузы, солома, и опилки, в возобновляемые источники энергии. Другие сельскохозяйственные остатки, такие как жмых сахарного тростника и энергетические культуры Такие как просо также могут быть источники сбраживаемого сахара.[97]
Тестирование


Пивоварни и биотопливо заводы используют два метода измерения концентрации этанола. Инфракрасные датчики этанола измеряют частоту колебаний растворенного этанола, используя полосу C − H при 2900 см.−1. В этом методе используется относительно недорогой твердотельный датчик, который сравнивает диапазон C-H с эталонным диапазоном для расчета содержания этанола. В расчетах используется Закон Бера – Ламберта. В качестве альтернативы, измеряя плотность исходного материала и плотность продукта, используя ареометр, изменение удельного веса во время ферментации указывает на содержание алкоголя. Этот недорогой и косвенный метод имеет долгую историю в пивоварении.
Очищение
Дистилляция
При гидратации этилена или при пивоварении получается смесь этанол-вода. Для большинства промышленных и топливных целей этанол необходимо очищать. Фракционная перегонка при атмосферном давлении можно концентрировать этанол до 95,6% по весу (89,5% мол.). Эта смесь является азеотроп с температурой кипения 78,1 ° C (172,6 ° F), и не можешь подлежат дальнейшей очистке перегонкой. Добавление увлекающего агента, такого как бензол, циклогексан, или же гептан, позволяет сформировать новый тройной азеотроп, содержащий этанол, воду и уносящий агент. Этот трехкомпонентный азеотроп с более низкой температурой кипения предпочтительно удаляют, что приводит к безводному этанолу.[85]
При давлениях ниже атмосферного состав азеотропа этанол-вода смещается в сторону более богатых этанолом смесей, а при давлениях менее 70торр (9,333 кПа), азеотропа нет, и можно отгонять абсолютный этанол из смеси этанол-вода. В то время как вакуумная перегонка этанола в настоящее время не является экономичной, перегонка под давлением является предметом текущих исследований. В этом методе перегонка при пониженном давлении сначала дает смесь этанол-вода, содержащую более 95,6% этанола. Затем фракционная перегонка этой смеси при атмосферном давлении приводит к отгонке 95,6% азеотропа, оставляя на дне безводный этанол.[нужна цитата ]
Молекулярные сита и осушители
Эта секция нужны дополнительные цитаты для проверка. (Декабрь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
Помимо перегонки, этанол можно сушить добавлением осушитель, Такие как молекулярные сита, целлюлоза, и кукурузная мука. Десиканты можно сушить и использовать повторно.[85] Молекулярные сита может использоваться для избирательного поглощения воды из 95,6% раствора этанола.[98] Синтетический цеолит в форме гранул, а также различные абсорбенты растительного происхождения, включая кукурузная мука, солома, и опилки. Слой цеолита можно регенерировать практически неограниченное количество раз, высушивая его струей горячего воздуха. углекислый газ. Кукурузная мука и другие абсорбенты растительного происхождения не могут быть легко регенерированы, но если этанол получают из зерна, они часто доступны по низкой цене. Абсолютный этанол, произведенный таким образом, не содержит остаточного бензола и может быть использован для обогащения портвейна и хереса на традиционных винодельческих предприятиях.
Мембраны и обратный осмос
Мембраны также можно использовать для разделения этанола и воды. Разделение на основе мембраны не подлежит ограничениям азеотропа вода-этанол, поскольку разделения не основаны на равновесии пара и жидкости. Мембраны часто используются в процессе так называемой гибридной мембранной дистилляции. В этом процессе используется дистилляционная колонна предварительного концентрирования в качестве первой стадии разделения. Дальнейшее разделение затем выполняется с помощью мембраны, работающей в режиме паропроницаемости или первапорации. Для паропроницаемости используется подача через паровую мембрану, а при первапорации - через жидкую мембранную подачу.
Другие техники
Обсуждались и другие различные методы, включая следующие:[85]
- Посол с использованием карбонат калия использование его нерастворимости вызовет разделение фаз с этанолом и водой. Это дает очень небольшую примесь карбоната калия в спирте, который можно удалить перегонкой. Этот метод очень полезен при очистке этанола дистилляцией, поскольку этанол образует азеотроп с водой.
- Прямой электрохимическое восстановление диоксида углерода в этанол в условиях окружающей среды с использованием наночастицы меди на углеродной наношиповой пленке в качестве катализатора;[99]
- Извлечение этанола из зернового сусла методом сверхкритический диоксид углерода;
- Первапорация;
- Фракционная заморозка также используется для концентрирования ферментированных спиртовых растворов, например, традиционно приготовленных Эпплджек (напиток);
- Адсорбция при переменном давлении.[100]
Сорта этанола
Денатурированный спирт
Чистый этанол и алкогольные напитки сильно облагаемый налогом как психоактивные препараты, но этанол имеет много применений, не связанных с его употреблением. Чтобы облегчить налоговое бремя этих видов использования, большинство юрисдикций отказываются от налога, когда к этанолу добавляется агент, делающий его непригодным для употребления. К ним относятся горькие вещества Такие как денатония бензоат и токсины, такие как метанол, нафта, и пиридин. Такие изделия называются денатурированный спирт.[101][102]
Абсолютный алкоголь
Абсолютный или безводный спирт относится к этанолу с низким содержанием воды. Существуют различные сорта с максимальным содержанием воды от 1% до нескольких частей на миллион (ppm). Если азеотропная дистилляция используется для удаления воды, он будет содержать следовые количества агента разделения материалов (например, бензола).[103] Абсолютный алкоголь не предназначен для употребления человеком. Абсолютный этанол используется в качестве растворителя в лабораторных и промышленных целях, где вода вступает в реакцию с другими химическими веществами, а также в качестве топливного спирта. Спектроскопический этанол - это абсолютный этанол с низким поглощением в ультрафиолетовый и видимый свет, пригодный для использования в качестве растворителя в ультрафиолетовая и видимая спектроскопия.[104]
Чистый этанол классифицируется как 200 доказательство в США, что эквивалентно 175 градусам доказательства в системе Великобритании.[105]
Ректифицированные спирты
Ректификованный спирт, азеотропный состав 96% этанола, содержащий 4% воды, используется вместо безводного этанола для различных целей. Винные спирты на 94% состоят из этанола (188 доказательство ). Примеси отличаются от примесей в 95% -ном (190) лабораторном этаноле.[106]
Реакции
Этанол классифицируется как первичный спирт, а это означает, что углерод, к которому присоединяется его гидроксильная группа, также имеет присоединенные к нему по крайней мере два атома водорода. Многие реакции этанола происходят на его гидроксил группа.
Образование сложного эфира
В присутствии кислотных катализаторов этанол реагирует с карбоновые кислоты производить этил сложные эфиры и вода:
- RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2О
Эта реакция, которая проводится в крупных промышленных масштабах, требует удаления воды из реакционной смеси по мере ее образования. Сложные эфиры реагируют в присутствии кислоты или основания, возвращая спирт и соль. Эта реакция известна как омыление потому что он используется при приготовлении мыла. Этанол также может образовывать сложные эфиры с неорганическими кислотами. Диэтилсульфат и триэтилфосфат получают путем обработки этанола триоксидом серы и пятиокись фосфора соответственно. Диэтилсульфат является полезным этилирующим агентом в органический синтез. Этилнитрит, полученный реакцией этанола с нитрат натрия и серная кислота, ранее использовалась как мочегонное средство.
Обезвоживание
В присутствии кислотных катализаторов этанол превращается в этилен. Обычно твердые кислоты такие как кремнезем используются:[107]
- CH3CH2ОН → Н2C = CH2 + H2О
Полученный таким образом этилен конкурирует с этиленом нефтеперерабатывающих заводов и гидроразрыва пласта.
В альтернативных условиях диэтиловый эфир полученные результаты:
- 2 канала3CH2ОН → СН3CH2ОСН2CH3 + H2О
Горение
Полный горение форм этанола углекислый газ и воды:
- C2ЧАС5ОН (л) + 3 О2 (г) → 2 СО2 (г) + 3 H2О (л); −ΔHc = 1371 кДж / моль[108] = 29,8 кДж / г = 327 ккал / моль = 7,1 ккал / г
- C2ЧАС5ОН (л) + 3 О2 (г) → 2 СО2 (г) + 3 H2О (г); −ΔHc = 1236 кДж / моль = 26,8 кДж / г = 295,4 ккал / моль = 6,41 ккал / г[109]
Удельная теплоемкость = 2,44 кДж / (кг · К)
Кислотно-основная химия
Этанол - нейтральная молекула, и pH раствора этанола в воде почти 7.00. Этанол можно количественно превратить в его сопряженное основание, то этоксид ион (CH3CH2О−), по реакции с щелочной металл Такие как натрий:[62]
- 2 канала3CH2ОН + 2 Na → 2 СН3CH2ONa + H2
или очень сильная база, такая как гидрид натрия:
- CH3CH2ОН + NaH → CH3CH2ONa + H2
Кислотности воды и этанола почти одинаковы, на что указывает их pKa 15,7 и 16 соответственно. Таким образом, этилат натрия и едкий натр существуют в равновесии, которое хорошо сбалансировано:
- CH3CH2ОН + NaOH ⇌ СН3CH2ONa + H2О
Галогенирование
Этанол в промышленности не используется в качестве предшественника этилгалогенидов, но реакции носят иллюстративный характер. Этанол реагирует с галогениды водорода производить этилгалогениды Такие как этилхлорид и этилбромид через SN2 реакция:
- CH3CH2ОН + HCl → CH3CH2Cl + H2О
Эти реакции требуют катализатора, такого как хлорид цинка.[90]HBr требует рефлюкс с серная кислота катализатор.[90] Этилгалогениды, в принципе, также могут быть получены путем обработки этанола более специализированными галогенирующие агенты, Такие как тионилхлорид или же трибромид фосфора.[62][90]
- CH3CH2OH + SOCl2 → CH3CH2Cl + SO2 + HCl
При обработке галогенами в присутствии основания этанол дает соответствующий галоформ (CHX3, где X = Cl, Br, I). Это преобразование называется галоформная реакция.[110] "Промежуточным продуктом в реакции с хлором является альдегид называется хлорал, который образует хлоралгидрат при реакции с водой:[111]
- 4 Cl2 + CH3CH2OH → CCl3CHO + 5 HCl
- CCl3CHO + H2O → CCl3С (ОН)2ЧАС
Окисление
Этанол может окисляться до ацетальдегид и далее окисляется до уксусная кислота в зависимости от реагентов и условий.[90] Это окисление не имеет промышленного значения, но в организме человека эти реакции окисления катализируются фермент алкогольдегидрогеназа печени. Продукт окисления этанола, уксусная кислота, является питательным веществом для человека, являясь предшественником ацетил-КоА, где ацетильная группа может быть потрачена как энергия или использована для биосинтеза.
Безопасность
Чистый этанол раздражает кожу и глаза.[112] Тошнота, рвота, и интоксикация являются симптомами проглатывания. Длительное употребление внутрь может привести к серьезному повреждению печени.[113] Концентрации в атмосфере выше одной из тысячи превышают уровни Европейского Союза. пределы профессионального облучения.[113]
В ходе COVID-19 пандемия, то Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США нашел ряд дезинфицирующие средства для рук продаваемые, которые были помечены как содержащие этанол, но дали положительный результат на метанол загрязнение.[114] Из-за токсического действия метанола при всасывании через кожу или проглатывании, в отличие от относительно более безопасного этанола, FDA распорядилось отозвать такие дезинфицирующие средства для рук, содержащие метанол, и выпустило предупреждение об импорте, чтобы предотвратить незаконный выход этих продуктов на рынок США .[115]
История
В ферментация сахара в этанол является одним из первых биотехнологии используется людьми. Опьяняющие эффекты употребления этанола известны с древних времен. Этанол использовался людьми с доисторических времен как опьяняющий ингредиент Алкогольные напитки. Засохшие остатки глиняной посуды возрастом 9000 лет, найденной в Китае, позволяют предположить, что Неолит люди употребляли алкогольные напитки.[116]
В средневековые мусульмане использовал дистилляция широко и применил его к перегонка спирта. Арабский химик Аль-Кинди однозначно описана дистилляция вина в 9 веке.[117][118][119] Персидский врач, алхимик, эрудит и философ. Мухаммад ибн Закария ар-Рази (854 г. н.э. - 925 г. н.э.) приписывают открытие этанола.[120]Позже процесс распространился из Средний Восток в Италию.[117][121] Производство спирта из дистиллированного вина было позже зарегистрировано Школа Салерно алхимики в 12 веке.[122] Упоминание об абсолютном алкоголе, в отличие от водно-спиртовых смесей, было позднее сделано Раймонд Лулль в 14 веке.[122]
В Китай, археологические данные показывают, что настоящая дистилляция алкоголя началась в 12 веке. Джин или же Южная Песня династии.[123] А Все еще был найден на археологическом участке в Цинлуне, Хэбэй, датируемые 12 веком.[123] В Индия, настоящая дистилляция алкоголя была завезена с Ближнего Востока и широко использовалась в Делийский султанат к 14 веку.[121]
В 1796 году немецко-русский химик Иоганн Тобиас Ловиц получил чистый этанол, смешав частично очищенный этанол (азеотроп спирт-вода) с избытком безводной щелочи и затем перегоня смесь на медленном огне.[124] Французский химик Антуан Лавуазье описал этанол как соединение углерода, водорода и кислорода, а в 1807 г. Николя-Теодор де Соссюр определена химическая формула этанола.[125][126] Пятьдесят лет спустя Арчибальд Скотт Купер опубликовала структурную формулу этанола. Это была одна из первых определенных структурных формул.[127]
Этанол был впервые получен синтетическим путем в 1825 г. Майкл Фарадей. Он обнаружил, что серная кислота может поглощать большие объемы угольный газ.[128] Полученное решение он отдал Генри Хеннелл, британский химик, который в 1826 году обнаружил, что он содержит «сульфовиновую кислоту» (этилгидросульфат ).[129] В 1828 году Хеннель и французский химик Жорж-Симон Серуллас независимо обнаружил, что сульфовиновая кислота может разлагаться до этанола.[130][131] Таким образом, в 1825 году Фарадей невольно обнаружил, что этанол можно производить из этилен (компонент угольного газа) на кислотно-катализированный гидратация, процесс, подобный текущему промышленному синтезу этанола.[132]
Этанол использовался в качестве топлива для ламп в Соединенных Штатах еще в 1840 году, но в течение гражданская война сделали это использование неэкономичным. Налог был отменен в 1906 году.[133] Использование в качестве автомобильного топлива восходит к 1908 году, когда Ford Модель T может работать на бензин (бензин) или этанол.[134] Это подпитывает некоторые спиртовые лампы.
Этанол, предназначенный для промышленного использования, часто получают из этилен.[135] Этанол широко используется в качестве растворителя веществ, предназначенных для контакта или потребления человеком, включая запахи, ароматизаторы, красители и лекарства. В химии это одновременно и растворитель, и сырье для синтеза других продуктов. Он имеет долгую историю как топливо для тепла и света, а в последнее время как топливо для двигатель внутреннего сгорания.
Смотрите также
Рекомендации
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 30. Дои:10.1039/9781849733069-00001. ISBN 978-0-85404-182-4.
- ^ «Метанол». PubChem. PubChem. Получено 2 сентября 2020.
- ^ а б c d Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 3.246. ISBN 1439855110.
- ^ Баллинджер П., Лонг Ф.А. (1960). «Константы кислотной ионизации спиртов. II. Кислотности некоторых замещенных метанолов и родственных соединений1,2». Журнал Американского химического общества. 82 (4): 795–798. Дои:10.1021 / ja01489a008.
- ^ Арнетт Э.М., Венкатасубраманиам К.Г. (1983). «Термохимические кислотности в трех сверхосновных системах». J. Org. Chem. 48 (10): 1569–1578. Дои:10.1021 / jo00158a001.
- ^ Лиде ДР, изд. (2012). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press / Тейлор и Фрэнсис. С. 6–232.
- ^ Лиде ДР, изд. (2008). CRC Справочник по химии и физике (89 изд.). Бока-Ратон: CRC Press. С. 9–55.
- ^ «Паспорт безопасности этанола» (PDF). Архивировано из оригинал (PDF) 25 марта 2012 г.. Получено 8 июля 2018.
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0262". Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Этанол - Резюме соединения». Проект PubChem. США: Национальный центр биотехнологической информации.
- ^ Либих J (1834). "Ueber die Construction des Aethers und seiner Verbindungen" [О строении эфира и его соединений]. Annalen der Pharmacie (на немецком). 9 (22): 1–39. Bibcode:1834AnP ... 107..337L. Дои:10.1002 / andp.18341072202.
Со страницы 18: "Bezeichnen wir die Kohlenwasserstoffverbindung 4C + 10H als das Radikal des Aethers mit E2 und nennen es этил, ... "(Обозначим углеводородное соединение 4C + 10H радикалом эфира с E2 и назовите его этил ...).
- ^ Харпер, Дуглас. "этил". Интернет-словарь этимологии.
- ^ Отчет о Международной конференции по химической номенклатуре 1892 года см .:
- Армстронг Х (1892 г.). «Международная конференция по химической номенклатуре». Природа. 46 (1177): 56–59. Bibcode:1892Натура..46 ... 56А. Дои:10.1038 / 046056c0.
- Отчет Армстронга перепечатан с резолюциями на английском языке на следующих языках: Армстронг Х (1892 г.). «Международная конференция по химической номенклатуре». Журнал аналитической и прикладной химии. 6 (1177): 390–400 (398). Bibcode:1892Натура..46 ... 56А. Дои:10.1038 / 046056c0.
Спирты и фенолы будут называться после названия углеводорода, из которого они получены, с суффиксом на конце. ол (например, пентанол, пентинол и т. д.)
- ^ OED; etymonline.com
- ^ Погорецкий, Лариса А .; Брик, Джон (январь 1988 г.). «Фармакология этанола». Фармакология и терапия. 36 (2–3): 335–427. Дои:10.1016 / 0163-7258 (88) 90109-X. PMID 3279433.
- ^ Макдоннелл Г., Рассел А.Д. (январь 1999 г.). «Антисептики и дезинфицирующие средства: активность, действие, устойчивость». Обзоры клинической микробиологии. 12 (1): 147–79. Дои:10.1128 / CMR.12.1.147. ЧВК 88911. PMID 9880479.
- ^ «Химические дезинфицирующие средства | Рекомендации по дезинфекции и стерилизации | Библиотека руководств | Инфекционный контроль | CDC». www.cdc.gov. Получено 29 января 2018.
- ^ «Почему 70% этанол используется для протирки микробиологических рабочих зон?». ResearchGate. Получено 29 января 2018.
- ^ "Этиловый спирт". www.drugbank.ca. Получено 28 января 2019.
- ^ Скалли Р. (сентябрь 2002 г.). «Лечение отравления этиленгликолем». Американский семейный врач. 66 (5): 807–813. PMID 12322772. Получено 15 января 2018.
- ^ Beauchamp, GA; Валенто, М. (сентябрь 2016 г.). «Проглатывание токсичного алкоголя: быстрое распознавание и лечение в отделении неотложной помощи». Практика неотложной медицинской помощи. 18 (9): 1–20. PMID 27538060.
- ^ «Содержание алкоголя в обычных препаратах» (PDF). Медицинское общество штата Нью-Йорк. Получено 8 октября 2019.
- ^ Адамс К.Е., Ранс Т.С. (декабрь 2013 г.). «Побочные реакции на алкоголь и алкогольные напитки». Анналы аллергии, астмы и иммунологии. 111 (6): 439–45. Дои:10.1016 / j.anai.2013.09.016. PMID 24267355.
- ^ Zuccotti GV, Fabiano V (июль 2011 г.). «Вопросы безопасности этанола в качестве вспомогательного вещества в лекарствах, предназначенных для педиатрического применения». Экспертное заключение о безопасности лекарственных средств. 10 (4): 499–502. Дои:10.1517/14740338.2011.565328. PMID 21417862. S2CID 41876817.
- ^ а б Харгер Р.Н. (1958). «Фармакология и токсикология алкоголя». Журнал Американской медицинской ассоциации. 167 (18): 2199–202. Дои:10.1001 / jama.1958.72990350014007. PMID 13563225.
- ^ Валлнер М, Олсен Р.В. (2008). "Физиология и фармакология алкоголя: сайт антагониста имидазобензодиазепинового спирта на подтипах рецепторов ГАМК как возможность для разработки лекарств?". Британский журнал фармакологии. 154 (2): 288–98. Дои:10.1038 / bjp.2008.32. ЧВК 2442438. PMID 18278063.
- ^ Употребление алкоголя и безопасное питье. Национальные институты здоровья США.
- ^ «Приложение B - Книга данных по транспортной энергии». Центр транспортного анализа из Национальная лаборатория Окриджа.
- ^ а б Эйдоган М, Оззезен АН, Чанакчи М, Тюрккан А (2010). «Влияние топливных смесей спирт-бензин на рабочие характеристики и характеристики сгорания двигателя SI». Топливо. 89 (10): 2713–2720. Дои:10.1016 / j.fuel.2010.01.032.
- ^ а б Томас, Джордж: «Обзор водородной программы Министерства энергетики США по развитию систем хранения» (PDF). Архивировано из оригинал (PDF) 21 февраля 2007 г. (99,6 КБ). Ливермор, Калифорния. Сандийские национальные лаборатории. 2000 г.
- ^ Томас Дж. (2000). «Обзор водородной программы Министерства энергетики США по развитию систем хранения» (PDF). Сандийские национальные лаборатории. Получено 1 августа 2009.
- ^ «Доступность источников Е85». Чистый воздух Trust. Получено 27 июля 2015.
- ^ Катушка М (19 августа 2006 г.). «Путь Бразилии к энергетической независимости». Вашингтон Пост.
- ^ Chow D (26 апреля 2010 г.). «Rocket Racing League представляет новый летающий хотрод». Space.com. Получено 27 апреля 2010.
- ^ Грин Р. "Модель Т Ford Club Australia (Inc.)". Архивировано из оригинал 14 января 2014 г.. Получено 24 июн 2011.
- ^ «Этанол 101». Американская коалиция за этанол.
- ^ Коалиция за энергетическое будущее. "Часто задаваемые вопросы о биотопливе". Справочник по биотопливу. Фонд ООН. Архивировано из оригинал 19 февраля 2011 г.
- ^ Малакиас, Аугусто Сезар Тейшейра; Нетто, Нилтон Антонио Диниз; Филью, Фернандо Антонио Родригес; да Коста, Роберто Берлини Родригеш; Лангеани, Маркос; Бета, Хосе Гильерме Коэльо (18 ноября 2019 г.). «Вводящая в заблуждение полная замена двигателей внутреннего сгорания электродвигателями и исследование важности бразильского этанола для устойчивого будущего мобильности: обзор». Журнал Бразильского общества механических наук и инженерии. 41 (12): 567. Дои:10.1007 / s40430-019-2076-1. ISSN 1806-3691.
- ^ Калифорнийский совет по воздушным ресурсам (октябрь 1989 г.). «Определение транспортного средства с низким уровнем выбросов в соответствии с положениями раздела 39037.05 Кодекса охраны труда и техники безопасности, второй выпуск». Архивировано из оригинал 18 февраля 2018 г.. Получено 18 февраля 2018.
- ^ Лоуи А., Картер В.П. (март 1990 г.). Метод оценки воздействия на атмосферный озон фактических выбросов транспортных средств. S.A.E. Технический документ. Варрендейл, Пенсильвания.
- ^ Джонс ТТ (2008). «Отчет о чистом топливе: количественное сравнение моторного топлива, связанных с ним загрязнений и технологий». researchchandmarkets.com. Архивировано из оригинал 9 сентября 2012 г.
- ^ Тао Р (16–20 августа 2010 г.). Электро-реологические жидкости и магнитореологические суспензии. Материалы 12-й Международной конференции.. Филадельфия, США: World Scientific. ISBN 9789814340229.
- ^ Бьелло Д. «Хотите уменьшить загрязнение воздуха? Не полагайтесь на этанол обязательно». Scientific American. Получено 11 июля 2017.
- ^ «Принятие мер по контролю над переносимыми по воздуху токсичными веществами для снижения выбросов формальдегида из композитных древесных материалов». США: Ассоциация производителей окон и дверей. 30 июля 2008 г. Архивировано с оригинал 9 марта 2010 г.
- ^ «Мировое производство топливного этанола в 2008 году». США: Ассоциация возобновляемых источников топлива.
- ^ "Tecnologia flex atrai estrangeiros". Agência Estado.
- ^ «Объявлен первый коммерческий завод по биопереработке целлюлозного этанола в США». Ассоциация возобновляемых источников топлива. 20 ноября 2006 г.. Получено 31 мая 2011.
- ^ Сорго сладкое для еды, кормов и топлива Новый агроном, январь 2008 г.
- ^ Развитие производственно-сбытовой цепочки сладкого сорго этанола ИКРИСАТ, 2013
- ^ Хорн М., Крупп Ф (16 марта 2009 г.). Земля: Продолжение: Гонка за переосмысление энергии и прекращение глобального потепления. Физика сегодня. 62. С. 63–65. Bibcode:2009ФТ .... 62д..63К. Дои:10.1063/1.3120901. ISBN 978-0-393-06810-8.
- ^ Механики видят, что этанол повреждает малые двигатели, NBC News, 8 января 2008 г.
- ^ Кларк, Джон Д. (2017). Ingnition! Неофициальная история жидкого ракетного топлива. Нью-Брансуик, Нью-Джерси: Издательство Университета Рутгерса. п. 9. ISBN 978-0-8135-9583-2.
- ^ Дарлинг Д. "Интернет-энциклопедия науки: V-2".
- ^ а б Брауниг, Роберт А. «Ракетное топливо». (Интернет сайт). Rocket & Space Technology, 2006. Проверено 23 августа 2007 г.
- ^ «Краткая история ракетной техники». Исторический архив НАСА, через science.ksc.nasa.gov.
- ^ Бадвал С.П., Гиддей С., Кулкарни А., Гоэль Дж., Басу С. (май 2015 г.). «Топливные элементы на этаноле прямого действия для транспортных и стационарных применений - всесторонний обзор». Прикладная энергия. 145: 80–103. Дои:10.1016 / j.apenergy.2015.02.002.
- ^ "Могут ли этанольные камины быть уютными?". Wall Street Journal. Получено 2 марта 2016.
- ^ «Ваш путеводитель по экстракции этанола». Cannabis Business Times. Получено 9 апреля 2019.
- ^ а б c Лиде ДР, изд. (2000). CRC Справочник по химии и физике 81-е издание. CRC Press. ISBN 978-0-8493-0481-1.
- ^ "Что такое тройная точка алкоголя?". Webanswers.com. 31 декабря 2010 г. Архивировано с оригинал 14 мая 2013 г.[необходима научная цитата ]
- ^ а б c d Виндхольц М (1976). Индекс Merck: энциклопедия химикатов и лекарств (9-е изд.). Рэуэй, Нью-Джерси, США: Merck. ISBN 978-0-911910-26-1.[страница нужна ]
- ^ а б c Моррисон RT, Бойд RN (1972). Органическая химия (2-е изд.). Allyn and Bacon, inc. ISBN 978-0-205-08452-4.[страница нужна ]
- ^ Дальманн У., Шнайдер GM (1989). «(Жидкость + жидкость) фазовые равновесия и критические кривые (этанол + додекан или тетрадекан, или гексадекан, или 2,2,4,4,6,8,8-гептаметилнонан) от 0,1 МПа до 120,0 МПа». J Chem Thermodyn. 21 (9): 997–1004. Дои:10.1016/0021-9614(89)90160-2.
- ^ "Этиловый спирт". Энциклопедия химической технологии. 9. 1991. стр. 813.
- ^ Костиган М.Дж., Ходжес Л.Дж., Марш К.Н., Стоукс Р.Х., Таксфорд К.В. (1980). «Изотермический калориметр смещения: модификации конструкции для измерения экзотермических энтальпий смешения». Aust. J. Chem. 33 (10): 2103. Bibcode:1982AuJCh..35.1971I. Дои:10.1071 / CH9802103.
- ^ Лэй З., Ван Х., Чжоу Р., Дуань З. (2002). «Влияние соли, добавляемой в растворитель, на экстрактивную перегонку». Chem. Англ. J. 87 (2): 149–156. Дои:10.1016 / S1385-8947 (01) 00211-X.
- ^ Пембертон RC, Маш CJ (1978). «Термодинамические свойства водных смесей неэлектролитов II. Давление пара и избыточная энергия Гиббса для воды + этанола при 303,15–363,15 К, определенные точным статическим методом». J Chem Thermodyn. 10 (9): 867–888. Дои:10.1016 / 0021-9614 (78) 90160-Х.
- ^ Индекс химических веществ и лекарств Мерк, 9 изд .; монографии с 6575 по 6669
- ^ «Точка воспламенения и точка возгорания». Nttworldwide.com. Архивировано из оригинал 14 декабря 2010 г.
- ^ а б NFPA 325: Руководство по пожароопасным свойствам легковоспламеняющихся жидкостей, газов и летучих твердых веществ. Куинси, Массачусетс: Национальная ассоциация противопожарной защиты (NFPA). 1 января 1994 г.
- ^ а б «49 CFR § 173.120 - Класс 3 - Определения». Кодекс федерального регулирования. Название 49.
легковоспламеняющаяся жидкость (класс 3) означает жидкость с температурой вспышки не более 60 ° C (140 ° F).
- ^ а б c d е ж грамм час я j k Мартинес, П.Дж .; Русь, Э .; Compaña, J.M. «Определение температуры вспышки бинарных смесей спиртов, кетонов и воды». Departamento de Ingeniería Química. Facultad de Ciencias.: 3.
Стр. 3, Таблица 4
- ^ "49 CFR § 172.101 - Назначение и использование таблицы опасных материалов". Кодекс федерального регулирования. Название 49.
Описание опасных материалов и надлежащие отгрузочные наименования: этанол или этиловый спирт, или растворы этанола или растворы этилового спирта; Класс опасности: 3; Идентификационные номера: UN1170; PG: II; Коды этикеток: 3;
- ^ а б c d е ж грамм час я j Ха, Дон-Мён; Пак, Санг Хун; Ли, Сонджин (апрель 2015 г.). «Измерение температуры вспышки систем вода-метанол и вода-этанол с помощью тестера Seta Flash Closed Cup Tester». Пожарная наука и инженерия. 29 (2): 39–43. Дои:10.7731 / KIFSE.2015.29.2.039.
Стр. 4, Таблица 3
- ^ «Температуры вспышки водных растворов на основе этанола». Engineeringtoolbox.com. Получено 23 июн 2011.
- ^ Дадли Р. (август 2004 г.). «Этанол, созревание плодов и исторические истоки человеческого алкоголизма у плодоядных приматов». Интегративная и сравнительная биология. 44 (4): 315–23. Дои:10.1093 / icb / 44.4.315. PMID 21676715.
- ^ Грабер C (2008). «Факт или вымысел? Животные любят напиваться». Scientific American. Получено 23 июля 2010.
- ^ Leblová S, Sinecká E, Vaníčková V (1974). «Метаболизм пирувата в прорастающих семенах при естественном анаэробиозе». Biologia Plantarum. 16 (6): 406–411. Дои:10.1007 / BF02922229. S2CID 34605254.
- ^ Schriver A, Schriver-Mazzuoli L, Ehrenfreund P, d'Hendecourt L (2007). "Одно возможное происхождение этанола в межзвездной среде: фотохимия смешанного CO.2–C2ЧАС6 фильмы при 11 К. Исследование FTIR ». Химическая физика. 334 (1–3): 128–137. Bibcode:2007CP .... 334..128S. Дои:10.1016 / j.chemphys.2007.02.018.
- ^ Тернер С., Спанель П., Смит Д. (2006). «Продольное исследование этанола и ацетальдегида в выдыхаемом воздухе здоровых добровольцев с использованием масс-спектрометрии с проточной трубкой с отобранными ионами». Быстрые коммуникации в масс-спектрометрии. 20 (1): 61–8. Bibcode:2006RCMS ... 20 ... 61 т. Дои:10.1002 / rcm.2275. PMID 16312013.
- ^ Doucleff M (17 сентября 2013 г.). «Синдром автопивоварни: очевидно, пиво можно варить в кишечнике». ЭНЕРГЕТИЧЕСКИЙ ЯДЕРНЫЙ РЕАКТОР.
- ^ Миллс Г.А., Эклунд Э.Е. (1987). «Спирты как компоненты транспортного топлива». Ежегодный обзор энергетики. 12: 47–80. Дои:10.1146 / annurev.eg.12.110187.000403.
- ^ Витткофф HA, Рубен BG, Плоткин JS (2004). Промышленные органические химикаты. Джон Вили и сыновья. С. 136–. ISBN 978-0-471-44385-8.
- ^ Робертс Дж. Д., Caserio MC (1977). Основные принципы органической химии. W. A. Benjamin, Inc. ISBN 978-0-8053-8329-4.[страница нужна ]
- ^ а б c d Kosaric N, Duvnjak Z, Farkas A, Sahm H, Bringer-Meyer S, Goebel O, Mayer D (2011). "Этиловый спирт". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. С. 1–72. Дои:10.1002 / 14356007.a09_587.pub2. ISBN 9783527306732.(требуется подписка)
- ^ "Этиловый спирт". Энциклопедия химической технологии. 9. 1991. стр. 82.
- ^ Этиловый спирт. Essentialchemicalindustry.org
- ^ Харрисон, Тим (май 2014 г.) Веб-страницы Catalysis для доуниверситетских студентов V1_0. Bristol ChemLabS, Школа химии, Бристольский университет
- ^ Lodgsdon JE (1991). "Этиловый спирт". В Howe-Grant, Mary, Kirk, Raymond E., Othmer, Donald F., Kroschwitz, Jacqueline I. (ред.). Энциклопедия химической технологии. 9 (4-е изд.). Нью-Йорк: Вили. п. 817. ISBN 978-0-471-52669-8.
- ^ а б c d е Streitwieser A, Хиткок СН (1976). Введение в органическую химию. Макмиллан. ISBN 978-0-02-418010-0.
- ^ Шу Ся и Теодор Визнер (июнь 2008 г.). Биологическое производство этанола из CO2, производимого электростанцией, работающей на ископаемом топливе. 3-я конференция IEEE по промышленной электронике и приложениям, 2008 г.. С. 1814–1819. Дои:10.1109 / ICIEA.2008.4582832. ISBN 978-1-4244-1717-9. S2CID 14095619.
- ^ Лью Ф., Хенстра А.М., Кёпке М., Винцер К., Симпсон С.Д., Минтон Н.П. (март 2017 г.). «Метаболическая инженерия Clostridium autoethanogenum для селективного производства алкоголя». Метаболическая инженерия. 40: 104–114. Дои:10.1016 / j.ymben.2017.01.007. ЧВК 5367853. PMID 28111249.
- ^ «Солнечная топливная система перерабатывает CO2 для получения этанола и этилена». Центр новостей. 18 сентября 2017 г.. Получено 19 сентября 2017.
- ^ «Исследователь ТУ Делфт делает спирт из воздуха». TU Delft. Получено 19 сентября 2017.
- ^ Ма, Мин; и другие. (Апрель 2016 г.). «Управляемое образование углеводородов в результате электрохимического восстановления СО2 с помощью массивов нанопроволок Cu». Angewandte Chemie. 55 (23): 6680–4. Дои:10.1002 / anie.201601282. PMID 27098996.
- ^ Menetrez MY (июль 2012 г.). «Обзор производства биотоплива из водорослей и потенциального воздействия на окружающую среду» (PDF). Экологические науки и технологии. 46 (13): 7073–85. Bibcode:2012EnST ... 46,7073M. CiteSeerX 10.1.1.665.3435. Дои:10.1021 / es300917r. PMID 22681590. Архивировано из оригинал (PDF) 8 августа 2017 г.. Получено 24 октября 2017.
- ^ Clines T (июль 2006 г.). «Лучше варить этанол». Популярная наука в Интернете. Архивировано из оригинал 3 ноября 2007 г.
- ^ Химики, Американская ассоциация зерновых (1986). Достижения в области зерновой науки и технологий. Американская ассоциация химиков зерновых, Incorporated. ISBN 9780913250457.
- ^ Сонг Й, Пэн Р., Хенсли Д. К., Боннесен П. В., Лян Л., Ву З., Мейер Н. М., Чи М., Ма С., Самптер Б. Г., Рондиноне А. Дж. (2016). «Электрохимическое превращение CO2 в этанол с высокой селективностью с использованием электрода с наночастицами меди / N-легированного графена». ХимияВыбрать. 1 (Препринт): 6055–6061. Дои:10.1002 / slct.201601169.
- ^ Чон Дж, Чжон Х, Ко К, Чунг Би, Чой Джи (2012). «Производство безводного этанола с использованием различных процессов PSA (адсорбция при переменном давлении) на пилотной установке». Возобновляемая энергия. 42: 41–45. Дои:10.1016 / j.renene.2011.09.027.
- ^ «Программа U-M по сокращению потребления безналогового алкоголя; денатурированный спирт - более безопасная и менее дорогая альтернатива» (PDF). Университет Мичигана. Архивировано из оригинал (PDF) 27 ноября 2007 г.. Получено 29 сентября 2007.
- ^ Великобритания (2005 г.). Положения о денатурированном алкоголе 2005 г.. Законодательный акт 2005 г. № 1524.
- ^ Бансал РК, Бернтсен А (2003). Учебник органической химии. New Age International Limited. С. 402–. ISBN 978-81-224-1459-2.
- ^ Кристиан Г.Д. (2004). «Растворители для спектрометрии». Аналитическая химия. 1 (6-е изд.). Хобокен, штат Нью-Джерси: John Wiley & Sons. п.473. ISBN 978-0471214724.
- ^ Эндрюс С. (1 августа 2007 г.). Учебник еды и Bevrge Mgmt. Тата Макгроу-Хилл Образование. С. 268–. ISBN 978-0-07-065573-7.
- ^ Kunkee RE, Amerine MA (июль 1968 г.). «Сахарная и спиртовая стабилизация дрожжей в сладком вине». Прикладная микробиология. 16 (7): 1067–75. Дои:10.1128 / AEM.16.7.1067-1075.1968. ЧВК 547590. PMID 5664123.
- ^ Циммерманн, Хайнц; Вальц, Роланд (2008). «Этилен». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a10_045.pub3. ISBN 978-3527306732.
- ^ Россини Ф.Д. (1937). «Теплоты образования простых органических молекул». Ind. Eng. Chem. 29 (12): 1424–1430. Дои:10.1021 / ie50336a024.
- ^ Рассчитано по теплотам образования из CRC Handbook of Chemistry and Physics, 49th Edition, 1968–1969.
- ^ Чакрабартти С.К. (1978). Трахановский В.С. (ред.). Окисление в органической химии. Нью-Йорк: Academic Press. С. 343–370.
- ^ Рейнхард Дж., Копп Э., МакКусик BC, Рёдерер Г., Бош А., Флейшманн Г. (2007). «Хлорацетальдегиды». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a06_527.pub2. ISBN 978-3527306732.
- ^ Протокол собрания. Технический комитет по классификации и свойствам опасных химических веществ (12–13 января 2010 г.).
- ^ а б «Данные о безопасности этилового спирта». Оксфордский университет. 9 мая 2008 г.. Получено 3 января 2011.
- ^ «Дезинфицирующие средства для рук COVID-19». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 9 июля 2020.
- ^ «FDA обновляет дезинфицирующие средства для рук, которые потребители не должны использовать». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 31 июля 2020.
- ^ Роуч Дж (18 июля 2005 г.). «Пиво 9000-летней выдержки, воссозданное по китайскому рецепту». Новости National Geographic. Получено 3 сентября 2007.
- ^ а б аль-Хасан А.Ю. (2001). Наука и технологии в исламе: технологии и прикладные науки. ЮНЕСКО. С. 65–69.
- ^ Хасан А.Ю.. «Алкоголь и дистилляция вина из арабских источников». История науки и техники в исламе. Получено 19 апреля 2014.
- ^ «Жидкий огонь - арабы открыли, как перегонять спирт. Они до сих пор делают это лучше всех, говорят некоторые». Экономист. 18 декабря 2003 г.
- ^ Шлоссер, Стефан (2011). «Дистилляция - от бронзового века до наших дней». Конференция: 38-я Междунар. Конф. SSCHE, в Татранске-Матлиаре (Словакия).
- ^ а б Хабиб, Ирфан (2011). Экономическая история средневековой Индии, 1200-1500 гг.. Pearson Education India. С. 55–. ISBN 978-81-317-2791-1.
- ^ а б Forbes RJ (1948). Краткая история искусства дистилляции. Брилл. п. 89. ISBN 978-9004006171.
- ^ а б Haw SG (2006). «Вино, женщины и яд». Марко Поло в Китае. Рутледж. С. 147–148. ISBN 978-1-134-27542-7. Получено 10 июля 2016.
Самым ранним периодом, по-видимому, является династия Восточная Хань ... наиболее вероятный период для начала истинной дистилляции спиртных напитков в Китае - во времена династий Цзинь и Южная Сун.
- ^ Ловиц Т (1796 г.). "Anzeige eines, zur volkommen Entwasserung des Weingeistes nothwendig zu beobachtenden, Handgriffs" [Отчет о задаче, которая должна быть выполнена для полного обезвоживания винных спиртов [т.е. азеотропа спирт-вода])]. Chemische Annalen für die Freunde der Naturlehre, Aerznengelartheit, Haushaltungskunde und Manufakturen (на немецком). 1: 195–204.
См. Стр. 197–198: Lowitz обезвоживает азеотроп, смешивая его с 2: 1 избытком безводной щелочи и затем перегоняя смесь на медленном огне.
- ^ Чисхолм, Хью, изд. (1911). . Британская энциклопедия. 1 (11-е изд.). Издательство Кембриджского университета. С. 525–527.
- ^ де Соссюр Т (1807). "Воспоминания о композиции алкоголя и серного эфира". Journal de Physique, de Chimie, d'Histoire Naturelle et des Arts. 64: 316–354. В своей статье 1807 года Соссюр лишь приблизительно определил состав этанола; Более точный анализ этанола представлен на странице 300 его статьи 1814 года: де Соссюр, Теодор (1814). "Новые наблюдения за составом алкоголя и серы". Annales de Chimie et de Physique. 89: 273–305.
- ^ Купер А.С. (1858 г.). «О новой химической теории» (онлайн-перепечатка). Философский журнал. 16 (104–16). Получено 3 сентября 2007.
- ^ Фарадей М (1825 г.). «О новых соединениях углерода и водорода и некоторых других продуктах, полученных при разложении нефти под действием тепла». Философские труды Лондонского королевского общества. 115: 440–466. Дои:10.1098 / рстл.1825.0022. В сноске на странице 448 Фарадей отмечает действие серной кислоты на угольный газ и угольно-газовый дистиллят; в частности, «[серная] кислота соединяется непосредственно с углеродом и водородом; и я обнаружил, что когда [полученное соединение] объединяется с основаниями, [оно] образует особый класс солей, несколько напоминающих сульфовинаты [то есть этилсульфаты], но все еще отличается от них ".
- ^ Хеннелл Х (1826 г.). «О взаимном действии серной кислоты и спирта с наблюдениями за составом и свойствами полученного соединения». Философские труды Лондонского королевского общества. 116: 240–249. Дои:10.1098 / рстл.1826.0021. S2CID 98278290. На странице 248 Хеннелл упоминает, что Фарадей дал ему серную кислоту, в которой растворялся угольный газ, и что он (Хеннелл) обнаружил, что она содержит «сульфовиновую кислоту» (этилгидросульфат).
- ^ Хеннелл Х (1828). «О взаимном действии серной кислоты и спирта и о природе процесса образования эфира». Философские труды Лондонского королевского общества. 118: 365–371. Дои:10.1098 / рстл.1828.0021. S2CID 98483646. На странице 368 компания Hennell производит этанол из «сульфовиновой кислоты» (этилгидросульфат ).
- ^ Серуллас G (1828). Гайтон де Морво Л., Гей-Люссак Дж. Л., Араго Ф., Мишель Эжен Шеврёль, Марселен Бертло, Элеутер Эли, Николя Маскар, Альбин Халлер (ред.). "De l'action de l'acide sulfique sur l'alcool, et des produits qui en résultent". Annales de Chimie et de Physique. 39: 152–186. На странице 158 Серуллас упоминает производство спирта из «сульфатной кислоты д'гидрогена карбонэ» (сульфата углеводородной кислоты).
- ^ В 1855 г. французский химик Марселлен Бертло подтвердил открытие Фарадея, приготовив этанол из чистого этилена. Бертело М (1855). Араго Ф., Гей-Люссак Дж. Л. (ред.). "Sur la education de l'alcool au moyen du bicarbure d'hydrogène (Об образовании спирта с помощью этилена)". Annales de Chimie et de Physique. 43: 385–405. (Примечание: химические формулы в статье Бертло неверны, потому что химики в то время использовали неправильные атомные массы для элементов; например, углерод (6 вместо 12), кислород (8 вместо 16) и т. Д.)
- ^ Сигель Р. (15 февраля 2007 г.). «Этанол, которого когда-то обходили, теперь стремительно растет». энергетический ядерный реактор. Получено 22 сентября 2007.
- ^ ДиПардо Х. «Перспективы производства и спроса на этанол из биомассы» (PDF). Министерство энергетики США. Архивировано из оригинал (PDF) 24 сентября 2015 г.. Получено 22 сентября 2007.
- ^ Майерс Р.Л., Майерс Р.Л. (2007). 100 важнейших химических соединений: справочное руководство. Вестпорт, Коннектикут: Greenwood Press. п. 122. ISBN 978-0-313-33758-1.
дальнейшее чтение
- Бойс Дж. М., Питте Д. (2003). «Гигиена рук в медицинских учреждениях». Атланта, Грузия, Соединенные Штаты: Центры по контролю за заболеваниями..
- Onuki S, Koziel JA, van Leeuwen J, Jenks WS, Grewell D, Cai L (июнь 2008 г.). Методы производства, очистки и анализа этанола: обзор. Ежегодное международное собрание ASABE, 2008 г. Провиденс, Род-Айленд. Получено 16 февраля 2013.
- «Разъяснение обозначений денатурированного спирта в США». Научные игрушки.
- Ланге, Норберт Адольф (1967). Джон Ори Дин (ред.). Справочник Ланге по химии (10-е изд.). Макгроу-Хилл.CS1 maint: ref = harv (связь)
внешняя ссылка
- Спирт (этанол) в Периодическая таблица видео (Ноттингемский университет)
- Международная организация труда информация о безопасности этанола
- Национальный реестр загрязнителей - Информационный бюллетень по этанолу
- CDC - Карманное руководство NIOSH по химической опасности - этиловый спирт
- Национальный институт стандартов и технологий химические данные об этаноле
- Чикагская торговая палата новости и рыночные данные по фьючерсам на этанол
- Расчет давление газа, плотность жидкости, динамическая вязкость жидкости, поверхностное натяжение этанола
- История этанола Взгляд в историю этанола
- ChemSub Online: Этиловый спирт
- Технологическая схема производства промышленного этанола с использованием этилена и серной кислоты