Уксусная кислота - Acetic acid
| |||
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Уксусная кислота[3] | |||
| Систематическое название ИЮПАК Этановая кислота | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 3DMet | |||
| Сокращения | AcOH | ||
| 506007 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.528 | ||
| Номер ЕС |
| ||
| Номер E | E260 (консерванты) | ||
| 1380 | |||
| КЕГГ | |||
| MeSH | Уксусная + кислота | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2789 | ||
| |||
| |||
| Характеристики | |||
| C2ЧАС4О2 | |||
| Молярная масса | 60.052 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Сильно похож на уксус | ||
| Плотность | 1,049 г см−3 (жидкость); 1,27 г см−3 (твердый) | ||
| Температура плавления | От 16 до 17 ° С; От 61 до 62 ° F; От 289 до 290 К | ||
| Точка кипения | От 118 до 119 ° С; От 244 до 246 ° F; От 391 до 392 К | ||
| Смешиваемый | |||
| бревно п | -0.28[4] | ||
| Кислотность (пKа) | |||
| Основность (пKб) | 9,24 (основность ацетат-иона) | ||
| Основание конъюгата | Ацетат | ||
| -31.54·10−6 см3/ моль | |||
| 1,371 (ВD = 18,19) | |||
| Вязкость | 1,22 мПа с | ||
| 1,74 Д | |||
| Термохимия | |||
Теплоемкость (C) | 123,1 Дж К−1 моль−1 | ||
Стандартный моляр энтропия (S | 158.0 Дж К−1 моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -483,88–483,16 кДж моль−1 | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | -875,50–874,82 кДж моль−1 | ||
| Фармакология | |||
| G01AD02 (ВОЗ) S02AA10 (ВОЗ) | |||
| Опасности | |||
| Паспорт безопасности | Видеть: страница данных | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H226, H314 | |||
| P280, P305 + 351 + 338, P310 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 40 ° С (104 ° F, 313 К) | ||
| 427 ° С (801 ° F, 700 К) | |||
| Пределы взрываемости | 4–16% | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 3,31 г кг−1, оральный (крыса) | ||
LC50 (средняя концентрация ) | 5620 частей на миллион (мышь, 1 час) 16000 частей на миллион (крыса, 4 часа)[8] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 10 частей на миллион (25 мг / м3)[7] | ||
REL (Рекомендуемые) | TWA 10 частей на миллион (25 мг / м3) ST 15 частей на миллион (37 мг / м3)[7] | ||
IDLH (Непосредственная опасность) | 50 частей на миллион[7] | ||
| Родственные соединения | |||
Связанный карбоновые кислоты | Муравьиная кислота Пропионовая кислота | ||
Родственные соединения | Ацетальдегид Ацетамид | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
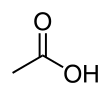
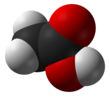
Уксусная кислота /əˈsятɪk/, систематически названный этановая кислота /ˌɛθəˈпoʊɪk/, представляет собой бесцветную жидкость органическое соединение с химическая формула CH3COOH (также пишется как CH3CO2H, C2ЧАС4О2, или HC2ЧАС3О2). В неразбавленном виде его иногда называют ледяная уксусная кислота. Уксус содержит не менее 4% уксусной кислоты по объему, что делает уксусную кислоту основным компонентом уксуса, помимо воды. Уксусная кислота имеет характерный кисловатый вкус и резкий запах. Помимо домашнего уксуса, его в основном производят как предшественник поливинилацетат и ацетат целлюлозы. Классифицируется как слабая кислота так как это только частично диссоциирует в растворе, но концентрированная уксусная кислота вызывает коррозию и может повредить кожу.
Уксусная кислота - вторая простейшая карбоновая кислота (после Муравьиная кислота ). Он состоит из метильная группа прикреплен к карбоксильная группа. Это важный химический реагент и промышленные химикаты, используемые в основном в производстве ацетат целлюлозы за фотопленка, поливинилацетат для дерева клей, синтетические волокна и ткани. В домашних условиях разбавленную уксусную кислоту часто используют в средства для удаления накипи. в пищевая промышленность, уксусная кислота контролируется код пищевой добавки E260 как регулятор кислотности и в качестве приправы. В биохимия, ацетильная группа, полученная из уксусной кислоты, имеет фундаментальное значение для всех форм жизни. Когда привязан к кофермент А, это центральное место в метаболизм из углеводы и жиры.
Мировой спрос на уксусную кислоту составляет около 6,5 млн. метрических тонн в год (Мт / год), из которых примерно 1,5 Мт / год приходится на переработку; остальная часть произведена из метанол.[9] Уксус - это в основном разбавленная уксусная кислота, которую часто производят ферментация и последующее окисление этиловый спирт.
Номенклатура
В банальное имя уксусная кислота является наиболее часто используемым и предпочтительное название ИЮПАК. Систематическое название этановая кислотадействующий ИЮПАК имя, составлено согласно заместительной номенклатуре.[10] Название уксусная кислота происходит от ацетум, то латинский слово для уксус, и связано со словом кислота сам.
Ледяная уксусная кислота это название безводного (безводный ) уксусная кислота. Подобно Немецкий имя Eisessig (ледяной уксус), название происходит от ледяных кристаллов, которые образуются при температуре 16,6 ° C (61,9 ° F) при температуре чуть ниже комнатной (присутствие 0,1% воды понижает температуру плавления на 0,2 ° C).[11]
Обычный символ для уксусной кислоты AcOH, куда Ac это символ псевдоэлемента представляющий ацетил группа CH
3−C (= O) -; то сопряженное основание, ацетат (CH
3COO−), таким образом, представляется как AcO−.[12] (The Ac не следует путать с символом элемента актиний; контекст предотвращает путаницу среди химиков-органиков). Чтобы лучше отразить ее структуру, уксусную кислоту часто пишут как CH
3–C (O) OH, CH
3−C (= O) ОН, CH
3COOH и CH
3CO
2ЧАС. В контексте кислотно-основные реакции, сокращение HAc иногда используется,[13] куда Ac в данном случае это символ ацетата (а не ацетила). Ацетат - это ион в результате потери ЧАС+
из уксусной кислоты. Название ацетат может также относиться к поваренная соль содержащий этот анион, или сложный эфир уксусной кислоты.[14]
Характеристики

Кислотность
Водородный центр в карбоксильная группа (-COOH) в карбоновых кислотах, таких как уксусная кислота, может отделяться от молекулы путем ионизации:
- CH3COOH ⇌ CH3CO2− + H+
Из-за этого выпуска протон (ЧАС+), уксусная кислота имеет кислый характер. Уксусная кислота - слабый монопротовая кислота. В водном растворе имеет pKа значение 4,76.[15] это сопряженное основание является ацетат (CH3COO−). А 1.0M раствор (о концентрации домашнего уксуса) имеет pH 2,4, что указывает на то, что диссоциирует только 0,4% молекул уксусной кислоты.[16] Однако в очень разбавленных (<10−6 M) раствор уксусной кислоты диссоциирован на> 90%.


Структура
В твердой уксусной кислоте молекулы образуют цепочки, причем отдельные молекулы соединяются между собой водородные связи.[17] В паре при 120 ° C (248 ° F) можно обнаружить димеры. Димеры также встречаются в жидкой фазе в разбавленных растворах в растворителях, не связывающих водородные связи, и в некоторой степени в чистой уксусной кислоте,[18] но разрушаются растворителями, связывающими водородные связи. Диссоциация энтальпия димера оценивается в 65,0–66,0 кДж / моль, а энтропия диссоциации - в 154–157 Дж / моль.−1 K−1.[19] Другие карбоновые кислоты участвуют в подобных взаимодействиях межмолекулярных водородных связей.[20]
Свойства растворителя
Жидкость уксусная кислота - это гидрофильный (полярный ) протонный растворитель, похожий на этиловый спирт и воды. С умеренным относительная статическая диэлектрическая проницаемость (диэлектрическая проницаемость) 6,2, он растворяет не только полярные соединения, такие как неорганические соли и сахара, но также и неполярные соединения, такие как масла, а также полярные растворенные вещества. Смешивается с полярными и неполярными растворители например, вода, хлороформ, и гексан. С высшими алканами (начиная с октан ), уксусная кислота не смешивающийся при всех составах, а растворимость уксусной кислоты в алканах снижается с более длинными н-алканами.[21] Растворитель и смешиваемость свойства уксусной кислоты делают ее полезным промышленным химическим веществом, например, в качестве растворителя при производстве диметилтерефталат.[9]
Биохимия
При физиологических значениях pH уксусная кислота обычно полностью ионизируется до ацетат.
В ацетил группа, формально производное от уксусной кислоты, имеет фундаментальное значение для всех форм жизни. Когда привязан к кофермент А, это центральное место в метаболизм из углеводы и жиры. В отличие от карбоновых кислот с более длинной цепью ( жирные кислоты ) уксусная кислота не встречается в природных триглицериды. Однако искусственный триглицерид триацетин (триацетат глицерина) - обычная пищевая добавка, содержащаяся в косметике и лекарствах местного действия.[22]
Производится уксусная кислота и выделенный к уксуснокислые бактерии, особенно род Ацетобактер и Clostridium acetobutylicum. Эти бактерии повсеместно встречаются в продовольственные товары, воды, и почва, а уксусная кислота вырабатывается естественным путем при порче фруктов и других продуктов. Уксусная кислота также входит в состав вагинальная смазка из люди и другие приматы, где он, кажется, служит мягким антибактериальный агент.[23]
Производство

Уксусная кислота производится промышленным путем как синтетическим, так и бактериальным способом. ферментация. Около 75% уксусной кислоты, используемой в химической промышленности, производится карбонилирование из метанол, объяснено ниже.[9] На биологический путь приходится лишь около 10% мирового производства, но он остается важным для производства уксуса, поскольку многие законы о чистоте пищевых продуктов требуют, чтобы уксус, используемый в пищевых продуктах, имел биологическое происхождение. К другим процессам относятся изомеризация метилформиата, преобразование синтез-газа в уксусную кислоту и газофазное окисление этилена и этанола.[24] Уксусная кислота часто является побочным продуктом различных реакций, например, при гетерогенно-каталитическом синтезе акриловой кислоты.[25][26][27] или ферментативное производство молочной кислоты.[28] По состоянию на 2003–2005 годы общее мировое производство первичной уксусной кислоты[29] оценивалась в 5 млн т / год (миллион тонн в год), примерно половина из которых была произведена в Соединенные Штаты. Европейский добыча составляла примерно 1 млн т / год и снижалась, в то время как Японский добыча составила 0,7 млн т / год. Еще 1,5 млн т перерабатывались каждый год, в результате чего общий мировой рынок достиг 6,5 млн т / год.[30][31] С тех пор мировая добыча увеличилась до 10,7 млн т / год (в 2010 г.) и далее; однако прогнозируется замедление роста производства.[32] Два крупнейших производителя первичной уксусной кислоты: Celanese и BP Химикаты. Другие крупные производители включают Millennium Chemicals, Стерлинг Кемикалс, Samsung, Eastman, и Свенск Этанолкеми.[33]
Карбонилирование метанола
Большая часть уксусной кислоты производится из метанола. карбонилирование. В этом процессе метанол и монооксид углерода реагируют с образованием уксусной кислоты по уравнению:
Процесс включает йодметан в качестве промежуточного звена и происходит в три этапа. А катализатор, карбонил металла, необходим для карбонилирования (шаг 2).[34]
- CH3OH + HI → CH3I + H2О
- CH3I + CO → CH3COI
- CH3COI + H2O → CH3COOH + HI
Два связанных процесса карбонилирования метанола: катализируемый родием Монсанто процесс, а катализируемый иридием Cativa процесс. Последний процесс зеленее и более эффективно[35] и в значительной степени вытеснил прежний процесс, часто на тех же производственных предприятиях. В обоих процессах используется каталитическое количество воды, но для процесса Cativa требуется меньше, поэтому реакция конверсии водяного газа подавляется, и образуется меньше побочных продуктов.
Изменяя условия процесса, уксусный ангидрид также могут производиться на том же заводе с использованием родиевых катализаторов.[36]
Окисление ацетальдегида
До коммерциализации процесса Monsanto большая часть уксусной кислоты производилась путем окисления ацетальдегид. Это остается вторым по важности методом производства, хотя обычно он не конкурирует с карбонилированием метанола. Ацетальдегид может производиться гидратация ацетилена. Это была доминирующая технология в начале 1900-х годов.[37]
Свет нафта компоненты легко окисляются кислородом или даже воздухом с образованием перекиси, которые разлагаются с образованием уксусной кислоты в соответствии с химическое уравнение, проиллюстрировано бутаном:
- 2 С4ЧАС10 + 5 O2 → 4 канала3CO2H + 2 H2О
Такое окисление требует металлического катализатора, такого как нафтенат. соли из марганец, кобальт, и хром.
Типичная реакция проводится при температуры и давления, рассчитанные на то, чтобы быть максимально горячим, но при этом бутан оставался жидким. Типичные условия реакции: 150 ° C (302 ° F) и 55 атм.[38] Также могут образовываться побочные продукты, в том числе бутанон, этилацетат, Муравьиная кислота, и пропионовая кислота. Эти побочные продукты также имеют коммерческую ценность, и условия реакции могут быть изменены для получения большего количества их, если необходимо. Однако отделение уксусной кислоты от этих побочных продуктов увеличивает стоимость процесса.[39]
В аналогичных условиях и при использовании аналогичных катализаторы как используются для окисления бутана, кислород в воздуха производить уксусную кислоту может окислять ацетальдегид.[39]
- 2 канала3CHO + O2 → 2 канала3CO2ЧАС
При использовании современных катализаторов эта реакция может иметь выход уксусной кислоты более 95%. Основные побочные продукты: этилацетат, Муравьиная кислота, и формальдегид, все из которых имеют более низкий точки кипения чем уксусная кислота и легко разделяются дистилляция.[39]
Окисление этилена
Ацетальдегид можно получить из этилен через Wacker процесс, а затем окислили, как указано выше.
В последнее время химическая компания Сева Денко, открывшая завод по окислению этилена в г. Ōita, Япония в 1997 г. ввела в производство более дешевую одностадийную конверсию этилена в уксусную кислоту.[40] Процесс катализируется палладий металлический катализатор, нанесенный на гетерополикислота Такие как кремневольфрамовая кислота. В аналогичном процессе используется тот же металлический катализатор на кремневольфрамовой кислоте и диоксиде кремния:[41]
- C2ЧАС4 + O2 → CH3CO2ЧАС
Считается, что он конкурентоспособен с карбонилированием метанола для небольших заводов (100–250 кт / год), в зависимости от местной цены на этилен. Подход будет основан на использовании новой технологии селективного фотокаталитического окисления для селективного окисления этилена и этана. до уксусной кислоты. В отличие от традиционных катализаторов окисления, процесс селективного окисления будет использовать ультрафиолетовый свет для производства уксусной кислоты при температуре и давлении окружающей среды.
Окислительное брожение
На протяжении большей части истории человечества уксуснокислые бактерии этого рода Ацетобактер сделали уксусную кислоту в виде уксуса. При достаточном количестве кислорода эти бактерии могут производить уксус из различных пищевых продуктов, содержащих алкоголь. Обычно используемые фиды включают яблочный сидр, вино, и ферментированный зерно, солод, рис, или же картофель пюре. Общая химическая реакция, которой способствуют эти бактерии:
- C2ЧАС5ОН + О2 → CH3COOH + H2О
Разбавленный спиртовой раствор, содержащий Ацетобактер и хранится в теплом, просторном месте, через несколько месяцев превратится в уксус. Промышленные методы производства уксуса ускоряют этот процесс, улучшая поставку кислород к бактериям.[42]
Первые партии уксуса, произведенные путем ферментации, вероятно, следовали ошибкам в виноделие процесс. Если должен ферментируется при слишком высокой температуре, acetobacter подавляет дрожжи встречающиеся в природе на виноград. Поскольку спрос на уксус для кулинарных, медицинских и санитарных целей увеличился, виноделы быстро научились использовать другие органические материалы для производства уксуса в жаркие летние месяцы, прежде чем виноград созрел и был готов для переработки в вино. Однако этот метод был медленным и не всегда успешным, поскольку виноделы не понимали этот процесс.[43]
Одним из первых современных коммерческих процессов был «быстрый метод» или «немецкий метод», впервые примененный в Германии в 1823 году. В этом процессе ферментация происходит в башне, заполненной древесной стружкой или уголь. Спиртосодержащий корм поступает в верхнюю часть башни, и свежий воздуха подается снизу естественным или принудительным конвекция. Улучшенная подача воздуха в этом процессе сократила время на приготовление уксуса с месяцев до недель.[44]
В настоящее время большая часть уксуса производится в погружных резервуарах. культура, впервые описанный в 1949 году Отто Громаткой и Генрихом Эбнером.[45] В этом методе спирт ферментируется до уксуса в резервуаре с непрерывным перемешиванием, а кислород подается путем барботирования воздуха через раствор. Используя современные способы применения этого метода, уксус с 15% -ной уксусной кислотой может быть приготовлен всего за 24 часа при периодическом процессе, даже 20% при 60-часовом периодическом процессе с подпиткой.[43]
Анаэробное брожение
Виды анаэробные бактерии, включая представителей рода Clostridium или Ацетобактерии может преобразовывать сахара в уксусную кислоту напрямую, без образования этанола в качестве промежуточного продукта. Общая химическая реакция, проводимая этими бактериями, может быть представлена как:
- C6ЧАС12О6 → 3 канала3COOH
Эти ацетогенный бактерии производят уксусную кислоту из одноуглеродных соединений, включая метанол, монооксид углерода, или смесь углекислый газ и водород:
- 2 CO2 + 4 часа2 → CH3COOH + 2 H2О
Эта способность Clostridium непосредственно метаболизировать сахар или производить уксусную кислоту из менее дорогостоящих ресурсов, предполагает, что эти бактерии могут производить уксусную кислоту более эффективно, чем окислители этанола, такие как Ацетобактер. Однако, Clostridium бактерии менее устойчивы к кислоте, чем Ацетобактер. Даже самый кислотоустойчивый Clostridium штаммы могут производить уксус в концентрации всего несколько процентов по сравнению с Ацетобактер штаммы, которые могут производить уксус в концентрации до 20%. В настоящее время по-прежнему более рентабельно производить уксус с использованием Ацетобактер, а не использовать Clostridium и концентрируя его. В результате, хотя ацетогенные бактерии известны с 1940 года, их промышленное использование ограничивается несколькими нишами.[46]
Использует
Уксусная кислота - химическое вещество реагент для производства химических соединений. Самый большой разовый вид использования уксусной кислоты - производство винилацетата. мономер с последующим образованием уксусного ангидрида и сложного эфира. Объем уксусной кислоты, используемой в уксусе, сравнительно невелик.[9][31]
Винилацетатный мономер
Основное использование уксусной кислоты - производство винилацетат мономер (ВАМ). По оценкам, в 2008 году это приложение потребляло треть мирового производства уксусной кислоты.[9] Реакция состоит из этилен и уксусная кислота с кислород через палладий катализатор, проведенный в газовой фазе.[47]
- 2 ч3С − COOH + 2 С2ЧАС4 + O2 → 2 H3С-СО-О-СН = СН2 + 2 часа2О
Винилацетат можно полимеризовать до поливинилацетат или другой полимеры, которые являются компонентами в краски и клеи.[47]
Производство эфиров
Главная сложные эфиры уксусной кислоты обычно используются в качестве растворителей для чернила, краски и покрытия. Сложные эфиры включают этилацетат, п-бутил ацетат, изобутилацетат, и пропилацетат. Обычно они производятся катализированный реакция от уксусной кислоты и соответствующей алкоголь:
- ЧАС3С − COOH + HO − R → H3С − CO − O − R + H2O, (R = общий алкильная группа )
Однако большинство эфиров ацетата получают из ацетальдегид с использованием Тищенко реакция. Кроме того, ацетаты эфира используются в качестве растворителей для нитроцеллюлоза, акриловые лаки, лак средства для удаления пятен и морилки. Во-первых, моноэфиры гликоля получают из окись этилена или оксид пропилена со спиртом, которые затем этерифицируются уксусной кислотой. Тремя основными продуктами являются ацетат моноэтилового эфира этиленгликоля (EEA), ацетат монобутилового эфира этиленгликоля (EBA) и ацетат монометилового эфира пропиленгликоля (PMA, более известный как PGMEA в процессах производства полупроводников, где он используется в качестве резистивного растворителя. ). Это приложение потребляет от 15% до 20% мировой уксусной кислоты. Было показано, что ацетаты эфира, например EEA, вредны для репродуктивной системы человека.[31]
Уксусный ангидрид
Продукт конденсация двух молекул уксусной кислоты составляет уксусный ангидрид. Мировое производство уксусного ангидрида является одним из основных приложений, и на него уходит от 25% до 30% мирового производства уксусной кислоты. Основной процесс включает обезвоживание уксусной кислоты с получением кетен при 700–750 ° С. После этого кетен реагирует с уксусной кислотой с получением ангидрида:[48]
- CH3CO2H → CH2= C = O + H2О
- CH3CO2H + CH2= C = O → (CH3CO)2О
Уксусный ангидрид - это ацетилирование агент. Таким образом, его основное приложение предназначено для ацетат целлюлозы синтетический текстиль также используется для фотопленка. Уксусный ангидрид также является реагентом для производства героин и другие соединения.[48]
Использовать как растворитель
Ледяная уксусная кислота - отличный полярный протонный растворитель, как указано над. Часто используется в качестве растворителя для перекристаллизация для очистки органических соединений. Уксусная кислота используется как растворитель в производстве терефталевая кислота (TPA), сырье для полиэтилентерефталат (ПЭТ). В 2006 году для производства ТФК было использовано около 20% уксусной кислоты.[31]
Уксусная кислота часто используется в качестве растворителя для реакций с участием карбокатионы, такие как Алкилирование Фриделя-Крафтса. Например, одна стадия промышленного производства синтетических камфора включает в себя Перегруппировка Вагнера-Меервейна из камфена к изоборнилацетат; здесь уксусная кислота действует как растворитель и как нуклеофил поймать переставил карбокатион.[49]
Ледяная уксусная кислота используется в аналитической химии для определения слабощелочных веществ, таких как органические амиды. Ледяная уксусная кислота намного слабее основание чем вода, поэтому амид играет в этой среде сильное основание. Затем его можно титровать, используя раствор в ледяной уксусной кислоте очень сильной кислоты, такой как хлорная кислота.[50]
Медицинское использование
Инъекция уксусной кислоты в опухоль использовалась для лечения рака с 1800-х годов.[51][52]
Уксусная кислота используется в составе скрининг на рак шейки матки во многих областях в Развивающийся мир.[53] Кислота наносится на шейка матки и если примерно через минуту появляется белая область, тест положительный.[53]
Уксусная кислота является эффективным антисептиком при использовании в виде 1% раствора с широким спектром действия против стрептококков, стафилококков, псевдомонад, энтерококков и других.[54][55][56] Его можно использовать для лечения кожных инфекций, вызванных штаммами псевдомонад, устойчивыми к обычным антибиотикам.[57]
Хотя разбавленная уксусная кислота используется в ионтофорез, нет доказательств высокого качества, подтверждающих это лечение болезни вращательной манжеты плеча.[58][59]
Как лечение наружный отит, это на Список основных лекарственных средств Всемирной организации здравоохранения, самые безопасные и эффективные лекарства, необходимые в система здоровья.[60]
Еда
Уксусная кислота имеет 349 ккал на 100 г.[61] Уксус обычно содержит не менее 4% уксусной кислоты по массе.[62][63][64] Правовые ограничения на содержание уксусной кислоты различаются в зависимости от юрисдикции. Уксус используется непосредственно как приправа, а в травление овощей и других продуктов. Столовый уксус имеет тенденцию быть более разбавленным (от 4% до 8% уксусной кислоты), в то время как для промышленного травления пищевых продуктов используются более концентрированные растворы. Доля уксусной кислоты, используемой во всем мире в качестве уксуса, не так велика, как в коммерческих целях, но на сегодняшний день это старейшее и наиболее известное применение.[65]
Реакции
Органическая химия
Уксусная кислота подвергается типичному химические реакции карбоновой кислоты. После обработки стандартной основой превращается в металл. ацетат и воды. С сильными основаниями (например, литийорганическими реагентами) его можно дважды депротонировать с образованием LiCH2CO2Ли. Восстановление уксусной кислоты дает этанол. Группа ОН является основным участком реакции, о чем свидетельствует превращение уксусной кислоты в ацетилхлорид. Другие производные замещения включают уксусный ангидрид; это ангидрид производится потеря воды из двух молекул уксусной кислоты. Сложные эфиры уксусной кислоты также может образовываться Этерификация Фишера, и амиды может быть сформирован. При нагревании выше 440 ° C (824 ° F) уксусная кислота разлагается с образованием углекислый газ и метан, или произвести кетен и вода:[66][67][68]
- CH3COOH → CH4 + CO2
- CH3COOH → CH2CO + H2О
Реакции с неорганическими соединениями
Уксусная кислота мягко разъедающий к металлы в том числе утюг, магний, и цинк, формируя водород газ и соли, называемые ацетаты:
- Mg + 2 CH3COOH → (CH3COO)2Mg + H2
Потому что алюминий образует пассивирующий кислотостойкая пленка из оксид алюминия, алюминиевые цистерны используются для перевозки уксусной кислоты. Ацетаты металлов также можно получить из уксусной кислоты и подходящего основание, как в популярном "пищевая сода + уксус »реакция:
- NaHCO3 + CH3COOH → CH3COONa + CO2 + H2О
А цветовая реакция для солей уксусной кислоты хлорид железа (III) раствор, который приобретает темно-красный цвет, который исчезает после подкисления.[69] Более чувствительный тест использует нитрат лантана с йодом и аммиаком, чтобы получить синий раствор.[70] Ацетаты при нагревании с триоксид мышьяка форма какодил оксид, что можно обнаружить по его зловонный пары.[71]
Прочие производные
Органические или неорганические соли получают из уксусной кислоты. Некоторые коммерчески значимые производные:
- Ацетат натрия, используемый в текстиль промышленность и как еда консервант (E262 ).
- Ацетат меди (II), используется как пигмент и фунгицид.
- Ацетат алюминия и ацетат железа (II) -используется как протравы за красители.
- Ацетат палладия (II), используемый в качестве катализатора реакций органического сочетания, таких как Чертовски реакция.
Галогенированные уксусные кислоты получают из уксусной кислоты. Некоторые коммерчески значимые производные:
- Хлоруксусная кислота (монохлоруксусная кислота, MCA), дихлоруксусная кислота (считается побочным продуктом) и трихлоруксусная кислота. MCA используется в производстве краситель индиго.
- Бромуксусная кислота, который этерифицируется с образованием реагента этилбромацетат.
- Трифторуксусная кислота, который является обычным реагентом в органический синтез.
Количество уксусной кислоты, используемой в этих других областях, вместе составляет еще 5–10% от общего использования уксусной кислоты во всем мире.[31]
История
Уксус был известен в начале цивилизации как естественный результат воздействия пиво и вино в воздух, потому что бактерии, продуцирующие уксусную кислоту, присутствуют во всем мире. Использование уксусной кислоты в алхимия простирается до 3 века до нашей эры, когда Греческий философ Теофраст описал, как уксус воздействует на металлы, производя пигменты полезно в искусстве, в том числе белый свинец (карбонат свинца ) и Verdigris, зеленая смесь медь соли, включая ацетат меди (II). Древний Римляне вареное кислое вино для производства сладкого сиропа, называемого сапа. Сапа который производился в свинцовых горшках, был богат ацетат свинца, сладкое вещество, также называемое сахар свинца или сахар Сатурн, что способствовало отравление свинцом среди римской аристократии.[72]
В 16 веке Немецкий алхимик Андреас Либавиус описал производство ацетон от сухая перегонка ацетата свинца, кетоновое декарбоксилирование. Присутствие воды в уксусе настолько сильно влияет на свойства уксусной кислоты, что на протяжении веков химики считали, что ледяная уксусная кислота и кислота, содержащаяся в уксусе, - это два разных вещества. Французский химик Пьер Адэ оказалось, что они идентичны.[72][73]

В 1845 г. немецкий химик Герман Кольбе синтезированный уксусная кислота из неорганические соединения в первый раз. Эта последовательность реакций состояла из хлорирование из сероуглерод к четыреххлористый углерод, с последующим пиролиз к тетрахлорэтилен и водное хлорирование до трихлоруксусная кислота и заключил электролитический снижение до уксусной кислоты.[74]
К 1910 году большую часть ледяной уксусной кислоты получали из пирогенный ликер, продукт перегонки древесины. Уксусную кислоту выделяли обработкой известковое молоко, и в результате ацетат кальция затем был подкислен серная кислота для восстановления уксусной кислоты. В то время Германия производила 10 000 тонны ледяной уксусной кислоты, около 30% которой было использовано для производства краситель индиго.[72][75]
Потому что оба метанол и монооксид углерода являются товарным сырьем, карбонилирование метанола долгое время являлось привлекательным прекурсором уксусной кислоты. Анри Дрейфус в Британский Celanese разработал пилотную установку карбонилирования метанола еще в 1925 году.[76] Однако отсутствие практических материалов, которые могли бы содержать коррозионную реакционную смесь при высоких давление необходимо (200 банкомат или более) не поощряли коммерциализацию этих маршрутов. Первый коммерческий процесс карбонилирования метанола, в котором использовался кобальт катализатор, разработан немецкой химической компанией BASF в 1963 г. В 1968 г. родий катализатор на основе (СНГ- [Rh (CO)2я2]−) было обнаружено, что он может эффективно работать при более низком давлении практически без побочных продуктов. Химическая компания США Компания Monsanto построил первый завод с использованием этого катализатора в 1970 году, и катализируемое родием карбонилирование метанола стало доминирующим методом производства уксусной кислоты (см. Монсанто процесс ). В конце 1990-х годов химическая компания BP Химикаты коммерциализировали Cativa катализатор ([Ir (CO)2я2]−), который продвигает иридий[77] для большей эффективности. Этот иридий катализированный Cativa процесс является зеленее и более эффективно[35] и в значительной степени вытеснил процесс Monsanto, часто на тех же производственных предприятиях.
Межзвездная среда
Межзвездный уксусная кислота была открыта в 1996 году группой под руководством Дэвида Мерингера.[78] используя первый Ассоциация Беркли-Иллинойс-Мэриленд массив в Радиообсерватория Hat Creek и бывший Миллиметровая матрица расположен в Радиообсерватория Оуэнс-Вэлли. Впервые он был обнаружен в Стрелец В2 Северное молекулярное облако (также известное как Sgr B2 Большая молекула Heimat источник). Уксусная кислота является первой молекулой, обнаруженной в межзвездной среде, использующей исключительно радиоинтерферометры; Во всех предыдущих молекулярных открытиях ISM, сделанных в миллиметровом и сантиметровом режимах длин волн, радиотелескопы с одной тарелкой были по крайней мере частично ответственны за обнаружение.[78]
Воздействие на здоровье и безопасность
Концентрированная уксусная кислота - это разъедающий к коже.[79][80] Эти ожоги или волдыри могут появиться только через несколько часов после воздействия.
Длительное вдыхание (восемь часов) паров уксусной кислоты в концентрации 10 ppm может вызвать раздражение глаз, носа и горла; при 100 ppm может возникнуть заметное раздражение легких и возможное повреждение легких, глаз и кожи. Концентрация паров 1000 ppm вызывает заметное раздражение глаз, носа и верхних дыхательных путей и недопустима. Эти прогнозы были основаны на экспериментах на животных и промышленном воздействии.
У 12 рабочих, подвергавшихся в течение двух или более лет воздействию уксусной кислоты в воздухе со средней концентрацией 51 ppm (оценочная), возникли симптомы раздражения конъюнктивы, раздражения верхних дыхательных путей и гиперкератотического дерматита. Воздействие 50 ppm или более недопустимо для большинства людей и приводит к интенсивному слезотечению и раздражению глаз, носа и горла, с отеком глотки и хроническим бронхитом. Неакклиматизированные люди испытывают сильное раздражение глаз и носа при концентрациях, превышающих 25 ppm, и сообщалось о конъюнктивите при концентрациях ниже 10 ppm. В исследовании пяти рабочих, подвергавшихся в течение семи-12 лет пиковым концентрациям от 80 до 200 ppm, основными результатами были почернение и гиперкератоз кожи рук, конъюнктивит (но без повреждения роговицы), бронхит и фарингит и эрозия. открытых зубов (резцов и клыков).[81]
Опасности растворов уксусной кислоты зависят от концентрации. В следующей таблице перечислены Классификация ЕС растворов уксусной кислоты:[82]
| Концентрация по весу | Молярность | Классификация | R-фразы |
|---|---|---|---|
| 10–25% | 1,67–4,16 моль / л | Раздражающий (Си) | R36 / 38 |
| 25–90% | 4,16–14,99 моль / л | Едкий (C) | R34 |
| >90% | > 14,99 моль / л | Едкий (C) Легковоспламеняющиеся (F) | R10, R35 |
Концентрированная уксусная кислота может с трудом воспламениться при стандартной температуре и давлении, но при температурах выше 39 ° C (102 ° F) она представляет опасность воспламенения и может образовывать взрывоопасные смеси с воздухом при более высоких температурах (пределы взрываемости: 5.4–16%).
Смотрите также
Рекомендации
- ^ Обзоры научной литературы об общепризнанных безопасных пищевых ингредиентах (GRAS). Национальная служба технической информации. 1974. стр. 1.
- ^ «Химия», том 5, Британская энциклопедия, 1961, стр. 374
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 745. Дои:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ "уксусная кислота_msds".
- ^ Хейнс, Уильям М., изд. (2016). CRC Справочник по химии и физике (97-е изд.). CRC Press. С. 5–88. ISBN 9781498754293.
- ^ Bordwell, F.G .; Алгрим, Дональд (1976). «Азотные кислоты. 1. Карбоксамиды и сульфаниламиды». Журнал органической химии. 41 (14): 2507–2508. Дои:10.1021 / jo00876a042.
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0002". Национальный институт охраны труда и здоровья (NIOSH).
- ^ "Уксусная кислота". Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б c d е Чунг, Осия; Танке, Робин С .; Торренс, Дж. Пол. "Уксусная кислота". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a01_045.pub2.
- ^ Предварительные рекомендации IUPAC 2004 г. Глава P-12.1; стр. 4
- ^ Armarego, W.L.F .; Чай, Кристина (2009). Очистка лабораторных химикатов, 6-е издание. Баттерворт-Хайнеманн. ISBN 978-1-85617-567-8.
- ^ Купер, Кэролайн (9 августа 2010 г.). Настольный справочник химика-органика (2-е изд.). CRC Press. С. 102–104. ISBN 978-1-4398-1166-5.
- ^ ДеСуза, Луис Р. (1995). Общие медицинские сокращения. Cengage Learning. п.97. ISBN 978-0-8273-6643-5.
- ^ Хендриксон, Джеймс Б.; Cram, Дональд Дж .; Хаммонд, Джордж С. (1970). Органическая химия (3-е изд.). Токио: Макгроу Хилл Когакуша. п. 135.
- ^ Goldberg, R .; Кишор, Н .; Леннен, Р. (2002). «Термодинамические величины для реакций ионизации буферов» (PDF). Журнал физических и химических справочных данных. 31 (2): 231–370. Bibcode:2002JPCRD..31..231G. Дои:10.1063/1.1416902. Архивировано из оригинал (PDF) 6 октября 2008 г.
- ^ [ЧАС3О+] = 10−2.4 = 0.4%
- ^ Jones, R.E .; Темплтон, Д. Х. (1958). «Кристаллическая структура уксусной кислоты» (PDF). Acta Crystallographica. 11 (7): 484–487. Дои:10.1107 / S0365110X58001341. HDL:2027 / mdp.39015077597907.
- ^ Бриггс, Джеймс М .; Тоан Б. Нгуен; Уильям Л. Йоргенсен (1991). «Моделирование методом Монте-Карло жидкой уксусной кислоты и метилацетата с потенциальными функциями OPLS». Журнал физической химии. 95 (8): 3315–3322. Дои:10.1021 / j100161a065.
- ^ Тогеас, Джеймс Б. (2005). «Пары уксусной кислоты: 2. Статистическая механическая критика экспериментов по плотности пара». Журнал физической химии А. 109 (24): 5438–5444. Bibcode:2005JPCA..109.5438T. Дои:10.1021 / jp058004j. PMID 16839071.
- ^ Макмерри, Джон (2000). Органическая химия (5-е изд.). Брукс / Коул. п. 818. ISBN 978-0-534-37366-5.
- ^ Zieborak, K .; Ольшевский, К. (1958). Bulletin de l'Académie Polonaise des Sciences-Série des Sciences Chimiques Géologiques et Géographiques. 6 (2): 3315–3322.CS1 maint: журнал без названия (ссылка на сайт)
- ^ Fiume, M. Z .; Группа экспертов по обзору косметических ингредиентов (июнь 2003 г.). «Заключительный отчет по оценке безопасности триацетина». Международный журнал токсикологии. 22 (Дополнение 2): 1–10. Дои:10.1080/747398359. PMID 14555416.
- ^ Букингем, Дж., Изд. (1996). Словарь органических соединений. 1 (6-е изд.). Лондон: Чепмен и Холл. ISBN 978-0-412-54090-5.
- ^ Йонеда, Нориюки; Кусано, Сатору; Ясуи, Макото; Пухадо, Питер; Уилчер, Стив (2001). «Последние достижения в области процессов и катализаторов производства уксусной кислоты». Прикладной катализ A: Общие. 221 (1–2): 253–265. Дои:10.1016 / S0926-860X (01) 00800-6.
- ^ Кинетические исследования окисления пропана на смешанных оксидных катализаторах на основе Mo и V (PDF). 2011.
- ^ Науманн д'Алнонкур, Рауль; Чепеи, Ленард-Иштван; Хэвекер, Майкл; Girgsdies, Франк; Schuster, Manfred E .; Шлёгль, Роберт; Траншке, Аннетт (2014). «Реакционная сеть при окислении пропана на фазово-чистых оксидных катализаторах MoVTeNb M1» (PDF). Журнал катализа. 311: 369–385. Дои:10.1016 / j.jcat.2013.12.008. HDL:11858 / 00-001M-0000-0014-F434-5. Архивировано из оригинал (PDF) 15 февраля 2016 г.. Получено 29 октября 2017.
- ^ Хэвекер, Майкл; Врабец, Сабина; Кронерт, Ютта; Чепеи, Ленард-Иштван; Науманн д'Алнонкур, Рауль; Коленько, Юрий В .; Girgsdies, Франк; Шлёгль, Роберт; Траншке, Аннетт (2014). «Химия поверхности фазово-чистого оксида M1 MoVTeNb при работе с селективным окислением пропана до акриловой кислоты» (PDF). Журнал катализа. 285: 48–60. Дои:10.1016 / j.jcat.2011.09.012. HDL:11858 / 00-001M-0000-0012-1BEB-F. Архивировано из оригинал (PDF) 30 октября 2016 г.. Получено 29 октября 2017.
- ^ Коста, Ванесса Морейра; Бассо, Тьяго Олита; Анжелони, Луис Энрике Полето; Эттерер, Марилия; Бассо, Луис Карлос (2008). «Производство уксусной кислоты, этанола и оптических изомеров молочной кислоты штаммом Lactobacillus, выделенным из промышленных ферментаций этанола». Ciência e Agrotecnologia. 32 (2): 503–509. Дои:10.1590 / S1413-70542008000200025.
- ^ Уксусная кислота, которая производится намеренно, а не извлекается при переработке (например, при производстве ацетатов целлюлозы, операциях с поливиниловым спиртом и ацилировании многочисленных уксусных ангидридов).
- ^ «Производственный отчет». Новости химии и машиностроения: 67–76. 11 июля 2005 г.
- ^ а б c d е Мальведа, Майкл; Фунада, Чиё (2003). "Уксусная кислота". Справочник по экономике химических веществ. SRI International. п. 602,5000. Архивировано из оригинал 14 октября 2011 г.
- ^ Уксусная кислота. НИИ Консалтинг.
- ^ «Reportlinker добавляет глобальный анализ и прогнозы рынка уксусной кислоты». База данных маркетинговых исследований. Июнь 2014. с. содержание.
- ^ Yoneda, N .; Kusano, S .; Ясуи, М .; Pujado, P .; Уилчер, С. (2001). «Последние достижения в области процессов и катализаторов производства уксусной кислоты». Прикладной катализ A: Общие. 221 (1–2): 253–265. Дои:10.1016 / S0926-860X (01) 00800-6.
- ^ а б Ланкастер, Майк (2002). Зеленая химия, вводный текст. Кембридж: Королевское химическое общество. стр.262–266. ISBN 978-0-85404-620-1.
- ^ Zoeller, J. R .; Agreda, V. H .; Cook, S. L .; Lafferty, N.L .; Polichnowski, S.W .; Понд, Д. М. (1992). "Процесс уксусного ангидрида компании Eastman Chemical". Катализ сегодня. 13 (1): 73–91. Дои:10.1016 / 0920-5861 (92) 80188-С.
- ^ Хинтерманн, Лукас; Лабонн, Орели (2007). «Каталитическая гидратация алкинов и ее применение в синтезе». Синтез. 2007 (8): 1121. Дои:10.1055 / с-2007-966002.
- ^ Шенье, Филип Дж. (2002). Обзор промышленной химии (3-е изд.). Springer. п. 151. ISBN 978-0-306-47246-6.
- ^ а б c Сано, Кен-ичи; Учида, Хироши; Вакабаяси, Сёитиро (1999). «Новый процесс производства уксусной кислоты прямым окислением этилена». Исследования катализа из Японии. 3 (1): 55–60. Дои:10.1023 / А: 1019003230537. ISSN 1384-6574. S2CID 93855717.
- ^ Сано, Кен-ичи; Учида, Хироши; Вакабаяси, Сёитиро (1999). «Новый процесс производства уксусной кислоты прямым окислением этилена». Обзоры катализаторов из Японии. 3: 66–60. Дои:10.1023 / А: 1019003230537. S2CID 93855717.
- ^ Мисоно, Макото (2009). «Недавний прогресс в практическом применении гетерополикислот и перовскитных катализаторов: Каталитическая технология для устойчивого общества». Катализ сегодня. 144 (3–4): 285–291. Дои:10.1016 / j.cattod.2008.10.054.
- ^ Chotani, Gopal K .; Gaertner, Alfred L .; Арбидже, Майкл В .; Додж, Тимоти С. (2007). «Промышленная биотехнология: от открытия до доставки». Справочник Кента и Ригеля по промышленной химии и биотехнологии. Справочник Кента и Ригеля по промышленной химии и биотехнологии. Springer. С. 32–34. Bibcode:2007карх.книга ....... ISBN 978-0-387-27842-1.
- ^ а б Хроматка, Отто; Эбнер, Генрих (1959). «Уксус погруженного окислительного брожения». Промышленная и инженерная химия. 51 (10): 1279–1280. Дои:10.1021 / ie50598a033.
- ^ Партридж, Эверетт П. (1931). «Уксусная кислота и ацетат целлюлозы в Соединенных Штатах. Общий обзор экономического и технического развития». Промышленная и инженерная химия. 23 (5): 482–498. Дои:10.1021 / ie50257a005.
- ^ Хроматка, О .; Эбнер, Х. (1949). «Исследования по ферментации уксуса: Генератор для процедур ферментации и аэрации уксуса». Энзимология. 13: 369.
- ^ Сим, Цзя Хуэй; Камаруддин, Азлина Харун; Лонг, Вэй Синг; Наджафпур, Гасем (2007). «Clostridium aceticum - потенциальный организм, катализирующий превращение окиси углерода в уксусную кислоту: применение методологии поверхности отклика». Ферментные и микробные технологии. 40 (5): 1234–1243. Дои:10.1016 / j.enzmictec.2006.09.017.
- ^ а б Рошер, Гюнтер. «Виниловые эфиры». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a27_419.
- ^ а б Хелд, Хеймо; Rengstl, Альфред; Майер, Дитер. «Ангидрид уксусной кислоты и смешанные ангидриды жирных кислот». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a01_065.
- ^ Продай, Чарльз С. (2006). «4.2.15 Бициклические монотерпеноиды». Химия ароматов: от парфюма к потребителю. Серия РСК в мягкой обложке. 38 (2-е изд.). Великобритания: Королевское химическое общество. п. 80. ISBN 978-0-85404-824-3.
- ^ Фельгнер, Андреа. «Определение содержания воды в хлорной кислоте 0,1 моль / л в уксусной кислоте с помощью титрования по Карлу Фишеру». Сигма-Олдрич. Получено 27 июля 2017.
- ^ Барклай, Джон (1866). «Инъекция уксусной кислоты при раке». Br Med J. 2 (305): 512. Дои:10.1136 / bmj.2.305.512-а. ЧВК 2310334.
- ^ Шибата Н. (1998). «Чрескожная инъекция этанола и уксусной кислоты при метастазах рака толстой кишки в печень». Ган Кагаку Риохо. 25 (5): 751–5. PMID 9571976.
- ^ а б Fokom-Domgue, J .; Combescure, C .; Фоком-Дефо, В .; Тебеу, П. М .; Vassilakos, P .; Kengne, A. P .; Петинья, П. (3 июля 2015 г.). «Эффективность альтернативных стратегий первичного скрининга рака шейки матки в странах Африки к югу от Сахары: систематический обзор и метаанализ исследований точности диагностических тестов». BMJ (под ред. Клинических исследований). 351: h3084. Дои:10.1136 / bmj.h3084. ЧВК 4490835. PMID 26142020.
- ^ Мадхусудхан, В. Л. (8 апреля 2015 г.). «Эффективность 1% уксусной кислоты при лечении хронических ран, инфицированных синегнойной палочкой: проспективное рандомизированное контролируемое клиническое исследование». Международный журнал ран. 13 (6): 1129–1136. Дои:10.1111 / iwj.12428. ISSN 1742-481X. PMID 25851059. S2CID 4767974.
- ^ Ryssel, H .; Kloeters, O .; Germann, G .; Schäfer, Th; Wiedemann, G .; Oehlbauer, M. (1 августа 2009 г.). «Антимикробный эффект уксусной кислоты - альтернатива обычным местным антисептикам?». Ожоги: журнал Международного общества ожоговых травм. 35 (5): 695–700. Дои:10.1016 / j.burns.2008.11.009. ISSN 1879-1409. PMID 19286325.
- ^ «Антисептики на ранах: область споров». www.medscape.com. Получено 15 августа 2016.
- ^ Nagoba, B.S .; Selkar, S.P .; Wadher, B.J .; Ганди, Р. К. (декабрь 2013 г.). «Лечение уксусной кислотой псевдомонадных раневых инфекций - обзор». Журнал инфекций и общественного здравоохранения. 6 (6): 410–5. Дои:10.1016 / j.jiph.2013.05.005. PMID 23999348.
- ^ Пейдж, М. Дж .; Green, S .; Mrocki, M. A .; Surace, S.J .; Deitch, J .; McBain, B .; Lyttle, N .; Бухбиндер, Р. (10 июня 2016 г.). «Методы электротерапии при болезни вращательной манжеты плеча». Кокрановская база данных систематических обзоров (6): CD012225. Дои:10.1002 / 14651858.CD012225. PMID 27283591.
- ^ Хабиф, Томас П. (2009). Клиническая дерматология (5-е изд.). Elsevier Health Sciences. п. 367. ISBN 978-0-323-08037-8.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Гринфилд, Хизер; Саутгейт, D.A.T. (2003). Данные о составе пищевых продуктов: производство, управление и использование. Рим: ФАО. п. 146. ISBN 9789251049495.
- ^ "CPG Sec. 525.825 Уксус, Определения" (PDF). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Март 1995 г.
- ^ «Ведомственная консолидация Закона о пищевых продуктах и лекарствах и Положений о пищевых продуктах и лекарствах - Часть B - Раздел 19» (PDF). Министерство здравоохранения Канады. Август 2018. с. 591.
- ^ «Регламент Комиссии (ЕС) 2016/263». Официальный журнал Европейского Союза. Европейская комиссия. Февраль 2016 г.
- ^ Bernthsen, A .; Садборо, Дж. Дж. (1922). Органическая химия. Лондон: Блэки и сын. п. 155.
- ^ Blake, P.G .; Джексон, Г. Э. (1968). «Термическое разложение уксусной кислоты». Журнал химического общества B: Physical Organic: 1153–1155. Дои:10.1039 / J29680001153.
- ^ Bamford, C.H .; Дьюар, М. Дж. С. (1949). «608. Термическое разложение уксусной кислоты». Журнал химического общества: 2877. Дои:10.1039 / JR9490002877.
- ^ Дуань, Сяофэн; Пейдж, Майкл (1995). «Теоретическое исследование конкурирующих механизмов термического мономолекулярного разложения уксусной кислоты и реакции гидратации кетена». Журнал Американского химического общества. 117 (18): 5114–5119. Дои:10.1021 / ja00123a013. ISSN 0002-7863.
- ^ Шарло, G .; Мюррей, Р. Г. (1954). Качественный неорганический анализ (4-е изд.). CUP Архив. п. 110.
- ^ Neelakantam, K .; Роу, Л. Рамачангра (1940). «Тест нитрата лантана для качественного анализа ацетатина» (PDF). Получено 5 июн 2013.
- ^ Brantley, L.R .; Cromwell, T. M .; Мид, Дж. Ф. (1947). «Обнаружение ацетат-иона по реакции с оксидом мышьяка с образованием какодилоксида». Журнал химического образования. 24 (7): 353. Bibcode:1947JChEd..24..353B. Дои:10.1021 / ed024p353. ISSN 0021-9584.
- ^ а б c Мартин, Джеффри (1917). Промышленная и производственная химия (Часть 1, Органическая ред.). Лондон: Кросби Локвуд. стр.330 –331.
- ^ Адет, П. А. (1798). "Mémoire sur l'acide acétique (Воспоминание об уксусной кислоте)". Annales de Chimie. 27: 299–319.
- ^ Голдвайт, Гарольд (сентябрь 2003 г.). «Этот месяц в химической истории» (PDF). Бюллетень секции Нью-Хейвена Американское химическое общество. 20 (3): 4. Архивировано из оригинал (PDF) 4 марта 2009 г.
- ^ Швеппе, Гельмут (1979). «Идентификация красителей на старых тканях». Журнал Американского института охраны природы. 19 (1/3): 14–23. Дои:10.2307/3179569. JSTOR 3179569. Архивировано из оригинал 29 мая 2009 г.. Получено 12 октября 2005.
- ^ Вагнер, Франк С. (1978). "Уксусная кислота". В Грейсоне, Мартин (ред.). Энциклопедия химической технологии Кирка-Отмера (3-е изд.). Нью-Йорк: Джон Уайли и сыновья.
- ^ Промышленные органические химикаты, Гарольд А. Витткофф, Брайан Г. Рубен, Джеффри С. Плоткин
- ^ а б Mehringer, David M .; и другие. (1997). «Обнаружение и подтверждение наличия межзвездной уксусной кислоты». Письма в астрофизический журнал. 480 (1): L71. Bibcode:1997ApJ ... 480L..71M. Дои:10.1086/310612.
- ^ «ICSC 0363 - УКСУСНАЯ КИСЛОТА». Международная программа химической безопасности. 5 июня 2010 г.
- ^ «Руководство по безопасности и гигиене труда для уксусной кислоты» (PDF). Центры по контролю и профилактике заболеваний. Получено 8 мая 2013.
- ^ Шерерц, Питер К. (1 июня 1994 г.), Уксусная кислота (PDF), Департамент здравоохранения штата Вирджиния по контролю за опасностями для здоровья, заархивировано оригинал (PDF) 4 марта 2016 г.
- ^ Йи, Аллан (10 мая 2013 г.). «Сводный список HSIS - алфавитный указатель». Безопасная работа в Австралии. Получено 11 июн 2013.
внешняя ссылка
- Международная карта химической безопасности 0363
- Национальный реестр загрязнителей - информационный бюллетень по уксусной кислоте
- Карманный справочник NIOSH по химической опасности
- Метод отбора проб и анализа
- 29 CFR 1910.1000, таблица Z-1 (Допустимые пределы воздействия в США)
- ChemSub Online: Уксусная кислота
- Расчет давление газа, плотность жидкости, динамическая вязкость жидкости, поверхностное натяжение уксусной кислоты
- Уксусная кислота, связанная с белками в PDB
- Шведское химическое агентство. Информационный лист - Уксусная кислота
- Технологическая схема производства уксусной кислоты Карбонилирование метанола