Метилацетат - Methyl acetate
 | |
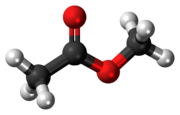 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Метилацетат | |
| Систематическое название ИЮПАК Метил этаноат | |
| Другие имена Метиловый эфир уксусной кислоты | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.001.078 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C3ЧАС6О2 | |
| Молярная масса | 74.079 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Ароматный, фруктовый[2] |
| Плотность | 0,932 г см−3 |
| Температура плавления | -98 ° С (-144 ° F, 175 К) |
| Точка кипения | 56,9 ° С (134,4 ° F, 330,0 К) |
| ~ 25% (20 ° С) | |
| Давление газа | 173 мм рт. Ст. (20 ° С)[2] |
| -42.60·10−6 см3/ моль | |
| 1.361 | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материалов |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | −10 ° С; 14 ° F; 263 К [2] |
| Пределы взрываемости | 3.1%-16%[2] |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 3700 мг / кг (перорально, кролик)[3] |
LCLo (самый низкий опубликованный ) | 11039 частей на миллион (мышь, 4 часа) 21,753 частей на миллион (кошка, 1 час) 32000 частей на миллион (крыса, 4 часа)[3] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 200 частей на миллион (610 мг / м3)[2] |
REL (Рекомендуемые) | TWA 200 частей на миллион (610 мг / м3) ST 250 частей на миллион (760 мг / м3)[2] |
IDLH (Непосредственная опасность) | 3100 частей на миллион[2] |
| Родственные соединения | |
Связанный сложные эфиры | Метилформиат Этилацетат Этилформиат Метил фторацетат |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Метилацетат, также известен как MeOAc, метиловый эфир уксусной кислоты или метилэтаноат, представляет собой карбоксилат сложный эфир с формулой CH3КУХНЯ3. Это легковоспламеняющаяся жидкость с характерным приятным запахом, напоминающим некоторые клеи и жидкости для снятия лака. Метилацетат иногда используется в качестве растворитель, будучи слабополярным и липофильный, но его близкий родственник этилацетат является более распространенным растворителем, менее токсичным и менее растворимым в воде. Метилацетат имеет растворимость 25% в воде комнатной температуры. При повышенной температуре его растворимость в воде намного выше. Метилацетат нестабилен в присутствии сильных водных базы или водный кислоты. Метилацетат не считается ЛОС в США.[4][5]
Подготовка и реакции
Метилацетат промышленно производится на карбонилирование из метанол как побочный продукт производства уксусная кислота.[6] Метилацетат также образуется этерификация уксусной кислоты с метанолом в присутствии сильных кислот, таких как серная кислота; этот производственный процесс известен благодаря Eastman Kodak усиленный процесс с использованием реактивная перегонка.
Реакции
При наличии сильных оснований, таких как гидроксид натрия или сильные кислоты, такие как соляная кислота или серной кислоты это гидролизованный обратно в метанол и уксусную кислоту, особенно при повышенной температуре. Превращение метилацетата обратно в его компоненты под действием кислоты является реакцией первого порядка по отношению к сложный эфир. Реакция метилацетата и основания, например гидроксид натрия, является реакцией второго порядка по обоим реагентам.
Метилацетат - это основание Льюиса, которое образует аддукты 1: 1 с различными кислотами Льюиса. Классифицируется как твердая база и является базой в Модель ECW с EB = 1,63 и CB = 0.95.
Приложения
В основном метилацетат используется как летучий малотоксичный растворитель в клеях, красках и жидкостях для снятия лака.
Уксусный ангидрид производится карбонилирование метилацетата в процессе, вдохновленном Синтез уксусной кислоты Monsanto.[7]
Смотрите также
использованная литература
- ^ Индекс Merck, 12-е издание, 6089.
- ^ а б c d е ж г Карманный справочник NIOSH по химической опасности. "#0391". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Метилацетат». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Зено, У. Уикс, младший, Фрэнк Н. Джонс, С. Питер Паппас и Дуглас А. Уикс (2007). Органические покрытия. Хобокен, Нью-Джерси: Wiley. ISBN 978-0-471-69806-7.CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ «Обновление: летучие органические соединения, освобожденные Агентством по охране окружающей среды США». Американская ассоциация покрытий. 2018-01-30. Получено 2019-03-20.
- ^ Осия Чунг, Робин С. Танке, Дж. Пол Торренс «Уксусная кислота» в Энциклопедия промышленной химии Ульмана, 2002, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a01_045
- ^ Zoeller, J. R .; Agreda, V. H .; Cook, S. L .; Lafferty, N.L .; Polichnowski, S.W .; Понд, Д. М. (1992). "Процесс уксусного ангидрида компании Eastman Chemical". Катализ сегодня. 13: 73–91. Дои:10.1016 / 0920-5861 (92) 80188-С.


