Бензонитрил - Википедия - Benzonitrile
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Бензонитрил | |||
| Систематическое название ИЮПАК Бензолкарбонитрил | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 3DMet | |||
| 506893 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.002.596 | ||
| Номер ЕС |
| ||
| 2653 | |||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2224 | ||
| |||
| |||
| Характеристики | |||
| C 6ЧАС 5(CN) | |||
| Молярная масса | 103,12 г / моль | ||
| Плотность | 1,0 г / мл | ||
| Температура плавления | -13 ° С (9 ° F, 260 К) | ||
| Точка кипения | От 188 до 191 ° C (от 370 до 376 ° F, от 461 до 464 K) | ||
| <0,5 г / 100 мл (22 ° C) | |||
| -65.19·10−6 см3/ моль | |||
| 1.5280 | |||
| Опасности | |||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Предупреждение | ||
| H302, H312 | |||
| P264, P270, P280, P301 + 312, P302 + 352, P312, P322, P330, P363, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 75 ° С (167 ° F, 348 К) | ||
| 550 ° С (1022 ° F, 823 К) | |||
| Пределы взрываемости | 1.4–7.2% | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
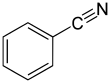
Бензонитрил это химическое соединение с формулой C
6ЧАС
5(CN), сокращенно Ph CN. Этот ароматный органическое соединение представляет собой бесцветную жидкость со сладким запахом горького миндаля. Он в основном используется как предшественник смолы. бензогуанамин.
Производство
Он подготовлен аммоксидирование из толуол, это его реакция на аммиак и кислород (или воздух) при температуре от 400 до 450 ° C (от 752 до 842 ° F).[1]
- C
6ЧАС
5CH
3 + 3/2 О
2 + NH
3 → C
6ЧАС
5(CN) + 3 ч
2О
В лаборатории его можно приготовить путем обезвоживания бензамид или Реакция Розенмунда – фон Брауна с помощью цианид меди или же NaCN /ДМСО и бромбензол.
Приложения
Лаборатория использует
Бензонитрил - полезный растворитель и универсальный предшественник многих производных. Он реагирует с аминами с образованием N-замещенных бензамидов после гидролиза.[2] Это предшественник дифенилкетимина. Ph
2C = NH (т.кип.151 ° C, 8 мм рт. ст.) в результате реакции с фенилмагний бромид с последующим метанолиз.[3]
Бензонитрильные формы координационные комплексы с переходными металлами, которые растворимы в органических растворителях и легко лабильны. Одним из примеров является PdCl
2(PhCN)
2. Бензонитрильные лиганды легко замещаются более сильными лигандами, что делает бензонитрильные комплексы полезными синтетическими промежуточными продуктами.[4]
История
О бензонитриле сообщил Герман Фелинг в 1844 г. Он обнаружил это соединение как продукт термической дегидратации бензоат аммония. Он вывел ее структуру из уже известного аналога реакции формиат аммония с образованием формонитрила. Он также придумал название бензонитрил, которое дало название всей группе нитрилы.[5]
В 2018 году бензонитрил был обнаружен в межзвездная среда.[6]
Рекомендации
- ^ Маки, Такао; Такеда, Кадзуо (июнь 2000 г.). «Бензойная кислота и производные». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a03_555. ISBN 3527306730.
- ^ Cooper, F.C .; Партридж, М. У. (1963). «N-фенилбензамидин». Органический синтез.; Коллективный объем, 4, п. 769
- ^ Pickard, P. L .; Толберт, Т. Л. (1973). «Дифенил кетимин». Органический синтез.; Коллективный объем, 5, п. 520
- ^ Андерсон, Гордон К .; Лин, Минрен (1990). «Бис (бензонитрил) дихлорные комплексы палладия и платины». Реагенты для комплексов переходных металлов и металлоорганических синтезов. Неорганические синтезы. 28. Джон Вили и сыновья. С. 60–63. Дои:10.1002 / 9780470132593.ch13. ISBN 978-0-470-13259-3.
- ^ Фелинг, Герман (1844). "Ueber die Zersetzung des benzoësauren Ammoniaks durch die Wärme" (PDF). Annalen der Chemie und Pharmacie. 49 (1): 91–97. Дои:10.1002 / jlac.18440490106.
- ^ McGuire, Brett A .; и другие. (Январь 2018). «Обнаружение ароматической молекулы бензонитрила (c − C
6ЧАС
5CN) в межзвездной среде ». Наука. 359 (6372): 202–205. arXiv:1801.04228. Bibcode:2018Научный ... 359..202M. Дои:10.1126 / science.aao4890. PMID 29326270.