Антрацен - Anthracene
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Антрацен | |
| Систематическое название ИЮПАК Трицикло [8.4.0.03,8] тетрадека-1,3,5,7,9,11,13-гептаен | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 1905429 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.974 |
| Номер ЕС |
|
| 67837 | |
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C14ЧАС10 | |
| Молярная масса | 178.234 г · моль−1 |
| Внешность | Бесцветный |
| Запах | Слабый ароматный |
| Плотность | 1,28 г / см3 (25 ° С)[1] 0,969 г / см3 (220 ° С) |
| Температура плавления | 216 ° С (421 ° F, 489 К)[1] при 760 мм рт. |
| Точка кипения | 341,3 ° С (646,3 ° F, 614,5 К)[1] при 760 мм рт. |
| 0,022 мг / л (0 ° С) 0,044 мг / л (25 ° С) 0,29 мг / л (50 ° С) 0,00045% по массе (100 ° C, 3,9 МПа)[2] | |
| Растворимость | Растворим в алкоголь, (C2ЧАС5)2О, ацетон, C6ЧАС6, CHCl3,[1] CS2[3] |
| Растворимость в этиловый спирт | 0,76 г / кг (16 ° С) 1,9 г / кг (19,5 ° С) 3,28 г / кг (25 ° С)[3] |
| Растворимость в метанол | 18 г / кг (19,5 ° С)[3] |
| Растворимость в гексан | 3,7 г / кг[3] |
| Растворимость в толуол | 9,2 г / кг (16,5 ° С) 129,4 г / кг (100 ° С)[3] |
| Растворимость в четыреххлористый углерод | 7,32 г / кг[3] |
| бревно п | 4.56 |
| Давление газа | 0,01 кПа (125,9 ° C) 0,1 кПа (151,5 ° C)[4] 13,4 кПа (250 ° C)[5] |
Закон Генри постоянный (kЧАС) | 0,0396 л · атм / моль[6] |
| УФ-видимый (λМаксимум) | 345,6 нм, 363,2 нм[5] |
| −129.8×10−6 см3/ моль[7] | |
| Теплопроводность | 0,1416 Вт / (м · К) (240 ° C) 0,1334 Вт / (м · К) (270 ° C) 0,1259 Вт / (м · К) (300 ° C)[8] |
| Вязкость | 0,602 сП (240 ° C) 0,498 сП (270 ° C) 0,429 сП (300 ° C)[8] |
| Структура | |
| Моноклиника (290 К)[9] | |
| P21/ b[9] | |
| D5 2ч[9] | |
а = 8,562 Å, б = 6,038 Å, c = 11,184 Å[9] α = 90 °, β = 124,7 °, γ = 90 ° | |
| Термохимия[10] | |
Теплоемкость (C) | 210,5 Дж / (моль · К) |
Стандартный моляр энтропия (S | 207,5 Дж / (моль · К) |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | 129,2 кДж / моль |
Станд. Энтальпия горение (ΔcЧАС⦵298) | 7061 кДж / моль[5] |
| Опасности | |
| Пиктограммы GHS |   [11] [11] |
| Сигнальное слово GHS | Предупреждение |
| H315, H319, H335, H410[11] | |
| P261, P273, P305 + 351 + 338, P501[11] | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 121 ° С (250 ° F, 394 К)[11] |
| 540 ° С (1004 ° F, 813 К)[11] | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 4900 мг / кг (крысы, перорально) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Антрацен твердый полициклический ароматический углеводород (ПАУ) формулы C14ЧАС10, состоящий из трех слитных бензол кольца. Это компонент каменноугольная смола. Антрацен используется в производство красного краситель ализарин и другие красители. Антрацен бесцветен, но имеет синий цвет (пик 400–500 нм). флуоресценция под ультрафиолетовый радиация.[13]
Возникновение и производство
Каменноугольная смола, которая содержит около 1,5% антрацена, остается основным источником этого материала. Общие примеси: фенантрен и карбазол. Минеральная форма антрацена называется фрейталит и связана с месторождением угля.[14] Классический лабораторный метод получения антрацена - это циклодегидратация о-метил- или о-метилен-замещенных диарилкетонов в так называемых Реакция Эльбса.
Реакции
Снижение
Восстановление антрацена щелочными металлами дает сильно окрашенные анион-радикальные соли M+[антрацен]− (M = Li, Na, K). Гидрирование дает 9,10-дигидроантрацен, сохраняя ароматичность двух боковых колец.
Циклоприсоединения
Антрацен фотодимеризуется действием УФ свет:
В димер, называемый диантраценом (или иногда парантраценом), связан парой новых углерод-углеродных связей, что является результатом [4 + 4] циклоприсоединение. Он превращается в антрацен термически или с УФ облучение ниже 300 нм. Аналогично ведут себя замещенные производные антрацена. На реакцию влияет наличие кислород.[15][16]
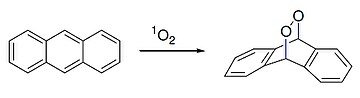
Антрацен также реагирует с диенофилом. синглетный кислород в [4 + 2] -циклоприсоединении (Реакция Дильса – Альдера ):
С электрофилами
Химическая окисление происходит легко, давая антрахинон, С14ЧАС8О2 (ниже), например, используя пероксид водорода и ванадилацетилацетонат.[17]
Электрофильное замещение антрацена происходит в положении 9. Например, формилирование дает 9-антраценкарбоксальдегид. Замещение в других положениях осуществляется косвенно, например, начиная с антрохинона.[18]
Использует
Антрацен превращается в основном в антрахинон, предшественник красителей.[19]
Ниша
Антрацен, широкая запрещенная зона органический полупроводник используется как сцинтиллятор для детекторов высокой энергии фотоны, электроны и альфа-частицы. Пластмассы, такие как поливинилтолуол, может быть допирован антраценом для получения пластикового сцинтиллятора, который примерно эквивалентен воде для использования в радиационная терапия дозиметрия. Антрацена спектр излучения пики в диапазоне от 400 нм до 440 нм.
Он также используется в дерево консерванты, инсектициды, и покрытие материалы.[нужна цитата ]
Антрацен обычно используется в качестве индикатора ультрафиолетового излучения в защитных покрытиях, наносимых на печатные монтажные платы. Индикатор антрацена позволяет контролировать конформное покрытие в УФ-свете.[20] Антрацен также используется при производстве антрахинона.
Производные

Различные производные антрацена находят специализированное применение. Производные, имеющие гидроксильная группа представляют собой 1-гидроксиантрацен и 2-гидроксиантрацен, гомологичные фенол и нафтолы и гидроксиантрацен (также называемый антролом и антраценолом)[21][22] находятся фармакологически активный. Антрацен также может иметь несколько гидроксильных групп, как в 9,10-дигидроксиантрацен.
Вхождение
Антрацен, как и многие другие полициклические ароматические углеводороды, образуется в процессе горения. Воздействие на человека происходит в основном через табачный дым и прием пищи, загрязненной продуктами сгорания.
Токсикология
Многие исследования показывают, что антрацен не является канцерогенным: «неизменно отрицательные результаты многочисленных тестов на генотоксичность in vitro и in vivo». Ранние эксперименты свидетельствовали об обратном, поскольку образцы сырой нефти были загрязнены другими веществами. полициклические ароматические соединения. Кроме того, он легко разлагается в почве. Он особенно подвержен разложению в присутствии света.[19]
Смотрите также
- 9,10-дитиоантрацен, производное с двумя тиоловыми группами, добавленными к центральному кольцу
- Фенантрен
- Тетрацен
Рекомендации
- ^ а б c d Хейнс, стр. 3,28
- ^ Хейнс, стр. 5,157
- ^ а б c d е ж Зейделл, Атертон; Линке, Уильям Ф. (1919). Растворимость неорганических и органических соединений (2-е изд.). Нью-Йорк: Компания Д. Ван Ностранд. стр.81.
- ^ Хейнс, стр. 6,116
- ^ а б c Антрацен в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69, Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (Дата обращения 22.06.2014)
- ^ Хейнс, стр. 5,157
- ^ Хейнс, стр. 3,579
- ^ а б «Свойства антрацена». www.infotherm.com. Wiley Information Services GmbH. Архивировано из оригинал на 2014-11-01. Получено 2014-06-22.
- ^ а б c d Дуглас, Боди Э .; Хо, Ши-Мин (2007). Структура и химический состав кристаллических твердых тел. Нью-Йорк: Springer Science + Business Media, Inc., стр. 289. ISBN 978-0-387-26147-8.
- ^ Хейнс, стр. 5,41
- ^ а б c d е Сигма-Олдрич Ко., Антрацен. Проверено 22 июня 2014.
- ^ «Паспорт безопасности вещества антрацена». www.fishersci.ca. Fisher Scientific. Получено 2014-06-22.
- ^ Линдси, Джонатан; и другие. «Антрацен». PhotochemCAD. Получено 20 февраля 2014.
- ^ Фрейталит, Миндат, https://www.mindat.org/min-54360.html
- ^ Рикборн, Брюс (1998). "Реакция Ретро-Дильса-Альдера. Часть I. C − C диенофилы". Органические реакции. С. 1–393. Дои:10.1002 / 0471264180.or052.01. ISBN 978-0471264187.
- ^ Буа-Лоран, Анри; Десвернь, Жан-Пьер; Кастелян, Ален; Lapouyade, Рене (2000). «Фотодимеризация антраценов в жидком растворе: структурные аспекты». Обзоры химического общества. 29: 43–55. Дои:10.1039 / a801821i.
- ^ Чарлтон, Кимберли Д. М .; Прокопчук, Эрнест М. (2011). «Координационные комплексы как катализаторы: окисление антрацена перекисью водорода в присутствии VO (acac) 2». Журнал химического образования. 88 (8): 1155–1157. Bibcode:2011JChEd..88.1155C. Дои:10.1021 / ed100843a.
- ^ Шкаламера, Жани; Велькович, Елена; Птичек, Люция; Самбол, Матия; Млинарич-Майерски, Ката; Басарич, Никола (2017). «Синтез асимметрично дизамещенных антраценов». Тетраэдр. 73 (40): 5892–5899. Дои:10.1016 / j.tet.2017.08.038.
- ^ а б Коллин, Герд; Höke, Hartmut и Talbiersky, Jörg (2006) «Антрацен» в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a02_343.pub2
- ^ Цайтлер, Алекс (27.06.2012) Конформное покрытие 101: общий обзор, разработка процесса и методы контроля. BTW, Inc.
- ^ 1-гидроксиантрацен. Страница данных NIST
- ^ 2-гидроксиантрацен. Страница данных NIST
Цитированные источники
- Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). CRC Press. ISBN 1439855110.