Ультрафиолетовая видимая спектроскопия - Ultraviolet–visible spectroscopy
эта статья нужны дополнительные цитаты для проверка. (Апрель 2018 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |

Ультрафиолетовая видимая спектроскопия или спектрофотометрия в ультрафиолетовом и видимом диапазоне (УФ – Вид или УФ / Вид) относится к абсорбционная спектроскопия или спектроскопия отражения в части ультрафиолетовый и полный, прилегающий видимый спектральные области. Это означает, что он использует свет в видимом и соседнем диапазонах. Поглощение или отражение в видимом диапазоне напрямую влияет на воспринимаемое цвет химикатов участвует. В этом регионе электромагнитный спектр, атомы и молекулы пройти электронные переходы. Абсорбционная спектроскопия дополняет флуоресцентная спектроскопия, в этом флуоресценция занимается переходами из возбужденное состояние к основное состояние, а поглощение измеряет переходы из основного состояния в возбужденное.[1]
Принцип поглощения ультрафиолета – видимого света
Молекулы, содержащие связывающие и несвязывающие электроны (n-электроны), могут поглощать энергию в форме ультрафиолетового или видимого света, чтобы возбудить эти электроны на более высокие антисвязывающие молекулярные орбитали.[2] Чем легче возбуждаются электроны (т.е. тем меньше энергетический зазор между HOMO и LUMO ), тем большую длину волны света он может поглотить. Существует четыре возможных типа переходов (π – π *, n – π *, σ – σ * и n – σ *), и их можно упорядочить следующим образом: σ – σ *> n – σ *> π– π *> n – π *.[нужна цитата ]
Приложения
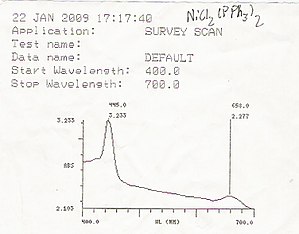
УФ / видимая спектроскопия обычно используется в аналитическая химия для количественный определение различных аналитов, таких как переходный металл ионы, очень сопряженный органические соединения, и биологические макромолекулы. Спектроскопический анализ обычно проводится в растворах, но также могут быть изучены твердые вещества и газы.
- Растворы ионов переходных металлов могут быть окрашены (т.е. поглощать видимый свет), поскольку d электроны внутри атомы металла могут быть возбуждены из одного электронного состояния в другое. На цвет растворов ионов металлов сильно влияет присутствие других частиц, таких как определенные анионы или лиганды. Например, цвет разбавленного раствора сульфат меди очень светло-голубой; добавление аммиак усиливает цвет и изменяет длину волны максимального поглощения (λМаксимум).
- Органические соединения, особенно с высокой степенью спряжение, также поглощают свет в УФ или видимой областях электромагнитный спектр. Растворителями для этих определений часто являются вода для водорастворимых соединений или этиловый спирт для органических растворимых соединений. (Органические растворители могут иметь значительное УФ-поглощение; не все растворители подходят для использования в УФ-спектроскопии. Этанол очень слабо поглощает при большинстве длин волн.) Полярность растворителя и pH могут влиять на спектр поглощения органического соединения. Тирозин, например, увеличивает максимумы поглощения и коэффициент молярной экстинкции, когда pH увеличивается с 6 до 13 или когда полярность растворителя уменьшается.
- В то время как комплексы с переносом заряда также порождают цвета, цвета часто слишком интенсивные, чтобы их можно было использовать для количественных измерений.
В Закон Бера – Ламберта утверждает, что поглощение раствора прямо пропорционально концентрации поглощающих частиц в растворе и длине пути.[3] Таким образом, для фиксированной длины пути УФ / видимая спектроскопия может использоваться для определения концентрации поглотителя в растворе. Необходимо знать, насколько быстро изменяется поглощение при концентрации. Это можно взять из литературы (таблицы молярные коэффициенты экстинкции ), а точнее, определяется из калибровочная кривая.
Спектрофотометр УФ / видимого диапазона может использоваться в качестве детектора для ВЭЖХ. Присутствие аналита дает ответ, который, как предполагается, пропорционален его концентрации. Для получения точных результатов реакцию прибора на неизвестный аналит следует сравнивать с ответом на стандарт; это очень похоже на использование калибровочных кривых. Отклик (например, высота пика) для конкретной концентрации известен как коэффициент отклика.
Длины волн пиков поглощения могут быть соотнесены с типами связей в данной молекуле и важны для определения функциональных групп внутри молекулы. В Правила Вудворда – Физера, например, представляют собой набор эмпирических наблюдений, используемых для предсказания λМаксимум, длина волны наиболее интенсивного поглощения УФ / видимого света для сопряженных органических соединений, таких как диены и кетоны. Однако сам по себе спектр не является специфическим тестом для какого-либо конкретного образца. Природа растворителя, pH раствора, температура, высокие концентрации электролита и присутствие мешающих веществ могут влиять на спектр поглощения. Экспериментальные вариации, такие как ширина щели (эффективная полоса пропускания) спектрофотометра, также изменят спектр. Чтобы применить УФ / видимую спектроскопию к анализу, эти переменные необходимо контролировать или учитывать, чтобы идентифицировать присутствующие вещества.[4]
Метод чаще всего используется количественно для определения концентраций поглощающих веществ в растворе с использованием Закон Бера – Ламберта:
- ,
где А измеряется поглощение (в единицах абсорбции (AU)), - интенсивность падающего света при данном длина волны, - передаваемая интенсивность, L длина пути через образец, и c то концентрация поглощающих видов. Для каждого вида и длины волны ε - постоянная величина, известная как молярная поглощающая способность или коэффициент затухания. Эта постоянная является фундаментальным молекулярным свойством в данном растворителе, при определенной температуре и давлении, и имеет единицы измерения: .
Поглощение и угасание ε иногда определяются в терминах натуральный логарифм вместо десятичного логарифма.
Закон Бера-Ламберта полезен для характеристики многих соединений, но не является универсальным соотношением для концентрации и поглощения всех веществ. Полиномиальная связь 2-го порядка между поглощением и концентрацией иногда встречается для очень больших сложных молекул, таких как органические красители (Ксиленол Апельсин или Нейтральный красный, Например).[нужна цитата ]
УФ-видимая спектроскопия также используется в полупроводниковой промышленности для измерения толщины и оптических свойств тонких пленок на пластине. УФ-видимые спектрометры используются для измерения коэффициента отражения света и могут быть проанализированы с помощью Дисперсионные уравнения Форухи – Блумера. для определения показателя преломления (n) и коэффициента экстинкции (k) данной пленки в измеренном спектральном диапазоне.[нужна цитата ]
Практические соображения
Закон Бера-Ламберта содержит неявные предположения, которые должны быть выполнены экспериментально, чтобы его можно было применить; в противном случае возможны отклонения от закона.[5] Например, химический состав и физическая среда образца могут изменить его коэффициент экстинкции. Поэтому химические и физические условия испытуемого образца должны соответствовать эталонным измерениям, чтобы выводы были достоверными. Во всем мире фармакопеи, такие как Американская (USP) и Европейская (Ph. Eur.) Фармакопеи, требуют, чтобы спектрофотометры работали в соответствии со строгими нормативными требованиями, включая такие факторы, как рассеянный свет.[6] и точность длины волны.[7]
Спектральная полоса пропускания
Важно иметь монохроматический источник излучения для света, падающего на ячейку с образцом.[5] Монохроматичность измеряется как ширина «треугольника», образованного всплеском интенсивности, равная половине максимальной интенсивности. Данный спектрометр имеет спектральную пропускная способность это характеризует как монохромный падающий свет.[требуется разъяснение ] Если эта полоса пропускания сопоставима (или больше) ширина линии поглощения, то измеренный коэффициент экстинкции будет ошибочным. При эталонных измерениях ширина полосы частот прибора (ширина полосы падающего света) поддерживается ниже ширины спектральных линий. Когда исследуемый материал измеряется, ширина полосы падающего света также должна быть достаточно узкой. Уменьшение ширины спектральной полосы уменьшает энергию, передаваемую детектору, и, следовательно, потребует более длительного времени измерения для достижения того же отношения сигнал / шум.
Ошибка длины волны
В жидкостях коэффициент экстинкции обычно медленно изменяется с длиной волны. Пик кривой поглощения (длина волны, при которой поглощение достигает максимума) - это место, где скорость изменения поглощения с длиной волны наименьшая.[5] Измерения обычно производятся на пике, чтобы минимизировать ошибки, вызванные ошибками в длине волны в приборе, то есть ошибками из-за того, что коэффициент ослабления отличается от предполагаемого.
Рассеянный свет
Еще один важный фактор - это чистота используемого света. Наиболее важным фактором, влияющим на это, является рассеянный свет уровень монохроматора.[5]
Используемый детектор - широкополосный; он реагирует на весь свет, который его достигает. Если значительное количество света, прошедшего через образец, содержит длины волн, которые имеют гораздо более низкие коэффициенты экстинкции, чем номинальный, прибор сообщит о неверно низком поглощении. Любой прибор достигнет точки, когда увеличение концентрации образца не приведет к увеличению зарегистрированного поглощения, потому что детектор просто реагирует на рассеянный свет. На практике концентрацию образца или длину оптического пути необходимо отрегулировать так, чтобы неизвестное поглощение попадало в диапазон, допустимый для прибора. Иногда эмпирическая калибровочная функция разрабатывается с использованием известных концентраций образца, чтобы позволить измерения в той области, где прибор становится нелинейным.
Приблизительно, прибор с одним монохроматором обычно имеет уровень паразитного света, соответствующий примерно 3 единицам поглощения (AU), что делает измерения выше примерно 2 AU проблематичными. Более сложный инструмент с двойной монохроматор будет иметь уровень рассеянного света, соответствующий примерно 6 а.е., что, следовательно, позволит измерять гораздо более широкий диапазон поглощения.
Отклонения от закона Бера – Ламберта
При достаточно высоких концентрациях полосы поглощения будут насыщаться и обнаруживать выравнивание поглощения. Пик поглощения кажется сглаженным, потому что почти 100% света уже поглощается. Концентрация, при которой это происходит, зависит от конкретного измеряемого соединения. Один из тестов, который можно использовать для проверки этого эффекта, - это изменение длины пути измерения. В законе Бера-Ламберта изменение концентрации и длины пути имеет эквивалентный эффект - разбавление раствора в 10 раз дает тот же эффект, что и сокращение длины пути в 10 раз. Если доступны ячейки с разной длиной пути, тестирование если это соотношение верно, это один из способов судить, происходит ли выравнивание поглощения.
Неоднородные растворы могут отклоняться от закона Бера – Ламберта из-за явления сплющивания поглощения. Это может произойти, например, когда поглощающее вещество находится внутри взвешенных частиц.[8][9] Отклонения будут наиболее заметны в условиях низкой концентрации и высокого поглощения. В последней ссылке описан способ исправления этого отклонения.
Некоторые растворы, такие как хлорид меди (II) в воде, визуально изменяются при определенной концентрации из-за изменения условий вокруг окрашенного иона (иона двухвалентной меди). Для хлорида меди (II) это означает переход от синего к зеленому,[10] что означало бы, что монохроматические измерения будут отклоняться от закона Бера – Ламберта.
Источники неопределенности измерения
Вышеуказанные факторы способствуют погрешность измерения результатов, полученных с помощью УФ / видимой спектрофотометрии. Если в количественном химическом анализе используется УФ / видимая спектрофотометрия, то на результаты дополнительно влияют источники неопределенности, возникающие из-за природы измеряемых соединений и / или растворов. К ним относятся спектральные помехи, вызванные перекрытием полос поглощения, выцветанием цвета поглощающих частиц (вызванным разложением или реакцией) и возможным несоответствием состава между образцом и калибровочным раствором.[11]
Спектрофотометр видимого и ультрафиолетового диапазонов
В инструмент используется в ультрафиолетовой и видимой спектроскопии, называется UV / Vis спектрофотометр. Он измеряет интенсивность света после прохождения через образец () и сравнивает ее с интенсивностью света до того, как он пройдет через образец (). Соотношение называется коэффициент пропускания, и обычно выражается в процентах (% T). В поглощение, , основан на коэффициенте пропускания:
Спектрофотометр УФ-видимого диапазона также может быть настроен для измерения отражательной способности. В этом случае спектрофотометр измеряет интенсивность света, отраженного от образца () и сравнивает ее с интенсивностью света, отраженного от эталонного материала () (например, белая плитка). Соотношение называется отражательная способность, и обычно выражается в процентах (% R).
Основными частями спектрофотометра являются источник света, держатель для образца, дифракционная решетка в монохроматор или призма для разделения разных длин волн света и детектора. Источником излучения часто является Вольфрам нить накала (300–2500 нм), дейтериевая дуговая лампа, непрерывный в ультрафиолетовой области (190–400 нм), Ксеноновая дуговая лампа, которая непрерывна от 160 до 2000 нм; или совсем недавно светодиоды (LED)[1] для видимых длин волн. Детектор обычно представляет собой фотоумножитель, а фотодиод, фотодиодная матрица или устройство с зарядовой связью (ПЗС). Детекторы с одним фотодиодом и фотоэлектронные умножители используются со сканирующими монохроматорами, которые фильтруют свет так, что только свет одной длины волны достигает детектора за один раз. Сканирующий монохроматор перемещает дифракционную решетку для "сквозного" перехода на каждую длину волны, так что ее интенсивность может быть измерена как функция длины волны. Фиксированные монохроматоры используются с ПЗС-матрицами и матрицами фотодиодов. Поскольку оба этих устройства состоят из множества детекторов, сгруппированных в одно- или двухмерные массивы, они могут собирать свет с разной длиной волны на разных пикселях или группах пикселей одновременно.
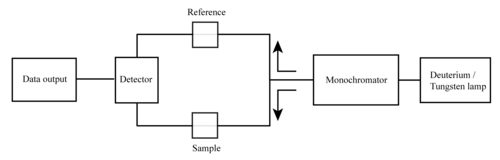
Спектрофотометр может быть либо одинарный луч или двойной луч. В однолучевом приборе (таком как Спектроник 20 ) весь свет проходит через кювету с образцом. должны быть измерены путем удаления образца. Это был самый ранний дизайн, который до сих пор широко используется как в учебных, так и в промышленных лабораториях.
В двухлучевом приборе свет разделяется на два луча, прежде чем достигнет образца. Один луч используется как эталонный; другой луч проходит через образец. За эталонную интенсивность луча принимается 100% пропускание (или 0 абсорбция), а отображаемое измерение представляет собой отношение двух интенсивностей луча. Некоторые двухлучевые приборы имеют два детектора (фотодиоды), и образец и эталонный луч измеряются одновременно. В других инструментах два луча проходят через луч измельчитель, который блокирует по одному лучу за раз. Детектор попеременно измеряет образец пучка и опорный пучок синхронно с прерывателем. В цикле измельчения также может быть один или несколько темных интервалов. В этом случае измеренные интенсивности луча могут быть скорректированы путем вычитания интенсивности, измеренной в темном интервале, прежде чем будет принято соотношение.
В однолучевом приборе сначала необходимо измерить кювету, содержащую только растворитель. Компания Mettler Toledo разработала однолучевой спектрофотометр, который позволяет проводить быстрые и точные измерения в УФ / видимом диапазоне. Источник света состоит из ксеноновой лампы-вспышки для ультрафиолетового (УФ), а также для видимого (VIS) и ближнего инфракрасного диапазона длин волн, охватывающего спектральный диапазон от 190 до 1100 нм. Вспышки лампы фокусируются на стекловолокне, которое направляет луч света на кювету, содержащую раствор образца. Луч проходит через образец, и его компоненты поглощают волны определенной длины. Оставшийся свет собирается после кюветы стекловолокном и направляется в спектрограф. Спектрограф состоит из дифракционной решетки, которая разделяет свет на разные длины волн, и ПЗС-датчика для записи данных соответственно. Таким образом, одновременно измеряется весь спектр, что позволяет производить быструю запись.[12]
Образцы для УФ / видимой спектрофотометрии чаще всего представляют собой жидкости, хотя также можно измерить поглощение газов и даже твердых веществ. Образцы обычно помещаются в прозрачный ячейка, известная как кювета. Кюветы обычно имеют прямоугольную форму, обычно с внутренней шириной 1 см. (Эта ширина становится длиной пути, , в законе Бера – Ламберта.) Пробирки также может использоваться как кювета в некоторых инструментах. Тип используемого контейнера для образца должен позволять излучению проходить через интересующую спектральную область. Наиболее распространенные кюветы изготовлены из высококачественных материалов. плавленый кварц или кварцевое стекло потому что они прозрачны в УФ, видимом и ближнем инфракрасном диапазонах. Также широко распространены стеклянные и пластиковые кюветы, хотя стекло и большинство пластиков поглощают УФ-излучение, что ограничивает их пригодность для видимых длин волн.[1]
Изготовлены и специализированные инструменты. К ним относятся прикрепление спектрофотометров к телескопам для измерения спектров астрономических объектов. Микроспектрофотометры УФ – видимого диапазона состоят из УФ – видимого диапазона. микроскоп интегрирован со спектрофотометром УФ – видимого диапазона.
Полный спектр поглощения на всех интересующих длинах волн часто может быть получен непосредственно с помощью более сложного спектрофотометра. В более простых приборах поглощение определяется по длине волны за раз, а затем оператором составляется спектр. Удалив зависимость от концентрации, можно определить коэффициент экстинкции (ε) как функцию длины волны.
Микроспектрофотометрия
УФ – видимая спектроскопия микроскопических образцов выполняется путем интеграции оптического микроскопа с УФ – видимой оптикой, источниками белого света, монохроматор, и чувствительный детектор, такой как устройство с зарядовой связью (CCD) или фотоумножитель трубка (ФЭУ). Поскольку доступен только один оптический путь, это однолучевые приборы. Современные инструменты способны измерять УФ-видимые спектры как по отражательной способности, так и по пропусканию в областях отбора проб микронного размера. Преимущества использования таких инструментов заключаются в том, что они могут измерять микроскопические образцы, но также могут измерять спектры более крупных образцов с высоким пространственным разрешением. Таким образом, они используются в судебно-медицинской лаборатории для анализа красителей и пигментов в отдельных текстильных волокнах,[13] микроскопические сколы краски [14] и цвет осколков стекла. Они также используются в материаловедении и биологических исследованиях, а также для определения содержания энергии в угле и нефтематеринских породах путем измерения витринит отражательная способность. Микроспектрофотометры используются в полупроводниковой и микрооптической промышленности для контроля толщины тонких пленок после их нанесения. В полупроводниковой промышленности они используются, потому что критические размеры схемы микроскопические. Типичный тест полупроводниковой пластины предполагает получение спектров из многих точек на пластине с рисунком или без него. Толщину нанесенных пленок можно рассчитать из картина интерференции спектров. Кроме того, спектрофотометрия ультрафиолетового и видимого диапазонов может использоваться для определения толщины, а также показателя преломления и коэффициента экстинкции тонких пленок, как описано в Показатель преломления и коэффициент экстинкции тонкопленочных материалов. Затем можно создать карту толщины пленки по всей пластине и использовать ее для контроля качества.[15]
Дополнительные приложения
УФ / видимый свет можно применять для определения кинетики или константы скорости химическая реакция. Реакция, протекающая в растворе, должна демонстрировать изменение цвета или яркости от реагентов к продуктам, чтобы использовать УФ / видимый свет для этого применения.[2] Например, молекула дитизоната ртути имеет желто-оранжевый цвет в разбавленном растворе (1 * 10 ^ -5 M) и становится синим при воздействии определенных длин волн видимого света (и УФ) через конформационное изменение, но эта реакция обратимо обратно в желтое «основное состояние».[16]
Используя оптические волокна в качестве передающего элемента спектра горючих газов, можно определить химический состав топлива, температуру газов и соотношение воздух-топливо.[17]
Константу скорости конкретной реакции можно определить путем измерения спектра поглощения УФ / видимой области через определенные интервалы времени. Снова используя дитизонат ртути в качестве примера, можно направить свет на образец, чтобы раствор стал синим, а затем запускать УФ / видимый тест каждые 10 секунд (переменная), чтобы увидеть, как уровни поглощенной и отраженной длин волн меняются с течением времени в соответствии с раствор снова становится желтым из возбужденного синего энергетического состояния. По этим измерениям можно рассчитать концентрацию двух видов.[18] Реакция дитизоната ртути от одной конформации к другой является реакцией первого порядка и будет иметь интегральный закон скорости первого порядка: ln [A] (время t) = - kt + ln [A] (начальное). Поэтому, построив график натурального логарифма (ln) концентрации [A] в зависимости от времени, вы получите линию с наклоном -k или отрицательной константой скорости. Различные порядки скорости имеют разные интегрированные законы скорости в зависимости от механизма реакции.
Константу равновесия также можно рассчитать с помощью УФ / видимой спектроскопии. После определения оптимальных длин волн для всех частиц, участвующих в равновесии, можно запустить реакцию: равновесие, а также концентрация веществ, определенная с помощью спектроскопии на различных известных длинах волн. Константу равновесия можно рассчитать как K (экв) = [Продукты] / [Реагенты].
Смотрите также
- Изобестическая точка важен в кинетических измерениях. Длина волны, при которой поглощение не изменяется по мере протекания реакции.
- Ультрафиолетовая видимая спектроскопия стереоизомеров
- Инфракрасная спектроскопия и Рамановская спектроскопия другие распространенные спектроскопические методы, обычно используемые для получения информации о структуре соединений или для идентификации соединений. Оба являются формами колебательная спектроскопия.
- Фурье-спектроскопия
- Спектроскопия в ближнем инфракрасном диапазоне
- Колебательная спектроскопия
- Вращательная спектроскопия
- Прикладная спектроскопия
- Наклонная спектроскопия
- Метод Бенези – Хильдебранда
- Спектрофотометрия
- Спектрофотометр ДУ - первый прибор UV – Vis
- Спектроскопия модуляции заряда
использованная литература
- ^ а б c Скуг, Дуглас А .; Холлер, Ф. Джеймс; Крауч, Стэнли Р. (2007). Принципы инструментального анализа (6-е изд.). Бельмонт, Калифорния: Томсон Брукс / Коул. стр.169 –173. ISBN 978-0-495-01201-6.
- ^ а б Мета, Акул (13 декабря 2011 г.). "Принцип". PharmaXChange.info.
- ^ Мета, Акул (22 апреля 2012 г.). «Вывод закона Бера – Ламберта». PharmaXChange.info.
- ^ Мишра, Прабхакар; Дубинский, Марк, ред. (2002). Ультрафиолетовая спектроскопия и УФ-лазеры. Нью-Йорк: Марсель Деккер. ISBN 978-0-8247-0668-5.[страница нужна ]
- ^ а б c d Мета, Акул (14 мая 2012 г.). «Ограничения и отклонения закона Бера – Ламберта». PharmaXChange.info.
- ^ «Рассеянный свет и проверка работоспособности».
- ^ «Точность длины волны в УФ / видимой спектрофотометрии».
- ^ Берберан-Сантос, М. Н. (сентябрь 1990 г.). "Новый взгляд на закон пива". Журнал химического образования. 67 (9): 757. Bibcode:1990JChEd..67..757B. Дои:10.1021 / ed067p757.
- ^ Виттунг, Пернилла; Каянус, Йохан; Кубиста, Микаэль; Мальмстрем, Бо Г. (19 сентября 1994 г.). «Уплощение поглощения в оптических спектрах веществ, захваченных липосомами». Письма FEBS. 352 (1): 37–40. Дои:10.1016/0014-5793(94)00912-0. PMID 7925937. S2CID 11419856.
- ^ Ansell, S; Тромп, Р. Н; Нилсон, Г. В. (20 февраля 1995 г.). «Структура растворенного вещества и акваиона в концентрированном водном растворе хлорида меди (II)». Журнал физики: конденсированное вещество. 7 (8): 1513–1524. Bibcode:1995JPCM .... 7.1513A. Дои:10.1088/0953-8984/7/8/002.
- ^ Sooväli, L .; Рыым, Э.-И .; Kütt, A .; и другие. (2006). «Источники неопределенности в спектрофотометрических измерениях в УФ – видимой области». Аккредитация и гарантия качества. 11 (5): 246–255. Дои:10.1007 / s00769-006-0124-x. S2CID 94520012.
- ^ Все права защищены, Mettler-Toledo International Inc. «Применение и основы спектрофотометрии». www.mt.com. Получено 10 июля 2018.
- ^ Руководство по судебной экспертизе волокна, Материалы научной рабочей группы, 1999 г., http://www.swgmat.org/fiber.htm
- ^ Стандартное руководство по микроспектрофотометрии и измерению цвета в судебном анализе красок, Материалы научной рабочей группы, 1999 г., http://www.swgmat.org/paint.htm
- ^ Horie, M .; Fujiwara, N .; Кокубо, М .; Кондо, Н. (1994). «Спектроскопическая система измерения толщины тонких пленок для полупроводниковой промышленности». Материалы конференций. 10 лет. IMTC / 94. Передовые технологии в I & M. Конференция по измерительным приборам и технологиям IEEE, 1994 г. (каталожный номер 94CH3424-9). С. 677–682. Дои:10.1109 / IMTC.1994.352008. ISBN 0-7803-1880-3. S2CID 110637259.
- ^ Сертова, Н .; Петков, И .; Нунзи, Ж.-М. (Июнь 2000 г.). «Фотохромизм дитизоната ртути (II) в растворе». Журнал фотохимии и фотобиологии A: Химия. 134 (3): 163–168. Дои:10.1016 / с1010-6030 (00) 00267-7.
- ^ Мехренгин, М.В .; Мешковский, И.К .; Ташкинов, В.А .; Гурьев, В.И .; Сухинец, А.В .; Смирнов, Д.С. (июнь 2019). «Многоспектральный пирометр для измерения высоких температур внутри камеры сгорания газотурбинных двигателей». Измерение. 139: 355–360. Дои:10.1016 / j.measurement.2019.02.084.
- ^ Калифорнийский университет в Дэвисе (2 октября 2013 г.). «Закон о тарифах». ChemWiki. Получено 11 ноября 2014.









