Координационный комплекс - Coordination complex
А координационный комплекс состоит из центрального атом или же ион, что обычно металлический и называется координационный центр, и окружающий массив граница молекулы или ионы, которые, в свою очередь, известны как лиганды или комплексообразователи.[1][2][3] Многие металлсодержащие соединения, особенно переходные металлы, являются координационными комплексами.[4] Координационный комплекс, центром которого является атом металла, называют металлическим комплексом блочного элемента d.
Номенклатура и терминология
Координационные комплексы настолько распространены, что их структуры и реакции описываются по-разному, иногда сбивая с толку. Атом внутри лиганда, который связан с центральным атомом или ионом металла, называется донорный атом. В типичном комплексе ион металла связан с несколькими донорными атомами, которые могут быть одинаковыми или разными. А полидентатный (многосвязный) лиганд представляет собой молекулу или ион, который связывается с центральным атомом через несколько атомов лиганда; лиганды с 2, 3, 4 или даже 6 связями к центральному атому являются обычными. Эти комплексы называются хелатные комплексы; образование таких комплексов называется хелатированием, комплексообразованием и координацией.
Центральный атом или ион вместе со всеми лигандами составляют сфера координации.[5][6] Центральные атомы или ион и донорные атомы составляют первую координационную сферу.
Координация относится к «координатным ковалентным связям» (диполярные связи ) между лигандами и центральным атомом. Первоначально комплекс подразумевал обратимую ассоциацию молекулы, атомы, или же ионы через такой слабый химические связи. Применительно к координационной химии это значение претерпело эволюцию. Некоторые комплексы металлов образуются практически необратимо, и многие из них связаны довольно прочными связями.[7][8]
Число донорных атомов, присоединенных к центральному атому или иону, называется координационный номер. Наиболее распространенными координационными числами являются 2, 4 и особенно 6. Гидратированный ион - это один из видов комплексного иона (или просто комплексного), разновидность, образующаяся между центральным ионом металла и одним или несколькими окружающими лигандами, молекулами или ионами, которые содержат хотя бы одну неподеленную пару электронов.
Если все лиганды монодентатный, то количество донорных атомов равно количеству лигандов. Например, ион гексагидрата кобальта (II) или ион гексааквакобальта (II) [Co (H2O)6]2+ представляет собой гидратированный комплексный ион, который состоит из шести молекул воды, прикрепленных к иону металла Co. Степень окисления и координационное число отражают количество связей, образованных между ионом металла и лигандами в комплексном ионе. Однако координационное число Pt (en )2+
2 равно 4 (а не 2), поскольку он имеет два бидентатных лиганда, которые содержат всего четыре донорных атома.
Любой донорный атом даст пару электронов. Есть некоторые донорные атомы или группы, которые могут предлагать более одной пары электронов. Такие называются бидентатными (предлагает две пары электронов) или полидентатными (предлагает более двух пар электронов). В некоторых случаях атом или группа предлагает пару электронов двум подобным или различным центральным атомам или акцепторам металла - путем разделения электронной пары - на один трехцентровая двухэлектронная связь. Их называют мостиковыми лигандами.
История
Координационные комплексы известны с начала современной химии. Ранние известные координационные комплексы включают красители, такие как Берлинская лазурь. Их свойства были впервые хорошо изучены в конце 1800-х годов, после работы 1869 года Кристиан Вильгельм Бломстранд. Бломстранд разработал то, что стало известно как теория сложной ионной цепочки. Согласно теории, координационные комплексы образуются потому, что в растворе ионы связываются аммиачными цепями.[требуется разъяснение ] Он сравнил этот эффект со способом образования различных углеводных цепей.
Следуя этой теории, датский ученый Софус Мадс Йоргенсен внесли в него улучшения. В своей версии теории Йоргенсен утверждал, что когда молекула диссоциирует в растворе, возможны два исхода: ионы связываются через аммиачные цепи, описанные Бломстрандом, или ионы связываются непосредственно с металлом.
Лишь в 1893 году наиболее широко распространенная версия теории была опубликована на сегодняшний день. Альфред Вернер. Работа Вернера включала два важных изменения в теории Бломстранда. Во-первых, Вернер описал две возможности с точки зрения местоположения в координационной сфере. Он утверждал, что если ионы образуют цепочку, это происходит за пределами координационной сферы, в то время как ионы, которые связываются непосредственно с металлом, делают это внутри координационной сферы.[9] Однако в одном из своих самых важных открытий Вернер опроверг большую часть теории цепей. Вернер обнаружил пространственное расположение лигандов, которые участвовали в образовании сложного гексакоординированного кобальта. Его теория позволяет понять разницу между координированным лигандом и ионом, уравновешивающим заряд, в соединении, например, хлорид-ионом в хлоридах кобальтаммина, и объяснить многие ранее необъяснимые изомеры.
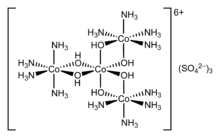
В 1911 году Вернер впервые разрешил координационный комплекс гексол в оптические изомеры, опровергая теорию о том, что только соединения углерода могут обладать хиральность.[10]
Структуры
Ионы или молекулы, окружающие центральный атом, называются лиганды. Лиганды классифицируются как L или X (или их комбинация), в зависимости от того, сколько электронов они обеспечивают для связи между лигандом и центральным атомом. L-лиганды обеспечивают два электрона от одинокая электронная пара, в результате чего координировать ковалентную связь. Лиганды X образуют один электрон, а центральный атом обеспечивает другой электрон, таким образом образуя регулярный Ковалентная связь. Говорят, что лиганды согласованный к атому. За алкены, то пи-облигации может координироваться с атомами металла. Примером является этилен в комплексе [PtCl3(C2ЧАС4)]−.
Геометрия
В координационной химии структура сначала описывается ее координационный номер, количество лигандов, прикрепленных к металлу (точнее, количество донорных атомов). Обычно можно подсчитать присоединенные лиганды, но иногда даже подсчет может быть неоднозначным. Координационные числа обычно составляют от двух до девяти, но большое количество лигандов не является редкостью для лантаноидов и актинидов. Количество облигаций зависит от размера, заряда и электронная конфигурация иона металла и лигандов. Ионы металлов могут иметь более одного координационного числа.
Обычно в химии комплексов переходных металлов преобладают взаимодействия между s и p молекулярные орбитали донорных атомов в лигандах и d-орбиталях ионов металлов. На s-, p- и d-орбиталях металла может находиться 18 электронов (см. Правило 18 электронов ). Таким образом, максимальное координационное число для определенного металла связано с электронной конфигурацией иона металла (точнее, с числом пустых орбиталей) и с соотношением размеров лигандов и иона металла. Большие металлы и маленькие лиганды приводят к высоким координационным числам, например [Пн (CN)8]4−. Мелкие металлы с большими лигандами приводят к низким координационным числам, например Pt [P (CMe3)]2. Благодаря большому размеру, лантаноиды, актиниды, и ранние переходные металлы, как правило, имеют высокие координационные числа.
Большинство структур следуют образцу точек на сфере (или, как если бы центральный атом находился в середине многогранник где углы этой формы являются местоположениями лигандов), где перекрытие орбиталей (между орбиталями лиганда и металла) и отталкивание лиганд-лиганд имеет тенденцию приводить к определенной регулярной геометрии. Наиболее наблюдаемые геометрии перечислены ниже, но есть много случаев, когда они отклоняются от обычной геометрии, например из-за использования лигандов различных типов (что приводит к нерегулярной длине связи; координационные атомы не следуют образцу точки на сфере), из-за размера лигандов или из-за электронные эффекты (см., например, Искажение Яна – Теллера ):
- Линейный для двухкоординации
- Тригональный планарный для трехкоординации
- Тетраэдр или же квадратный плоский для четырехкоординации
- Тригональный бипирамидный для пятикоординации
- Восьмигранный для шестиступенчатой
- Пятиугольный бипирамидальный для семи координат
- Квадратный антипризматический для восьмиступенчатой
- Трехгранный треугольный призматический для девятикоординации
Идеализированные описания 5-, 7-, 8- и 9-координации часто не отличаются геометрически от альтернативных структур с немного отличающимися углами L-M-L (лиганд-металл-лиганд), например разница между квадратно-пирамидальной и тригонально-бипирамидальной структурами.[11]
- Квадрат пирамидальный для пятиступенчатой[12]
- Крытый восьмигранный или же закрытый тригонально-призматический для семи координат[13]
- Додекаэдр или же двуглавый тригонально-призматический для восьмиступенчатой[14]
- Квадратный антипризматический колпачок для девятикоординации
В системах с низким d количество электронов, из-за специальных электронных эффектов, таких как (второго порядка) Ян-Теллер стабилизация,[15] определенные геометрические формы (в которых координационные атомы не следуют схеме точки на сфере) стабилизируются относительно других возможностей, например для некоторых соединений тригонально-призматическая геометрия стабилизируется по сравнению с октаэдрическими структурами для шестикоординации.
- Согнутый для двухкоординации
- Тригонально-пирамидальный для трехкоординации
- Тригонально-призматический для шестиступенчатой
Изомерия
Расположение лигандов фиксировано для данного комплекса, но в некоторых случаях оно может изменяться в результате реакции, которая образует другой стабильный изомер.
Существует много видов изомерия в координационных комплексах, как и во многих других соединениях.
Стереоизомерия
Стереоизомерия происходит с одинаковыми связями в разных ориентациях. Стереоизомерию можно разделить на:[16]
Цис-транс-изомерия и фациально-меридиональная изомерия
Цис-транс-изомерия встречается в октаэдрическом и квадратный плоский комплексы (но не тетраэдрические). Когда два лиганда находятся рядом, они называются СНГ, когда друг напротив друга, транс. Когда три идентичных лиганда занимают одну грань октаэдра, изомер называется лицевым, или фак. В фак изомер, любые два идентичных лиганда являются соседними или СНГ друг другу. Если эти три лиганда и ион металла находятся в одной плоскости, изомер называется меридиональным, или мер. А мер изомер можно рассматривать как комбинацию транс и СНГ, поскольку он содержит как транс-, так и цис-пары идентичных лигандов.

СНГ- [CoCl2(NH3)4]+

транс- [CoCl2(NH3)4]+

фак- [CoCl3(NH3)3]

мер- [CoCl3(NH3)3]
Оптическая изомерия
Оптическая изомерия возникает, когда комплекс не совмещается с его зеркальным отображением. Это так называется потому, что каждый из двух изомеров оптически активный, то есть вращают плоскость поляризованный свет в противоположных направлениях. В первой показанной молекуле символ Λ (лямбда ) используется в качестве префикса для описания левого поворота пропеллера, образованного тремя бидентатными лигандами. Вторая молекула является зеркальным отображением первой с символом Δ (дельта ) в качестве приставки для крутки правого винта. Третья и четвертая молекулы представляют собой подобную пару изомеров Λ и Δ, в данном случае с двумя бидентатными лигандами и двумя идентичными монодентатными лигандами.[17]

Δ- [Fe (окс)3]3−

Δ-СНГ- [CoCl2(en)2]+
Структурная изомерия
Структурная изомерия происходит, когда связи сами по себе разные. Различают четыре типа структурной изомерии: ионизационная изомерия, сольватная или гидратная изомерия, изомерия связи и координационная изомерия.
- Ионизационная изомерия - изомеры дают разные ионы в растворе, хотя они имеют одинаковый состав. Этот тип изомерии возникает, когда противоион комплекса также является потенциальным лигандом. Например, сульфат пентаамминбромокобальта (III) [Co (NH3)5Br] SO4 имеет красно-фиолетовый цвет, и в растворе образуется осадок с хлоридом бария, подтверждающий присутствие сульфат-иона, в то время как бромид пентаамминсульфатекобальта (III) [Co (NH3)5ТАК4] Br имеет красный цвет и дает отрицательный результат на сульфат-ион в растворе, но вместо этого дает осадок AgBr с нитратом серебра.[18]
- Сольватная или гидратная изомерия - изомеры имеют одинаковый состав, но различаются числом молекул растворителя, которые служат лигандом, по сравнению с просто занимающими узлы в кристалле. Примеры: [Cr (H2O)6] Cl3 имеет фиолетовый цвет, [CrCl (H2O)5] Cl2·ЧАС2O сине-зеленый, а [CrCl2(ЧАС2O)4] Cl · 2H2О темно-зеленый. Видеть кристаллизационная вода.[18]
- Изомерия сцепления происходит с амбидентатными лигандами, которые могут связываться более чем в одном месте. Например, НЕТ2 является амбидентатным лигандом: он может связываться с металлом либо по атому N, либо по атому O.[19]
- Координационная изомерия - это происходит, когда как положительные, так и отрицательные ионы соли являются комплексными ионами, а два изомера различаются распределением лигандов между катионом и анионом. Например, [Co (NH3)6] [Cr (CN)6] и [Cr (NH3)6] [Co (CN)6].[18]
Электронные свойства
Многие свойства комплексов переходных металлов продиктованы их электронным строением. Электронная структура может быть описана относительно ионной моделью, которая приписывает формальные заряды металлам и лигандам. В этом подходе - суть теория кристаллического поля (ЦФТ). Теория кристаллического поля, введенная Ганс Бете в 1929 г. дает квантово-механически обоснованная попытка понимания комплексов. Но теория кристаллического поля рассматривает все взаимодействия в комплексе как ионные и предполагает, что лиганды могут быть аппроксимированы отрицательными точечными зарядами.
Более сложные модели охватывают ковалентность, и этот подход описан теория поля лигандов (LFT) и Молекулярная орбитальная теория (МО). Теория поля лигандов, представленная в 1935 году и основанная на теории молекулярных орбиталей, может работать с более широким кругом комплексов и может объяснять комплексы, в которых взаимодействия ковалентный. Химические применения теория групп может помочь в понимании теории поля кристаллов или лигандов, позволяя простые решения формальных уравнений на основе симметрии.
Химики склонны использовать простейшую модель, необходимую для предсказания интересующих свойств; по этой причине CFT был фаворитом для обсуждений, когда это было возможно. Теории МО и НЧ сложнее, но дают более реалистичную перспективу.
Электронная конфигурация комплексов придает им некоторые важные свойства:

Цвет комплексов переходных металлов
Комплексы переходных металлов часто имеют эффектные цвета, вызванные электронными переходами в результате поглощения света. По этой причине их часто применяют как пигменты. Большинство переходов, связанных с окрашенными комплексами металлов, являются либо переходами d – d, либо полосы передачи заряда. При d-d переходе электрон на d-орбитали на металле возбуждается фотоном на другую d-орбиталь с более высокой энергией, поэтому d-d-переходы происходят только для частично заполненных d-орбитальных комплексов (d1–9). Для комплексов с d0 или d10 конфигурации, перенос заряда по-прежнему возможен, хотя переходы d – d невозможны. Зона переноса заряда влечет за собой продвижение электрона с металлической орбитали на пустую орбиталь на основе лиганда (перенос заряда от металла к лиганду или MLCT). Также происходит обратное: возбуждение электрона с орбитали на основе лиганда на пустую орбиталь на основе металла (перенос заряда лиганда на металл или LMCT). Эти явления можно наблюдать с помощью электронной спектроскопии; также известен как УФ-видимый.[20] Для простых соединений с высокой симметрией переходы d – d можно отнести с помощью Диаграммы Танабэ – Сугано. Эти задания получают все большую поддержку с вычислительная химия.
| Fe2+ | Fe3+ | Co2+ | Cu2+ | Al3+ | Cr3+ | |
|---|---|---|---|---|---|---|
| Гидратированный ион | [Fe (H2O)6]2+ Бледно-зеленый Решение | [Fe (H2O)6]3+ Желтый / коричневый Решение | [Co (H2O)6]2+ Розовый Решение | [Cu (H2O)6]2+ Синий Решение | [Al (H2O)6]3+ Бесцветный Решение | [Cr (H2O)6]3+ Зеленый Решение |
| (ОЙ)−, разбавить | [Fe (H2O)4(ОЙ)2] Темно-зеленый Осадок | [Fe (H2O)3(ОЙ)3] коричневый Осадок | [Co (H2O)4(ОЙ)2] Цвет морской волны Осадок | [Cu (H2O)4(ОЙ)2] Синий Осадок | [Al (H2O)3(ОЙ)3] белый Осадок | [Cr (H2O)3(ОЙ)3] Зеленый Осадок |
| (ОЙ)−, концентрированный | [Fe (H2O)4(ОЙ)2] Темно-зеленый Осадок | [Fe (H2O)3(ОЙ)3] коричневый Осадок | [Co (H2O)4(ОЙ)2] Цвет морской волны Осадок | [Cu (H2O)4(ОЙ)2] Синий Осадок | [Al (OH)4]− Бесцветный Решение | [Cr (OH)6]3− Зеленый Решение |
| NH3, разбавить | [Fe (NH3)6]2+ Темно-зеленый Осадок | [Fe (NH3)6]3+ коричневый Осадок | [Co (NH3)6]2+ Соломенный цвет Решение | [Cu (NH3)4(ЧАС2O)2]2+ Темно-синий Решение | [Al (NH3)3]3+ белый Осадок | [Cr (NH3)6]3+ Фиолетовый Решение |
| NH3, концентрированный | [Fe (NH3)6]2+ Темно-зеленый Осадок | [Fe (NH3)6]3+ коричневый Осадок | [Co (NH3)6]2+ Соломенный цвет Решение | [Cu (NH3)4(ЧАС2O)2]2+ Темно-синий Решение | [Al (NH3)3]3+ белый Осадок | [Cr (NH3)6]3+ Фиолетовый Решение |
| (CO3)2- | FeCO3 Темно-зеленый Осадок | Fe2(CO3)3 коричневый Осадок + пузыри | CoCO3 Розовый Осадок | CuCO3 Цвет морской волны Осадок |
Цвета комплексов лантаноидов
Внешне лантаноид комплексы аналогичны комплексам переходных металлов в том, что некоторые из них окрашены. Однако для обычного Ln3+ ионы (Ln = лантаноид) все цвета бледные и практически не зависят от природы лиганда. Цвета обусловлены переходами 4f-электронов. Поскольку 4f-орбитали в лантаноидах «похоронены» в ксеноновом ядре и экранированы от лиганда 5s- и 5p-орбиталями, они не подвержены влиянию лигандов в значительной степени, что приводит к гораздо меньшему кристаллическое поле расщепление, чем в переходных металлах. Спектры поглощения Ln3+ ион приближается к иону свободного иона, где электронные состояния описываются спин-орбитальная связь. Это контрастирует с переходными металлами, где основное состояние расщепляется кристаллическим полем. Поглощения для Ln3+ являются слабыми, поскольку электрические дипольные переходы запрещены по четности (Лапорт запрещен ), но может приобретать интенсивность из-за влияния поля лигандов с низкой симметрией или смешения с более высокими электронными состояниями (например d орбитали). Полосы поглощения f-f чрезвычайно резкие, что контрастирует с наблюдаемыми для переходных металлов, которые обычно имеют широкие полосы.[21][22] Это может привести к чрезвычайно необычным эффектам, таким как значительные изменения цвета при различных формах освещения.
Магнетизм
Комплексы металлов, которые имеют неспаренные электроны, являются магнитный. Рассматривая только монометаллические комплексы, неспаренные электроны возникают из-за нечетного числа электронов в комплексе или из-за дестабилизации спаривания электронов. Таким образом, мономерные частицы Ti (III) имеют один «d-электрон» и должны быть (пара) магнитный, независимо от геометрии или природы лигандов. Ti (II) с двумя d-электронами образует некоторые комплексы, в которых есть два неспаренных электрона, а в других - нет. Этот эффект иллюстрируется соединениями TiX2[(CH3)2PCH2CH2P (CH3)2]2: когда X =Cl комплекс парамагнитен (крутой конфигурации), тогда как при X =CH3, он диамагнитен (низкоскоростной конфигурация). Важно понимать, что лиганды являются важным средством регулирования основное состояние характеристики.
В би- и полиметаллических комплексах, в которых отдельные центры имеют нечетное число электронов или являются высокоспиновыми, ситуация более сложная. Если существует взаимодействие (прямое или через лиганд) между двумя (или более) металлическими центрами, электроны могут соединяться (антиферромагнитная связь, приводя к диамагнитному соединению), или они могут усиливать друг друга (ферромагнитная связь ). Когда нет взаимодействия, два (или более) отдельных металлических центра ведут себя как две отдельные молекулы.
Реактивность
Комплексы показывают множество возможных реактивностей:[23]
- Электронные переводы
- Электронный перенос (ET) между ионами металлов может происходить посредством двух различных механизмов: внутренний и перенос электронов во внешнюю сферу. В реакции внутренней сферы мостиковый лиганд служит проводником для ET.
- (Вырожденный) обмен лиганда
- Одним из важных показателей реактивности является скорость вырожденного обмена лигандов. Например, скорость обмена координатами воды в [M (H2O)6]п+ комплексов варьируется более чем на 20 порядков. Комплексы, в которых лиганды высвобождаются и быстро восстанавливаются, классифицируются как лабильные. Такие лабильные комплексы могут быть термодинамически достаточно стабильными. Типичные лабильные комплексы металлов либо имеют низкий заряд (Na+), электроны на d-орбиталях, которые разрушение относительно лигандов (Zn2+), либо отсутствие ковалентности (Ln3+, где Ln - любой лантаноид). Лабильность металлического комплекса также зависит от высокоспиновой конфигурации по сравнению с низкоспиновой, когда это возможно. Таким образом, высокоспиновые Fe (II) и Co (III) образуют лабильные комплексы, тогда как низкоспиновые аналоги инертны. Cr (III) может существовать только в низкоспиновом состоянии (квартет), которое является инертным из-за его высокой формальной степени окисления, отсутствия электронов на орбиталях, которые разрыхляют связи M – L, плюс некоторая «стабилизация поля лиганда», связанная с d3 конфигурация.
- Ассоциативные процессы
- Комплексы, которые имеют незаполненные или наполовину заполненные орбитали, часто проявляют способность реагировать с субстратами. Большинство субстратов имеют синглетное основное состояние; то есть у них есть неподеленные электронные пары (например, вода, амины, простые эфиры), поэтому этим субстратам нужна пустая орбиталь, чтобы иметь возможность реагировать с металлическим центром. Некоторые субстраты (например, молекулярный кислород) иметь триплетное основное состояние, что приводит к тому, что металлы с наполовину заполненными орбиталями имеют тенденцию реагировать с такими подложками (необходимо сказать, что дикислород молекула также имеет неподеленные пары, поэтому она также способна реагировать как «нормальное» основание Льюиса).
Если лиганды вокруг металла тщательно выбраны, металл может помочь в (стехиометрический или же каталитический ) превращения молекул или использоваться в качестве сенсора.
Классификация
Комплексы металлов, также известные как координационные соединения, включают практически все соединения металлов.[24] Изучение «координационной химии» - это изучение «неорганической химии» всего щелочь и щелочноземельные металлы, переходные металлы, лантаноиды, актиниды, и металлоиды. Таким образом, координационная химия - это химия большинства элементов таблицы Менделеева. Металлы и ионы металлов существуют, по крайней мере, в конденсированных фазах, только в окружении лигандов.
Области координационной химии можно классифицировать в соответствии с природой лигандов в общих чертах:
- Классический (или "Вернер Комплексы »): Лиганды в классической координационной химии связываются с металлами почти исключительно через их одинокие пары электронов, находящихся на атомах основной группы лиганда. Типичные лиганды - H2O, NH3, Cl−, CN−, en. Некоторые из простейших членов таких комплексов описаны в металлические акво комплексы, металлоамминные комплексы,
- Примеры: [Co (EDTA )]−, [Co (NH3)6]3+, [Fe (C2О4)3]
- Металлоорганическая химия: лиганды бывают органическими (алкены, алкины, алкилы), а также «органически-подобными» лигандами, такими как фосфины, гидрид и CO.
- Пример: (C5ЧАС5) Fe (CO)2CH3
- Биоинорганическая химия: лиганды предоставляются природой, особенно в том числе боковые цепи аминокислот и многие другие. кофакторы Такие как порфирины.
- Пример: гемоглобин содержит гем, порфириновый комплекс железа
- Пример: хлорофилл содержит порфириновый комплекс магния
- Многие природные лиганды являются «классическими», особенно вода.
- Кластерная химия: лиганды включают все вышеперечисленное, а также ионы или атомы других металлов.
- Пример Ru3(CO)12
- В некоторых случаях возможны комбинации разных полей:
- Пример: [Fe4S4(Сцистеинил)4]2−, в который кластер встроен в биологически активный вид.
Минералогия, материаловедение, и химия твердого тела - применительно к ионам металлов - это подмножества координационной химии в том смысле, что металлы окружены лигандами. Во многих случаях эти лиганды являются оксидами или сульфидами, но, тем не менее, металлы скоординированы, и применяются принципы и рекомендации, обсуждаемые ниже. В гидраты, по крайней мере, некоторые из лигандов представляют собой молекулы воды. Верно, что направление минералогии, материаловедения и химии твердого тела отличается от обычного направления координационной или неорганической химии. Первые связаны в первую очередь с полимерными структурами, свойствами, возникающими в результате коллективного воздействия многих сильно взаимосвязанных металлов. В отличие от этого координационная химия фокусируется на реакционной способности и свойствах комплексов, содержащих отдельные атомы металлов или небольшие ансамбли атомов металлов.
Номенклатура координационных комплексов
Основная процедура наименования комплекса:
- При названии комплексного иона лиганды называют перед ионом металла.
- Названия лигандов приведены в алфавитном порядке. Цифровые префиксы не влияют на порядок.
- Множественные монодентатные лиганды получают префикс в соответствии с количеством вхождений: ди-, три-, тетра-, пента-, или же гекса-.
- Множественные полидентатные лиганды (например, этилендиамин, оксалат) получают бис-, трис-, тетракис-, так далее.
- Анионы заканчиваются о. Это заменяет последний 'e', когда анион заканчивается на '-ide', '-ate' или '-ite', например хлористый становится хлоридо и сульфат становится сульфат. Раньше '-ide' было изменено на '-o' (например, хлор и циано), но это правило было изменено в рекомендациях IUPAC 2005 г., и теперь правильные формы для этих лигандов хлоридо и цианидо.[25]
- Нейтральным лигандам даны их обычные названия, за некоторыми исключениями: NH3 становится аммин; ЧАС2O становится аква или же акво; CO становится карбонил; НЕТ становится нитрозил.
- Напишите название центрального атома / иона. Если комплекс представляет собой анион, название центрального атома оканчивается на -съел, и будет использоваться его латинское название, если таковое имеется (кроме ртути).
- Степень окисления центрального атома должна быть указана (когда она является одной из нескольких возможных или нулевой) и должна быть записана римской цифрой (или 0) в круглых скобках.
- Названию катиона должно предшествовать название аниона. (если применимо, как в последнем примере)
Примеры:
| металл | изменился на |
|---|---|
| кобальт | кобальтат |
| алюминий | алюминат |
| хром | хромат |
| ванадий | ванадат |
| медь | купрат |
| утюг | феррат |
- [CD (CN)2(en)2] → дицианидобис (этилендиамин) кадмий (II)
- [CoCl (NH3)5]ТАК4 → сульфат пентаамминхлоридокобальта (III)
- [Cu (H2O)6] 2+ → гексааквакоппер (II) ион
- [CuCl5NH3]3− → ион амминпентахлоридкупрата (II)
- K4[Fe (CN)6] → гексацианидоферрат калия (II)
- [NiCl4]2− → тетрахлоридоникелат (II) ион (использование хлора было исключено из соглашения об именах IUPAC)[26]
Координационное число лигандов, присоединенных к более чем одному металлу (мостиковые лиганды), указывается в нижнем индексе греческого символа. μ помещается перед названием лиганда. Таким образом димер из трихлорид алюминия описан Al2Cl4(μ2-Cl)2.
Любая анионная группа может быть электронно стабилизирована любым катионом. Анионный комплекс может быть стабилизирован катионом водорода, превращаясь в кислотный комплекс, который может диссоциировать с высвобождением катионного водорода. Этот вид сложного соединения имеет название с добавлением буквы «ic» после центрального металла. Например, H2[Pt (CN)4] имеет название тетрацианоплатиновая (II) кислота.
Константа устойчивости
Сродство ионов металлов к лигандам описывается константой стабильности, также называемой константой образования, и обозначается символом Kж. Это константа равновесия для его сборки из составляющего металла и лигандов, и может быть рассчитан соответственно, как в следующем примере для простого случая:
- (X) Металл(водн.) + (Y) База Льюиса(водн.) ⇌ (Z) Комплексный ион(водн.)
где X, Y и Z - стехиометрический коэффициенты каждого вида. Константы образования сильно различаются. Большие значения указывают на то, что металл имеет высокое сродство к лиганду при условии, что система находится в равновесии.[27]
Иногда константа устойчивости может быть в другой форме, известной как константа неустойчивости. Эта константа выражается как величина, обратная константе образования, и обозначается как Kd = 1 / Кж .[28] Эта константа представляет собой обратную реакцию разложения комплексного иона на его индивидуальный металл и компоненты лиганда. При сравнении значений Kd, чем больше значение, тем нестабильнее комплексный ион.
В результате образования этих комплексных ионов в растворах они также могут играть ключевую роль в растворимости других соединений. Когда образуется комплексный ион, он может изменять концентрации его компонентов в растворе. Например:
- Ag+
(водн.) + 2NH4ОЙ(водн.) ⇌ Ag (NH3)+
2 + H2О
- AgCl(s) + H2О(l) ⇌ Ag+
(водн.) + Cl−
(водн.)
Если бы обе эти реакции происходили в одном реакционном сосуде, растворимость хлорида серебра повысилась бы за счет присутствия NH4ОН из-за образования комплекса Diammine argentum (I) потребляет значительную часть свободных ионов серебра из раствора. К Принцип Ле Шателье, это заставляет равновесную реакцию растворения хлорида серебра, который имеет ион серебра в качестве продукта, смещаться вправо.
Эту новую растворимость можно рассчитать с учетом значений Kж и Kзр для исходных реакций. Растворимость определяется, по существу, путем объединения двух отдельных равновесий в одну комбинированную равновесную реакцию, и эта комбинированная реакция является той, которая определяет новую растворимость. Итак, Kc, новая константа растворимости, обозначается:
Применение координационных соединений
Металлы существуют только в растворе в виде координационных комплексов, из этого следует, что этот класс соединений может быть полезен для различных целей.
Биоинорганическая химия
В биоинорганическая химия и биоорганометаллическая химия, координационные комплексы выполняют структурные или каталитические функции. Примерно 30% белков содержат ионы металлов. Примеры включают ярко окрашенные витамин B12, то гемовая группа в гемоглобин, то цитохромы, то группа хлорина в хлорофилл, и карбоксипептидаза, гидролитический фермент, важный для пищеварения. Другой комплексный ионный фермент - каталаза, который разлагает клеточные отходы пероксид водорода. Синтетические координационные соединения также используются для связывания с белками и особенно нуклеиновыми кислотами (например, противоопухолевые препараты. цисплатин ).
Промышленность
Гомогенный катализ является основным применением координационных соединений для производства органических веществ. Процессы включают гидрирование, гидроформилирование, окисление. В одном примере комбинация трихлорида титана и триэтилалюминия дает Катализаторы Циглера – Натта, используется для полимеризация этилена и пропилена с получением полимеров, имеющих большое коммерческое значение, таких как волокна, пленки и пластмассы.
Никель, кобальт и медь можно извлечь, используя гидрометаллургические процессы с участием сложных ионов. Их добывают из руд как аммин комплексы. Металлы также можно разделить, используя селективное осаждение и растворимость комплексных ионов. Цианид используется в основном для извлечения золота и серебра из их руд.
Фталоцианин комплексы - важный класс пигментов.
Анализ
Когда-то координационные соединения использовались для определения присутствия металлов в образце. Качественный неорганический анализ был в значительной степени вытеснен инструментальными методами анализа, такими как атомно-абсорбционная спектроскопия (AAS), атомно-эмиссионная спектроскопия с индуктивно связанной плазмой (ICP-AES) и масс-спектрометрия с индуктивно связанной плазмой (ИСП-МС).
Смотрите также
- Активированный комплекс
- Номенклатура неорганической химии ИЮПАК
- Координационная клетка
- Координационная геометрия
- Координационная изомерия
- Координационные полимеры, в которых координационные комплексы являются повторяющимися звеньями.
- Соединения включения
- Металлоорганическая химия имеет дело с особым классом координационных соединений, в которых органические фрагменты связаны с металлом, по крайней мере, через один атом углерода.
Рекомендации
- ^ Лоуренс, Джеффри А. (2010). Введение в координационную химию. Вайли. Дои:10.1002/9780470687123. ISBN 9780470687123.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "сложный ". Дои:10.1351 / goldbook.C01203
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "координационный орган ". Дои:10.1351 / goldbook.C01330
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ «Определение координационной сферы». Chemistry-dictionary.com.
- ^ "Что такое координационное соединение?". Химический факультет Университета Пердью.
- ^ Коттон, Фрэнк Альберт; Джеффри Уилкинсон; Карлос А. Мурильо (1999). Продвинутая неорганическая химия. п. 1355. ISBN 978-0-471-19957-1.
- ^ Мисслер, Гэри Л .; Дональд Артур Тарр (1999). Неорганическая химия. п. 642. ISBN 978-0-13-841891-5.
- ^ «Координационный компаунд».
- ^ Вернер, А. (май 1911 г.). "Zur Kenntnis des asymmetrischen Kobaltatoms. I". Berichte der deutschen chemischen Gesellschaft (на немецком). 44 (2): 1887–1898. Дои:10.1002 / cber.19110440297.
- ^ Уэллс А.Ф. (1984) Структурная неорганическая химия 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Анджело Р. Росси; Роальд. Хоффманн (1975). «Пентакоординация переходного металла». Неорганическая химия. 14 (2): 365–374. Дои:10.1021 / ic50144a032.
- ^ Роальд. Хоффманн; Барбара Ф. Байер; Эрл Л. Мюттертис; Анджело Р. Росси (1977). «Семь-координация. Исследование молекулярных орбиталей структуры, стереохимии и динамики реакций». Неорганическая химия. 16 (3): 511–522. Дои:10.1021 / ic50169a002.
- ^ Джереми К. Бёрдетт; Роальд Хоффманн; Роберт С. Фэй (1978). «Восьмерка-координация». Неорганическая химия. 17 (9): 2553–2568. Дои:10.1021 / ic50187a041.
- ^ Каупп, Мартин (2001). ""Структуры и соединения без VSEPR в d0 Системы ». Энгью. Chem. Int. Эд. Англ. 40 (1): 3534–3565. Дои:10.1002 / 1521-3773 (20011001) 40:19 <3534 :: AID-ANIE3534> 3.0.CO; 2- #.
- ^ фон Зелевский, А. "Стереохимия координационных соединений" Джон Вили: Чичестер, 1995. ISBN 0-471-95599-X.
- ^ Мисслер, Гэри Л .; Дональд Артур Тарр (1999). «9». Неорганическая химия. С. 315, 316. ISBN 978-0-13-841891-5.
- ^ а б c Хухи, Джеймс Э., Неорганическая химия (3-е изд., Harper & Row, 1983), стр. 524–5. ISBN 0-06-042987-9
- ^ Хухи, Джеймс Э., Неорганическая химия (3-е изд., Harper & Row, 1983), стр. 513–24. ISBN 0-06-042987-9
- ^ Harris, D .; Бертолуччи, М. (1989). Симметрия и спектроскопия. Dover Publications.
- ^ Коттон, Ф. Альберт; Уилкинсон, Джеффри; Мурильо, Карлос А .; Бохманн, Манфред (1999), Продвинутая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Коттон, Саймон (2006). Химия лантаноидов и актинидов. John Wiley & Sons Ltd.
- ^ Р. Г. Уилкинс Кинетика и механизм реакций комплексов переходных металлов, 2-е издание, VCH, Weinheim, 1991. ISBN 1-56081-125-0
- ^ Исключение: пары металлов, плазма, и сплавы.
- ^ «Номенклатура рекомендаций ИЮПАК по неорганической химии 2005 г.» (PDF). ИЮПАК. раздел 1.6.4 (стр. 10-11). Архивировано из оригинал (PDF) на 2014-12-22. Получено 2016-03-06.
- ^ «Номенклатура рекомендаций ИЮПАК по неорганической химии 2005 г.» (PDF). ИЮПАК. раздел 1.6.4 (стр. 10-11). Архивировано из оригинал (PDF) на 2014-12-22. Получено 2016-03-06.
- ^ «Комплексные ионные равновесия».
- ^ Стреттон, Том. «Растворимость и комплексно-ионные равновесия» (PDF).
дальнейшее чтение
- De Vito, D .; Вебер, Дж .; Мербах, А. Э. «Расчетные профили объема и энергии для водообмена на t2 г 6 Гексаакваионы родия (III) и иридия (III): неопровержимые доказательства Iа Механизм »Неорганическая химия, 2004, том 43, страницы 858–863. Дои:10.1021 / ic035096n
- Зумдал, Стивен С. Химические принципы, пятое издание. Нью-Йорк: Houghton Mifflin, 2005. 943–946, 957. OCLC 77760970
- Харрис Д., Бертолуччи М., Симметрия и спектроскопия. 1989 Нью-Йорк, Dover Publications











![{displaystyle K_ {f} = {frac {[{ext {Complex ion}}] ^ {Z}} {[{ext {Metal ion}}] ^ {X} [{ext {Lewis base}}] ^ {Y }}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f4126a8afae00c2b0773a00eea6e33c27517b0b2)
