Металл - Metal


А металл (из Греческий μέταλλον Металлон, «шахта, карьер, металл») - это материал который в свежеприготовленном, отполированном или сломанном виде имеет блестящий вид и проводит электричество и высокая температура относительно хорошо. Металлы обычно податливый (их можно забивать в тонкие листы) или пластичный (можно протянуть в провода). Металл может быть химический элемент Такие как утюг; ан сплав Такие как нержавеющая сталь; или молекулярное соединение, такое как полимерный нитрид серы.
В физике металл обычно рассматривается как любое вещество, способное проводить электричество при температуре абсолютный ноль.[1] Многие элементы и соединения, которые обычно не классифицируются как металлы, становятся металлическими под высоким давлением. Например, неметалл йод постепенно превращается в металл при давлении от 40 до 170 тысяч раз атмосферное давление. Точно так же некоторые материалы, которые считаются металлами, могут стать неметаллами. Натрий, например, становится неметаллом при давлении чуть менее двух миллионов атмосфер.
В химии два элемента, которые иначе квалифицировались бы (в физике) как хрупкие металлы:мышьяк и сурьма - вместо этого обычно распознаются как металлоиды из-за их химического состава (преимущественно неметаллический для мышьяка и баланс между металличностью и неметалличностью для сурьмы). Около 95 из 118 элементов в периодическая таблица являются металлами (или могут быть таковыми). Число неточно, так как границы между металлами, неметаллы, и металлоиды незначительно колеблются из-за отсутствия общепринятых определений соответствующих категорий.
В астрофизика термин «металл» используется более широко и относится ко всем химическим элементам в звезде, которые тяжелее двух самых легких, водород и гелий, а не только традиционные металлы. В этом смысле первые четыре «металла», собирающиеся в ядрах звезд в результате нуклеосинтеза, являются углерод, азот, кислород, и неон, все они строго неметаллы в химии. Звезда предохранители более легкие атомы, в основном водород и гелий, превращаются в более тяжелые за время своего существования. В этом смысле металличность астрономического объекта - это доля его вещества, состоящего из более тяжелых химических элементов.[2]
Металлы, как химические элементы, составляют 25% земной коры и присутствуют во многих аспектах современной жизни. Прочность и устойчивость некоторых металлов привели к их частому использованию, например, в высотных зданиях и мостах. строительство, как и большинство автомобилей, многие бытовая техника, инструменты, трубы и железнодорожные пути. Драгоценные металлы исторически использовались как чеканка, но в современную эпоху чеканка металлов распространились по крайней мере до 23 химических элементов.[3]
Считается, что история очищенных металлов началась с использования меди около 11000 лет назад. Золото, серебро, железо (как метеоритное железо), свинец и латунь также использовались до первого известного появления бронзы в 5-м тысячелетии до нашей эры. Последующие разработки включают производство ранних форм стали; открытие натрий -первый легкий металл - в 1809 г .; расцвет современного легированные стали; а после окончания Второй мировой войны - разработка более сложных сплавов.
Характеристики
Форма и структура

Металлы блестящие и блестящий, по крайней мере, в свежеприготовленном, отполированном или сломанном виде. Листы металла толщиной более нескольких микрометров кажутся непрозрачными, но сусальное золото пропускает зеленый свет.
Твердое или жидкое состояние металлов в значительной степени обусловлено способностью задействованных атомов металла легко терять электроны своей внешней оболочки. Вообще говоря, силы, удерживающие электроны внешней оболочки отдельного атома на месте, слабее, чем силы притяжения на тех же электронах, возникающие в результате взаимодействия между атомами в твердом или жидком металле. Вовлеченные электроны становятся делокализованными, и атомную структуру металла можно эффективно визуализировать как совокупность атомов, заключенных в облако относительно мобильных электронов. Такой тип взаимодействия называется металлическая связь.[4] Прочность металлических связей для различных элементарных металлов достигает максимума около центра переходный металл серии, поскольку эти элементы имеют большое количество делокализованных электронов.[n 1]
Хотя у большинства элементарных металлов выше плотности чем большинство неметаллы,[4] их плотность сильно различается, литий наименее плотный (0,534 г / см3) и осмий (22,59 г / см3) самый плотный. Магний, алюминий и титан легкие металлы имеет важное коммерческое значение. Их соответствующие плотности 1,7, 2,7 и 4,5 г / см3 можно сравнить с более старыми конструкционными металлами, такими как железо - 7,9 г / см3 - медь.3. Таким образом, железный шар будет весить примерно как три алюминиевых шара.

Металлы обычно податливы и пластичны, деформируются под нагрузкой без раскалывание.[4] Считается, что ненаправленный характер металлической связи в значительной степени способствует пластичности большинства металлических твердых тел. Напротив, в ионном соединении, таком как поваренная соль, когда плоскости ионная связь скользят друг мимо друга, в результате изменения местоположения смещаются ионы с одинаковым зарядом в непосредственной близости, в результате чего расщепление кристалла. Такой сдвиг не наблюдается в ковалентно связанный кристалл, такой как алмаз, где происходит разрушение и фрагментация кристалла.[5] Обратимый упругая деформация в металлах можно описать как Закон Гука для восстановления сил, где стресс линейно пропорциональна напряжение.
Тепло или силы больше, чем у металла предел упругости может вызвать постоянную (необратимую) деформацию, известную как Пластическая деформация или же пластичность. Приложенная сила может быть растяжение (тянущая) сила, а сжимающий (толкающая) сила, или срезать, изгиб или же кручение (скручивающая) сила. Изменение температуры может повлиять на движение или смещение структурные дефекты в металле, например границы зерен, точечные вакансии, линейные и винтовые дислокации, дефекты укладки и двойняшки в обоих кристаллический и некристаллический металлы. Внутренний соскальзывать, слизняк, и усталость металла может последовать.
Атомы металлических веществ обычно устроенный в одном из трех общих кристаллические структуры, а именно объемно-центрированный кубический (скрытая копия), гранецентрированная кубическая (fcc), и шестиугольный плотно упакованный (ГПУ). В bcc каждый атом расположен в центре куба из восьми других. В ГЦК и ГПУ каждый атом окружен двенадцатью другими, но расположение слоев разное. Некоторые металлы принимают различную структуру в зависимости от температуры.[6]
 Объемно-центрированная кубическая кристаллическая структура с 2-атомной элементарной ячейкой, как обнаружено, например, в хром, железо и вольфрам
Объемно-центрированная кубическая кристаллическая структура с 2-атомной элементарной ячейкой, как обнаружено, например, в хром, железо и вольфрам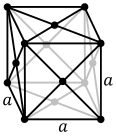 Гранецентрированная кубическая кристаллическая структура с 4-атомной элементарной ячейкой, как обнаружено, например, в алюминий, медь и золото
Гранецентрированная кубическая кристаллическая структура с 4-атомной элементарной ячейкой, как обнаружено, например, в алюминий, медь и золото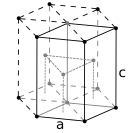 Гексагональная плотноупакованная кристаллическая структура с 6-атомной элементарной ячейкой, как обнаружено, например, в титан, кобальт и цинк
Гексагональная плотноупакованная кристаллическая структура с 6-атомной элементарной ячейкой, как обнаружено, например, в титан, кобальт и цинк
В ячейка каждая кристаллическая структура представляет собой наименьшую группу атомов, которая имеет общую симметрию кристалла и из которой может быть построена вся кристаллическая решетка путем повторения в трех измерениях. В случае объемно-центрированной кубической кристаллической структуры, показанной выше, элементарная ячейка состоит из центрального атома плюс один-восемь каждого из восьми угловых атомов.
Электрические и тепловые

Электронная структура металлов означает, что они относительно хороши проводники электричества. Электроны в веществе могут иметь только фиксированные, а не переменные уровни энергии, а в металле уровни энергии электронов в его электронном облаке, по крайней мере, до некоторой степени, соответствуют уровням энергии, на которых может происходить электрическая проводимость. В полупроводнике, таком как кремний, или в неметалле, таком как сера, существует энергетический зазор между электронами в веществе и уровнем энергии, на котором может возникать электрическая проводимость. Следовательно, полупроводники и неметаллы являются относительно плохими проводниками.
Элементарные металлы имеют значения электропроводности от 6,9 × 103 S / см для марганец до 6,3 × 105 См / см для серебро. Напротив, полупроводник металлоид, такой как бор имеет электропроводность 1,5 × 10−6 См / см. За одним исключением, металлические элементы снижают свою электропроводность при нагревании. Плутоний увеличивает свою электропроводность при нагревании в диапазоне температур от −175 до +125 ° C.
Металлы относительно хорошие проводники тепла. Электроны в электронном облаке металла очень подвижны и легко могут передавать вызванную теплом колебательную энергию.
Вклад электронов металла в его теплоемкость и теплопроводность, а также электропроводность самого металла можно рассчитать по формуле модель свободных электронов. Однако при этом не учитывается детальная структура ионной решетки металла. Учет положительного потенциала, вызванного расположением ионных остовов, позволяет учитывать электронная зонная структура и энергия связи металла. Применимы различные математические модели, простейшая из которых модель почти свободных электронов.
Химическая
Металлы обычно склонны к образованию катионы из-за потери электронов.[4] Большинство из них реагирует с кислородом воздуха с образованием оксиды в разные сроки (калий горит за секунды, пока гладит ржавеет в течение многих лет). Некоторые другие, например палладий, платина и золото, вообще не реагируйте с атмосферой. В оксиды металлов обычно базовый, в отличие от неметаллы, которые кислый или нейтральный. Исключение составляют оксиды с очень высокой состояния окисления такие как CrO3, Mn2О7, и OsO4, которые имеют строго кислые реакции.
Картина, анодирование или же покрытие металлы - хороший способ предотвратить их коррозия. Однако более химически активный металл в электрохимическая серия следует выбирать для покрытия, особенно когда ожидается скалывание покрытия. Вода и два металла образуют электрохимическая ячейка, и если покрытие менее реактивно, чем основной металл, покрытие фактически продвигает коррозия.
Распределение периодической таблицы
В химии элементы, которые обычно считаются металлами при обычных условиях, показаны желтым цветом в таблице Менделеева ниже. Элементы, показанные как имеющие неизвестные свойства, вероятно, являются металлами. Остальные элементы представляют собой либо металлоиды (обычно называемые таковыми B, Si, Ge, As, Sb и Te), либо неметаллы. Астатин (At) обычно классифицируется как неметалл или металлоид; Было предсказано, что это металл, и именно так он показан здесь.
Металлы – металлоиды – неметаллы в периодическая таблица | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| Группа → | ||||||||||||||||||||||||||||||||
| ↓ Период | ||||||||||||||||||||||||||||||||
| 1 | ЧАС | Он | ||||||||||||||||||||||||||||||
| 2 | Ли | Быть | B | C | N | О | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | п | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | В качестве | Se | Br | Kr | ||||||||||||||
| 5 | Руб. | Sr | Y | Zr | Nb | Пн | Tc | RU | Rh | Pd | Ag | CD | В | Sn | Sb | Te | я | Xe | ||||||||||||||
| 6 | CS | Ба | Ла | Ce | Pr | Nd | Вечера | См | Европа | Б-г | Tb | Dy | Хо | Э | Тм | Yb | Лу | Hf | Та | W | Re | Операционные системы | Ir | Pt | Au | Hg | Tl | Pb | Би | По | В | Rn |
| 7 | Пт | Ра | Ac | Чт | Па | U | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og |
МеталлМеталлоидНеметаллНеизвестные свойстваФоновый цвет показывает тенденцию металл – металлоид – неметалл в периодическая таблица | ||||||||||||||||||||||||||||||||
Сплавы

Сплав - это вещество, имеющее металлические свойства и состоящее из двух или более элементы по крайней мере, один из которых - металл. Сплав может иметь переменный или фиксированный состав. Например, золото и серебро образуют сплав, в котором пропорции золота или серебра можно свободно регулировать; титан и кремний образуют сплав Ti2Si, в котором соотношение двух компонентов фиксировано (также известный как интерметаллид ).

Большинство чистых металлов слишком мягкие, хрупкие или химически активные для практического использования. Комбинирование металлов в различных соотношениях в качестве сплавов изменяет свойства чистых металлов для получения желаемых характеристик. Обычно цель изготовления сплавов - сделать их менее хрупкими, твердыми, устойчивыми к коррозии или иметь более желаемый цвет и блеск. Из всех металлических сплавов, используемых сегодня, сплавы утюг (стали, нержавеющая сталь, чугун, инструментальная сталь, легированная сталь ) составляют наибольшую долю как по количеству, так и по коммерческой стоимости. Железо, легированное углеродом в различных пропорциях, дает низко-, средне- и высокоуглеродистые стали, при этом повышенное содержание углерода снижает пластичность и вязкость. Добавление кремний будет производить чугуны, а добавление хром, никель и молибден к углеродистым сталям (более 10%) приводит к нержавеющим сталям.
Другими значительными металлическими сплавами являются сплавы алюминий, титан, медь и магний. Медные сплавы были известны с доисторических времен -бронза дал Бронзовый век его имя - и сегодня они имеют множество применений, в первую очередь в электропроводке. Сплавы трех других металлов были разработаны относительно недавно; из-за своей химической активности они требуют электролитический процессы экстракции. Сплавы алюминия, титана и магния ценятся за их высокое отношение прочности к массе; магний также может обеспечить электромагнитное экранирование.[нужна цитата ] Эти материалы идеальны для ситуаций, когда высокое отношение прочности к весу более важно, чем стоимость материала, например, в аэрокосмической и автомобильной промышленности.
Сплавы, специально разработанные для применения с высокими требованиями, например реактивные двигатели, может содержать более десяти элементов.
Категории
| Металлические элементы |
|---|
| Щелочных металлов |
| Щелочноземельные металлы |
| Переходные металлы |
| Постпереходные металлы |
| Лантаноиды |
| Актиниды |
| Элементы, которые, возможно, являются металлами |
| Элементы, которые иногда считают металлами |
Металлы можно разделить на категории по их физическим или химическим свойствам. Категории, описанные в подразделах ниже, включают железо и цветной металлы; хрупкие металлы и тугоплавкие металлы; белые металлы; тяжелый и свет металлы; и основание, благородный, и драгоценный металлы. В Металлические элементы В таблице в этом разделе элементарные металлы на основе их химических свойств классифицируются на щелочь и щелочноземельный металлы; переход и постпереход металлы; и лантаноиды и актиниды. Другие категории возможны, в зависимости от критериев включения. Например, ферромагнитный металлы - те металлы, которые обладают магнитными свойствами при комнатной температуре - это железо, кобальт и никель.
Черные и цветные металлы
Термин «железо» происходит от латинский слово, означающее «содержащий железо». Это может быть чистое железо, например кованое железо, или сплав, такой как стали. Черные металлы часто магнитный, но не исключительно. В цветных металлах - сплавах - отсутствует заметное количество железа.
Хрупкий металл
В то время как почти все металлы являются ковкими или пластичными, некоторые из них - бериллий, хром, марганец, галлий и висмут - являются хрупкими.[7] Мышьяк и сурьма, если их признать металлами, являются хрупкими. Низкие значения удельного веса модуль упругости к модуль сдвига (Критерий Пью ) указывают на внутреннюю хрупкость.
Тугоплавкий металл
В материаловедении, металлургии и технике тугоплавкий металл - это металл, который чрезвычайно устойчив к нагреванию и износу. Какие металлы относятся к этой категории, варьируется; наиболее распространенное определение включает ниобий, молибден, тантал, вольфрам и рений. Все они имеют температуру плавления выше 2000 ° C и высокую твердость при комнатной температуре.
 Кристаллы ниобия и 1 см3 анодированный куб ниобия для сравнения
Кристаллы ниобия и 1 см3 анодированный куб ниобия для сравнения Кристаллы молибдена и 1 см3 кубик молибдена для сравнения
Кристаллы молибдена и 1 см3 кубик молибдена для сравнения Монокристалл тантала, некоторые кристаллические фрагменты и 1 см3 куб тантала для сравнения
Монокристалл тантала, некоторые кристаллические фрагменты и 1 см3 куб тантала для сравнения Вольфрамовые стержни с испаренными кристаллами, частично окисленными красочным налетом, и диаметром 1 см.3 вольфрамовый куб для сравнения
Вольфрамовые стержни с испаренными кристаллами, частично окисленными красочным налетом, и диаметром 1 см.3 вольфрамовый куб для сравнения Монокристалл рения, переплавленный стержень и 1 см3 кубик рения для сравнения
Монокристалл рения, переплавленный стержень и 1 см3 кубик рения для сравнения
Белый металл
А белый металл представляет собой любой из ряда металлов белого цвета (или их сплавов) с относительно низкими температурами плавления. К таким металлам относятся цинк, кадмий, олово, сурьма (здесь считается металлом), свинец и висмут, некоторые из которых довольно токсичны. В Великобритании торговцы изобразительным искусством используют термин «белый металл» в каталогах аукционов для описания иностранных серебряных изделий, на которых нет знаков Британской пробирной палаты, но которые, тем не менее, считаются серебром и имеют соответствующую цену.
Тяжелые и легкие металлы
Хэви-метал - это любой относительно плотный металл или металлоид.[8] Были предложены более конкретные определения, но ни одно из них не получило широкого признания. Некоторые тяжелые металлы имеют нишевое применение или особенно токсичны; некоторые из них необходимы в следовых количествах. Все остальные металлы - легкие.
Цветные, благородные и драгоценные металлы
В химия, период, термин основной металл неофициально используется для обозначения металла, который легко окисленный или же ржавый, например, легкая реакция с разбавленным соляная кислота (HCl) с образованием хлорида металла и водород. Примеры включают железо, никель, вести и цинк. Медь считается основным металлом, поскольку она относительно легко окисляется, хотя и не реагирует с HCl.

Период, термин благородный металл обычно используется в противовес основной металл. Благородные металлы устойчивы к коррозия или же окисление,[9] в отличие от большинства неблагородные металлы. Это, как правило, драгоценные металлы, часто из-за кажущейся редкости. Примеры включают золото, платину, серебро, родий, иридий и палладий.
В алхимия и нумизматика, термин основной металл противопоставляется драгоценный металл, то есть имеющие высокую экономическую ценность.[10]Давней целью алхимиков было превращение неблагородных металлов в драгоценные металлы, включая такие чеканка металлов как серебро и золото. Большинство монет сегодня сделано из недрагоценных металлов с нет внутренней стоимости, в прошлом монеты часто определяли свою ценность в первую очередь из драгоценный металл содержание.
В химическом отношении драгоценные металлы (например, благородные металлы) менее реактивный чем большинство элементов, имеют высокий блеск и высокая электропроводность. Исторически драгоценные металлы были важны как валюта, но теперь рассматриваются в основном как инвестиционные и промышленные товары. Золото, серебро, платина и палладий у каждого есть ISO 4217 код валюты. Самые известные драгоценные металлы - золото и серебро. Хотя оба они имеют промышленное применение, они более известны своим использованием в Изобразительное искусство, ювелирные украшения, и чеканка. Другие драгоценные металлы включают платиновая группа металлы: рутений, родий, палладий, осмий, иридий и платина, из которых платина является наиболее продаваемой.
Спрос на драгоценные металлы определяется не только их практическим использованием, но и их ролью в качестве инвестиций и средство сбережения.[11] По состоянию на осень 2018 года палладий и платина оценивались примерно в три четверти цены золота. Серебро значительно дешевле, чем эти металлы, но часто традиционно считается драгоценным металлом из-за его роли в чеканке монет и ювелирных изделий.
Жизненный цикл
Формирование
Металлы в земной коре: | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| численность и основное проявление или источник, по массе[n 2] | |||||||||||||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | ЧАС | Он | |||||||||||||||||
| 2 | Ли | Быть | B | C | N | О | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | п | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | В качестве | Se | Br | Kr | |
| 5 | Руб. | Sr | Y | Zr | Nb | Пн | RU | Rh | Pd | Ag | CD | В | Sn | Sb | Te | я | Xe | ||
| 6 | CS | Ба | Ла | Hf | Та | W | Re | Операционные системы | Ir | Pt | Au | Hg | Tl | Pb | Би | ||||
| 7 | |||||||||||||||||||
| Ce | Pr | Nd | См | Европа | Б-г | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||||||
| Чт | U | ||||||||||||||||||
Наиболее многочисленны (до 82000 частей на миллион) | |||||||||||||||||||
Обильный (100–999 частей на миллион) | |||||||||||||||||||
Нечасто (1–99 частей на миллион) | |||||||||||||||||||
Редкий (0.01–0.99 частей на миллион) | |||||||||||||||||||
Очень редкий (0.0001–0.0099 частей на миллион) | |||||||||||||||||||
| Металлы слева от разделительной линии встречаются (или поступают) в основном в виде литофилы; правые, как халькофилы кроме золота (а сидерофил ) и олово (литофил). | |||||||||||||||||||
- В этом подразделе рассматривается формирование элементарных металлов периодической таблицы, поскольку они составляют основу металлических материалов, как определено в этой статье.
Металлы до близость железа (в периодической таблице) в основном производятся через звездный нуклеосинтез. В этом процессе более легкие элементы от водорода до кремний пройти последовательный слияние реакции внутри звезд, высвобождая свет и тепло и образуя более тяжелые элементы с более высокими атомными номерами.[12]
Более тяжелые металлы обычно не образуются таким образом, поскольку реакции синтеза с участием таких ядер будут потреблять, а не выделять энергию.[13] Скорее, они в значительной степени синтезируются (из элементов с более низким атомным номером) посредством захват нейтронов, причем двумя основными режимами этого повторяющегося захвата являются s-процесс и r-процесс. В s-процессе («s» означает «медленный») сингулярные захваты разделены годами или десятилетиями, что позволяет менее стабильным ядрам бета-распад,[14] в то время как в r-процессе («быстром») захваты происходят быстрее, чем ядра могут распадаться. Следовательно, s-процесс идет более или менее понятным путем: например, стабильные ядра кадмия-110 последовательно бомбардируются свободными нейтронами внутри звезды, пока они не образуют ядра кадмия-115, которые являются нестабильными и распадаются с образованием индия-115 (который почти стабильный, с периодом полураспада 30000 раз возраст Вселенной). Эти ядра захватывают нейтроны и образуют нестабильный индий-116, который распадается с образованием олова-116 и т. Д.[12][15][n 3] Напротив, в r-процессе такого пути нет. S-процесс останавливается на висмуте из-за коротких периодов полураспада следующих двух элементов, полония и астатина, которые распадаются на висмут или свинец. R-процесс настолько быстр, что может пропустить эту зону нестабильности и перейти к созданию более тяжелых элементов, таких как торий и уран.[17]
Металлы конденсируются на планетах в результате процессов звездной эволюции и разрушения. Звезды теряют большую часть своей массы, когда выброшен в конце их жизни, а иногда и впоследствии в результате нейтронная звезда слияние[18][n 4] тем самым увеличивая содержание элементов тяжелее гелия в межзвездная среда. Когда гравитационное притяжение заставляет эту материю объединяться и коллапсировать образуются новые звезды и планеты.[20]
Изобилие и встречаемость

Земная кора состоит приблизительно из 25% металлов по весу, из которых 80% составляют легкие металлы, такие как натрий, магний и алюминий. Остальную часть корки составляют неметаллы (~ 75%). Несмотря на общий дефицит некоторых более тяжелых металлов, таких как медь, они могут концентрироваться в экономически извлекаемых количествах в результате горообразования, эрозии или других геологических процессов.
Металлы в основном встречаются в виде литофилов (горных пород) или халькофилов (рудолюбивых). Литофильные металлы - это в основном элементы s-блока, более реактивные из элементов d-блока. и элементы f-блока. Они имеют сильное сродство к кислороду и в основном существуют в виде силикатных минералов с относительно низкой плотностью. Халькофильные металлы - это в основном менее реакционноспособные элементы с d-блоком и металлы с периодом 4–6 p-блока. Обычно они находятся в (нерастворимых) сульфидных минералах. Будучи более плотными, чем литофилы и, следовательно, погружаясь ниже в кору во время ее затвердевания, халькофилы, как правило, менее многочисленны, чем литофилы.
С другой стороны, золото - сидерофил или элемент, любящий железо. Он не образует легко соединений ни с кислородом, ни с серой. Во время формирования Земли, как наиболее благородный (инертный) из металлов, золото погрузилось в ядро из-за своей склонности к образованию металлических сплавов высокой плотности. Следовательно, это относительно редкий металл. Некоторые другие (менее) благородные металлы - молибден, рений, металлы платиновой группы (рутений, родий, палладий, осмий, иридий и платина), германий и олово - могут считаться сидерофилами, но только с точки зрения их первичного присутствия в Земля (ядро, мантия и кора), а точнее кора. В остальном эти металлы присутствуют в коре в небольших количествах, главным образом в виде халькофилов (в меньшей степени в их естественной форме).[n 5]
Вращающееся жидкое внешнее ядро внутренней части Земли, состоящее в основном из железа, считается источником защитного магнитного поля Земли.[n 6] Ядро находится над твердым внутренним ядром Земли и ниже ее мантии. Если бы его можно было перестроить в колонну высотой 5 м.2 (54 кв. Фута) его высота составила бы почти 700 световых лет. Магнитное поле экранирует Землю от заряженных частиц солнечного ветра и космических лучей, которые в противном случае лишили бы верхние слои атмосферы (включая озоновый слой, ограничивающий передачу ультрафиолетового излучения).
Добыча
Металлы часто извлекаются из Земли путем добычи руд, которые являются богатыми источниками необходимых элементов, таких как боксит. Руда находится на разведка техники с последующей разведкой и изучением месторождений. Минеральные источники обычно делятся на наземные мины, которые добываются земляными работами с использованием тяжелой техники, и подземные шахты. В некоторых случаях продажная цена на металл / металлы делает экономически целесообразным добычу из источников с более низкой концентрацией.
Как только руда добыта, металлы должны быть извлеченный обычно путем химического или электролитического восстановления. Пирометаллургия использует высокие температуры для преобразования руды в необработанные металлы, а гидрометаллургия нанимает водный химия с той же целью. Используемые методы зависят от металла и его загрязнителей.
Когда металлическая руда представляет собой ионное соединение этого металла и неметалла, руда обычно должна быть плавил - нагревается восстановителем - для извлечения чистого металла. Многие обычные металлы, такие как железо, плавятся с использованием углерод как восстановитель. Некоторые металлы, такие как алюминий и натрий, не имеют коммерчески практичного восстановителя и экстрагируются с использованием электролиз вместо.[21][22]
Сульфид руды не восстанавливаются непосредственно до металла, а обжигаются на воздухе для преобразования их в оксиды.
Использует

Металлы присутствуют практически во всех аспектах современной жизни. Утюг, а тяжелый металл, может быть наиболее распространенным, поскольку на его долю приходится 90% всех очищенных металлов; алюминий, а легкий металл, является следующим по популярности металлом. Чистое железо может быть самым дешевым из всех металлических элементов по цене около 0,07 доллара США за грамм. Его руды широко распространены; это легко уточнять; а соответствующие технологии разрабатывались на протяжении сотен лет. Чугун еще дешевле - 0,01 доллара США за грамм, потому что нет необходимости в последующей очистке. Платина, по цене около 27 долларов за грамм, может быть наиболее распространенной, учитывая ее очень высокую температуру плавления, устойчивость к коррозии, электропроводность и долговечность. Считается, что он содержится в 20% всех потребительских товаров или используется для его производства. Полоний, вероятно, будет самым дорогим металлом с номинальной стоимостью около 100000000 долларов за грамм.[нужна цитата ] из-за его редкости и мелкомасштабного производства.
Некоторые металлы и металлические сплавы обладают высокой структурной прочностью на единицу массы, что делает их полезными материалами для несения больших нагрузок или сопротивления ударным повреждениям. Металлические сплавы могут иметь высокое сопротивление сдвигу, крутящему моменту и деформации. Однако тот же металл также может быть уязвим к усталостному повреждению при многократном использовании или в результате внезапного разрушения под напряжением при превышении допустимой нагрузки. Прочность и устойчивость металлов привели к их частому использованию в строительстве высотных зданий и мостов, а также в большинстве транспортных средств, многих бытовых приборов, инструментов, труб и железнодорожных путей.
Металлы являются хорошими проводниками, что делает их ценными в электроприборах и для передачи электрического тока на расстояние с небольшими потерями энергии. Электросети используют металлические кабели для распределения электроэнергии. Домашние электрические системы по большей части имеют медный провод из-за его хороших проводящих свойств.
Теплопроводность металлов полезна для контейнеров для нагрева материалов над пламенем. Металлы также используются для радиаторы для защиты чувствительного оборудования от перегрева.
Высокая отражательная способность некоторых металлов позволяет использовать их в зеркалах, в том числе в точных астрономических инструментах, и добавляет эстетики металлическим украшениям.
Некоторые металлы имеют специальное применение; ртуть является жидкостью при комнатной температуре и используется в переключателях для замыкания цепи, когда она протекает через контакты переключателя. Радиоактивные металлы, такие как уран и плутоний используются в атомная электростанция производить энергию через ядерное деление. Сплавы с памятью формы используются для таких применений, как трубы, крепежи и сосуды стенты.
Металлы могут быть допированный с чужеродными молекулами - органическими, неорганическими, биологическими и полимерными. Это легирование приводит к появлению у металла новых свойств, которые индуцируются молекулами-гостями. Были разработаны приложения в катализе, медицине, электрохимических ячейках, коррозии и многом другом.[23]
Переработка отходов

Спрос на металлы тесно связан с экономическим ростом, учитывая их использование в инфраструктуре, строительстве, производстве и производстве потребительских товаров. В течение ХХ века разнообразие металлов, используемых в обществе, быстро росло. Сегодня развитие крупных стран, таких как Китай и Индия, а также технический прогресс подпитывают еще больший спрос. Результатом является то, что горнодобывающая деятельность расширяется, и все больше и больше мировых запасов металлов используются над землей, а не под землей в качестве неиспользованных запасов. Примером может служить используемый запас медь. С 1932 по 1999 год потребление меди в США выросло с 73 г до 238 г на человека.[24]
Металлы по своей природе пригодны для вторичной переработки, поэтому в принципе их можно использовать снова и снова, сводя к минимуму негативное воздействие на окружающую среду и экономя энергию. Например, 95% энергии, используемой для производства алюминия из бокситовой руды, экономится за счет использования переработанного материала.[25]
В мировом масштабе рециркуляция металлов в целом низкая. В 2010 г. Международная панель ресурсов, организованный Программа ООН по окружающей среде опубликовал отчеты о запасах металлов, существующих в обществе[26] и степень их переработки.[24] Авторы отчета отметили, что запасы металла в обществе могут служить огромными шахтами над землей. Они предупредили, что скорость переработки некоторых редких металлов, используемых в таких приложениях, как мобильные телефоны, аккумуляторные батареи для гибридных автомобилей и топливные элементы, настолько низка, что, если в будущем скорость переработки отходов не будет значительно увеличена, эти критически важные металлы станут недоступны для использование в современной технике.
Биологические взаимодействия
У людей некоторые металлы являются незаменимыми питательными веществами (обычно железо, кобальт, и цинк ) или относительно безвредны (например, рутений, серебро и индий ), но может быть токсичным в больших количествах или в определенных формах. Другие металлы, такие как кадмий, ртуть и свинец очень ядовиты. Возможные источники отравления металлами включают: добыча полезных ископаемых, хвосты, промышленные отходы, сельскохозяйственные стоки, профессиональное облучение, краски и обработанная древесина.
История
Предыстория
Медь, которая встречается в самородной форме, возможно, была первым обнаруженным металлом, учитывая ее характерный внешний вид, тяжесть и пластичность по сравнению с другими камнями или галькой. Золото, серебро и железо (как метеоритное железо) и свинец также были открыты в доисторические времена. Формы латунь, сплав меди и цинка, полученный путем одновременной плавки руд этих металлов, происходят из этого периода (хотя чистый цинк не был выделен до 13 века). Податливость твердых металлов привела к первым попыткам изготовления металлических украшений, инструментов и оружия. Время от времени обнаруживалось метеоритное железо, содержащее никель, и в некоторых отношениях оно превосходило любую промышленную сталь, произведенную до 1880-х годов, когда стали заметны легированные стали.[нужна цитата ]
 Золотые кристаллы
Золотые кристаллы Кристаллическое серебро
Кристаллическое серебро Кусочек метеоритного железа
Кусочек метеоритного железа
 Латунная гиря (35 г)
Латунная гиря (35 г)
Античность

Открытие бронза (сплав меди с мышьяком или оловом) позволил людям создавать металлические предметы, которые были более твердыми и долговечными, чем это было возможно раньше. Бронзовые инструменты, оружие, доспехи и строительные материалы например, декоративные плитки были тверже и долговечнее, чем их камень и медь ("Энеолит ") предшественников. Изначально бронзу делали из меди и мышьяк (формирование мышьяковая бронза ) путем выплавки природных или искусственно смешанных руд меди и мышьяка.[27] Раннее артефакты до сих пор известно из Иранское плато в 5-м тысячелетии до н. э.[28] Только позже банка В конце 3-го тысячелетия до н. э. он стал основным не содержащим меди ингредиентом бронзы.[29] Само чистое олово было впервые выделено в 1800 г. до н.э. китайскими и японскими мастерами-металлистами.
Меркурий был известен древним китайцам и индийцам до 2000 г. до н.э. и был найден в египетских гробницах, датируемых 1500 г. до н. Э.
Самое раннее известное производство стали, сплава железа с углеродом, было замечено в металлических изделиях, выкопанных из археологические раскопки в Анатолия (Каман-Калехойюк ) и им почти 4000 лет, они датируются 1800 годом до нашей эры.[30][31]
Примерно с 500 г. до н.э. мастера-мечники Толедо, Испания делали ранние формы легированная сталь добавив минерал под названием вольфрамит, содержащие вольфрам и марганец, до железной руды (и углерода). Результирующий Толедо сталь привлек внимание Рима, когда его использовал Ганнибал в Пунические войны. Вскоре он стал основой вооружения римских легионов; их мечи, как говорили, были «настолько острыми, что нет шлема, который нельзя было бы прорезать ими».[нужна цитата ][n 8]
В доколумбовой Америке, предметы из Тумбага, сплав меди и золота, начали производить в Панаме и Коста-Рике между 300 и 500 годами нашей эры. Маленькие металлические скульптуры были обычным явлением, и обширный спектр украшений из тумбага (и золота) составлял обычные регалии лиц высокого статуса.
Примерно в то же время коренные жители Эквадора комбинируют золото с природным платиновым сплавом, содержащим небольшое количество палладия, родия и иридия, для производства миниатюр и масок из сплава белого золота с платиной. Металлисты использовали нагретое золото с зерна сплава платины до тех пор, пока золото не расплавилось, и в этот момент металлы платиновой группы стали связаны в золоте. После охлаждения полученный конгломерат измельчали и повторно нагревали до тех пор, пока он не стал настолько гомогенным, как если бы все рассматриваемые металлы были расплавлены вместе (достижение точек плавления соответствующих металлов платиновой группы было за пределами технологии того времени).[32][n 9]
 Капля застывшего расплавленного олова
Капля застывшего расплавленного олова
 Электрум, природный сплав серебра и золота, часто использовался для изготовления монет. Изображен римский бог Аполлон, а на лицевой стороне - тренога Дельфы (около 310–305 гг. До н. Э.).
Электрум, природный сплав серебра и золота, часто использовался для изготовления монет. Изображен римский бог Аполлон, а на лицевой стороне - тренога Дельфы (около 310–305 гг. До н. Э.). Тарелка из оловянный, сплав 85–99% олова и (обычно) меди. Впервые олово использовалось в начале бронзового века на Ближнем Востоке.
Тарелка из оловянный, сплав 85–99% олова и (обычно) меди. Впервые олово использовалось в начале бронзового века на Ближнем Востоке. Нагрудный (орнаментальный нагрудник) из Тумбага, сплав золота и меди
Нагрудный (орнаментальный нагрудник) из Тумбага, сплав золота и меди
Средний возраст
Медь для умельца, хитрого в своем деле.
"Хороший!" сказал барон, сидя в своем зале,
«Но Железное - Холодное Железо - властно над ними».
Арабский и средневековый алхимики считал, что все металлы и вещества состоят из принципа серы, отца всех металлов и несущего горючие свойства, и принципа ртути, матери всех металлов[n 10] и носитель свойств ликвидности, плавкости и волатильности. Эти принципы не обязательно были обычными сера и Меркурий найдено в большинстве лабораторий. Эта теория укрепляла веру в то, что всем металлам суждено стать золотом в недрах земли благодаря правильному сочетанию тепла, пищеварения, времени и устранения загрязняющих веществ, все из которых можно развить и ускорить с помощью знаний и методов алхимии. .[n 11]
Стали известны мышьяк, цинк, сурьма и висмут, хотя сначала их называли полуметаллами или нелегальными металлами из-за их неплавкости. Все четыре, возможно, использовались случайно в прежние времена, не осознавая их природы. Альбертус Магнус считается, что первым в 1250 году выделил мышьяк из соединения путем нагревания мыла вместе с трисульфид мышьяка. Металлический цинк, хрупкий, если не чистый, был выделен в Индии к 1300 году нашей эры. Первое описание процедуры выделения сурьмы находится в книге 1540 г. De la pirotechnia к Ваннокчо Бирингуччо. Висмут был описан Агриколой в Ископаемое De Natura (ок. 1546 г.); Раньше его путали с оловом и свинцом из-за его сходства с этими элементами.
 Мышьяк, запечатанный в контейнере для предотвращения потускнения
Мышьяк, запечатанный в контейнере для предотвращения потускнения Фрагменты цинка и 1 см3 куб
Фрагменты цинка и 1 см3 куб Сурьма, проявляющая свой блестящий блеск
Сурьма, проявляющая свой блестящий блеск Висмут в кристаллической форме с очень тонким слоем окисления и толщиной 1 см.3 куб висмута
Висмут в кристаллической форме с очень тонким слоем окисления и толщиной 1 см.3 куб висмута
Ренессанс




Первый систематический текст по горному делу и металлургии был De la Pirotechnia (1540) пользователя Ваннокчо Бирингуччо, который занимается исследованием, плавкой и обработкой металлов.
Шестнадцать лет спустя Георгиус Агрикола опубликовано De Re Metallica в 1556 г. - ясное и полное описание профессии горного дела, металлургии, сопутствующих искусств и наук, а также квалификация как величайший трактат по химической промышленности шестнадцатого века.
Он дал следующее описание металла в своем Ископаемое De Natura (1546):
Металл - это минеральное тело, по своей природе жидкое или твердое. Последний может расплавиться жаром огня, но когда он снова остынет и потеряет все тепло, он снова станет твердым и принимает свою надлежащую форму. В этом отношении он отличается от камня, плавящегося в огне, потому что, хотя последний восстанавливает свою твердость, он все же теряет свою первоначальную форму и свойства.
Традиционно существует шесть различных металлов, а именно золото, серебро, медь, железо, олово и свинец. Есть действительно другие, ибо ртуть металл, хотя алхимики не согласны с нами по этому поводу, и висмут это также. Похоже, что древнегреческие писатели ничего не знали о висмуте, поэтому Аммоний справедливо утверждает, что существует множество видов металлов, животных и растений, которые нам неизвестны. Stibium когда он плавится в тигле и очищается, он имеет такое же право считаться подлинным металлом, как писатели приписывают свинцу. Если при плавлении некоторая часть добавляется к олову, получается книжный сплав, из которого делают шрифт, который используют те, кто печатает книги на бумаге.
Каждый металл имеет свою форму, которую он сохраняет при отделении от тех металлов, которые были с ним смешаны. Поэтому ни электрум ни Stannum [не имея в виду наше олово] сам по себе не является настоящим металлом, а скорее сплавом двух металлов. Электрум - это сплав золота и серебра, олова свинца и серебра. И все же, если отделить серебро от электра, тогда останется золото, а не электрум; если отнять серебро у Stannum, то останется свинец, а не Stannum.
Однако, является ли латунь самородным металлом, нельзя сказать с уверенностью. Известна только искусственная латунь, состоящая из меди, окрашенной в цвет минерала. каламин. И все же, если что-то и откопать, это будет настоящий металл. Черная и белая медь кажутся отличными от красной.
Следовательно, металл по своей природе либо твердый, как я уже сказал, либо жидкий, как в уникальном случае ртути.
Но теперь достаточно о простых видах.[34]
Платина, третий драгоценный металл после золота и серебра, была открыта в Эквадоре в период с 1736 по 1744 год испанским астрономом Антонио де Уллоа и его коллегой математиком Хорхе Хуаном-и-Сантацилия. Уллоа был первым, кто написал научное описание металла в 1748 году.
В 1789 году немецкий химик Мартин Генрих Клапрот смог выделить оксид урана, который, как он думал, был самим металлом. Впоследствии Клапрот был признан первооткрывателем урана. Только в 1841 году французский химик Эжен-Мельхиор Пелиго смог приготовить первый образец металлического урана. Анри Беккерель впоследствии обнаружил радиоактивность в 1896 году, используя уран.
В 1790-х годах Джозеф Пристли и голландский химик Мартинус ван Марум наблюдали преобразующее действие металлических поверхностей на дегидрирование спирта, что впоследствии привело в 1831 году к промышленному синтезу серной кислоты с использованием платинового катализатора.
В 1803 году церий был первым из металлов-лантанидов, который был открыт в Бастнесе, Швеция, Йенсом Якобом Берцелиусом и Вильгельмом Хизингером и независимо Мартином Генрихом Клапротом в Германии. Металлы-лантаноиды в значительной степени считались странностями до 1960-х годов, когда были разработаны методы более эффективного отделения их друг от друга. Впоследствии они нашли применение в сотовых телефонах, магнитах, лазерах, освещении, батареях, каталитических преобразователях и в других приложениях, обеспечивающих современные технологии.
Другими металлами, открытыми и приготовленными в это время, были кобальт, никель, марганец, молибден, вольфрам и хром; и некоторые из платиновая группа металлы, палладий, осмий, иридий и родий.
Легкие металлы
Все металлы, открытые до 1809 года, имели относительно высокую плотность; их тяжесть считалась исключительно отличительным критерием. С 1809 года были выделены легкие металлы, такие как натрий, калий и стронций. Их низкая плотность бросает вызов общепринятым представлениям о природе металлов. Однако химически они вели себя как металлы и впоследствии были признаны таковыми.
Алюминий был открыт в 1824 году, но только в 1886 году был разработан промышленный метод крупномасштабного производства. Цены на алюминий упали, и в 1890-х и начале 20-го века алюминий стал широко использоваться в ювелирных изделиях, предметах повседневного обихода, оправ для очков, оптических инструментах, посуде и фольге. Способность алюминия образовывать твердые, но легкие сплавы с другими металлами обеспечила этому металлу множество применений в то время. Во время Первой мировой войны правительства крупных стран требовали больших партий алюминия для легких прочных планеров. Самый распространенный металл, используемый сегодня для передачи электроэнергии, - это алюминиевый провод, армированный сталью. Также вижу много пользы провод из алюминиевого сплава. Алюминий используется, потому что он весит примерно вдвое меньше, чем медный кабель сравнимого сопротивления (хотя и большего диаметра из-за меньшего удельная проводимость ), а также дешевле. Медь была более популярна в прошлом и до сих пор используется, особенно при более низких напряжениях и для заземления.
Хотя чистый металлический титан (99,9%) был впервые получен в 1910 году, он не использовался за пределами лаборатории до 1932 года. В 1950-х и 1960-х годах Советский Союз впервые применил титан в военных и подводных применениях в рамках программ, связанных с холодом. Война. Начиная с начала 1950-х годов, титан стал широко использоваться в военной авиации, особенно в высокопроизводительных реактивных самолетах, начиная с таких самолетов, как F-100 Супер Сабля и Локхид А-12 и СР-71.
Металлический скандий был впервые произведен в 1937 году. Первый фунт металлического скандия чистотой 99% был произведен в 1960 году. Производство алюминиево-скандиевых сплавов началось в 1971 году после получения патента США. Алюминиево-скандиевые сплавы также были разработаны в СССР.
 Натрий
Натрий Калийный жемчуг под парафиновым маслом. Размер самой крупной жемчужины 0,5 см.
Калийный жемчуг под парафиновым маслом. Размер самой крупной жемчужины 0,5 см. Кристаллы стронция
Кристаллы стронция Алюминиевый кусок,
Алюминиевый кусок,
2,6 грамма, 1 х 2 см- Слиток кристаллов титана
 Скандий, в том числе 1 см3 куб
Скандий, в том числе 1 см3 куб
Возраст стали

Современная эпоха в сталеплавильное производство началось с введения Генри Бессемер с Бессемеровский процесс в 1855 г. сырьем для производства был чугун. Его метод позволял ему производить сталь в больших количествах по дешевке, таким образом мягкая сталь стали использоваться для большинства целей, для которых раньше использовалось кованое железо. Процесс Гилкриста-Томаса (или базовый бессемеровский процесс) был усовершенствованием бессемеровского процесса, сделанным путем футеровки конвертера базовый материал для удаления фосфора.
Из-за высокого предел прочности и низкой стоимости, сталь стала основным компонентом, используемым в здания, инфраструктура, инструменты, корабли, автомобили, машины, бытовая техника и оружие.
В 1872 году англичане Кларк и Вудс запатентовали сплав, который сегодня считается нержавеющей сталью. Коррозионная стойкость железо-хромовых сплавов была признана в 1821 году французским металлургом Пьером Бертье. Он отметил их устойчивость к воздействию некоторых кислот и предложил использовать их в столовых приборах. Металлурги 19-го века были неспособны произвести комбинацию низкоуглеродистого и высокохромистого металла, содержащуюся в большинстве современных нержавеющих сталей, а сплавы с высоким содержанием хрома, которые они могли производить, были слишком хрупкими, чтобы их можно было использовать на практике. Только в 1912 году индустриализация сплавов нержавеющей стали произошла в Англии, Германии и Соединенных Штатах.
Последние стабильные металлические элементы
К 1900 году три металла с атомные номера Менее чем свинец (№ 82), самый тяжелый стабильный металл, оставался открытым: элементы 71, 72, 75.
Фон Вельсбах в 1906 году доказал, что старый иттербий также содержит новый элемент (№ 71), который он назвал кассиопей. Урбен одновременно доказал это, но его образцы были очень нечистыми и содержали только следовые количества нового элемента. Несмотря на это, его выбранное имя лютеций был принят.
В 1908 году Огава обнаружил в торианите элемент 75, но присвоил ему элемент 43 вместо 75 и назвал его. ниппоний. В 1925 году Уолтер Ноддак, Ида Ева Тэке и Отто Берг объявили о своем отделении от гадолинита и дали ему нынешнее название, рений.
Жорж Урбен утверждал, что обнаружил элемент 72 в остатках редкоземельных элементов, а Владимир Вернадский независимо нашел его в ортите. Ни одно из утверждений не было подтверждено из-за Первой мировой войны, и ни то, ни другое не могло быть подтверждено позже, поскольку химический состав, о котором они сообщили, не соответствует тому, что теперь известно гафний. После войны, в 1922 году, Костер и Хевеши обнаружили его с помощью рентгеноспектрального анализа норвежского циркона. Таким образом, гафний был последним открытым стабильным элементом.
 Лютеций, в том числе 1 см3 куб
Лютеций, в том числе 1 см3 куб Рений, в том числе 1 см3 куб
Рений, в том числе 1 см3 куб Гафний в виде стержня весом 1,7 кг
Гафний в виде стержня весом 1,7 кг
К концу Второй мировой войны ученые синтезировали четыре постурановых элемента, все из которых являются радиоактивными (нестабильными) металлами: нептуний (в 1940 г.), плутоний (1940–41 гг.), А также кюрий и америций (1944 г.), представляющие собой элементы 93. до 96. Первые два из них в конечном итоге были обнаружены и в природе. Кюрий и америций были побочными продуктами Манхэттенского проекта, в результате которого в 1945 году была создана первая в мире атомная бомба. Бомба была основана на ядерном расщеплении урана, металла, который, как считается, впервые был открыт почти 150 лет назад.
События после Второй мировой войны
Суперсплавы
Суперсплавы состоящие из комбинаций Fe, Ni, Co и Cr и меньшего количества W, Mo, Ta, Nb, Ti и Al были разработаны вскоре после Второй мировой войны для использования в высокопроизводительных двигателях, работающих при повышенных температурах (выше 650 ° C (1200 ° F)). Они сохраняют большую часть своей прочности в этих условиях в течение продолжительных периодов времени и сочетают в себе хорошую низкотемпературную пластичность с устойчивостью к коррозии или окислению. Суперсплавы теперь можно найти в широком диапазоне применений, включая наземные, морские и аэрокосмические турбины, а также химические и нефтяные заводы.
Транкурийные металлы
Успешная разработка атомной бомбы в конце Второй мировой войны подтолкнула к дальнейшим усилиям по синтезу новых элементов, почти все из которых являются или, как ожидается, будут металлами, и все они радиоактивны. Только в 1949 году элемент 97 (берклий), следующий после элемента 96 (кюрий), был синтезирован путем выстрела альфа-частицами америциевой мишени. В 1952 году элемент 100 (фермий) был обнаружен в обломках первой взрыва водородной бомбы; водород, неметалл, был идентифицирован как элемент почти 200 лет назад. С 1952 г. были синтезированы элементы от 101 (менделевий) до 118 (оганессон).
Объемные металлические очки
Металлическое стекло (также известное как аморфный или стеклообразный металл) представляет собой твердый металлический материал, обычно сплав, с неупорядоченной структурой атомного масштаба. Большинство чистых и легированных металлов в твердом состоянии имеют атомы, расположенные в высокоупорядоченной кристаллической структуре. Аморфные металлы имеют некристаллическую стеклоподобную структуру. Но в отличие от обычных стекол, таких как оконное стекло, которые обычно являются электрическими изоляторами, аморфные металлы обладают хорошей электропроводностью.Аморфные металлы производятся несколькими способами, включая чрезвычайно быстрое охлаждение, физическое осаждение из паровой фазы, твердофазную реакцию, ионное облучение и механическое легирование. Первым металлическим стеклом, о котором было сообщено, был сплав (Au75Si25), произведенный в Калифорнийском технологическом институте в 1960 году. Совсем недавно были произведены партии аморфной стали, в три раза превышающей прочность обычных стальных сплавов. В настоящее время наиболее важные приложения основаны на особых магнитных свойствах некоторых ферромагнитных металлических стекол. Низкие потери намагничивания используются в трансформаторах с высоким КПД. В идентификационных бирках для борьбы с кражами и в других схемах наблюдения за предметами часто используются металлические очки из-за этих магнитных свойств.
Сплавы с памятью формы
Сплав с памятью формы (SMA) - это сплав, который «запоминает» свою первоначальную форму и при деформации возвращается к своей предварительно деформированной форме при нагревании. Хотя эффект памяти формы был впервые обнаружен в 1932 году в сплаве Au-Cd, только в 1962 году, когда было обнаружено случайное открытие эффекта в сплаве Ni-Ti, серьезное исследование началось, а еще за десять лет до коммерческого приложения появились. SMA находят применение в робототехнике, автомобилестроении, аэрокосмической и биомедицинской промышленности. Существует еще один тип SMA, называемый ферромагнитным сплавом с памятью формы (FSMA), который меняет форму под действием сильных магнитных полей. Эти материалы представляют особый интерес, поскольку магнитный отклик имеет тенденцию быть быстрее и эффективнее, чем отклик, вызванный температурой.
Квазицирсталинные сплавы
В 1984 году израильский химик Дан Шехтман обнаружил алюминиево-марганцевый сплав, обладающий пятикратной симметрией, что противоречит кристаллографическим принципам того времени, согласно которым кристаллические структуры могут иметь только двух-, трех-, четырех- или шестикратную симметрию. Из-за страха реакции научного сообщества ему потребовалось два года, чтобы опубликовать результаты, за которые он был удостоен Нобелевской премии по химии в 2011 году. С тех пор сотни квазикристаллов были зарегистрированы и подтверждены. Они существуют во многих металлических сплавах (и некоторых полимерах). Квазикристаллы чаще всего встречаются в алюминиевых сплавах (Al-Li-Cu, Al-Mn-Si, Al-Ni-Co, Al-Pd-Mn, Al-Cu-Fe, Al-Cu-V и др.), Но также известны многочисленные другие составы (Cd-Yb, Ti-Zr-Ni, Zn-Mg-Ho, Zn-Mg-Sc, In-Ag-Yb, Pd-U-Si и т.д.). Квазикристаллы фактически имеют бесконечно большие элементарные ячейки. Икосаэдрит Al63Cu24Fe13первый квазикристалл, обнаруженный в природе, был обнаружен в 2009 году. Большинство квазикристаллов имеют керамические свойства, включая низкую электропроводность (приближающуюся к значениям, наблюдаемым в изоляторах) и низкую теплопроводность, высокую твердость, хрупкость, устойчивость к коррозии и антипригарное покрытие. характеристики. Квазикристаллы использовались для разработки теплоизоляции, светодиодов, дизельных двигателей и новых материалов, преобразующих тепло в электричество. В новых сферах применения можно использовать преимущества низкого коэффициента трения и твердости некоторых квазикристаллических материалов, например, заделку частиц в пластик для изготовления прочных, износостойких пластиковых шестерен с низким коэффициентом трения. Другие потенциальные применения включают селективные поглотители солнечной энергии для преобразования энергии, отражатели с широким диапазоном длин волн, а также для ремонта костей и протезов, где требуются биосовместимость, низкое трение и коррозионная стойкость.
Сложные металлические сплавы
Сложные металлические сплавы (CMA) представляют собой интерметаллические соединения, характеризующиеся крупными элементарными ячейками, содержащими от нескольких десятков до тысяч атомов; наличие четко определенных кластеров атомов (часто с икосаэдрической симметрией); и частичный беспорядок в их кристаллических решетках. Они состоят из двух или более металлических элементов, иногда с металлоидами или халькогениды добавлен. К ним относятся, например, NaCd2 с 348 атомами натрия и 768 атомами кадмия в элементарной ячейке. Линус Полинг попытался описать структуру NaCd2 в 1923 году, но не добился успеха до 1955 года. Сначала интерес к CMA, как их стали называть, не увеличивался до 2002 года, когда была опубликована статья под названием «Структурно сложные фазы сплава». ", данный на 8-я Международная конференция по квазикристаллам. Возможные применения CMA включают в себя теплоизоляцию; солнечное отопление; магнитные холодильники; использование отработанного тепла для выработки электроэнергии; и покрытия для лопаток турбин в двигателях военного назначения.
Сплавы с высокой энтропией
Сплавы с высокой энтропией (HEA), такие как AlLiMgScTi, состоят из равных или почти равных количеств пяти или более металлов. По сравнению с обычными сплавами, состоящими только из одного или двух основных металлов, HEA имеют значительно лучшее отношение прочности к массе, более высокую прочность на разрыв и большую устойчивость к разрушению, коррозии и окислению. Хотя HEA были описаны еще в 1981 году, значительный интерес проявился только в 2010-х годах; они продолжают оставаться в центре исследований в области материаловедения и инженерии из-за их потенциала в отношении желаемых свойств.
Фазовые сплавы MAX
| МАКСИМУМ | M | А | Икс |
|---|---|---|---|
| Hf2SnC | Hf | Sn | C |
| Ti4AlN3 | Ti | Al | N |
| Ti3SiC2 | Ti | Si | C |
| Ti2AlC | Ti | Al | C |
| Cr2AlC2 | Cr | Al | C |
| Ti3AlC2 | Ti | Al | C |
В Фазовый сплав MAX, M металл раннего перехода, А является элементом группы A (в основном группы IIIA и IVA или группы 13 и 14), и Икс либо углерод, либо азот. Примеры: Hf2SnC и Ti4AlN3. Такие сплавы обладают одними из лучших свойств металлов и керамики. Эти свойства включают высокую электрическую и теплопроводность, сопротивление тепловому удару, устойчивость к повреждениям, обрабатываемость, высокую упругую жесткость и низкие коэффициенты теплового расширения.[35] Их можно полировать до металлического блеска из-за их превосходной электропроводности. В ходе механических испытаний было обнаружено, что поликристаллический Ti3SiC2 Цилиндры могут многократно сжиматься при комнатной температуре до напряжений 1 ГПа и полностью восстанавливаться после снятия нагрузки. Некоторые фазы MAX также обладают высокой устойчивостью к химическому воздействию (например, Ti3SiC2) и высокотемпературное окисление на воздухе (Ti2AlC, Cr2AlC2, а Ti3AlC2). Возможные применения фазовых сплавов MAX включают: в качестве прочных, поддающихся механической обработке, термостойких огнеупоров; высокотемпературные нагревательные элементы; покрытия для электрических контактов; и детали, устойчивые к нейтронному облучению, для ядерных применений. Хотя фазовые сплавы MAX были открыты в 1960-х годах, первая статья на эту тему не была опубликована до 1996 года.
Смотрите также
Примечания
- ^ Это упрощенное объяснение; другие факторы могут включать радиус атома, ядерный заряд, номер облигации орбитали, перекрытие орбитальных энергий и кристаллическая форма.[4]
- ^ Микроэлементы с содержанием, равным или намного меньшим одной части на триллион (а именно Tc, Вечера, По, В, Ра, Ac, Па, Np, и Пу ) не показаны.
- ^ В некоторых случаях, например при наличии гамма-лучи высоких энергий или в среда, богатая водородом при очень высоких температурах, рассматриваемые ядра могут испытывать потерю нейтронов или усиление протонов, что приводит к образованию (сравнительно редко) нейтронно-дефицитные изотопы.[16]
- ^ Выброс вещества при столкновении двух нейтронных звезд объясняется взаимодействием их приливные силы, возможное разрушение корки и шоковый нагрев (что происходит, если вы нажимаете педаль акселератора в автомобиле, когда двигатель холодный).[19]
- ^ Железо, кобальт, никель и олово также являются сидерофилами с точки зрения всей Земли.
- ^ Еще одна жизненно важная роль железа - это ключевой компонент гемоглобин, который обеспечивает транспортировку кислорода из легких к остальному телу.
- ^ Бронза представляет собой сплав, состоящий в основном из меди, обычно с около 12% олова и часто с добавлением других металлов (таких как алюминий, марганец, никель или цинк), а иногда и неметаллов или металлоидов, таких как мышьяк, фосфор или кремний.
- ^ Одновременно халийские народы Понта в Малой Азии прославлялись за работу с железом и сталью. Они не знали, что их железо содержит большое количество марганца, что позволяет производить сталь высшего качества.
- ^ В Дамаске, Сирия, кузнецы клинков могли выковывать ножи и мечи с характерным рисунком поверхности, состоящим из закрученных узоров из выгравированных светом областей на почти черном фоне. Эти клинки обладали легендарными режущими способностями. Железо, которое использовали кузнецы был получен из Индии и содержал один или несколько карбидообразующих элементов, таких как V, Mo, Cr, Mn и Nb. Современный анализ этого оружия показал, что эти элементы способствовали каталитическому образованию углеродных нанотрубок, что, в свою очередь, способствовало образованию цементит (Fe3В) нанопроволоки. Податливость углеродных нанотрубок компенсирует хрупкость цементита и наделяет полученную сталь уникальным сочетанием прочности и гибкости. Знание того, как сделать то, что стало называться Дамасская сталь вымер в восемнадцатом веке, возможно, из-за истощения источников руды с правильным сочетанием примесей. Используемые методы не были открыты заново до 2009 года.
- ^ В древности свинец считался отцом всех металлов.
- ^ Парацельс, позже Немецкий ренессанс писатель добавил третий принцип соли, несущей нелетучие и негорючие свойства, в своем триа прима доктрина. Эти теории сохранили четыре классических элемента, лежащих в основе состава серы, ртути и соли.
Рекомендации
- ^ Ёнэдзава, Ф (2017). Физика переходов металл-неметалл. Амстердам: IOS Press. п. 257. ISBN 978-1-61499-786-3.
сэр Невилл Мотт (1905-1996) написал письмо коллеге-физику, Проф. Питер П. Эдвардс, в котором он отмечает ... Я много думал о том, что такое металл? и я думаю, что ответить на вопрос можно только на Т = 0 (абсолютный ноль температуры). Там металл проводит, а неметалл - нет.
- ^ Джон К. Мартин. «Что мы узнаем из содержания металла звезды». Новый анализ кинематики лиры RR в солнечной окрестности. Архивировано из оригинал 29 июня 2016 г.. Получено 7 сентября, 2005.
- ^ Роу, Дж; Роу, М. (1992). «В мировой чеканке используются 24 химических элемента». Мировые новости чеканки. 19 (4, 5): 24–25, 18–19.
- ^ а б c d е Мортимер, Чарльз Э. (1975). Химия: концептуальный подход (3-е изд.). Нью-Йорк: Компания Д. Ван Нострада.
- ^ Пластичность - прочность материалов
- ^ Holleman, A.F .; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5.
- ^ Russell, A.M; Ли, К. Л. (2005). Структурно-имущественные отношения в цветных металлах. Структурно-имущественные отношения в цветных металлах. Хобокен, Нью-Джерси: Джон Уайли и сыновья. стр. passim. Bibcode:2005срнм.книга ..... R. ISBN 978-0-471-64952-6.
- ^ Загрязнение металлов. Издания Quae. 2006 г. ISBN 978-2-7592-0011-5.
- ^ Тунай, Олчай; Кабдасли, Исик; Арслан-Алатон, Идил; Ольмез-Ханчи, Тугба (2010). Применение химического окисления промышленных сточных вод. Издательство IWA. ISBN 978-1-84339-307-8.
- ^ Вальтер, Джон В. (2013). Природные ресурсы Земли. Издательство "Джонс и Бартлетт". ISBN 978-1-4496-3234-2.
- ^ Абдул-Рахман, Яхья (2014). Искусство RF (без риба) Исламский банкинг и финансы: инструменты и методы для банковского обслуживания на уровне сообществ. Джон Вили и сыновья. ISBN 978-1-118-77096-2.
- ^ а б Кокс 1997, стр. 73–89
- ^ Кокс 1997, стр.32, 63, 85
- ^ Подосек 2011, п. 482
- ^ Падманабхан 2001, п. 234
- ^ Rehder 2010, стр.32, 33
- ^ Хофманн 2002, стр. 23–24
- ^ Хадхази 2016
- ^ Чоптуик, Ленер и Преториас 2015, п. 383
- ^ Кокс 1997, стр. 83, 91, 102–103
- ^ «Лос-Аламосская национальная лаборатория - Натрий». Получено 2007-06-08.
- ^ «Лос-Аламосская национальная лаборатория - алюминий». Получено 2007-06-08.
- ^ Авнир, Давид (2014). «Молекулярно легированные металлы». Соотв. Chem. Res. 47 (2): 579–592. Дои:10.1021 / ar4001982. PMID 24283194.
- ^ а б Темпы переработки металлов: отчет о состоянии В архиве 2016-01-01 в Wayback Machine 2010, Международная панель ресурсов, Программа ООН по окружающей среде
- ^ Действовать осторожно: атака алюминия Кэролайн Фрай, Guardian.co.uk, 22 февраля 2008 г.
- ^ Запасы металлов в обществе: научный синтез В архиве 2016-01-01 в Wayback Machine 2010, Международная панель ресурсов, Программа ООН по окружающей среде
- ^ Тайлекот, Р.Ф. (1992). История металлургии, второе издание. Лондон: издательство Maney Publishing для Института материалов. ISBN 978-1-902653-79-2. Архивировано из оригинал 2015-04-02.
- ^ Thornton, C .; Lamberg-Karlovsky, C.C .; Лизерс, М .; Янг, С.М. (2002). «На булавках и иглах: отслеживание эволюции легирования на основе меди в Тепе Яхья, Иран, с помощью анализа обычных предметов с помощью ИСП-МС». Журнал археологической науки. 29 (12): 1451–1460. Дои:10.1006 / jasc.2002.0809.
- ^ Кауфман, Бретт. «Металлургия и археологические изменения на Древнем Ближнем Востоке». Backdirt: Годовой обзор. 2011: 86.
- ^ Аканума, Х. (2005). «Значение состава раскопанных фрагментов железа, взятых из слоя III на территории Каман-Калехююк, Турция». Анатолийские археологические исследования. Токио: Японский институт анатолийской археологии. 14: 147–158.
- ^ "Металлические изделия, обнаруженные в Турции, считаются старейшей сталью". Индуистский. Ченнаи, Индия. 2009-03-26. Архивировано из оригинал на 2009-03-29. Получено 2009-03-27.
- ^ Кнаут, П. (1976). Металлисты, исправленное издание. Лондон: Time-Life International. С. 133, 137.
- ^ Опубликовано в Дилинатор, Сентябрь 1909. Перепечатано как введение к Награды и феи в 1910 г.
- ^ Георгиус Агрикола, De Re Metallica (1556) Тр. Герберт Кларк Гувер и Лу Генри Гувер (1912); Цитата в сноске Ископаемое De Natura (1546), стр. 180
- ^ Макс фазовые композиты Материаловедение и инженерия A
дальнейшее чтение
- Кроу Дж. М. 2016, «Невозможные сплавы: как делать невиданные ранее металлы», Новый Ученый, 12 октября
- Приход Р.В. 1977, Металлические элементы, Лонгман, Лондон, ISBN 978-0-582-44278-8
- Раймонд Р. 1984, Из огненной печи: влияние металлов на историю человечества, Macmillan Australia, Мельбурн, ISBN 978-0-333-38024-6
- Рассел А. И Ли К. Л. 2005, Структурно-имущественные отношения в цветных металлах, John Wiley & Sons, Хобокен, Нью-Джерси, ISBN 978-0-471-64952-6
- Стрит А. и Александр В. 1998, Металлы на службе у человека (11-е изд.), Penguin Books, Лондон, ISBN 978-0-14-025776-2
- Уилсон А.Дж. 1994, Живая скала: история металлов с древнейших времен и их влияние на развивающуюся цивилизацию, Издательство Woodhead Publishing, Кембридж, ISBN 978-1-85573-154-7
внешняя ссылка
- ASM International (ранее Американское общество металлов)
- Прочный, как титан, дешевый, как грязь: новый стальной сплав сияет
- Домашняя страница Общества минералов, металлов и материалов































