Ниобий - Niobium
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ниобий | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /паɪˈoʊбяəм/ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешность | серый металлик, голубоватый при окислении | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес Аг, стд(Nb) | 92.90637(1)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ниобий в периодическая таблица | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер (Z) | 41 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | d-блок | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Категория элемента | Переходный металл | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [Kr ] 4d4 5 с1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 12, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза вSTP | твердый | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 2750 K (2477 ° С, 4491 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 5017 К (4744 ° С, 8571 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | 8,57 г / см3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 30 кДж / моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 689,9 кДж / моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 24.60 Дж / (моль · К) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Давление газа
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Состояния окисления | −3, −1, 0, +1, +2, +3, +4, +5 (мягко кислый окись) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Масштаб Полинга: 1,6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус атома | эмпирические: 146вечера | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 164 ± 18 часов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | изначальный | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристальная структура | объемно-центрированный кубический (скрытая копия) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкий стержень | 3480 м / с (при 20 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 7,3 мкм / (м · К) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 53,7 Вт / (м · К) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 152 нОм · м (при 0 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | парамагнитный | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль для младших | 105 ГПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 38 ГПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 170 ГПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.40 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Моосу | 6.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Виккерсу | 870–1320 МПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 735–2450 МПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Количество CAS | 7440-03-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| История | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Именование | после Ниоба в греческой мифологии, дочь Тантал (тантал ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие | Чарльз Хэтчетт (1801) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Первая изоляция | Кристиан Вильгельм Бломстранд (1864) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Признанный отдельным элемент к | Генрих Роуз (1844) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Главный изотопы ниобия | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ниобий, также известный как колумбий, это химический элемент с символ Nb (ранее Cb) и атомный номер 41. Ниобий - светло-серый, кристаллический и пластичный переходный металл. Чистый ниобий имеет Твердость по Моосу рейтинг аналогичен чистому титан,[2] и обладает такой же пластичностью, как утюг. Ниобий окисляется в земных атмосфера очень медленно, поэтому его используют в ювелирных изделиях как гипоаллергенный Альтернативой никель. Ниобий часто встречается в минералах. пирохлор и колумбит отсюда и прежнее название «колумбий». Его название происходит от Греческая мифология, конкретно Ниоба, которая была дочерью Тантал, тезка тантал. Название отражает большое сходство между двумя элементами по их физическим и химическим свойствам, из-за чего их трудно различить.[3]
Английский химик Чарльз Хэтчетт сообщил о новом элементе, похожем на тантал, в 1801 году и назвал его колумбием. В 1809 г. английский химик Уильям Хайд Волластон ошибочно пришли к выводу, что тантал и колумбий идентичны. Немецкий химик Генрих Роуз В 1846 году он определил, что танталовые руды содержат второй элемент, который он назвал ниобием. В 1864 и 1865 годах ряд научных открытий прояснил, что ниобий и колумбий являются одним и тем же элементом (в отличие от тантала), и в течение столетия оба названия использовались как синонимы. Ниобий был официально принят в качестве названия элемента в 1949 году, но название колумбий по-прежнему используется в металлургии США.
Только в начале 20 века ниобий впервые стал использоваться в коммерческих целях. Бразилия - ведущий производитель ниобия и феррониобий, сплав 60–70% ниобия с железом. Ниобий используется в основном в сплавах, большая часть в специальных стали например, что используется в газе трубопроводы. Хотя эти сплавы содержат максимум 0,1%, небольшой процент ниобия увеличивает прочность стали. Температурная стабильность ниобийсодержащих суперсплавы важно для его использования в струя и ракетные двигатели.
Ниобий используется в различных сверхпроводящий материалы. Эти сверхпроводящие сплавы, также содержащий титан и банка, широко используются в сверхпроводящие магниты из МРТ сканеры. Другие применения ниобия включают сварку, атомную промышленность, электронику, оптику, нумизматика, и ювелирные изделия. В последних двух применениях низкая токсичность и радужность, вызванная анодирование очень желанные свойства. Ниобий считается технологически важный элемент.
История


Ниобий был идентифицированный английский химик Чарльз Хэтчетт в 1801 г.[4][5][6] Он обнаружил новый элемент в образце минерала, который был отправлен в Англию из Коннектикут, Соединенные Штаты в 1734 году Джоном Уинтропом F.R.S. (внук Джон Уинтроп Младший ) и назвал минерал колумбит и новый элемент колумбий после Колумбия, поэтическое название Соединенных Штатов.[7][8][9] В колумбий обнаруженный Хэтчеттом, вероятно, был смесью нового элемента с танталом.[7]
Впоследствии возникла значительная путаница.[10] по разнице между колумбием (ниобием) и близким ему танталом. В 1809 г. английский химик Уильям Хайд Волластон сравнили оксиды, полученные из обоих колумбий-колумбит, с плотностью 5,918 г / см3, а тантал -танталит, плотностью более 8 г / см3, и пришел к выводу, что два оксида, несмотря на значительную разницу в плотности, были идентичны; таким образом он сохранил название тантал.[10] Этот вывод был оспорен в 1846 г. немецким химиком. Генрих Роуз, которые утверждали, что в образце танталита присутствуют два разных элемента, и назвали их в честь детей Тантал: ниобий (из Ниоба ) и пелопий (из Pelops ).[11][12] Эта путаница возникла из-за минимальных наблюдаемых различий между танталом и ниобием. Заявленные новые элементы пелопий, ильмений, и дианиум[13] были фактически идентичны ниобию или смесям ниобия и тантала.[14]
Различия между танталом и ниобием были недвусмысленно продемонстрированы в 1864 г. Кристиан Вильгельм Бломстранд[14] и Анри Этьен Сент-Клер Девиль, а также Луи Дж. Трост, определивший формулы некоторых соединений в 1865 г.[14][15] и наконец швейцарским химиком Жан Шарль Галиссар де Мариньяк[16] в 1866 году, которые все доказали, что существует только два элемента. Статьи о ильмений продолжал появляться до 1871 года.[17]
Де Мариньяк первым подготовил металл в 1864 году, когда он уменьшенный хлорид ниобия, нагревая его в атмосфере водород.[18] Хотя к 1866 году де Мариньяк смог производить ниобий, не содержащий тантала, в больших масштабах, только в начале 20 века ниобий использовался в лампа накаливания филаменты, первое коммерческое применение.[15] Это использование быстро устарело из-за замены ниобия на вольфрам, который имеет более высокую температуру плавления. Этот ниобий улучшает прочность стали был впервые обнаружен в 1920-х годах, и это приложение остается основным его применением.[15] В 1961 году американский физик Юджин Кунцлер и коллеги в Bell Labs обнаружил, что ниобий-олово продолжает проявлять сверхпроводимость в присутствии сильных электрических токов и магнитных полей,[19] что делает его первым материалом, поддерживающим высокие токи и поля, необходимые для использования мощных магнитов и электроэнергии. машины. Это открытие позволило - два десятилетия спустя - производить длинные многожильные кабели, намотанные в катушки для создания больших и мощных электромагниты для вращающегося оборудования, ускорителей частиц и детекторов частиц.[20][21]
Название элемента
Колумбий (символ «Cb»)[22] Это название было дано Хэтчеттом после открытия металла в 1801 году.[5] Название отражало, что типовой образец руда приехал из Америки (Колумбия ).[23] Это название осталось в употреблении в американских журналах - последняя статья, опубликованная Американское химическое общество с колумбий в названии датируется 1953 г.[24]-пока ниобий использовался в Европе. Чтобы положить конец этой путанице, имя ниобий был выбран для элемента 41 на 15-й конференции Союза химиков в Амстердаме в 1949 году.[25] Год спустя это название было официально принято Международный союз теоретической и прикладной химии (ИЮПАК) после 100 лет споров, несмотря на хронологический приоритет названия колумбий.[25] Это был своего рода компромисс;[25] ИЮПАК принял вольфрам вместо вольфрама в знак уважения к употреблению в Северной Америке; и ниобий вместо колумбий из уважения к европейскому использованию. Хотя многие химические общества и правительственные организации США обычно используют официальное название ИЮПАК, некоторые металлурги и общества металлургов все еще используют оригинальное американское название ".колумбий".[26][27][28][29]
Характеристики
Физический
Ниобий - это блестящий, серый, пластичный, парамагнитный металл в группа 5 из периодическая таблица (см. таблицу), с электронной конфигурацией во внешнем снаряды нетипично для группы 5. (Это можно наблюдать в районе рутений (44), родий (45), и палладий (46).)
| Z | Элемент | Количество электронов / оболочка |
|---|---|---|
| 23 | ванадий | 2, 8, 11, 2 |
| 41 | ниобий | 2, 8, 18, 12, 1 |
| 73 | тантал | 2, 8, 18, 32, 11, 2 |
| 105 | дубний | 2, 8, 18, 32, 32, 11, 2 |
Хотя считается, что объемно-центрированный кубический кристаллической структуры от абсолютного нуля до ее точки плавления, измерения теплового расширения с высоким разрешением по трем кристаллографическим осям выявляют анизотропию, несовместимую с кубической структурой.[30] Поэтому ожидаются дальнейшие исследования и открытия в этой области.
Ниобий становится сверхпроводник в криогенный температуры. При атмосферном давлении он имеет самую высокую критическую температуру из элементарных сверхпроводников - 9,2.K.[31] Ниобий имеет наибольшее глубина магнитного проникновения любого элемента.[31] Кроме того, это один из трех элементалей. Сверхпроводники II типа, вместе с ванадий и технеций. Сверхпроводящие свойства сильно зависят от чистоты металлического ниобия.[32]
В очень чистом виде он сравнительно мягкий и пластичный, но примеси делают его более твердым.[33]
Металл имеет низкий сечение захвата для теплового нейтроны;[34] таким образом, он используется в ядерной промышленности, где требуются нейтронно-прозрачные структуры.[35]
Химическая
Металл приобретает голубоватый оттенок при длительном пребывании на воздухе при комнатной температуре.[36] Несмотря на высокую температуру плавления в элементарной форме (2468 ° C), он имеет более низкую плотность, чем другие тугоплавкие металлы. Кроме того, он устойчив к коррозии, проявляет свойства сверхпроводимости и образует диэлектрик окись слои.
Ниобия чуть меньше электроположительный и более компактный, чем его предшественник в периодической таблице, цирконий, тогда как он практически идентичен по размеру с более тяжелыми атомами тантала в результате сокращение лантаноидов.[33] В результате химические свойства ниобия очень похожи на таковые для тантала, который находится непосредственно под ниобием в периодическая таблица.[15] Хотя его коррозионная стойкость не такая выдающаяся, как у тантала, более низкая цена и большая доступность делают ниобий привлекательным для менее требовательных применений, таких как футеровка чанов на химических заводах.[33]
Изотопы
Ниобий в земной коре составляет одну стабильную изотоп, 93Nb.[37] К 2003 г. не менее 32 радиоизотопы были синтезированы, в диапазоне атомная масса от 81 до 113. Самым стабильным из них является 92Nb с период полураспада 34,7 миллиона лет. Один из наименее стабильных - 113Nb, с расчетным периодом полураспада 30 миллисекунд. Изотопы легче конюшни 93Nb имеет тенденцию распадаться на β+ разлагаться, а те, что тяжелее, имеют тенденцию распадаться β− разлагаться, за некоторыми исключениями. 81Nb, 82Nb и 84Nb имеют минор β+ отложенный испускание протона пути распада, 91Nb распадается на захват электронов и позитронное излучение, и 92Nb распадается как β+ и β− разлагаться.[37]
Не менее 25 ядерные изомеры были описаны в диапазоне атомных масс от 84 до 104. В этом диапазоне только 96Nb, 101Nb и 103Nb не имеет изомеров. Наиболее стабильным из изомеров ниобия является 93мNb с периодом полураспада 16,13 года. Наименее стабильный изомер 84мNb с периодом полураспада 103 нс. Все изомеры ниобия распадаются изомерный переход или бета-распад кроме 92 млNb, имеющий небольшую ветвь захвата электронов.[37]
Вхождение
Ниобий оценивается как 34-й самый распространенный элемент в земной коре, с 20промилле.[38] Некоторые думают, что количество на Земле намного больше, и что высокая плотность элемента сконцентрировала его в ядре Земли.[27] Свободный элемент не встречается в природе, но ниобий встречается в минералах в сочетании с другими элементами.[33] Минералы, содержащие ниобий, часто также содержат тантал. Примеры включают колумбит ((Fe, Mn) (Nb, Ta)2О6) и колумбит-танталит (или же колтан, (Fe, Mn) (Ta, Nb)2О6).[39] Колумбит-танталитные минералы (наиболее распространенными видами являются колумбит (Fe) и танталит (Fe), где «- (Fe)» - суффикс Левинсона, указывающий на преобладание железа над другими элементами, такими как марганец).[40][41][42][43]) чаще всего встречаются как акцессорные минералы в пегматит интрузий и в щелочных интрузивных породах. Реже встречаются ниобаты кальций, уран, торий и редкоземельные элементы. Примеры таких ниобатов: пирохлор ((Na, Ca)2Nb2О6(OH, F)) (теперь название группы, с относительно распространенным примером, например, фторкальциопирохлор[44][45][42][43][46]) и эвксенит (правильно названный эвксенит- (Y)[47][42][43]) ((Y, Ca, Ce, U, Th) (Nb, Ta, Ti)2О6). Эти большие месторождения ниобия были обнаружены, связанные с карбонатиты (карбонат -силикат Магматические породы ) и как составная часть пирохлора.[48]
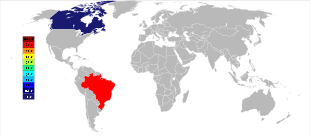
Три крупнейших в настоящее время месторождения пирохлора, два в Бразилии и одно в Канаде, были обнаружены в 1950-х годах и до сих пор являются основными производителями концентратов ниобиевых минералов.[15] Самое крупное месторождение расположено внутри интрузии карбонатитов в г. Араша, состояние Минас-Жерайс, Бразилия, принадлежит CBMM (Companhia Brasileira de Metalurgia e Mineração ); другое активное бразильское месторождение находится недалеко от Каталао, состояние Гояс, и принадлежит Китай молибден, также размещены в пределах интрузии карбонатитов.[49] Вместе эти две шахты производят около 88% мировых запасов.[50] Бразилия также имеет большое, но еще не освоенное месторождение недалеко от Сан-Габриэль да Кашуэйра, состояние Amazonas, а также несколько более мелких месторождений, особенно в состоянии Рорайма.[50][51]
Третий по величине производитель ниобия - карбонатитовый Ниобек мой, в Сент-Оноре, возле Chicoutimi, Квебек, Канада, принадлежит Ресурсы Magris.[52] Он производит от 7% до 10% мировых поставок.[49][50]
Производство
После отделения от других минералов смешанные оксиды тантала Та2О5 и ниобий Nb2О5 получены. Первым этапом обработки является реакция оксидов с плавиковая кислота:[39]
- Та2О5 + 14 HF → 2 H2[TaF7] + 5 H2О
- Nb2О5 + 10 HF → 2 H2[NbOF5] + 3 H2О
Первая промышленная сепарация, разработанная де Мариньяк, использует различную растворимость сложного ниобия и тантала. фториды, моногидрат оксипентафторониобата дикалия (K2[NbOF5]·ЧАС2O) и гептафтортанталат дикалия (K2[TaF7]) в воде. В более новых процессах используется жидкая экстракция фторидов из водный решение органические растворители подобно циклогексанон.[39] Комплексные фториды ниобия и тантала извлекаются отдельно от органический растворитель с водой и осаждают добавлением фторид калия для получения комплекса фторида калия или осаждение аммиак как пятиокись:[53]
- ЧАС2[NbOF5] + 2 KF → K2[NbOF5] ↓ + 2 ВЧ
С последующим:
- 2 ч2[NbOF5] + 10 NH4OH → Nb2О5↓ + 10 NH4F + 7 H2О
Несколько методов используются для снижение металлическому ниобию. В электролиз расплавленной смеси K2[NbOF5] и хлорид натрия является одним; другой - восстановление фторида с натрий. С помощью этого метода можно получить ниобий относительно высокой чистоты. При крупносерийном производстве Nb2О5 восстанавливается водородом или углеродом.[53] в алюминотермическая реакция, смесь оксид железа и оксид ниобия реагирует с алюминий:
- 3 Nb2О5 + Fe2О3 + 12 Al → 6 Nb + 2 Fe + 6 Al2О3
Небольшие количества окислителей, например нитрат натрия добавляются для усиления реакции. Результат оксид алюминия и феррониобий, сплав железа и ниобия, используемый в производстве стали.[54][55] Феррониобий содержит от 60 до 70% ниобия.[49] Без оксида железа для производства ниобия используется алюминотермический процесс. Дальнейшая очистка необходима для достижения степени сверхпроводящий сплавы. Электронно-лучевая плавка под вакуумом - метод, используемый двумя основными поставщиками ниобия.[56][57]
По состоянию на 2013 год[Обновить], CBMM из Бразилии контролировала 85 процентов мирового производства ниобия.[58] В Геологическая служба США По оценкам, производство увеличилось с 38 700 тонн в 2005 году до 44 500 тонн в 2006 году.[59][60] Мировые ресурсы оцениваются в 4 400 000 тонн.[60] За десятилетний период с 1995 по 2005 год производство увеличилось более чем вдвое, начиная с 17 800 тонн в 1995 году.[61] В период с 2009 по 2011 год добыча оставалась стабильной на уровне 63 000 тонн в год.[62] с небольшим снижением в 2012 году до 50 000 тонн в год.[63]
| Страна | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 160 | 230 | 290 | 230 | 200 | 200 | 200 | ? | ? | ? | ? | ? | ? | ? | |
| 30,000 | 22,000 | 26,000 | 29,000 | 29,900 | 35,000 | 40,000 | 57,300 | 58,000 | 58,000 | 58,000 | 58,000 | 45,000 | 53,100 | |
| 2,290 | 3,200 | 3,410 | 3,280 | 3,400 | 3,310 | 4,167 | 3,020 | 4,380 | 4,330 | 4,420 | 4,630 | 4,710 | 5,260 | |
| ? | 50 | 50 | 13 | 52 | 25 | ? | ? | ? | ? | ? | ? | ? | ? | |
| ? | ? | 5 | 34 | 130 | 34 | 29 | ? | ? | ? | ? | ? | ? | ? | |
| 35 | 30 | 30 | 190 | 170 | 40 | 35 | ? | ? | ? | ? | ? | ? | ? | |
| 28 | 120 | 76 | 22 | 63 | 63 | 80 | ? | ? | ? | ? | ? | ? | ? | |
| Мир | 32,600 | 25,600 | 29,900 | 32,800 | 34,000 | 38,700 | 44,500 | 60,400 | 62,900 | 62,900 | 62,900 | 63,000 | 50,100 | 59,400 |
Меньшие суммы находятся на месторождении Каньяка Малави (Шахта Каньяка ).
Соединения
Во многом ниобий похож на тантал и цирконий. Он реагирует с большинством неметаллов при высоких температурах; с фтор при комнатной температуре; с хлор при 150 ° C и водород при 200 °C; и с азот при 400 ° C, с продуктами, которые часто являются промежуточными и нестехиометрическими.[33] Металл начинает окислять на воздухе при 200 °C.[53] Он устойчив к коррозии за счет плавления щелочи и кислотами, в том числе царская водка, соляной, серный, азотный и фосфорные кислоты.[33] Ниобий подвергается нападению плавиковая кислота и смеси фтористоводородной / азотной кислоты.
Хотя ниобий проявляет все формальные степени окисления от +5 до -1, наиболее распространенные соединения имеют ниобий в состоянии +5.[33] Обычно соединения со степенями окисления менее 5+ обнаруживают связь Nb – Nb. В водных растворах ниобий проявляет только степень окисления +5. Он также легко подвержен гидролизу и мало растворяется в разбавленных растворах соляной, серный, азотный и фосфорные кислоты за счет осаждения водного оксида Nb.[56] Nb (V) также плохо растворяется в щелочной среде из-за образования растворимых полиоксониобатов.[65][66]
Оксиды и сульфиды
Формы ниобия оксиды в состояния окисления +5 (Nb2О5 ),[67] +4 (NbO2 ), +3 (Nb
2О
3),[53] и более редкая степень окисления +2 (NbO ).[68] Наиболее распространенным является пентоксид, предшественник почти всех соединений и сплавов ниобия.[53][69] Ниобаты образуются путем растворения пентоксида в базовый гидроксид растворов или плавлением в оксидах щелочных металлов. Примеры ниобат лития (LiNbO3) и ниобата лантана (LaNbO4). В ниобате лития тригонально искаженный перовскит -подобная структура, тогда как ниобат лантана содержит одиночные NbO3−
4 ионы.[53] Слоистый сульфид ниобия (NbS2) также известен.[33]
Материалы могут быть покрыты тонкой пленкой оксида ниобия (V). химическое осаждение из паровой фазы или же осаждение атомного слоя процессы, возникающие при термическом разложении этоксид ниобия (V) выше 350 ° C.[70][71]
Галогениды


Ниобий образует галогениды в степенях окисления +5 и +4, а также различные субстехиометрические соединения.[53][56] Пентагалогениды (NbX
5) имеют октаэдрические центры Nb. Пентафторид ниобия (NbF5) представляет собой белое твердое вещество с температурой плавления 79,0 ° C и пентахлорид ниобия (NbCl5) имеет желтый цвет (см. изображение слева) с температурой плавления 203,4 ° C. Оба гидролизованный с образованием оксидов и оксигалогенидов, таких как NbOCl3. Пентахлорид - универсальный реагент, используемый для создания металлоорганический соединения, такие как дихлорид ниобоцена ((C
5ЧАС
5)
2NbCl
2).[72] Тетрагалогениды (NbX
4) - полимеры темного цвета со связями Nb-Nb; например, черный гигроскопичный тетрафторид ниобия (NbF4) и коричневый тетрахлорид ниобия (NbCl4).
Анионные галогенидные соединения ниобия хорошо известны, отчасти благодаря Кислотность Льюиса пентагалогенидов. Наиболее важным является [NbF7]2−, промежуточное соединение при отделении Nb и Ta от руд.[39] Этот гептафторид имеет тенденцию к образованию оксопентафторида более легко, чем соединение тантала. Другие галогенидные комплексы включают октаэдрические [NbCl6]−:
- Nb2Cl10 + 2 кл− → 2 [NbCl6]−
Как и в случае с другими металлами с низкими атомными номерами, известно множество восстановленных кластерных ионов галогенидов, главным примером которых является [Nb6Cl18]4−.[73]
Нитриды и карбиды
Другой бинарные соединения ниобия включают нитрид ниобия (NbN), который становится сверхпроводник при низких температурах и используется в детекторах инфракрасного света.[74] Главный карбид ниобия NbC, чрезвычайно жесткий, огнеупорный, керамика материал, коммерчески используемый при резке инструменты.
Приложения

Из 44 500 тонн ниобия, добытого в 2006 году, примерно 90% было использовано в производстве высококачественной конструкционной стали. Второе по величине приложение - суперсплавы.[75] Сверхпроводники и электронные компоненты из ниобиевых сплавов составляют очень небольшую долю в мировом производстве.[75]
Производство стали
Ниобий - эффективный микролегирование элемент для стали, внутри которого он формирует карбид ниобия и нитрид ниобия.[27] Эти составы улучшают измельчение зерна и замедляют рекристаллизацию и дисперсионное твердение. Эти эффекты, в свою очередь, увеличивают ударную вязкость, прочность, формуемость и свариваемость.[27] Внутри микролегированных нержавеющая сталь, содержание ниобия невелико (менее 0,1%[76]) но важное дополнение к высокопрочные низколегированные стали которые широко используются в конструкции современных автомобилей.[27] Иногда ниобий используется в значительно больших количествах для изготовления деталей машин и ножей с высокой износостойкостью, до 3% в нержавеющей стали Crucible CPM S110V.[77]
Эти же сплавы ниобия часто используются при строительстве трубопроводов.[78][79]
Суперсплавы

Количества ниобия используются в никеле-, кобальт -, и утюг -основан суперсплавы в пропорциях до 6,5%[76] для таких приложений, как реактивный двигатель составные части, газовые турбины, ракетные узлы, турбонагнетатели, жаропрочное и сжигательное оборудование. Ниобий выделяет упрочняющую γ '' - фазу в зеренной структуре суперсплава.[80]
Одним из примеров суперсплава является Инконель 718, состоящий примерно из 50% никель, 18.6% хром, 18.5% утюг, 5% ниобий, 3,1% молибден, 0.9% титан, и 0,4% алюминий.[81][82] Эти суперсплавы использовались, например, в усовершенствованных системах рамы для Программа Близнецы. Другой сплав ниобия использовался для сопла Сервисный модуль Apollo. Поскольку ниобий окисляется при температурах выше 400 ° C, для этих применений необходимо защитное покрытие, чтобы сплав не стал хрупким.[83]
Сплавы на основе ниобия
С-103 сплав был разработан в начале 1960-х годов совместно Wah Chang Corporation и Боинг Co. DuPont, Union Carbide Corp., General Electric Co. и несколько других компаний развивались Сплавы на основе ниобия одновременно, во многом благодаря Холодная война и Космическая гонка. Он состоит из 89% ниобия, 10% гафний и 1% титана и используется для жидкостная ракета сопла двигателя, такие как главный двигатель Лунные модули Аполлона.[83]

Сопло Мерлин Вакуум серия двигателей, разработанная SpaceX для верхней ступени своего Сокол 9 Ракета сделана из сплава ниобия.[84]
Реакционная способность ниобия с кислородом требует, чтобы он работал в вакуум или же инертная атмосфера, что значительно увеличивает стоимость и сложность производства. Вакуумно-дуговый переплав (VAR) и электронно-лучевая плавка (EBM), новые для того времени процессы, позволили разработать ниобий и другие химически активные металлы. Проект, в результате которого был получен C-103, начался в 1959 году с 256 экспериментальных сплавов ниобия в «серии C» (возможно, из columbium), которые можно растопить как пуговицы и скатать в простынь. У Ва Чанга был запас гафния, очищенного от ядерной чистоты. циркониевые сплавы, которую он хотел использовать в коммерческих целях. 103-й экспериментальный состав сплавов серии С, Nb-10Hf-1Ti, имел наилучшее сочетание формуемости и жаропрочных свойств. Ва Чанг изготовил первый нагревательный элемент C-103 весом 500 фунтов в 1961 году, слиток за листом, используя EBM и VAR. Предполагаемые приложения включены турбинные двигатели и жидкий металл теплообменники. Конкурирующие ниобиевые сплавы той эпохи включали FS85 (Nb-10W-28Ta-1Zr) от Fansteel Metallurgical Corp., Cb129Y (Nb-10W-10Hf-0.2Y) от Wah Chang and Boeing, Cb752 (Nb-10W-2.5Zr) от Union Carbide и Nb1Zr от Superior Tube Co.[83]
Сверхпроводящие магниты

Ниобий-германий (Nb
3Ge), ниобий-олово (Nb
3Sn), так же хорошо как ниобий-титановый сплавы используются как сверхпроводник II типа провод для сверхпроводящие магниты.[85][86] Эти сверхпроводящие магниты используются в магнитно-резонансная томография и ядерный магнитный резонанс инструменты, а также в ускорители частиц.[87] Например, Большой адронный коллайдер использует 600 тонн сверхпроводящих нитей, а Международный термоядерный экспериментальный реактор использует примерно 600 тонн Nb3Пряди Sn и 250 тонн нитей NbTi.[88] Только в 1992 году было построено систем клинической магнитно-резонансной томографии на сумму более 1 миллиарда долларов США с использованием ниобий-титановой проволоки.[20]
Другие сверхпроводники

В сверхпроводящая радиочастота (SRF) полости, используемые в лазеры на свободных электронах ВСПЫШКА (результат отмененного проекта линейного ускорителя ТЕСЛА) и XFEL сделаны из чистого ниобия.[89] А криомодуль команда в Фермилаб использовал ту же технологию SRF из проекта FLASH для разработки девятиэлементных резонаторов SRF с частотой 1,3 ГГц, изготовленных из чистого ниобия. Полости будут использоваться в 30-километровом (19 миль) линейный ускоритель частиц из Международный линейный коллайдер.[90] Та же технология будет использоваться в LCLS-II в Национальная ускорительная лаборатория SLAC и PIP-II в Фермилаб.[91]
Высокая чувствительность сверхпроводящего нитрид ниобия болометры сделать их идеальным детектором для электромагнитное излучение в ТГц диапазоне частот. Эти детекторы прошли испытания в Субмиллиметровый телескоп, то Телескоп Южного полюса, то Приемник лабораторный телескоп, а в APEX, и теперь используются в приборе HIFI на борту Космическая обсерватория Гершеля.[92]
Другое использование
Электрокерамика
Литий ниобат, который является сегнетоэлектрик, широко используется в мобильных телефонах и оптические модуляторы, и для изготовления поверхностная акустическая волна устройств. Он принадлежит к ABO3 структура сегнетоэлектриков типа танталат лития и титанат бария.[93] Конденсаторы ниобиевые доступны как альтернатива танталовые конденсаторы,[94] но танталовые конденсаторы по-прежнему преобладают. Ниобий добавляют в стекло для получения более высокой показатель преломления, делая возможным тоньше и легче корректирующие очки.
Гипоаллергенные применения: медицина и украшения.
Ниобий и некоторые сплавы ниобия физиологически инертны и гипоаллергенный. По этой причине ниобий используется в протезировании и имплантатах, таких как кардиостимуляторы.[95] Ниобий, обработанный едкий натр образует пористый слой, который помогает остеоинтеграция.[96]
Как титан, тантал и алюминий, ниобий можно нагревать и анодированный ("химически активный металл анодирование ") для создания широкого спектра радужный цвета для украшений,[97][98] где очень желательны его гипоаллергенные свойства.[99]
Нумизматика

Ниобий используется как драгоценный металл в памятных монетах, часто с серебром или золотом. Например, в Австрии производилась серия серебра и ниобия. евро монеты с 2003 г .; цвет этих монет создается дифракция света тонким слоем анодированного оксида.[100] В 2012 году доступны десять монет с изображением самых разных цветов в центре монеты: синего, зеленого, коричневого, пурпурного, фиолетового или желтого. Еще два примера - австрийские 25 евро 2004 г. Памятная монета 150 лет Земмеринга Альпийской железной дороге,[101] и австрийские 25 евро 2006 года Памятная монета Европейская спутниковая навигация.[102]Австрийский монетный двор с 2004 года выпускал для Латвии аналогичную серию монет.[103]с одним последователем в 2007 году.[104]В 2011 году Королевский монетный двор Канады начал производство монеты за 5 долларов. серебро 925 пробы и ниобиевая монета Луна Охотника[105]в котором ниобий был избирательно окислен, что позволило создать уникальную отделку, в которой нет двух абсолютно одинаковых монет.
Другой
Дуговые уплотнения высокого давления натриевые лампы изготавливаются из ниобия, иногда легированного 1% цирконий; ниобий имеет очень похожий коэффициент теплового расширения, соответствующий спеченный глинозем дуговая трубка керамика, полупрозрачный материал, устойчивый к химическому воздействию или снижение горячим жидким натрием и парами натрия, содержащимися внутри операционной лампы.[106][107][108]
Ниобий используется в дуговая сварка стержни для некоторых стабилизированных марок нержавеющей стали[109] и в анодах для систем катодной защиты на некоторых резервуарах для воды, которые затем обычно покрываются платиной.[110][111]
Ниобий является важным компонентом высокоэффективных гетерогенных катализаторов производства акриловой кислоты путем селективного окисления пропана.[112][113][114][115]
Ниобий используется для изготовления высоковольтного провода солнечная корона модуль рецептора частиц Солнечный зонд Parker.[116]
Меры предосторожности
| Опасности | |
|---|---|
| NFPA 704 (огненный алмаз) | |
Ниобий не имеет известной биологической роли. В то время как ниобиевая пыль вызывает раздражение глаз и кожи и потенциально опасна для возгорания, элементарный ниобий в более широком масштабе физиологически инертен (и, следовательно, гипоаллергенен) и безвреден. Он часто используется в ювелирных изделиях и был протестирован для использования в некоторых медицинских имплантатах.[117][118]
Большинство людей редко сталкивается с ниобийсодержащими соединениями, но некоторые из них токсичны и требуют осторожного обращения. Кратковременное и долгосрочное воздействие ниобатов и хлорида ниобия, двух водорастворимых химикатов, было протестировано на крысах. Крысы, получавшие однократную инъекцию пентахлорида ниобия или ниобатов, показывают средняя смертельная доза (LD50) от 10 до 100 мг / кг.[119][120][121] При пероральном приеме токсичность ниже; исследование на крысах дало LD50 через семь дней 940 мг / кг.[119]
Рекомендации
- ^ Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ Г.В. Самсонов, под ред. (1968). «Механические свойства элементов». Справочник физико-химических свойств элементов. Нью-Йорк, США: Пленум МФИ. С. 387–446. Дои:10.1007/978-1-4684-6066-7_7. ISBN 978-1-4684-6066-7. Архивировано из оригинал 2 апреля 2015 г.
- ^ Кнапп, Брайан (2002). Франций в полоний. Издательская компания Атлантическая Европа, стр. 40. ISBN 0717256774.
- ^ Хэтчетт, Чарльз (1802). «Анализ минерального вещества из Северной Америки, содержащего до сих пор неизвестный металл». Философские труды Лондонского королевского общества. 92: 49–66. Дои:10.1098 / rspl.1800.0045. JSTOR 107114.
- ^ а б Хэтчетт, Чарльз (1802), «Краткое описание свойств и привычек металлического вещества, недавно обнаруженного Чарльзом Хэтчеттом, эсквайром, и им названным Columbium», Журнал естественной философии, химии и искусств, I (январь): 32–34.
- ^ Хэтчетт, Чарльз (1802). "Eigenschaften und chemisches Verhalten des von Charles Hatchett entdeckten neuen Metalls, Columbium" [Свойства и химическое поведение нового металла, колумбия, (который был) открыт Чарльзом Хэтчеттом]. Annalen der Physik (на немецком). 11 (5): 120–122. Bibcode:1802AnP .... 11..120H. Дои:10.1002 / andp.18020110507.
- ^ а б Нойес, Уильям Альберт (1918). Учебник химии. H. Holt & Co. стр. 523.
- ^ Персиваль, Джеймс (январь 1853 г.). «Мидлтаун Серебряные и Свинцовые рудники». Журнал операций по добыче серебра и свинца. 1: 186. Получено 24 апреля 2013.
- ^ Гриффит, Уильям П .; Моррис, Питер Дж. Т. (2003). "Чарльз Хэтчетт FRS (1765–1847), химик и первооткрыватель ниобия". Примечания и отчеты Лондонского королевского общества. 57 (3): 299–316. Дои:10.1098 / RSNR.2003.0216. JSTOR 3557720. S2CID 144857368.
- ^ а б Волластон, Уильям Хайд (1809). «О тождестве колумбия и тантала». Философские труды Королевского общества. 99: 246–252. Дои:10.1098 / рстл.1809.0017. JSTOR 107264. S2CID 110567235.
- ^ Роза, Генрих (1844). "Ueber die Zusammensetzung der Tantalite und ein im Tantalite von Baiern enthaltenes neues Metall". Annalen der Physik (на немецком). 139 (10): 317–341. Bibcode:1844AnP ... 139..317R. Дои:10.1002 / andp.18441391006.
- ^ Роза, Генрих (1847). "Ueber die Säure im Columbit von Nordamérika". Annalen der Physik (на немецком). 146 (4): 572–577. Bibcode:1847AnP ... 146..572R. Дои:10.1002 / andp.18471460410.
- ^ Кобелл, В. (1860). "Ueber eine eigenthümliche Säure, Diansäure, in der Gruppe der Tantal- und Niob- verbindungen". Journal für Praktische Chemie. 79 (1): 291–303. Дои:10.1002 / prac.18600790145.
- ^ а б c Мариньяк, Бломстранд; Deville, H .; Troost, L .; Германн, Р. (1866). "Tantalsäure, Niobsäure, (Ilmensäure) und Titansäure". Журнал аналитической химии Фрезениуса. 5 (1): 384–389. Дои:10.1007 / BF01302537. S2CID 97246260.
- ^ а б c d е Gupta, C.K .; Сури, А. К. (1994). Добывающая металлургия ниобия. CRC Press. С. 1–16. ISBN 978-0-8493-6071-8.
- ^ Мариньяк, М. (1866). "Исследования по комбинезонам ниобия". Анналы химии и тела (На французском). 4 (8): 7–75.
- ^ Германн, Р. (1871). "Fortgesetzte Untersuchungen über die Verbindungen von Ilmenium und Niobium, sowie über die Zusammensetzung der Niobmineralien (Дальнейшие исследования соединений ильмения и ниобия, а также состава минералов ниобия)". Journal für Praktische Chemie (на немецком). 3 (1): 373–427. Дои:10.1002 / prac.18710030137.
- ^ «Ниобий». Universidade de Coimbra. Архивировано из оригинал 10 декабря 2007 г.. Получено 5 сентября 2008.
- ^ Geballe и другие. (1993) дает критическую точку при токах 150килоамперы и магнитные поля 8,8тесла.
- ^ а б Гебалле, Теодор Х. (октябрь 1993 г.). «Сверхпроводимость: от физики к технике». Физика сегодня. 46 (10): 52–56. Bibcode:1993ФТ .... 46ж..52Г. Дои:10.1063/1.881384.
- ^ Matthias, B.T .; Geballe, T. H .; Геллер, С .; Коренцвит, Э. (1954). «Сверхпроводимость Nb3Sn ». Физический обзор. 95 (6): 1435. Bibcode:1954ПхРв ... 95.1435М. Дои:10.1103 / PhysRev.95.1435.
- ^ Корёши, Ф. (1939). «Реакция тантала, колумбия и ванадия с йодом». Журнал Американского химического общества. 61 (4): 838–843. Дои:10.1021 / ja01873a018.
- ^ Николсон, Уильям, изд. (1809), Британская энциклопедия: или, Словарь искусств и наук, содержащий точный и популярный взгляд на нынешнее улучшенное состояние человеческих знаний, 2, Лонгман, Херст, Рис и Орм, п. 284.
- ^ Ikenberry, L .; Martin, J. L .; Бойер, У. Дж. (1953). «Фотометрическое определение колумбия, вольфрама и тантала в нержавеющих сталях». Аналитическая химия. 25 (9): 1340–1344. Дои:10.1021 / ac60081a011.
- ^ а б c Рейнер-Кэнхэм, Джефф; Чжэн, Чжэн (2008). «Называя элементы в честь ученых: отчет о противоречии». Основы химии. 10 (1): 13–18. Дои:10.1007 / s10698-007-9042-1. S2CID 96082444.
- ^ Кларк, Ф. В. (1914). «Колумбий против ниобия». Наука. 39 (995): 139–140. Bibcode:1914Sci .... 39..139C. Дои:10.1126 / science.39.995.139. JSTOR 1640945. PMID 17780662.
- ^ а б c d е Патель, Ж .; Хулька К. (2001). «Ниобий для сталеплавильного производства». Металлург. 45 (11–12): 477–480. Дои:10.1023 / А: 1014897029026. S2CID 137569464.
- ^ Норман Н., Гринвуд (2003). «Ванадий к дубнию: от путаницы через ясность к сложности». Катализ сегодня. 78 (1–4): 5–11. Дои:10.1016 / S0920-5861 (02) 00318-8.
- ^ «ASTM A572 / A572M-18, Стандартные технические условия для высокопрочной низколегированной конструкционной стали колумбий-ванадий». ASTM International, Западный Коншохокен. 2018 г.. Получено 12 февраля 2020.
- ^ Боллинджер, Р. К .; White, B.D .; Neumeier, J. J .; Sandim, H. R. Z .; Suzuki, Y .; душ Сантуш, К. А. М .; Avci, R .; Migliori, A .; Беттс, Дж. Б. (2011). «Наблюдение мартенситного структурного искажения в V, Nb и Ta». Письма с физическими проверками. 107 (7): 075503. Bibcode:2011ПхРвЛ.107г5503Б. Дои:10.1103 / PhysRevLett.107.075503. PMID 21902404.
- ^ а б Пейнигер, М .; Пиль, Х. (1985). "Сверхпроводящий Nb3Многоклеточная ускоряющая полость, покрытая Sn ". IEEE Transactions по ядерной науке. 32 (5): 3610–3612. Bibcode:1985ITNS ... 32.3610P. Дои:10.1109 / TNS.1985.4334443. S2CID 23988671.
- ^ Salles Moura, Hernane R .; Луремхо де Моура, Луремхо (2007). «Плавление и очистка ниобия». Материалы конференции AIP. 927 (927): 165–178. Bibcode:2007AIPC..927..165M. Дои:10.1063/1.2770689.
- ^ а б c d е ж грамм час Новак, Изабела; Зиолек, Мария (1999). «Соединения ниобия: получение, характеристика и применение в гетерогенном катализе». Химические обзоры. 99 (12): 3603–3624. Дои:10.1021 / cr9800208. PMID 11849031.
- ^ Jahnke, L.P .; Frank, R.G .; Редден, Т. К. (1960). «Сплавы Колумбия сегодня». Металл Прогр. 77 (6): 69–74. OSTI 4183692.
- ^ Никулина, А. В. (2003). «Цирконий-ниобиевые сплавы для основных элементов реакторов с водой под давлением». Металловедение и термическая обработка. 45 (7–8): 287–292. Bibcode:2003МШТ ... 45..287Н. Дои:10.1023 / А: 1027388503837. S2CID 134841512.
- ^ Лиде, Дэвид Р. (2004). "Элементы". CRC Справочник по химии и физике (85-е изд.). CRC Press. стр.4–21. ISBN 978-0-8493-0485-9.
- ^ а б c Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (2003), "ТогдаUBASE оценка ядерных и распадных свойств », Ядерная физика A, 729: 3–128, Bibcode:2003НуФА.729 .... 3А, Дои:10.1016 / j.nuclphysa.2003.11.001
- ^ Эмсли, Джон (2001). «Ниобий». Строительные блоки природы: руководство по элементам от А до Я. Оксфорд, Англия: Издательство Оксфордского университета. стр.283–286. ISBN 978-0-19-850340-8.
- ^ а б c d Суассон, Дональд Дж .; McLafferty, J. J .; Пьер, Джеймс А. (1961). «Отчет о сотрудничестве персонала и промышленности: тантал и ниобий». Промышленная и инженерная химия. 53 (11): 861–868. Дои:10.1021 / ie50623a016.
- ^ "Columbite- (Fe): информация о минералах, данные и местонахождение". www.mindat.org.
- ^ «Танталит- (Fe): информация о минералах, данные и местонахождение». www.mindat.org.
- ^ а б c Берк, Эрнст А.Дж. (2008). «Использование суффиксов в названиях минералов» (PDF). Элементы. 4 (2): 96. Получено 7 декабря 2019.
- ^ а б c «CNMNC». nrmima.nrm.se. Архивировано из оригинал 10 августа 2019 г.. Получено 6 октября 2018.
- ^ «Pyrochlore Group: информация о минералах, данные и местонахождение». www.mindat.org.
- ^ «Фторкальциопирохлор: информация о минералах, данные и местонахождение». www.mindat.org.
- ^ http://rruff.info/uploads/AM62_403.pdf
- ^ «Эвксенит- (Y): Минеральная информация, данные и местонахождение». www.mindat.org.
- ^ Лампкин, Грегори Р .; Юинг, Родни К. (1995). «Геохимические изменения минералов группы пирохлора: подгруппа пирохлора» (PDF). Американский минералог. 80 (7–8): 732–743. Bibcode:1995AmMin..80..732L. Дои:10.2138 / am-1995-7-810.
- ^ а б c Kouptsidis, J .; Peters, F .; Проч, Д .; Певец, В. "Ниоб фюр ТЕСЛА" (PDF) (на немецком). Deutsches Elektronen-Synchrotron DESY. Архивировано из оригинал (PDF) 17 декабря 2008 г.. Получено 2 сентября 2008.
- ^ а б c Альваренга, Дарлан (9 апреля 2013 г.). "'Monopólio 'brasileiro do nióbio gera cobiça mundial, controvérsia e mitos " [Бразильская монополия на ниобий порождает жадность, споры и мифы в мире]. G1 (на португальском). Сан-Паулу. Получено 23 мая 2016.
- ^ Сикейра-Гей, Джулиана; Санчес, Луис Э. (2020). «Держите амазонский ниобий в земле». Экологическая наука и политика. 111: 1–6. Дои:10.1016 / j.envsci.2020.05.012. ISSN 1462-9011.
- ^ "Magris Resources, официальный владелец Niobec" (Пресс-релиз). Ниобек. 23 января 2015 г.. Получено 23 мая 2016.
- ^ а б c d е ж грамм Холлеман, Арнольд Ф .; Виберг, Эгон; Виберг, Нильс (1985). «Ниоб». Lehrbuch der Anorganischen Chemie (на немецком языке) (91–100 изд.). Вальтер де Грюйтер. С. 1075–1079. ISBN 978-3-11-007511-3.
- ^ Tither, Джеффри (2001). Общество минералов, металлов и материалов (ред.). Прогресс на рынках и технологиях ниобия 1981–2001 гг. (PDF). Наука и технология ниобия: Материалы международного симпозиума Niobium 2001 (Орландо, Флорида, США). ISBN 978-0-9712068-0-9. Архивировано из оригинал (PDF) 17 декабря 2008 г.
- ^ Дюфрен, Клод; Гойетт, Гислен (2001). Общество минералов, металлов и материалов (ред.). Производство феррониобия на руднике Ниобек 1981–2001 гг. (PDF). Наука и технология ниобия: Материалы международного симпозиума Niobium 2001 (Орландо, Флорида, США). ISBN 978-0-9712068-0-9. Архивировано из оригинал (PDF) 17 декабря 2008 г.
- ^ а б c Агулянский, Анатолий (2004). Химия фторидных соединений тантала и ниобия.. Эльзевир. С. 1–11. ISBN 978-0-444-51604-6.
- ^ Чоудхури, Алок; Хенгсбергер, Эккарт (1992). «Электронно-лучевая плавка и рафинирование металлов и сплавов». Японский международный институт чугуна и стали. 32 (5): 673–681. Дои:10.2355 / isijinternational.32.673.
- ^ Луччези, Кристан; Куадрос, Алекс (апрель 2013 г.), «Минеральное богатство», Рынки Bloomberg (бумага), стр. 14
- ^ Папп, Джон Ф. «Ниобий (Колумбий)» (PDF). Сводка по товарам USGS за 2006 г.. Получено 20 ноября 2008.
- ^ а б Папп, Джон Ф. «Ниобий (Колумбий)» (PDF). Сводка по товарам USGS 2007. Получено 20 ноября 2008.
- ^ Папп, Джон Ф. «Ниобий (Колумбий)» (PDF). Сводка по товарам USGS 1997. Получено 20 ноября 2008.
- ^ Ниобий (колумбий) Геологическая служба США, сводки по минеральным ресурсам, январь 2011 г.
- ^ Ниобий (колумбий) Геологическая служба США, сводки по минеральным ресурсам, январь 2016 г.
- ^ Каннингем, Ларри Д. (5 апреля 2012 г.). «Информация о минералах USGS: ниобий (колумбий) и тантал». Minerals.usgs.gov. Получено 17 августа 2012.
- ^ Deblonde, Gauthier J. -P .; Чаннес, Александр; Белэр, Сара; Кот, Жерар (1 июля 2015 г.). «Растворимость ниобия (V) и тантала (V) в мягких щелочных условиях». Гидрометаллургия. 156: 99–106. Дои:10.1016 / j.hydromet.2015.05.015. ISSN 0304-386X.
- ^ Найман, май (2 августа 2011 г.). «Химия полиоксониобатов в 21 веке». Dalton Transactions. 40 (32): 8049–8058. Дои:10.1039 / C1DT10435G. ISSN 1477-9234. PMID 21670824.
- ^ Pubchem. «Оксид ниобия | Nb2O5 - ПабХим». pubchem.ncbi.nlm.nih.gov. Получено 29 июн 2016.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Кардарелли, Франсуа (2008). Справочник материалов. Springer London. ISBN 978-1-84628-668-1.
- ^ Rahtu, Antti (2002). Atomic Layer Deposition of High Permittivity Oxides: Film Growth and In Situ Studies (Тезис). Университет Хельсинки. HDL:10138/21065. ISBN 952-10-0646-3.
- ^ Maruyama, Toshiro (1994). "Electrochromic Properties of Niobium Oxide Thin Films Prepared by Chemical Vapor Deposition". Журнал Электрохимического общества. 141 (10): 2868–2871. Дои:10.1149/1.2059247.
- ^ Lucas, C. R.; Labinger, J. A.; Schwartz, J. (1990). Robert J. Angelici (ed.). Dichlorobis(η5-Cyclopentadienyl)Niobium(IV). Неорганические синтезы. 28. Нью-Йорк. pp. 267–270. Дои:10.1002/9780470132593.ch68. ISBN 978-0-471-52619-3.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Verevkin, A.; Перлман, А .; Slstrokysz, W.; Zhang, J .; и другие. (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Журнал современной оптики. 51 (12): 1447–1458. Дои:10.1080/09500340410001670866.
- ^ а б Papp, John F. "Niobium (Columbium ) and Tantalum" (PDF). USGS 2006 Minerals Yearbook. Получено 3 сентября 2008.
- ^ а б Heisterkamp, Friedrich; Carneiro, Tadeu (2001). Minerals, Metals and Materials Society (ed.). Niobium: Future Possibilities – Technology and the Market Place (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). ISBN 978-0-9712068-0-9. Архивировано из оригинал (PDF) 17 декабря 2008 г.
- ^ "Datasheet CPM S110V" (PDF). Crucible Industries LLC. Получено 20 ноября 2017.
- ^ Eggert, Peter; Priem, Joachim; Wettig, Eberhard (1982). "Niobium: a steel additive with a future". Economic Bulletin. 19 (9): 8–11. Дои:10.1007/BF02227064. S2CID 153775645.
- ^ Hillenbrand, Hans-Georg; Gräf, Michael; Kalwa, Christoph (2 May 2001). "Development and Production of High Strength Pipeline Steels" (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Архивировано из оригинал (PDF) 5 июня 2015 г.
- ^ Donachie, Matthew J. (2002). Superalloys: A Technical Guide. ASM International. стр.29 –30. ISBN 978-0-87170-749-9.
- ^ Bhadeshia, H. k. d. час "Nickel Based Superalloys". Кембриджский университет. Архивировано из оригинал 25 августа 2006 г.. Получено 4 сентября 2008.
- ^ Pottlacher, G.; Hosaeus, H.; Wilthan, B.; Kaschnitz, E.; Seifter, A. (2002). "Thermophysikalische Eigenschaften von festem und flüssigem Inconel 718". Thermochimica Acta (на немецком). 382 (1––2): 55–267. Дои:10.1016/S0040-6031(01)00751-1.
- ^ а б c Hebda, John (2 May 2001). "Niobium alloys and high Temperature Applications" (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Архивировано из оригинал (PDF) 17 декабря 2008 г.
- ^ Dinardi, Aaron; Capozzoli, Peter; Shotwell, Gwynne (2008). Low-cost Launch Opportunities Provided by the Falcon Family of Launch Vehicles (PDF). Fourth Asian Space Conference. Тайбэй. Архивировано из оригинал (PDF) 15 марта 2012 г.
- ^ Lindenhovius, J.L.H.; Hornsveld, E. M.; Den Ouden, A.; Wessel, W. A. J.; и другие. (2000). "Powder-in-tube (PIT) Nb/sub 3/Sn conductors for high-field magnets". IEEE Transactions on Applied Superconductivity. 10 (1): 975–978. Bibcode:2000ITAS...10..975L. Дои:10.1109/77.828394. S2CID 26260700.
- ^ Nave, Carl R. "Superconducting Magnets". Georgia State University, Department of Physics and Astronomy. Получено 25 ноября 2008.
- ^ Glowacki, B. A.; Yan, X. -Y.; Fray, D.; Chen, G .; Majoros, M.; Shi, Y. (2002). "Niobium based intermetallics as a source of high-current/high magnetic field superconductors". Physica C: сверхпроводимость. 372–376 (3): 1315–1320. arXiv:cond-mat/0109088. Bibcode:2002PhyC..372.1315G. Дои:10.1016/S0921-4534(02)01018-3. S2CID 118990555.
- ^ Grunblatt, G.; Mocaer, P.; Verwaerde Ch.; Kohler, C. (2005). "A success story: LHC cable production at ALSTOM-MSA". Fusion Engineering and Design (Proceedings of the 23rd Symposium of Fusion Technology). 75–79 (2): 3516. Bibcode:2005ITAS...15.3516M. Дои:10.1016/j.fusengdes.2005.06.216. S2CID 41810761.
- ^ Lilje, L.; Kako, E.; Kostin, D.; Matheisen, A.; и другие. (2004). "Achievement of 35 MV/m in the superconducting nine-cell cavities for TESLA". Ядерные инструменты и методы в физических исследованиях Секция A: ускорители, спектрометры, детекторы и связанное с ними оборудование. 524 (1–3): 1–12. arXiv:physics/0401141. Bibcode:2004NIMPA.524....1L. Дои:10.1016/j.nima.2004.01.045. S2CID 2141809.
- ^ The International Linear Collider Technical Design Report 2013. International Linear Collider. 2013. Получено 15 августа 2015.
- ^ "ILC-type cryomodule makes the grade". ЦЕРН Курьер. IOP Publishing. 27 ноября 2014 г.. Получено 15 августа 2015.
- ^ Cherednichenko, Sergey; Drakinskiy, Vladimir; Berg, Therese; Khosropanah, Pourya; и другие. (2008). "A Hot-electron bolometer terahertz mixers for the Herschel Space Observatory". Обзор научных инструментов. 79 (3): 0345011–03451010. Bibcode:2008RScI...79c4501C. Дои:10.1063/1.2890099. PMID 18377032.
- ^ Volk, Tatyana; Wohlecke, Manfred (2008). Lithium Niobate: Defects, Photorefraction and Ferroelectric Switching. Springer. стр.1 –9. ISBN 978-3-540-70765-3.
- ^ Pozdeev, Y. (1991). "Reliability comparison of tantalum and niobium solid electrolytic capacitors". Quality and Reliability Engineering International. 14 (2): 79–82. Дои:10.1002/(SICI)1099-1638(199803/04)14:2<79::AID-QRE163>3.0.CO;2-Y.
- ^ Mallela, Venkateswara Sarma; Ilankumaran, V.; Srinivasa Rao, N. (1 January 2004). "Trends in Cardiac Pacemaker Batteries". Indian Pacing Electrophysiol J. 4 (4): 201–212. ЧВК 1502062. PMID 16943934.
- ^ Godley, Reut; Starosvetsky, David; Gotman, Irena (2004). "Bonelike apatite formation on niobium metal treated in aqueous NaOH". Журнал материаловедения: материалы в медицине. 15 (10): 1073–1077. Дои:10.1023/B:JMSM.0000046388.07961.81. PMID 15516867. S2CID 44988090.
- ^ Biason Gomes, M. A.; Onofre, S.; Juanto, S.; Bulhões, L. O. de S. (1991). "Anodization of niobium in sulphuric acid media". Journal of Applied Electrochemistry. 21 (11): 1023–1026. Дои:10.1007/BF01077589. S2CID 95285286.
- ^ Chiou, Y. L. (1971). "A note on the thicknesses of anodized niobium oxide films". Тонкие твердые пленки. 8 (4): R37–R39. Bibcode:1971TSF.....8R..37C. Дои:10.1016/0040-6090(71)90027-7.
- ^ Azevedo, C. R. F.; Spera, G.; Silva, A. P. (2002). "Characterization of metallic piercings that caused adverse reactions during use". Journal of Failure Analysis and Prevention. 2 (4): 47–53. Дои:10.1361/152981502770351860.
- ^ Grill, Robert; Gnadenberge, Alfred (2006). "Niobium as mint metal: Production–properties–processing". International Journal of Refractory Metals and Hard Materials. 24 (4): 275–282. Дои:10.1016/j.ijrmhm.2005.10.008.
- ^ "25 Euro – 150 Years Semmering Alpine Railway (2004)". Austrian Mint. Архивировано из оригинал 21 июля 2011 г.. Получено 4 ноября 2008.
- ^ "150 Jahre Semmeringbahn" (на немецком). Austrian Mint. Архивировано из оригинал 20 июля 2011 г.. Получено 4 сентября 2008.
- ^ "Neraža – mēs nevarējām atrast meklēto lapu!" (на латышском языке). Банк Латвии. Архивировано из оригинал 9 января 2008 г.. Получено 19 сентября 2008.
- ^ "Neraža – mēs nevarējām atrast meklēto lapu!" (на латышском языке). Банк Латвии. Архивировано из оригинал 22 мая 2009 г.. Получено 19 сентября 2008.
- ^ "$5 Sterling Silver and Niobium Coin – Hunter's Moon (2011)". Королевский канадский монетный двор. Получено 1 февраля 2012.
- ^ Henderson, Stanley Thomas; Marsden, Alfred Michael; Hewitt, Harry (1972). Лампы и Освещение. Edward Arnold Press. С. 244–245. ISBN 978-0-7131-3267-0.
- ^ Eichelbrönner, G. (1998). "Refractory metals: crucial components for light sources". International Journal of Refractory Metals and Hard Materials. 16 (1): 5–11. Дои:10.1016/S0263-4368(98)00009-2.
- ^ Michaluk, Christopher A.; Huber, Louis E.; Ford, Robert B. (2001). Minerals, Metals and Materials Society (ed.). Niobium and Niobium 1% Zirconium for High Pressure Sodium (HPS) Discharge Lamps. Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). ISBN 978-0-9712068-0-9.
- ^ US patent 5254836, Okada, Yuuji; Kobayashi, Toshihiko; Sasabe, Hiroshi; Aoki, Yoshimitsu; Nishizawa, Makoto; Endo, Shunji, "Method of arc welding with a ferrite stainless steel welding rod", issued 19 October 1993
- ^ Moavenzadeh, Fred (14 March 1990). Concise Encyclopedia of Building and Construction Materials. MIT Press. С. 157–. ISBN 978-0-262-13248-0. Получено 18 февраля 2012.
- ^ Cardarelli, François (9 January 2008). Materials handbook: a concise desktop reference. Springer. С. 352–. ISBN 978-1-84628-668-1. Получено 18 февраля 2012.
- ^ Hävecker, Michael; Wrabetz, Sabine; Kröhnert, Jutta; Csepei, Lenard-Istvan; Naumann d'Alnoncourt, Raoul; Kolen'Ko, Yury V; Girgsdies, Frank; Schlögl, Robert; Trunschke, Annette (2012). "Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid" (PDF). Журнал катализа. 285: 48–60. Дои:10.1016/j.jcat.2011.09.012. HDL:11858/00-001M-0000-0012-1BEB-F.
- ^ Amakawa, Kazuhiko; Kolen'Ko, Yury V; Villa, Alberto; Schuster, Manfred E/; Csepei, Lénárd-István; Weinberg, Gisela; Wrabetz, Sabine; Naumann d'Alnoncourt, Raoul; Girgsdies, Frank; Prati, Laura; Schlögl, Robert; Trunschke, Annette (2013). "Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol". Катализ ACS. 3 (6): 1103. Дои:10.1021/cs400010q. HDL:11858/00-001M-0000-000E-FA39-1.
- ^ Csepei, Lénárd-István (2011). Kinetic studies of propane oxidation on Mo and V based mixed oxide catalysts. Technische Universität Berlin. pp. 157–166. Дои:10.14279/depositonce-2972.
- ^ Naumann d'Alnoncourt, Raoul; Csepei, Lénárd-István; Hävecker, Michael; Girgsdies, Frank; Schuster, Manfred E; Schlögl, Robert; Trunschke, Annette (2014). «Реакционная сеть при окислении пропана на фазово-чистых оксидных катализаторах MoVTeNb M1» (PDF). Журнал катализа. 311: 369–385. Дои:10.1016/j.jcat.2013.12.008. HDL:11858/00-001M-0000-0014-F434-5.
- ^ Dr. Tony Case (24 August 2018). Scientist Interview: Dr. Tony Case (Parker Solar Probe). Получено 24 августа 2018.
- ^ Vilaplana, J.; Romaguera, C.; Grimalt, F.; Cornellana, F. (1990). "New trends in the use of metals in jewellery". Контактный дерматит. 25 (3): 145–148. Дои:10.1111/j.1600-0536.1991.tb01819.x. PMID 1782765. S2CID 30201028.
- ^ Vilaplana, J.; Romaguera, C. (1998). "New developments in jewellery and dental materials". Контактный дерматит. 39 (2): 55–57. Дои:10.1111/j.1600-0536.1998.tb05832.x. PMID 9746182. S2CID 34271011.
- ^ а б Haley, Thomas J.; Komesu, N.; Raymond, K. (1962). "Pharmacology and toxicology of niobium chloride". Токсикология и прикладная фармакология. 4 (3): 385–392. Дои:10.1016/0041-008X(62)90048-0. PMID 13903824.
- ^ Downs, William L.; Scott, James K.; Yuile, Charles L.; Caruso, Frank S.; и другие. (1965). "The Toxicity of Niobium Salts". American Industrial Hygiene Association Journal. 26 (4): 337–346. Дои:10.1080/00028896509342740. PMID 5854670.
- ^ Schroeder, Henry A.; Mitchener, Marian; Nason, Alexis P. (1970). "Zirconium, Niobium, Antimony, Vanadium and Lead in Rats: Life term studies". Журнал питания. 100 (1): 59–68. Дои:10.1093/jn/100.1.59. PMID 5412131.
внешняя ссылка
- Los Alamos National Laboratory – Niobium
- Tantalum-Niobium International Study Center
- Niobium for particle accelerators eg ILC. 2005 г.
- . Британская энциклопедия (11-е изд.). 1911 г.
- Гилман, Д.С.; Peck, H.T .; Колби, Ф. М., ред. (1905). . Новая международная энциклопедия (1-е изд.). Нью-Йорк: Додд, Мид.
- Ниобий в Периодическая таблица видео (Ноттингемский университет)

