Стандартный атомный вес - Standard atomic weight
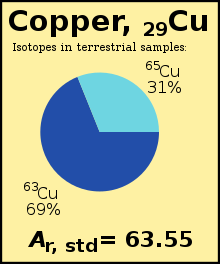
В стандартный атомный вес (Аr, стандарт(E)) химический элемент это взвешенное среднее арифметическое из относительные изотопные массы из всех изотопы этого элемента взвешенный по содержанию каждого изотопа на Земля. Например, изотоп 63Cu (Ар = 62,929) составляет 69% медь на Земле, остальные 65Cu (Ар = 64,927), поэтому
Поскольку относительные массы изотопов равны безразмерные величины, это средневзвешенное значение также безразмерно. Его можно преобразовать в меру массы (с измерение M), умножив его на Далтон, также известная как постоянная атомной массы.
Среди различных вариантов понятия атомный вес (Ар, также известен как относительная атомная масса ), используемый учеными, стандартный атомный вес (Аr, стандарт) является наиболее распространенным и практичным. Стандартный атомный вес каждого химического элемента определяется и публикуется Комиссия по изотопному содержанию и атомным весам (CIAAW) Международный союз теоретической и прикладной химии (IUPAC) на основе натуральных, стабильных, земной источники элемента. В определении указывается использование образцов из многих репрезентативных источников с Земли, так что это значение может широко использоваться как «атомный вес» для веществ, встречающихся в реальности, например, в фармацевтике и научных исследованиях. Нестандартизированные атомные веса элемента зависят от источников и образцов, например атомный вес углерода в конкретной кости из определенного археологического памятника. Стандартный атомный вес усредняет такие значения до диапазон атомных весов что химик мог бы ожидать получить из множества случайных образцов с Земли. Этот диапазон является основанием для обозначение интервала даны для некоторых стандартных значений атомной массы.
Из 118 известных химических элементов 80 имеют стабильные изотопы, а 84 имеют значение, основанное на земной среде. Обычно таким значением является, например, гелий: Аr, стандарт(Он) = 4.002602(2). «(2)» указывает на погрешность последней показанной цифры, чтобы читать 4.002602±0.000002. ИЮПАК также издает сокращенные значения, округленное до пяти значащих цифр. Для гелия Аr, сокращенный(Он) = 4.0026.
Для тринадцати элементов образцы расходятся по этому значению, потому что их источники образцов имели разную историю распада. Например, таллий (Tl) в осадочных породах имеет другой изотопный состав, чем в магматических породах и вулканических газах. Для этих элементов стандартный атомный вес обозначается интервалом: Аr, стандарт(Tl) = [204.38, 204.39]. С таким интервалом для менее сложных ситуаций IUPAC также публикует условное значение. Для таллия Аr, обычный(Tl) = 204.38.
Определение

В стандарт атомный вес - это особое значение относительной атомной массы. Он определяется как «рекомендуемые значения» относительных атомных масс источников. в местной среде земной коры и атмосфера как определено ИЮПАК Комиссия по атомным весам и изотопному содержанию (CIAAW).[2] В общем, значения из разных источников подвержены естественным колебаниям из-за разной радиоактивной истории источников. Таким образом, стандартные атомные веса - это ожидаемые значения атомных весов из ряда образцов или источников. Ограничивая источники только земным происхождением, значения, определенные CIAAW, имеют меньшую дисперсию и являются более точным значением для относительных атомных масс (атомных масс), фактически обнаруженных и используемых в мирских материалах.
В Ценности, опубликованные CIAAW используются, а иногда и требуются по закону при массовых расчетах. Значения имеют неопределенность (указано в скобках) или являются интервалом ожидания (см. Пример на иллюстрации непосредственно выше). Эта неопределенность отражает естественную изменчивость изотопного распределения для элемента, а не неопределенность измерения (которая намного меньше для качественных приборов).[3]
Хотя существует попытка охватить диапазон изменчивости на Земле стандартными значениями атомного веса, известны случаи, когда образцы минералов содержат элементы с атомным весом, который отличается от стандартного диапазона атомного веса.[2]
Для синтетические элементы образующийся изотоп зависит от средств синтеза, поэтому понятие естественного изотопного содержания не имеет значения. Следовательно, для синтетических элементов полное число нуклонов[сомнительный ] наиболее стабильного изотопа (т.е.изотопа с наибольшим периодом полураспада) указан в скобках вместо стандартного атомного веса.
Когда термин «атомный вес» используется в химии, обычно подразумевается более конкретный стандартный атомный вес. Это стандартные атомные веса, которые используются в периодических таблицах и во многих стандартных справочниках по обычной химии Земли.
Литий представляет собой уникальный случай, когда в некоторых случаях было обнаружено, что естественное содержание изотопов было нарушено деятельностью человека по разделению изотопов до такой степени, что это повлияло на неопределенность его стандартного атомного веса, даже в образцах, полученных из природных источников, таких как реки .[нужна цитата ][сомнительный ]
Наземное определение
Примером того, почему при указании стандартных значений атомной массы необходимо указать «обычные земные источники», является элемент аргон. Солнечная система атомный вес аргона варьируется до 10% из-за крайних различий в изотопном составе. Если основным источником аргона является распад 40
K в скалах, 40
Ar будет доминирующим изотопом. К таким локациям относятся планеты Меркурий и Марс, а также луна Титан. На Земле соотношение трех изотопов 36Ar:38Ar:40Ar примерно 5: 1: 1600, что дает земному аргону стандартный атомный вес 39,948 (1).
Однако в остальной вселенной дело обстоит иначе. Аргон производится напрямую звездный нуклеосинтез, преобладают альфа-процесс нуклид 36
Ar. Соответственно в солнечном аргоне содержится 84,6% 36
Ar (согласно с Солнечный ветер измерения),[4] и соотношение трех изотопов 36Ar:38Ar:40Ar в атмосферах внешних планет составляет 8400: 1600: 1.[5] Таким образом, атомный вес аргона на Солнце и в большей части Вселенной будет примерно 36,3.[6]
Причины неопределенности на Земле
Как известно, опубликованное значение атомной массы сопровождается неопределенностью. Эта неопределенность (и связанная с ней точность) следует из ее определения, поскольку источник является «наземным и стабильным». Систематические причины неопределенности:
- Пределы измерений. Как всегда, физическое измерение никогда не бывает конечным. Всегда есть больше подробностей, которые можно найти и прочитать. Это относится ко всем не замужем, чистый изотоп обнаружен. Например, сегодня масса основного природного изотопа фтора (фтор-19 ) можно измерить с точностью до одиннадцати знаков после запятой: 18.998403163(6). Но может появиться еще более точная система измерения, дающая больше десятичных знаков.
- Несовершенные смеси изотопов. В отобранных и измеренных образцах смешивание (относительное содержание) этих изотопов может варьироваться. Например медь. В то время как в общем два его изотопа составляют 69,15% и 30,85% каждый от всей найденной меди, естественной образец при измерении могло быть неполное «перемешивание», поэтому процентные значения отличаются. Разумеется, точность улучшается за счет измерения большего количества образцов, но остается эта причина неопределенности. (Пример: образцы свинца настолько разнятся, что точнее четырех цифр не подобрать: 207.2)
- Земные источники с разной историей. А источник - это большая исследуемая область, например, «вода океана» или «вулканическая порода» (в отличие от «образца»: единственная куча исследуемого материала). Похоже, что некоторые элементы имеют разные изотопная смесь на источник. Например, таллий в вулканической породе имеет больше легких изотопов, а в осадочной породе - больше тяжелых изотопов. Нет среднего земного числа. Эти элементы показывают обозначение интервала: Аr, стандарт(Tl) = [204.38, 204.39]. Из практических соображений публикуется также упрощенный «условный» номер (для Tl: 204,38).
Эти три неопределенности суммируются. Опубликованное значение является результатом всего этого.
Определение относительной атомной массы
Современные относительные атомные массы (термин, характерный для данного образца элемента) рассчитываются на основе измеренных значений атомной массы (для каждого нуклида) и изотопный состав образца. Доступны высокоточные атомные массы.[7][8] практически для всех нерадиоактивных нуклидов, но изотопные составы труднее измерить с высокой точностью и более подвержены различиям между образцами.[9][10] По этой причине относительные атомные массы 22 мононуклидные элементы (которые равны изотопным массам для каждого из отдельных встречающихся в природе нуклидов этих элементов) известны с особенно высокой точностью. Например, существует неопределенность только в одну часть из 38 миллионов для относительной атомной массы фтор, точность, превышающая текущее наилучшее значение для Константа Авогадро (одна часть на 20 миллионов).
| Изотоп | Атомная масса[8] | Изобилие[9] | |
|---|---|---|---|
| Стандарт | Ассортимент | ||
| 28Si | 27.976 926 532 46(194) | 92.2297(7)% | 92.21–92.25% |
| 29Si | 28.976 494 700(22) | 4.6832(5)% | 4.67–4.69% |
| 30Si | 29.973 770 171(32) | 3.0872(5)% | 3.08–3.10% |
Расчет приведен на примере кремний, относительная атомная масса которого особенно важна в метрология. Кремний существует в природе как смесь трех изотопов: 28Si, 29Si и 30Si. Атомные массы этих нуклидов известны с точностью до одной части на 14 миллиардов для 28Si и примерно одну миллиардную долю для остальных. Однако диапазон природное изобилие для изотопов такова, что стандартное содержание может составлять не более ± 0,001% (см. таблицу).
- Ар(Si) = (27,97693 × 0,922297) + (28,97649 × 0,046832) + (29,97377 × 0,030872) = 28,0854
Оценка неуверенность это сложно,[11] особенно как распределение выборки не обязательно симметрично: ИЮПАК стандартные относительные атомные массы указаны с расчетными симметричными погрешностями,[12] а для кремния - 28,0855 (3). Относительная стандартная неопределенность этого значения составляет 1×10–5 или 10 частей на миллион. Чтобы еще больше отразить эту естественную изменчивость, в 2010 году ИЮПАК принял решение перечислить относительные атомные массы 10 элементов как интервал, а не фиксированное число.[13]
Споры по именованию
Использование названия «атомный вес» вызвало много споров среди ученых.[14] Противники названия обычно предпочитают термин «относительная атомная масса» (не путать с атомная масса ). Основное возражение состоит в том, что атомный вес не является вес, это сила воздействовал на объект в гравитационное поле, измеряется в единицах силы, таких как ньютон или фунтал.
В ответ сторонники термина «атомный вес» указывают (среди прочих аргументов)[14] это
- название постоянно использовалось для одного и того же количества с тех пор, как оно было впервые сформулировано в 1808 году;[15]
- большую часть этого времени атомный вес действительно измерялся взвешиванием (то есть гравиметрический анализ ) и название физической величины не должно меняться просто потому, что изменился метод ее определения;
- термин «относительная атомная масса» следует зарезервировать для массы конкретного нуклид (или изотоп ), а "атомный вес"использоваться для взвешенный значить атомных масс по всем атомам в образце;
- нередко встречаются вводящие в заблуждение названия физических величин, которые сохраняются по историческим причинам, например,
- электродвижущая сила, что не является силой
- разрешающая способность, что не является мощность количество
- молярная концентрация, которое не является молярным количеством (количеством, выраженным на единицу количества вещества).
Можно добавить, что атомный вес часто не является действительно «атомным», поскольку он не соответствует свойству какого-либо отдельного атома. Тот же аргумент можно было бы привести против «относительной атомной массы», используемой в этом смысле.
Опубликованные значения
ИЮПАК публикует одно формальное значение для каждого стабильного элемента, называемое стандартный атомный вес.[16][17] Любые обновления публикуются два раза в год (в разные годы). В 2015 году был обновлен атомный вес иттербия.[16] За 2017 год было изменено 14 атомных весов, в том числе изменение аргона с однозначного на интервальное.[18][19]
Опубликованное значение может иметь неопределенность, как для неона: 20.1797(6), или может быть интервалом, как для бора: [10.806, 10.821].
Наряду с этими 84 значениями IUPAC также публикует сокращенный значения (только до пяти цифр на номер), а для двенадцати значений интервала обычный значения (однозначные значения).
Символ Ар относительная атомная масса, например, для определенного образца. Чтобы быть конкретным, стандартный атомный вес можно обозначить как Аr, стандарт(E), где (E) - символ элемента.
Сокращенный атомный вес
В сокращенный атомный вес, также опубликованный CIAAW, выводится из стандартного атомного веса, уменьшающего числа до пяти цифр (пяти значащих цифр). В названии не сказано «округлый».
Границы интервалов закруглены вниз для первой (самой нижней) границы и снизу вверх для вверх (верхняя) граница. Таким образом, полностью покрывается более точный исходный интервал.[20]
Примеры:
- Кальций: Аr, стандарт(Са) = 40,078 (4) → Аr, сокращенный(Са) = 40,078
- Гелий: Аr, стандарт(Он) = 4,002602 (2) → Аr, сокращенный(Он) = 4,0026
- Водород: Аr, стандарт(H) = [1,00784, 1,00811] → Аr, сокращенный(H) = [1,0078, 1,0082]
Условный атомный вес
Тринадцать химических элементов имеют стандартный атомный вес, который определяется не как одно число, а как интервал. Например, водород имеет Аr, стандарт(H) = [1,00 784, 1,00811]. Это обозначение указывает на то, что различные источники на Земле имеют существенно разные изотопные составы, и неопределенности включены в два числа. Для этих элементов не существует «среднего для Земли» строения, и «правильное» значение не является его средним (это будет 1,007975 для водорода с погрешностью (± 0,000135), которая заставит его просто покрыть интервал). Однако для ситуаций, когда приемлемо менее точное значение, CIAAW опубликовал однозначный условный атомный вес которые можно использовать например в торговле. Для водорода Аr, обычный(H) = 1,008. Тринадцать элементов: водород, литий, бор, углерод, азот, кислород, магний, кремний, сера, хлор, аргон, бром и таллий.[21]
Формальный короткий атомный вес
Используя сокращенное значение и обычное значение для тринадцати значений интервалов, можно дать короткое значение, определенное IUPAC (5 цифр плюс неопределенность), для всех стабильных элементов. Во многих ситуациях и в периодических таблицах это может быть достаточно подробно.[22]
Обзор: формальные ценности стандартный атомный вес[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Элемент (E) | Аr, стандарт(E) Таблица 1[17] | Тип значения | Аr, стандартное сокращенное(E) Таблица 2[20] | Аr, стандартное стандартное(E) Таблица 3[21] | Аr, стандартное формальное короткое(E) Таблицы 2 и 3[22] | Массовое число [самый стабильный изотоп] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| водород | 1ЧАС | [1.00784, 1.00811] | Интервал | [1.0078, 1.0082] | 1.008 | 1.008 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| азот | 7N | [14.00643, 14.00728] | Интервал | [14.006, 14.008] | 14.007 | 14.007 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| фтор | 9F | 18.998403163(6) | Значение (неопределенность) | 18.998 | 18.998 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| кальций | 20Ca | 40.078(4) | Значение (неопределенность) | 40.078(4) | 40.078(4) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| технеций | 43Tc | (никто) | Самый стабильный изотоп | [97] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Список атомных весов
Стандартный атомный вес элементов (ИЮПАК 2009–2017 гг.[ссылка 1]) | |||||||
|---|---|---|---|---|---|---|---|
| Z | Символ | имя | Аr, стандарт | сокращенный | обычный | → формальный, короткий | год изменился |
| 1 | ЧАС | водород | [1.00784, 1.00811] | [1.0078, 1.0082] | 1.008 | 1.008 | 2009 |
| 2 | Он | гелий | 4.002602(2) | 4.0026 | 4.0026 | 1983 | |
| 3 | Ли | литий | [6.938, 6.997] | [6.938, 6.997] | 6.94 | 6.94 | 2009 |
| 4 | Быть | бериллий | 9.0121831(5) | 9.0122 | 9.0122 | 2013 | |
| 5 | B | бор | [10.806, 10.821] | [10.806, 10.821] | 10.81 | 10.81 | 2009 |
| 6 | C | углерод | [12.0096, 12.0116] | [12.009, 12.012] | 12.011 | 12.011 | 2009 |
| 7 | N | азот | [14.00643, 14.00728] | [14.006, 14.008] | 14.007 | 14.007 | 2009 |
| 8 | О | кислород | [15.99903, 15.99977] | [15.999, 16.000] | 15.999 | 15.999 | 2009 |
| 9 | F | фтор | 18.998403163(6) | 18.998 | 18.998 | 2013 | |
| 10 | Ne | неон | 20.1797(6) | 20.180 | 20.180 | 1985 | |
| 11 | Na | натрий | 22.98976928(2) | 22.990 | 22.990 | 2005 | |
| 12 | Mg | магний | [24.304, 24.307] | [24.304, 24.307] | 24.305 | 24.305 | 2011 |
| 13 | Al | алюминий | 26.9815384(3) | 26.982 | 26.982 | 2017 | |
| 14 | Si | кремний | [28.084, 28.086] | [28.084, 28.086] | 28.085 | 28.085 | 2009 |
| 15 | п | фосфор | 30.973761998(5) | 30.974 | 30.974 | 2013 | |
| 16 | S | сера | [32.059, 32.076] | [32.059, 32.076] | 32.06 | 32.06 | 2009 |
| 17 | Cl | хлор | [35.446, 35.457] | [35.446, 35.457] | 35.45 | 35.45 | 2009 |
| 18 | Ar | аргон | [39.792, 39.963] | [39.792, 39.963] | 39.95[23] | 39.95 | 2017 |
| 19 | K | калий | 39.0983(1) | 39.098 | 39.098 | 1979 | |
| 20 | Ca | кальций | 40.078(4) | 40.078(4) | 40.078(4) | 1983 | |
| 21 | Sc | скандий | 44.955908(5) | 44.956 | 44.956 | 2013 | |
| 22 | Ti | титан | 47.867(1) | 47.867 | 47.867 | 1993 | |
| 23 | V | ванадий | 50.9415(1) | 50.942 | 50.942 | 1977 | |
| 24 | Cr | хром | 51.9961(6) | 51.996 | 51.996 | 1983 | |
| 25 | Mn | марганец | 54.938043(2) | 54.938 | 54.938 | 2017 | |
| 26 | Fe | утюг | 55.845(2) | 55.845(2) | 55.845(2) | 1993 | |
| 27 | Co | кобальт | 58.933194(3) | 58.933 | 58.933 | 2017 | |
| 28 | Ni | никель | 58.6934(4) | 58.693 | 58.693 | 2007 | |
| 29 | Cu | медь | 63.546(3) | 63.546(3) | 63.546(3) | 1969 | |
| 30 | Zn | цинк | 65.38(2) | 65.38(2) | 65.38(2) | 2007 | |
| 31 | Ga | галлий | 69.723(1) | 69.723 | 69.723 | 1987 | |
| 32 | Ge | германий | 72.630(8) | 72.630(8) | 72.630(8) | 2009 | |
| 33 | Так как | мышьяк | 74.921595(6) | 74.922 | 74.922 | 2013 | |
| 34 | Se | селен | 78.971(8) | 78.971(8) | 78.971(8) | 2013 | |
| 35 | Br | бром | [79.901, 79.907] | [79.901, 79.907] | 79.904 | 79.904 | 2011 |
| 36 | Kr | криптон | 83.798(2) | 83.798(2) | 83.798(2) | 2001 | |
| 37 | Руб. | рубидий | 85.4678(3) | 85.468 | 85.468 | 1969 | |
| 38 | Sr | стронций | 87.62(1) | 87.62 | 87.62 | 1969 | |
| 39 | Y | иттрий | 88.90584(1) | 88.906 | 88.906 | 2017 | |
| 40 | Zr | цирконий | 91.224(2) | 91.224(2) | 91.224(2) | 1983 | |
| 41 | Nb | ниобий | 92.90637(1) | 92.906 | 92.906 | 2017 | |
| 42 | Пн | молибден | 95.95(1) | 95.95 | 95.95 | 2013 | |
| 43 | Tc | технеций | - | - | |||
| 44 | RU | рутений | 101.07(2) | 101.07(2) | 101.07(2) | 1983 | |
| 45 | Rh | родий | 102.90549(2) | 102.91 | 102.91 | 2017 | |
| 46 | Pd | палладий | 106.42(1) | 106.42 | 106.42 | 1979 | |
| 47 | Ag | Серебряный | 107.8682(2) | 107.87 | 107.87 | 1985 | |
| 48 | Компакт диск | кадмий | 112.414(4) | 112.41 | 112.41 | 2013 | |
| 49 | В | индий | 114.818(1) | 114.82 | 114.82 | 2011 | |
| 50 | Sn | банка | 118.710(7) | 118.71 | 118.71 | 1983 | |
| 51 | Sb | сурьма | 121.760(1) | 121.76 | 121.76 | 1993 | |
| 52 | Te | теллур | 127.60(3) | 127.60(3) | 127.60(3) | 1969 | |
| 53 | я | йод | 126.90447(3) | 126.90 | 126.90 | 1985 | |
| 54 | Xe | ксенон | 131.293(6) | 131.29 | 131.29 | 1999 | |
| 55 | CS | цезий | 132.90545196(6) | 132.91 | 132.91 | 2013 | |
| 56 | Ба | барий | 137.327(7) | 137.33 | 137.33 | 1985 | |
| 57 | Ла | лантан | 138.90547(7) | 138.91 | 138.91 | 2005 | |
| 58 | Ce | церий | 140.116(1) | 140.12 | 140.12 | 1995 | |
| 59 | Pr | празеодим | 140.90766(1) | 140.91 | 140.91 | 2017 | |
| 60 | Nd | неодим | 144.242(3) | 144.24 | 144.24 | 2005 | |
| 61 | Вечера | прометий | - | - | |||
| 62 | См | самарий | 150.36(2) | 150.36(2) | 150.36(2) | 2005 | |
| 63 | ЕС | европий | 151.964(1) | 151.96 | 151.96 | 1995 | |
| 64 | Б-г | гадолиний | 157.25(3) | 157.25(3) | 157.25(3) | 1969 | |
| 65 | Tb | тербий | 158.925354(8) | 158.93 | 158.93 | 2017 | |
| 66 | Dy | диспрозий | 162.500(1) | 162.50 | 162.50 | 2001 | |
| 67 | Хо | гольмий | 164.930328(7) | 164.93 | 164.93 | 2017 | |
| 68 | Э | эрбий | 167.259(3) | 167.26 | 167.26 | 1999 | |
| 69 | Тм | тулий | 168.934218(6) | 168.93 | 168.93 | 2017 | |
| 70 | Yb | иттербий | 173.045(10) | 173.05 | 173.05 | 2015 | |
| 71 | Лу | лютеций | 174.9668(1) | 174.97 | 174.97 | 2007 | |
| 72 | Hf | гафний | 178.486(6) | 178.49 | 178.49(2) | 2019 | |
| 73 | Та | тантал | 180.94788(2) | 180.95 | 180.95 | 2005 | |
| 74 | W | вольфрам | 183.84(1) | 183.84 | 183.84 | 1991 | |
| 75 | Re | рений | 186.207(1) | 186.21 | 186.21 | 1973 | |
| 76 | Операционные системы | осмий | 190.23(3) | 190.23(3) | 190.23(3) | 1991 | |
| 77 | Ir | иридий | 192.217(2) | 192.22 | 192.22 | 2017 | |
| 78 | Pt | платина | 195.084(9) | 195.08 | 195.08 | 2005 | |
| 79 | Au | золото | 196.966570(4) | 196.97 | 196.97 | 2017 | |
| 80 | Hg | Меркурий | 200.592(3) | 200.59 | 200.59 | 2011 | |
| 81 | Tl | таллий | [204.382, 204.385] | [204.38, 204.39] | 204.38 | 204.38 | 2009 |
| 82 | Pb | вести | 207.2(1) | 207.2 | 207.2 | 1969 | |
| 83 | Би | висмут | 208.98040(1) | 208.98 | 208.98 | 2005 | |
| 84 | По | полоний | - | - | |||
| 85 | В | астатин | - | - | |||
| 86 | Rn | радон | - | - | |||
| 87 | Пт | франций | - | - | |||
| 88 | Ра | радий | - | - | |||
| 89 | Ac | актиний | - | - | |||
| 90 | Чт | торий | 232.0377(4) | 232.04 | 232.04 | 2013 | |
| 91 | Па | протактиний | 231.03588(1) | 231.04 | 231.04 | 2017 | |
| 92 | U | уран | 238.02891(3) | 238.03 | 238.03 | 1999 | |
| 93 | Np | нептуний | - | - | |||
| 94 | Пу | плутоний | - | - | |||
| 95 | Am | америций | - | - | |||
| 96 | См | кюрий | - | - | |||
| 97 | Bk | берклий | - | - | |||
| 98 | Cf | калифорний | - | - | |||
| 99 | Es | эйнштейний | - | - | |||
| 100 | FM | фермий | - | - | |||
| 101 | Мкр | менделевий | - | - | |||
| 102 | Нет | нобелий | - | - | |||
| 103 | Lr | лоуренсий | - | - | |||
| 104 | Rf | резерфорд | - | - | |||
| 105 | Db | дубний | - | - | |||
| 106 | Sg | сиборгий | - | - | |||
| 107 | Bh | бориум | - | - | |||
| 108 | Hs | хасиум | - | - | |||
| 109 | Mt | мейтнерий | - | - | |||
| 110 | Ds | Дармштадтиум | - | - | |||
| 111 | Rg | рентгений | - | - | |||
| 112 | Cn | Copernicium | - | - | |||
| 113 | Nh | нихоний | - | - | |||
| 114 | Fl | флеровий | - | - | |||
| 115 | Mc | москва | - | - | |||
| 116 | Lv | ливерморий | - | - | |||
| 117 | Ц | Tennessine | - | - | |||
| 118 | Og | Оганессон | - | - | |||
- ^ (Этот список: )CIAAW может публиковать изменения атомных весов (включая их точность и производные значения). Начиная с 1947 года, любое обновление происходит номинально в нечетные годы; фактическая дата публикации может быть позже.
- 2009 (вводя обозначение интервалов; Ge):
- «Атомный вес элементов 2009 (Технический отчет IUPAC)». Pure Appl. Chem. 83 (2): 359–396. 12 декабря 2010 г. Дои:10.1351 / PAC-REP-10-09-14.
- 2011 (интервал для Br, Mg):
- «Атомный вес элементов 2011 (Технический отчет IUPAC)». Pure Appl. Chem. 85 (5): 1047–1078. 29 апреля 2013 г. Дои:10.1351 / PAC-REP-13-03-02.
- 2013 (все элементы перечислены):
- Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- 2015 (иттербий изменен):
- "Стандартный атомный вес иттербия пересмотрен". Chemistry International. 37 (5–6): 26. Октябрь 2015. Дои:10.1515 / ci-2015-0512. eISSN 0193-6484. ISSN 0193-6484.
- 2017 (Изменено 14 значений):
- «Стандартные атомные веса 14 химических элементов пересмотрены». CIAAW. 2018-06-05.
- 2019 (значение гафния изменено): Мейя, Юрис; и другие. (2019-12-09). «Стандартный атомный вес гафния пересмотрен». CIAAW. Получено 2020-02-25.
Об обработке неопределенности значений, включая значения диапазона []:
- Поссоло, Антонио; van der Veen, Adriaan M.H .; Мейя, Юрис; и другие. (4 января 2018 г.). «Интерпретация и распространение неопределенности стандартных атомных весов (Технический отчет IUPAC)». Дои:10.1515 / pac-2016-0402. Получено 20 октября 2020.
В периодической таблице
| Группа | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Водород и щелочных металлов | Щелочноземельные металлы | Пниктогены | Халькогены | Галогены | благородные газы | ||||||||||||||
| Период | |||||||||||||||||||
| 2 | |||||||||||||||||||
| 3 | |||||||||||||||||||
| 4 | |||||||||||||||||||
| 5 | |||||||||||||||||||
| 6 | |||||||||||||||||||
| 7 | |||||||||||||||||||
1 (красный) =Газ 3 (черный) =Твердый 80 (зеленый) =Жидкость 109 (серый) = Неизвестно Цвет атомного номера показывает состояние дела (в 0 ° C и 1 атм )
- Ca:40.078 - Формальное краткое значение, округленное (без неопределенности)[24]
- По: [209] - массовое число самого стабильного изотопа
Фоновый цвет показывает подкатегорию в тренде металл – металлоид – неметалл:
| Металл | Металлоид | Неметалл | Неизвестно химический свойства | |||||||
| Щелочной металл | Щелочноземельный металл | Лантаноид | Актинид | Переходный металл | Пост переходный металл | Реактивный неметалл | благородный газ | |||
Смотрите также
- Международный союз теоретической и прикладной химии (ИЮПАК)
- Комиссия по изотопному содержанию и атомным весам
использованная литература
- ^ а б c Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ а б "Золотая книга ИЮПАК". Сборник химической терминологии. Получено 12 июля 2019.
стандартные атомные веса: рекомендуемые значения относительных атомных масс элементов, пересматриваемые раз в два года Комиссией ИЮПАК по атомным весам и изотопному содержанию и применимые к элементам в любом нормальном образце с высоким уровнем достоверности. Нормальный образец представляет собой любой разумно возможный источник элемента или его соединений в торговле для промышленности и науки и не подвергался значительным изменениям изотопного состава в течение короткого с геологической точки зрения периода.
- ^ Визер М.Е. (2006). «Атомный вес элементов 2005 (Технический отчет IUPAC)» (PDF). Чистая и прикладная химия. 78 (11): 2051–2066. Дои:10.1351 / pac200678112051. S2CID 94552853.
- ^ Лоддерс, К. (2008). «Содержание солнечного аргона». Астрофизический журнал. 674 (1): 607–611. arXiv:0710.4523. Bibcode:2008ApJ ... 674..607L. Дои:10.1086/524725. S2CID 59150678.
- ^ Кэмерон, А. Г. У. (1973). «Содержание элементарных и изотопных летучих элементов на внешних планетах». Обзоры космической науки. 14 (3–4): 392–400. Bibcode:1973ССРв ... 14..392С. Дои:10.1007 / BF00214750. S2CID 119861943.
- ^ Это можно определить из предыдущих цифр по определению атомного веса и WP: CALC
- ^ «Атомный вес и изотопный состав для всех элементов». Национальный институт стандартов и технологий.
- ^ а б Wapstra, A.H .; Audi, G .; Тибо, К. (2003), Оценка атомной массы AME2003 (Интернет-изд.), Национальный центр ядерных данных. По материалам:
- Wapstra, A.H .; Audi, G .; Тибо, К. (2003), "Оценка атомной массы AME2003 (I)", Ядерная физика A, 729: 129–336, Bibcode:2003НуФА.729..129Вт, Дои:10.1016 / j.nuclphysa.2003.11.002
- Audi, G .; Wapstra, A.H .; Тибо, К. (2003), "Оценка атомной массы AME2003 (II)", Ядерная физика A, 729: 337–676, Bibcode:2003НуФА.729..337А, Дои:10.1016 / j.nuclphysa.2003.11.003
- ^ а б Росман, К. Дж. Р .; Тейлор, П. Д. П. (1998), "Изотопные составы элементов 1997" (PDF), Чистая и прикладная химия, 70 (1): 217–35, Дои:10.1351 / pac199870010217
- ^ Coplen, T. B .; и другие. (2002), «Вариации изотопного содержания отдельных элементов» (PDF), Чистая и прикладная химия, 74 (10): 1987–2017, Дои:10.1351 / pac200274101987
- ^ Мейя, Юрис; Местер, Золтан (2008). «Распространение неопределенности результатов измерения атомной массы». Метрология. 45 (1): 53–62. Bibcode:2008метро..45 ... 53м. Дои:10.1088/0026-1394/45/1/008.
- ^ Холден, Норман Э. (2004). «Атомный вес и Международный комитет - исторический обзор». Chemistry International. 26 (1): 4–7.
- ^ «ИЮПАК - Международный союз теоретической и прикладной химии: атомные веса десяти химических элементов вот-вот изменятся».
- ^ а б де Бьевр, Поль; Пайзер, Х. Штеффен (1992). "'Атомный вес »- название, история, определение и единицы" (PDF). Чистая и прикладная химия. 64 (10): 1535–43. Дои:10.1351 / pac199264101535.
- ^ Далтон, Джон (1808). Новая система химической философии. Манчестер.
- ^ а б «Стандартный атомный вес 2015». Комиссия по изотопному содержанию и атомным весам. 12 Октябрь 2015. Получено 18 февраля 2017.
- ^ а б Meija 2016, Таблица 1.
- ^ «Стандартные атомные веса 14 химических элементов пересмотрены». CIAAW. 2018-06-05. Получено 2019-02-02.
- ^ "Стандартный атомный вес 14 химических элементов пересмотрен". Chemistry International. 40 (4): 23–24. 2018. Дои:10.1515 / ci-2018-0409. ISSN 0193-6484.
- ^ а б Meija 2016, Таблица 2.
- ^ а б Meija 2016, Таблица 3.
- ^ а б Meija 2016, Таблицы 2 и 3.
- ^ «Периодическая таблица элементов и изотопов ИЮПАК». Королевский центр визуализации в науке. ИЮПАК, Королевский центр визуализации в науке. Получено 8 октября 2019.
- ^ Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3). Стол 2, 3 вместе; неуверенность устранена. Дои:10.1515 / pac-2015-0305.

