Эйнштейний - Einsteinium
Эйнштейний это синтетический элемент с символ Es и атомный номер 99. Как член актинид серия, она седьмая трансурановый элемент.
Эйнштейний был обнаружен как компонент обломков первая водородная бомба взрыв в 1952 г. и назван в честь Альберт Эйнштейн. Самый распространенный изотоп эйнштейний-253 (период полураспада 20,47 дней) производится искусственно в результате распада калифорний -253 в нескольких выделенных мощных ядерные реакторы с общим доходом порядка одного миллиграмма в год. За реактором синтеза следует сложный процесс отделения эйнштейния-253 от других актинидов и продуктов их распада. Другие изотопы синтезируются в различных лабораториях, но в гораздо меньших количествах, путем бомбардировки тяжелых актинидных элементов легкими ионами. Из-за небольшого количества продуцируемого эйнштейния и короткого периода полураспада его наиболее легко производимого изотопа в настоящее время практически нет его практического применения за пределами фундаментальных научных исследований. В частности, эйнштейний был впервые использован для синтеза 17 атомов нового элемента. менделевий в 1955 г.
Эйнштейний - мягкий, серебристый, парамагнитный металл. Его химический состав типичен для поздних актинидов с преобладанием +3 степень окисления; степень окисления +2 также доступна, особенно в твердых телах. Высокая радиоактивность эйнштейния-253 вызывает видимое свечение и быстро повреждает его кристаллическую металлическую решетку с выделением тепла около 1000 Вт за грамм. Сложность изучения его свойств связана с распадом эйнштейния-253 на берклий -249, а затем калифорний-249 со скоростью около 3% в день. Изотоп эйнштейния с самым длинным периодом полураспада, эйнштейний-252 (период полураспада 471,7 дня), был бы более подходящим для исследования физических свойств, но оказалось, что его гораздо труднее производить и он доступен только в незначительных количествах, а не оптом.[1] Эйнштейний - элемент с самым высоким атомным номером, который наблюдался в макроскопических количествах в чистом виде, и это был обычный короткоживущий изотоп эйнштейний-253.[2]
Как и все синтетические трансурановые элементы, изотопы эйнштейния очень радиоактивный и считаются очень опасными для здоровья при проглатывании.[3]
История

Эйнштейний был впервые идентифицированный в декабре 1952 г. Альберт Гиорсо и коллеги по Калифорнийский университет в Беркли в сотрудничестве с Аргонн и Лос-Аламос Национальные лаборатории, в результате Айви Майк ядерное испытание. Испытание проводилось 1 ноября 1952 г. в г. Атолл Эниветак в Тихий океан и был первым успешным испытанием водородная бомба.[4] Первоначальное обследование обломков взрыва показало образование нового изотопа плутоний, 244
94Пу
, которые могли образоваться только при поглощении шести нейтроны по уран-238 ядро, за которым следуют два бета-распад.
В то время считалось, что многократное поглощение нейтронов - чрезвычайно редкий процесс, но идентификация 244
94Пу
указывает на то, что ядрами урана могло быть захвачено еще больше нейтронов, что привело к образованию новых элементов тяжелее калифорний.[4]

Гиорсо и его коллеги проанализировали фильтровальную бумагу, пролетевшую через облако взрыва в самолетах (та же методика отбора проб, которая использовалась для обнаружения 244
94Пу
).[5] Позднее из коралловых обломков атолла были выделены большие количества радиоактивного материала, которые были доставлены в США.[4] Разделение предполагаемых новых элементов проводилось при наличии лимонная кислота /аммоний буферный раствор в слабокислой среде (pH ≈ 3,5), используя ионный обмен при повышенных температурах; в итоге было извлечено менее 200 атомов эйнштейния.[6] Тем не менее, элемент 99 (эйнштейний), а именно его 253Изотоп Es может быть обнаружен по его характерному высокоэнергетическому альфа-распад при 6,6 МэВ.[4] Это было произведено захватывать из 15 нейтроны к уран-238 ядер, за которыми следовали семь бета-распадов, и период полураспада от 20,5 сут. Такое многократное поглощение нейтронов стало возможным благодаря высокой плотности потока нейтронов во время детонации, так что у вновь образовавшихся тяжелых изотопов было достаточно нейтронов для поглощения, прежде чем они могли распасться на более легкие элементы. Изначально захват нейтронов повысил массовое число без изменения атомный номер нуклида, и сопутствующие бета-распады привели к постепенному увеличению атомного номера:[4]
Немного 238Атомы U, однако, могли поглотить два дополнительных нейтрона (всего 17), в результате чего 255Es, как и в 255Изотоп Fm еще одного нового элемента, фермий.[7] Открытие новых элементов и связанные с ними новые данные о множественном захвате нейтронов первоначально держались в секрете по приказу вооруженных сил США до 1955 года из-за Холодная война напряженность и конкуренция с Советским Союзом в ядерных технологиях.[4][8][9] Однако быстрый захват такого количества нейтронов обеспечит необходимое прямое экспериментальное подтверждение так называемого r-процесс многократное поглощение нейтронов, необходимое для объяснения космического нуклеосинтез (производство) некоторых тяжелых химических элементов (тяжелее никеля) в сверхновая звезда взрывы, до бета-распад. Такой процесс необходим для объяснения существования многих стабильных элементов во Вселенной.[10]
Между тем, изотопы элемента 99 (а также нового элемента 100, фермий ) были произведены в лабораториях Беркли и Аргонн, в ядерная реакция между азот -14 и уран-238,[11] а затем интенсивным нейтронным облучением плутоний или же калифорний:
Эти результаты были опубликованы в нескольких статьях в 1954 году с оговоркой о том, что это не первые исследования, проведенные с элементами.[12][13][14][15][16] Команда Беркли также сообщила о некоторых результатах по химическим свойствам эйнштейния и фермия.[17][18] В Айви Майк результаты были рассекречены и опубликованы в 1955 году.[8]

В открытии элементов 99 и 100 американские команды соревновались с группой на Нобелевский институт физики, Стокгольм, Швеция. В конце 1953 - начале 1954 года шведской группе удалось синтезировать легкие изотопы элемента 100, в частности 250Fm, бомбардировкой урана ядрами кислорода. Эти результаты также были опубликованы в 1954 году.[19] Тем не менее, приоритет команды Беркли был общепризнанным, поскольку ее публикации предшествовали шведской статье и основывались на ранее нераскрытых результатах термоядерного взрыва 1952 года; таким образом, команде Беркли была предоставлена привилегия назвать новые элементы. Поскольку усилие, которое привело к созданию Айви Майк кодовое название Project PANDA,[20] элемент 99 был в шутку прозван «Пандамониум»[21] но официальные имена, предложенные группой Беркли, произошли от двух выдающихся ученых, Альберт Эйнштейн и Энрико Ферми: «Мы предлагаем название элемента с атомным номером 99, эйнштейний (символ E) в честь Альберта Эйнштейна, и для названия элемента с атомным номером 100, фермий (символ Fm), в честь Энрико Ферми».[8] И Эйнштейн, и Ферми умерли между моментом, когда имена были первоначально предложены, и когда они были объявлены. Об открытии этих новых элементов объявил Альберт Гиорсо на первой Женевской атомной конференции 8–20 августа 1955 г.[4] Символ эйнштейния сначала был обозначен как «E», а позже IUPAC изменил его на «Es».[22][23]
Характеристики
Физический

Эйнштейний - синтетический серебристо-белый радиоактивный металл. в периодическая таблица, он расположен справа от актинида калифорний, слева от актинида фермий и ниже лантаноида гольмий с которым у него много общего по физическим и химическим свойствам. Его плотность 8,84 г / см.3 ниже, чем у калифорния (15,1 г / см3) и почти такой же, как у гольмия (8,79 г / см3), несмотря на то, что атомный эйнштейний намного тяжелее гольмия. Температура плавления эйнштейния (860 ° C) также относительно низкая - ниже калифорний (900 ° С), фермий (1527 ° C) и гольмий (1461 ° C).[3][25] Эйнштейний - мягкий металл, с объемный модуль всего 15 ГПа, что является одним из самых низких показателей среди другихщелочных металлов.[26]
В отличие от более легких актинидов калифорний, берклий, кюрий и америций которые кристаллизуются в двойной шестиугольник структура в условиях окружающей среды, эйнштейний, как полагают, имеет гранецентрированная кубическая (fcc) симметрия с пространственной группой FM3м и постоянная решетки а = 575 часов. Однако есть сообщение о гексагональном металлическом эйнштейнии при комнатной температуре с а = 398 вечера и c = 650 пм, что преобразовано в fcc фаза при нагревании до 300 ° С.[27]
Саморазрушение, вызванное радиоактивностью эйнштейния, настолько велико, что быстро разрушает кристаллическую решетку,[28] и выделение энергии во время этого процесса, 1000 Вт на грамм 253Es вызывает видимое свечение.[2] Эти процессы могут способствовать относительно низкой плотности и температуре плавления эйнштейния.[29] Кроме того, из-за небольшого размера имеющихся образцов температуру плавления эйнштейния часто определяли, наблюдая за нагреванием образца в электронном микроскопе.[30] Таким образом, поверхностные эффекты в небольших образцах могут снизить значение точки плавления.
Металл двухвалентен и имеет заметно высокую летучесть.[31] Чтобы уменьшить повреждение от собственного излучения, большинство измерений твердого эйнштейния и его соединений проводят сразу после термического отжига.[32] Также некоторые соединения изучаются в атмосфере газа-восстановителя, например H2O +HCl для EsOCl, так что образец частично отрастает во время разложения.[33]
Помимо саморазрушения твердого эйнштейния и его соединений, к другим сложностям, присущим изучению этого элемента, относится дефицит - наиболее распространенный 253Изотоп Es доступен только один или два раза в год в количествах менее миллиграмма - и самозагрязнение из-за быстрого превращения эйнштейния в берклий, а затем в калифорний со скоростью около 3,3% в день:[34][35][36]
Таким образом, большинство образцов эйнштейния загрязнены, а их внутренние свойства часто выводятся путем экстраполяции экспериментальных данных, накопленных с течением времени. Другие экспериментальные методы, позволяющие обойти проблему загрязнения, включают избирательное оптическое возбуждение ионов эйнштейния перестраиваемым лазером, например, при изучении его люминесцентных свойств.[37]
Магнитные свойства были изучены для металлического эйнштейния, его оксида и фторида. Все три материала показали Кюри – Вайс парамагнитный поведение от жидкий гелий до комнатной температуры. Эффективные магнитные моменты рассчитывались как 10.4±0.3 µB для Es2О3 и 11.4±0,3 мкB для EsF3, которые являются самыми высокими значениями среди актинидов, и соответствующие Температуры Кюри равны 53 и 37 К.[38][39]
Химическая
Как и все актиниды, эйнштейний довольно реактивен. Его тривиальность степень окисления наиболее стабилен в твердых веществах и водном растворе, при этом имеет бледно-розовый цвет.[40] Существование двухвалентного эйнштейния твердо установлено, особенно в твердой фазе; такое состояние +2 не наблюдается у многих других актинидов, включая протактиний, уран, нептуний, плутоний, кюрий и берклий. Соединения эйнштейния (II) могут быть получены, например, восстановлением эйнштейния (III) с помощью хлорид самария (II).[41] Степень окисления +4 была постулирована на основе исследований пара и пока не определена.[42]
Изотопы
Девятнадцать изотопов и три ядерные изомеры известны эйнштейном, с массовые числа в диапазоне от 240 до 257. Все они радиоактивны и являются наиболее стабильными нуклидами, 252Es имеет период полураспада 471,7 дней.[43] Следующими наиболее стабильными изотопами являются 254Es (период полураспада 275,7 суток),[44] 255Es (39,8 суток) и 253Es (20,47 суток). Все оставшиеся изотопы имеют период полураспада менее 40 часов, и большинство из них распадаются менее чем за 30 минут. Из трех ядерных изомеров наиболее стабильным является 254 кв.м.Es с периодом полураспада 39,3 часа.[45]
Ядерное деление
Эйнштейний имеет высокий уровень ядерное деление что приводит к низкому критическая масса для устойчивого ядерная цепная реакция. Эта масса составляет 9,89 кг для голого шара. 254Es, и его можно снизить до 2,9, добавив сталь толщиной 30 сантиметров. отражатель нейтронов или даже до 2,26 кг с отражателем из воды толщиной 20 см. Однако даже эта малая критическая масса значительно превышает общее количество выделенного до сих пор эйнштейния, особенно редких 254Изотоп Es.[46]
Естественное явление
Из-за короткого периода полураспада всех изотопов эйнштейния любые изначальный эйнштейний - то есть эйнштейний, который, возможно, мог присутствовать на Земле во время ее образования - давно распался. Синтез эйнштейния из природных актинидов урана и тория в земной коре требует множественного захвата нейтронов, что крайне маловероятно. Таким образом, весь земной эйнштейний производится в научных лабораториях, ядерных реакторах большой мощности или в испытания ядерного оружия, и присутствует только в течение нескольких лет с момента синтеза.[6]
Трансурановые элементы из америций к фермий, включая эйнштейний, естественным образом встречались в естественный ядерный реактор деления в Окло, но больше не делайте этого.[47]
Эйнштейний наблюдался в Звезда Пшибыльского в 2008.[48]
Синтез и экстракция

Эйнштейний производится в ничтожных количествах путем бомбардировки более легких актинидов нейтронами в специальных высокопоточных ядерные реакторы. Основными источниками излучения в мире являются 85-мегаваттные Изотопный реактор с высоким потоком (HFIR) на Национальная лаборатория Окриджа в Теннесси, США,[50] и петлевой реактор СМ-2 на Научно-исследовательский институт атомных реакторов (НИИАР) в Димитровград, Россия,[51] которые оба предназначены для производства транскуриума (Z > 96) элементов. Эти объекты имеют аналогичные уровни мощности и магнитного потока и, как ожидается, будут иметь сопоставимые производственные мощности для трансуриевых элементов,[52] хотя объемы производства НИИАР широко не сообщаются. В «типичной кампании по переработке» в Ок-Ридже десятки граммов кюрий облучаются для получения количества дециграмм калифорний, миллиграммы берклия (249Bk) и эйнштейний и пикограммовые количества фермий.[53][54]
Первый микроскопический образец 253Ес образец весом около 10 нанограммы был подготовлен в 1961 году в HFIR. Для оценки его веса были разработаны специальные магнитные весы.[3][55] Позднее производились более крупные партии, начиная с нескольких килограммов плутония с выходами эйнштейния (в основном 253Es) 0,48 миллиграмма в 1967–1970 годах, 3,2 миллиграмма в 1971–1973 годах, с последующим стабильным производством около 3 миллиграммов в год в период с 1974 по 1978 год.[56] Однако эти величины относятся к целому количеству в мишени сразу после облучения. Последующие процедуры разделения уменьшили количество изотопно чистого эйнштейния примерно в десять раз.[52]
Лабораторный синтез
Облучение плутония интенсивными нейтронами приводит к образованию четырех основных изотопов эйнштейния: 253Es (α-излучатель с периодом полураспада 20,47 суток и периодом полураспада спонтанного деления 7 × 105 годы); 254мEs (β-излучатель с периодом полураспада 39,3 часа), 254Es (α-излучатель с периодом полураспада около 276 дней) и 255Es (β-излучатель с периодом полураспада 39,8 суток).[57][45] Альтернативный путь предполагает бомбардировку урана-238 высокоинтенсивными пучками ионов азота или кислорода.[58]
Эйнштейний-247 (период полураспада 4,55 минут) был получен путем облучения америция-241 углеродом или урана-238 ионами азота.[59] Последняя реакция была впервые реализована в 1967 году в Дубне, Россия, и привлеченные ученые были награждены Премия Ленинского Комсомола.[60]
Изотоп 248Es получали облучением 249Cf с дейтерий ионы. Он в основном распадается за счет испускания электронов на 248Cf с периодом полураспада 25±5 минут, но также высвобождает α-частицы с энергией 6,87 МэВ с отношением электронов к α-частицам около 400.[61]
Более тяжелые изотопы 249Es, 250Es, 251Es и 252Es были получены бомбардировкой 249Bk с α-частицами. В этом процессе высвобождаются от одного до четырех нейтронов, что делает возможным образование четырех различных изотопов в одной реакции.[62]
Эйнштейний-253 был получен облучением 0,1–0,2 миллиграмма. 252Cf мишень с тепловой нейтрон поток (2–5) × 1014 нейтроны · см−2· С−1 на 500–900 часов:[63]
Синтез при ядерных взрывах

Анализ завала на 10-мегатонна Айви Майк ядерное испытание было частью долгосрочного проекта. Одна из целей которого заключалась в изучении эффективности производства трансурановых элементов при ядерных взрывах большой мощности. Мотивация для этих экспериментов заключалась в том, что синтез таких элементов из урана требует многократного захвата нейтронов. Вероятность таких событий увеличивается с увеличением нейтронный поток, а ядерные взрывы - самые мощные искусственные источники нейтронов, обеспечивающие плотности порядка 1023 нейтронов / см2 в течение микросекунды или около 1029 нейтронов / (см2· С). Для сравнения, поток реактора HFIR составляет 5×1015 нейтронов / (см2· С). Специальная лаборатория была создана прямо на Атолл Эниветак для предварительного анализа обломков, так как некоторые изотопы могли распасться к тому времени, когда образцы обломков достигли материковой части США. Лаборатория как можно скорее получила образцы для анализа с самолетов, оснащенных бумажными фильтрами, которые пролетели над атоллом после испытаний. В то время как надеялись открыть новые химические элементы тяжелее фермия, ни один из них не был обнаружен даже после серии мегатонных взрывов, проведенных между 1954 и 1956 годами на атолле.[5]
Атмосферные результаты были дополнены данными подземных испытаний, накопленных в 1960-х гг. Испытательный полигон в Неваде, поскольку была надежда, что мощные взрывы, проведенные в замкнутом пространстве, могут привести к увеличению выхода и более тяжелым изотопам. Помимо традиционных урановых зарядов, комбинации урана с америцием и торий были опробованы, а также смешанный заряд плутония-нептуния, но они были менее успешными с точки зрения выхода и были приписаны более сильным потерям тяжелых изотопов из-за повышенной скорости деления в зарядах тяжелых элементов. Изоляция продукта была проблематичной, поскольку взрывы распространяли обломки за счет плавления и испарения окружающих пород на глубине 300–600 метров. Бурение на такую глубину для извлечения продуктов было медленным и неэффективным с точки зрения собранных объемов.[5][64]
Среди девяти подземных испытаний, проведенных с 1962 по 1969 год,[65][66] последний был самым мощным и имел наибольший выход трансурановых элементов. Миллиграммы эйнштейния, на которые обычно требуется год облучения в реакторе большой мощности, были произведены за микросекунду.[64] Однако главной практической проблемой всего предложения был сбор радиоактивных обломков, рассеянных мощным взрывом. Авиационные фильтры адсорбируют всего около 4×10−14 от общего количества, а сбор тонны кораллов на атолле Эниветак увеличил эту долю всего на два порядка. Добыча около 500 килограммов подземных пород через 60 дней после взрыва Хатча восстановила только около 1×10−7 от общей суммы заряда. Количество трансурановых элементов в этой партии весом 500 кг было всего в 30 раз больше, чем в породе весом 0,4 кг, взятой через 7 дней после испытания, которое продемонстрировало крайне нелинейную зависимость выхода трансурановых элементов от количества извлеченной радиоактивной породы.[67] Перед испытанием на площадке были просверлены стволы, чтобы ускорить сбор проб после взрыва, чтобы при взрыве радиоактивный материал вытеснялся из эпицентра через стволы и собирался в объемах, близких к поверхности. Этот метод был опробован в двух испытаниях и мгновенно предоставил сотни килограммов материала, но с концентрацией актинида в 3 раза ниже, чем в образцах, полученных после бурения. Хотя такой метод мог бы быть эффективным при научных исследованиях короткоживущих изотопов, он не мог улучшить общую эффективность сбора производимых актинидов.[68]
Хотя в обломках ядерных испытаний не было обнаружено никаких новых элементов (кроме эйнштейния и фермия), а общие выходы трансурановых элементов были разочаровывающе низкими, эти испытания действительно дали значительно более высокие количества редких тяжелых изотопов, чем ранее доступные в лабораториях.[69]
Разделение
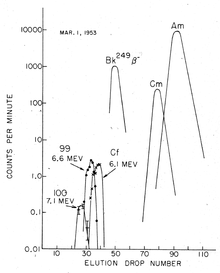
Процедура выделения эйнштейния зависит от метода синтеза. В случае бомбардировки легкими ионами внутри циклотрона мишень из тяжелых ионов прикрепляется к тонкой фольге, а образовавшийся эйнштейний просто смывается с фольги после облучения. Однако производимые количества в таких экспериментах относительно низкие.[70] Выходы намного выше при облучении реактора, но там продукт представляет собой смесь различных изотопов актинидов, а также лантаноидов, образующихся при распадах ядерного деления. В этом случае выделение эйнштейния является утомительной процедурой, которая включает несколько повторяющихся этапов катионного обмена при повышенных температуре и давлении и хроматографию. Отделение от берклия важно, потому что наиболее распространенный изотоп эйнштейния, производимый в ядерных реакторах, 253Es, распадается с периодом полураспада всего 20 дней до 249Bk, что является быстрым в масштабе большинства экспериментов. Такое разделение основывается на том факте, что берклий легко окисляется до твердого состояния +4 и выпадает в осадок, тогда как другие актиниды, включая эйнштейний, остаются в своем состоянии +3 в растворах.[71]
Отделение трехвалентных актинидов от продуктов деления лантаноидов может быть выполнено с помощью колонки с катионообменной смолой, используя раствор 90% воды / 10% этанола, насыщенный соляная кислота (HCl) как элюент. Обычно за ним следует анионообменная хроматография используя 6 коренной зуб HCl в качестве элюента. Колонка с катионообменной смолой (обменная колонка Dowex-50), обработанная солями аммония, затем используется для разделения фракций, содержащих элементы 99, 100 и 101. Эти элементы затем могут быть идентифицированы просто на основе их положения / времени элюирования с использованием α-гидроксиизобутирата. раствор (α-HIB), например, в качестве элюента.[72]
Разделение актинидов 3+ также может быть достигнуто с помощью экстракционной хроматографии с использованием бис- (2-этилгексил) фосфорной кислоты (сокращенно HDEHP) в качестве стационарной органической фазы и азотной кислоты в качестве подвижной водной фазы. Последовательность элюирования актинидов обратная по сравнению с колонкой с катионообменной смолой. Эйнштейний, отделенный этим методом, имеет то преимущество, что он не содержит органического комплексообразователя, по сравнению с разделением с использованием колонки со смолой.[72]
Подготовка металла
Эйнштейний обладает высокой реакционной способностью, поэтому для получения чистого металла из его соединений требуются сильные восстановители.[73] Этого можно добиться восстановлением фторида эйнштейния (III) металлическим литий:
- EsF3 + 3 Li → Es + 3 LiF
Однако из-за низкой температуры плавления и высокой скорости саморадиационного разрушения эйнштейний имеет высокое давление паров, которое выше, чем у фторида лития. Это делает эту реакцию восстановления довольно неэффективной. Его опробовали при первых попытках получения, и от него быстро отказались в пользу восстановления оксида эйнштейния (III) с помощью лантан металл:[27][29][74]
- Es2О3 + 2 La → 2 Es + La2О3
Химические соединения
| Сложный | Цвет | Симметрия | Космическая группа | Нет | Символ Пирсона | а (вечера ) | б (вечера) | c (вечера) |
|---|---|---|---|---|---|---|---|---|
| Es2О3 | Бесцветный | Кубический[35] | Я3 | 206 | cI80 | 1076.6 | ||
| Es2О3 | Бесцветный | Моноклиника[75] | C2 / м | 12 | мс30 | 1411 | 359 | 880 |
| Es2О3 | Бесцветный | Шестиугольный[75] | п3m1 | 164 | hP5 | 370 | 600 | |
| EsF3 | Шестиугольный[34] | |||||||
| EsF4 | Моноклиника[76] | C2 / c | 15 | мс60 | ||||
| EsCl3 | апельсин | Шестиугольный[77][78] | C63/ м | hP8 | 727 | 410 | ||
| EsBr3 | Желтый | Моноклиника[79] | C2 / м | 12 | mS16 | 727 | 1259 | 681 |
| EsI3 | Янтарь | Шестиугольный[80][81] | р3 | 148 | 24 грн. | 753 | 2084 | |
| EsOCl | Тетрагональный[80][82] | P4 / нм | 394.8 | 670.2 |
Оксиды
Оксид эйнштейния (III) (Es2О3) получали сжиганием нитрата эйнштейния (III). Он образует бесцветные кубические кристаллы, которые впервые были охарактеризованы на микрограммовых образцах размером около 30 нанометров.[28][35] Две другие фазы, моноклинический и гексагональные, известны для этого оксида. Формирование некой Es2О3 Фаза зависит от техники приготовления и истории образца, и четкой фазовой диаграммы нет. Взаимопревращения между тремя фазами могут происходить спонтанно, в результате самооблучения или самонагревания.[83] Гексагональная фаза изотипна с оксид лантана (III) где Es3+ ион окружен 6-координированной группой O2− ионы.[75][80]
Галогениды

Эйнштейний галогениды известны степени окисления +2 и +3.[82][84] Наиболее стабильное состояние +3 для всех галогенидов от фторида до иодида.
Фторид эйнштейния (III) (EsF3) может быть осажден из растворов хлорида эйнштейния (III) при реакции с фторид ионы. Альтернативная процедура подготовки заключается в воздействии на оксид эйнштейния (III) трифторид хлора (ClF3) или F2 газ при давлении 1–2 атмосферы и температуре от 300 до 400 ° C. EsF3 кристаллическая структура гексагональная, как у фторида калифорния (III) (CfF3) где Es3+ ионы 8-кратно координированы ионами фтора в двухклапанной тригональная призма расположение.[34][85][86]
Эйнштейний (III) хлорид (EsCl3) может быть получен отжигом оксида эйнштейния (III) в атмосфере сухих паров хлористого водорода при температуре около 500 ° C в течение примерно 20 минут. Он кристаллизуется при охлаждении примерно до 425 ° C в оранжевое твердое вещество с шестиугольник структура UCl3 тип, где атомы эйнштейния 9-кратно координированы атомами хлора в геометрии тригональной призмы.[78][85][87] Бромид эйнштейния (III) (EsBr3) представляет собой бледно-желтое твердое вещество с моноклинический структура AlCl3 тип, где атомы эйнштейния октаэдрически координируется бромом (координационное число 6).[81][85]
Двухвалентные соединения эйнштейния получают восстановлением трехвалентных галогенидов с помощью водород:[88]
- 2 EsX3 + H2 → 2 EsX2 + 2 HX, X = F, Cl, Br, I
Эйнштейний (II) хлорид (EsCl2),[89] бромид эйнштейния (II) (EsBr2),[90] и йодид эйнштейния (II) (EsI2)[82] были произведены и характеризовались оптическим поглощением, структурная информация пока отсутствует.[81]
Известные оксигалогениды эйнштейния включают EsOCl,[82] EsOBr[88] и EsOI.[82] Эти соли синтезируются путем обработки тригалогенида паровой смесью воды и соответствующего галогенида водорода: например, EsCl3 + H2O / HCl для получения EsOCl.[33]
Ойнштейниевые соединения
Высокая радиоактивность эйнштейния потенциально может использоваться в радиационная терапия, и металлоорганические комплексы были синтезированы для доставки атомов эйнштейния в соответствующий орган тела. Были проведены эксперименты по введению эйнштейния. цитрат (а также соединения фермия) собакам.[2] Эйнштейний (III) также был включен в бета-дикетон. хелат комплексов, поскольку аналогичные комплексы с лантаноидами ранее демонстрировали наиболее сильные УФ-возбужденные свечение среди металлоорганических соединений. При получении комплексов эйнштейния Es3+ ионы были разбавлены в 1000 раз Gd3+ ионы. Это позволило снизить радиационное повреждение, чтобы соединения не распадались в течение 20 минут, необходимых для измерений. Результирующая люминесценция от Es3+ был слишком слаб, чтобы его можно было обнаружить. Это объяснялось неблагоприятными относительными энергиями отдельных компонентов соединения, которые препятствовали эффективному переносу энергии от хелатной матрицы к Es3+ ионы. Аналогичный вывод был сделан для других актинидов америция, берклия и фермия.[91]
Люминесценция Es3+ однако наблюдались в растворах неорганической соляной кислоты, а также в органических растворах с ди (2-этилгексил) ортофосфорной кислотой. Он показывает широкий пик с длиной волны около 1064 нм (полуширина около 100 нм), который может резонансно возбуждаться зеленым светом (длина волны около 495 нм). Люминесценция имеет время жизни несколько микросекунд и квантовый выход менее 0,1%. Относительно высокая по сравнению с лантаноидами скорость безызлучательного распада в Es3+ связаны с более сильным взаимодействием f-электронов с внутренним Es3+ электроны.[92]
Приложения
Практически нет применения любого изотопа эйнштейния за пределами фундаментальных научных исследований, направленных на получение более высоких трансурановые элементы и трансактиниды.[93]
В 1955 г. менделевий был синтезирован путем облучения мишени, состоящей примерно из 109 атомы 253Es в 60-дюймовом циклотроне в лаборатории Беркли. Результирующий 253Es (α, n)256В результате реакции Md получено 17 атомов нового элемента с порядковым номером 101.[94]
Редкий изотоп эйнштейний-254 используется для производства сверхтяжелые элементы из-за его большой массы, относительно длительного периода полураспада, составляющего 270 дней, и доступности в значительных количествах в несколько микрограммов.[95] Следовательно, эйнштейний-254 был использован в качестве мишени при попытке синтеза унунениум (элемент 119) в 1985 году, обстреляв его кальций-48 ионы в superHILAC линейный ускоритель в Беркли, Калифорния. Атомы не были идентифицированы, установив верхний предел для сечения этой реакции 300 наноразрушители.[96]
Эйнштейний-254 использовали в качестве калибровочного маркера в спектрометре химического анализа ("анализатор альфа-рассеивающей поверхности ") из Сюрвейер 5 лунный зонд. Большая масса этого изотопа уменьшала спектральное перекрытие между сигналами от маркера и исследуемых более легких элементов лунной поверхности.[97]
Безопасность
Большинство доступных данных о токсичности эйнштейния основано на исследованиях на животных. При проглатывании крысами только около 0,01% эйнштейна попадает в кровоток. Оттуда около 65% попадает в кости, где остается около 50 лет, 25% - в легкие (биологический период полураспада около 20 лет, хотя это не имеет значения из-за короткого периода полураспада изотопов эйнштейния), 0,035 % к яичкам или 0,01% к яичникам, где эйнштейний остается неопределенно долго. Выводится около 10% проглоченного количества. Распределение эйнштейния по поверхности костей однородно и похоже на распределение плутония.[98]
Рекомендации
- ^ Эйнштейний. периодический.lanl.gov
- ^ а б c Волосы, п. 1579
- ^ а б c Хаммонд С. Р. "Элементы" в Лиде, Д. Р., изд. (2005). CRC Справочник по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5.
- ^ а б c d е ж грамм Гиорсо, Альберт (2003). «Эйнштейний и фермий». Новости химии и техники. 81 (36): 174–175. Дои:10.1021 / cen-v081n036.p174.
- ^ а б c Сиборг, п. 39
- ^ а б Джон Эмсли Строительные блоки природы: руководство по элементам от А до Я, Oxford University Press, 2003 г., ISBN 0-19-850340-7 стр. 133–135
- ^ 254Es, 254FM и 253Fm не будет производиться из-за отсутствия бета-распада в 254Cf и 253Es
- ^ а б c Ghiorso, A .; Thompson, S .; Higgins, G .; Сиборг, G .; Studier, M .; Поля, П .; Fried, S .; Diamond, H .; Mech, J .; Pyle, G .; Huizenga, J .; Hirsch, A .; Manning, W .; Browne, C .; Smith, H .; Спенс Р. (1955). «Новые элементы эйнштейний и фермий, атомные номера 99 и 100». Phys. Rev. 99 (3): 1048–1049. Bibcode:1955ПхРв ... 99.1048Г. Дои:10.1103 / PhysRev.99.1048. Google Книги
- ^ Поля, П .; Studier, M .; Diamond, H .; Mech, J .; Inghram, M .; Pyle, G .; Stevens, C .; Fried, S .; Manning, W .; Pyle, G .; Huizenga, J .; Hirsch, A .; Manning, W .; Browne, C .; Smith, H .; Спенс Р. (1956). «Трансплутониевые элементы в обломках термоядерных испытаний». Физический обзор. 102 (1): 180–182. Bibcode:1956ПхРв..102..180Ф. Дои:10.1103 / PhysRev.102.180. Google Книги
- ^ Бирн, Дж. Нейтроны, ядра и вещество, Dover Publications, Mineola, NY, 2011, ISBN 978-0-486-48238-5 (PBK) с. 267.
- ^ Гиорсо, Альберт; Росси, Г. Бернар; Харви, Бернард Г. и Томпсон, Стэнли Г. (1954). «Реакции U-238 с циклотронными ионами азота». Физический обзор. 93 (1): 257. Bibcode:1954ПхРв ... 93..257Г. Дои:10.1103 / PhysRev.93.257. S2CID 121499772.
- ^ Thompson, S.G .; Ghiorso, A .; Harvey, B.G .; Чоппин, Г. Р. (1954). «Изотопы транскурия, полученные при нейтронном облучении плутония». Физический обзор. 93 (4): 908. Bibcode:1954ПхРв ... 93..908Т. Дои:10.1103 / PhysRev.93.908.
- ^ Харви, Бернард; Томпсон, Стэнли; Гиорсо, Альберт; Чоппин, Грегори (1954). «Дальнейшее получение транскуриевых нуклидов нейтронным облучением». Физический обзор. 93 (5): 1129. Bibcode:1954PhRv ... 93.1129H. Дои:10.1103 / PhysRev.93.1129.
- ^ Studier, M .; Поля, П .; Diamond, H .; Mech, J .; Фридман, А .; Продавцы, П .; Pyle, G .; Stevens, C .; Magnusson, L .; Huizenga, J. (1954). «Элементы 99 и 100 из плутония, облученного котлом». Физический обзор. 93 (6): 1428. Bibcode:1954ПхРв ... 93.1428С. Дои:10.1103 / PhysRev.93.1428.
- ^ Чоппин, Г. Р .; Thompson, S.G .; Гиорсо, А.; Харви, Б.Г. (1954). «Ядерные свойства некоторых изотопов калифорния, элементы 99 и 100». Физический обзор. 94 (4): 1080–1081. Bibcode:1954PhRv ... 94.1080C. Дои:10.1103 / PhysRev.94.1080.
- ^ Поля, П .; Studier, M .; Mech, J .; Diamond, H .; Фридман, А .; Magnusson, L .; Huizenga, J. (1954). «Дополнительные свойства изотопов элементов 99 и 100». Физический обзор. 94 (1): 209–210. Bibcode:1954ПхРв ... 94..209Ф. Дои:10.1103 / PhysRev.94.209.
- ^ Сиборг, Г. Т .; Thompson, S.G .; Харви, Б.Г. и Чоппин, Г. (23 июля 1954 г.) «Химические свойства элементов 99 и 100», Радиационная лаборатория, Калифорнийский университет, Беркли, UCRL-2591
- ^ Thompson, S.G .; Harvey, B.G .; Чоппин, Г. Р .; Сиборг, Г. Т. (1954). «Химические свойства элементов 99 и 100». Журнал Американского химического общества. 76 (24): 6229–6236. Дои:10.1021 / ja01653a004.
- ^ Аттерлинг, Хьюго; Форслинг, Вильгельм; Холм, Леннарт; Меландер, Ларс; Остром, Бьорн (1954). "Элемент 100, полученный с помощью циклотронно-ускоренных ионов кислорода". Физический обзор. 95 (2): 585–586. Bibcode:1954ПхРв ... 95..585А. Дои:10.1103 / PhysRev.95.585.2.
- ^ Ричард Ли Миллер (1991). Под облаком: десятилетия ядерных испытаний. Two-Sixty Press. п. 115. ISBN 978-1-881043-05-8.
- ^ Джон Макфи (1980). Кривая связывающей энергии. Фаррар, Straus & Giroux Inc. стр. 116. ISBN 978-0-374-51598-0.
- ^ Волосы, п. 1577
- ^ Сиборг, Г. (1994) Современная алхимия: избранные статьи Гленна Т. Сиборга, World Scientific, стр. 6, ISBN 981-02-1440-5.
- ^ Волосы, п. 1580
- ^ Хайре, Р. Г. (1990) "Свойства трансплутониевых металлов (Am-Fm)", в: Справочник по металлам, Vol. 2, 10-е издание, (ASM International, Materials Park, Ohio), стр. 1198–1201.
- ^ Волосы, п. 1591
- ^ а б Хайре, Р. (1986). «Получение, свойства и некоторые недавние исследования актинидов металлов». Журнал менее распространенных металлов. 121: 379–398. Дои:10.1016/0022-5088(86)90554-0.
- ^ а б Гринвуд, п. 1268
- ^ а б Haire, R.G .; Байбарз, Р. Д. (1979). «Исследования металлического эйнштейния» (PDF). Le Journal de Physique. 40: C4–101. Дои:10.1051 / jphyscol: 1979431. черновик рукописи
- ^ Сиборг, п. 61
- ^ Kleinschmidt, Phillip D .; Уорд, Джон В .; Matlack, Джордж М .; Haire, Ричард Г. (1984). "Закон Генри исследования испарения и термодинамики металла эйнштейний-253, растворенного в иттербии". Журнал химической физики. 81 (1): 473–477. Bibcode:1984ЖЧФ..81..473К. Дои:10.1063/1.447328.
- ^ Сиборг, п. 52
- ^ а б Сиборг, п. 60
- ^ а б c Ensor, D. D .; Peterson, J. R .; Haire, R.G .; Янг, Дж. П. (1981). «Абсорбционное спектрофотометрическое исследование 253EsF3 и продукты его распада в твердом состоянии объемной фазы ». Журнал неорганической и ядерной химии. 43 (10): 2425–2427. Дои:10.1016/0022-1902(81)80274-6.
- ^ а б c Haire, R.G .; Байбарз, Р. Д. (1973). «Идентификация и анализ полуторного оксида эйнштейния методом электронной дифракции». Журнал неорганической и ядерной химии. 35 (2): 489–496. Дои:10.1016/0022-1902(73)80561-5.
- ^ Сиборг, п. 55
- ^ Сиборг, п. 76
- ^ Huray, P .; Неф, S .; Хайре, Р. (1983). «Магнетизм тяжелых 5f элементов». Журнал менее распространенных металлов. 93 (2): 293–300. Дои:10.1016/0022-5088(83)90175-3.
- ^ Huray, Paul G .; Nave, S. E .; Haire, R.G .; Мур, Дж. Р. (1984). «Магнитные свойства Es2О3 и EsF3". Неорганика Chimica Acta. 94 (1–3): 120–122. Дои:10.1016 / S0020-1693 (00) 94587-0.
- ^ Холлеман, п. 1956 г.
- ^ Сиборг, п. 53
- ^ Волосы, п. 1578
- ^ Ахмад, I .; Вагнер, Франк (1977). «Период полураспада наиболее долгоживущего изотопа эйнштейния-252Es». Журнал неорганической и ядерной химии. 39 (9): 1509–1511. Дои:10.1016/0022-1902(77)80089-4.
- ^ Макхаррис, Уильям; Стивенс, Ф .; Asaro, F .; Перлман, И. (1966). «Схема распада эйнштейния-254». Физический обзор. 144 (3): 1031–1045. Bibcode:1966ПхРв..144.1031М. Дои:10.1103 / PhysRev.144.1031.
- ^ а б Audi, G .; Кондев, Ф. Г .; Wang, M .; Huang, W. J .; Наими, С. (2017). «Оценка ядерных свойств NUBASE2016» (PDF). Китайская физика C. 41 (3): 030001. Bibcode:2017ЧФК..41с0001А. Дои:10.1088/1674-1137/41/3/030001.
- ^ Institut de Radioprotection et de Sûreté Nucléaire, «Оценка данных по безопасности ядерной критичности и пределов для актинидов на транспорте», п. 16.
- ^ Эмсли, Джон (2011). Строительные блоки природы: руководство по элементам от А до Я (Новое изд.). Нью-Йорк, Нью-Йорк: Издательство Оксфордского университета. ISBN 978-0-19-960563-7.
- ^ Гопка, В. Ф .; Ющенко, А. В .; Ющенко, В. А .; Панов, И. В .; Ким, гл. (2008). «Идентификация линий поглощения актинидов с коротким периодом полураспада в спектре звезды Пшибыльского (HD 101065)». Кинематика и физика небесных тел. 24 (2): 89–98. Bibcode:2008KPCB ... 24 ... 89 г. Дои:10.3103 / S0884591308020049.
- ^ Сиборг, п. 51
- ^ «Изотопный реактор с высоким потоком». Национальная лаборатория Окриджа. Получено 2010-09-23.
- ^ Радионуклидные источники и препараты (на русском). Научно-исследовательский институт атомных реакторов. Получено 2010-09-26.
- ^ а б Волосы, п. 1582
- ^ Гринвуд, п. 1262
- ^ Porter, C.E .; Riley, F. D., Jr .; Vandergrift, R.D .; Фелкер, Л. К. (1997). «Очистка фермия с использованием экстракционной хроматографии на смоле Teva». Сен. Technol. 32 (1–4): 83–92. Дои:10.1080/01496399708003188.
- ^ Hoffman, Darleane C .; Гиорсо, Альберт и Сиборг, Гленн Теодор (2000) Трансурановые люди: внутренняя история, Imperial College Press, стр. 190–191, ISBN 978-1-86094-087-3.
- ^ Сиборг, стр. 36–37
- ^ Jones, M .; Schuman, R .; Батлер, Дж .; Cowper, G .; Eastwood, T .; Джексон, Х. (1956). «Изотопы эйнштейния и фермия, полученные нейтронным облучением плутония». Физический обзор. 102 (1): 203–207. Bibcode:1956PhRv..102..203J. Дои:10.1103 / PhysRev.102.203.
- ^ Гусева, Л .; Филиппова, К .; Герлит, Ю .; Друин, В .; Мясоедов, Б .; Тарантин, Н. (1956). «Опыты по производству эйнштейния и фермия на циклотроне». Журнал ядерной энергии (1954). 3 (4): 341–346. Дои:10.1016 / 0891-3919 (56) 90064-Х.
- ^ Гарри Х. Биндер: Lexikon der chemischen Elemente, С. Хирцель Верлаг, Штутгарт, 1999 г., ISBN 3-7776-0736-3С. 18–23.
- ^ Эйнштейний (на русском языке популярная статья одного из привлеченных ученых)
- ^ Chetham-Strode, A .; Холм, Л. (1956). «Новый изотоп Эйнштейний-248». Физический обзор. 104 (5): 1314. Bibcode:1956ПхРв..104.1314С. Дои:10.1103 / PhysRev.104.1314.
- ^ Харви, Бернард; Четам-Строде, Альфред; Гиорсо, Альберт; Чоппин, Грегори; Томпсон, Стэнли (1956). «Новые изотопы Эйнштейния». Физический обзор. 104 (5): 1315–1319. Bibcode:1956ПхРв..104.1315Н. Дои:10.1103 / PhysRev.104.1315.
- ^ Кулюхин, С .; Ауэрман, Л. Н .; Новиченко, В.Л .; Михеев, Н. Б .; Rumer, I.A .; Каменская, А. Н .; Гончаров, Л. А .; Смирнов, А. И. (1985). «Производство микрограммов эйнштейния-253 путем облучения калифорния в реакторе». Неорганика Chimica Acta. 110: 25–26. Дои:10.1016 / S0020-1693 (00) 81347-X.
- ^ а б c Сиборг, п. 40
- ^ Они были под кодовым названием: «Анакостия» (5.2 килотонны, 1962), «Kennebec» (<5 килотонн, 1963), «Par» (38 килотонн, 1964), «Barbel» (<20 килотонн, 1964), «Tweed» (<20 килотонн, 1965), «Cyclamen» (13 килотонн, 1966), «Канкаки» (20-200 килотонн, 1966), «Вулкан» (25 килотонн, 1966) и «Хатч» (20-200 килотонн, 1969)
- ^ Ядерные испытания в США с июля 1945 года по сентябрь 1992 года. В архиве 15 июня 2010 г. Wayback Machine, DOE / NV - 209-REV 15 декабря 2000 г.
- ^ Сиборг, п. 43
- ^ Сиборг, п. 44
- ^ Сиборг, п. 47
- ^ Волосы, п. 1583
- ^ Волосы, стр. 1584–1585
- ^ а б Холл, Нина (2000). Новая химия. Издательство Кембриджского университета. С. 9–11. ISBN 978-0-521-45224-3.
- ^ Волосы, п. 1588
- ^ Волосы, п. 1590
- ^ а б c Хайр, Р. Г. и Эйринг, Л. (1994). «Химия лантаноидов и актинидов». В К.А. Gscheidner, Jr .; и другие. (ред.). Справочник по физике и химии редких земель. 18. Северная Голландия, Нью-Йорк. С. 414–505. ISBN 978-0-444-81724-2.
- ^ Кляйншмидт П. (1994). «Термохимия актинидов». Журнал сплавов и соединений. 213–214: 169–172. Дои:10.1016/0925-8388(94)90898-2.
- ^ Fujita, D .; Cunningham, B.B .; Парсонс, Т. К. (1969). «Кристаллические структуры и параметры решетки трихлорида эйнштейния и оксихлорида эйнштейния». Письма по неорганической и ядерной химии. 5 (4): 307–313. Дои:10.1016/0020-1650(69)80203-5.
- ^ а б Мясоедов Б.Ф. Аналитическая химия трансплутониевых элементов, Wiley, 1974 (оригинал из Калифорнийского университета). ISBN 0-470-62715-8, п. 99
- ^ Fellows, R .; Peterson, J. R .; Noé, M .; Young, J. P .; Хайре, Р. Г. (1975). «Рентгеноструктурные и спектроскопические исследования кристаллического бромида эйнштейния (III)», 253EsBr3". Письма по неорганической и ядерной химии. 11 (11): 737–742. Дои:10.1016/0020-1650(75)80090-0.
- ^ а б c Волосы, стр. 1595–1596
- ^ а б c Сиборг, п. 62
- ^ а б c d е Young, J. P .; Haire, R.G .; Peterson, J. R .; Ensor, D. D .; Товарищ, Р. Л. (1981). «Химические последствия радиоактивного распада. 2. Спектрофотометрическое исследование врастания берклия-249 и калифорния-249 в галогениды эйнштейния-253». Неорганическая химия. 20 (11): 3979–3983. Дои:10.1021 / ic50225a076.
- ^ Волосы, п. 1598
- ^ Холлеман, п. 1969 г.
- ^ а б c Гринвуд, п. 1270
- ^ Young, J. P .; Haire, R.G .; Fellows, R. L .; Петерсон, Дж. Р. (1978). «Спектрофотометрические исследования галогенидов и оксигалогенидов трансуриевых элементов в твердом состоянии». Журнал радиоаналитической химии. 43 (2): 479–488. Дои:10.1007 / BF02519508.
- ^ Fujita, D .; Cunningham, B.B .; Parsons, T. C .; Петерсон, Дж. Р. (1969). «Спектр поглощения раствора Es3+". Письма по неорганической и ядерной химии. 5 (4): 245–250. Дои:10.1016/0020-1650(69)80192-3.
- ^ а б Peterson, J.R .; и другие. (1979). «Приготовление, характеристика и распад эйнштейния (II) в твердом состоянии» (PDF). Le Journal de Physique. 40 (4): C4–111. CiteSeerX 10.1.1.729.8671. Дои:10.1051 / jphyscol: 1979435. черновик рукописи
- ^ Fellows, R.L .; Young, J.P .; Haire, R.G. и Петерсон Дж. Р. (1977) в: Дж. Дж. Маккарти и Дж. Дж. Райн (редакторы) Редкие земли в современной науке и технологиях, Plenum Press, New York, pp. 493–499.
- ^ Young, J.P .; Haire R.G., Fellows, R.L .; Ноэ, М. и Петерсон, Дж. Р. (1976) "Спектроскопические и рентгеновские дифракционные исследования бромидов калифорния-249 и эйнштейния-253", в: В. Мюллер и Р. Линднер (ред.) Плутоний 1975 г., Северная Голландия, Амстердам, стр. 227–234.
- ^ Наджент, Леонард Дж .; Burnett, J. L .; Baybarz, R.D .; Вернер, Джордж Нолл; Tanner, S.P .; Tarrant, J. R .; Келлер, О. Л. (1969). «Внутримолекулярный перенос энергии и сенсибилизированная люминесценция в хелатах актинидов (III) β-дикетонов». Журнал физической химии. 73 (5): 1540–1549. Дои:10.1021 / j100725a060.
- ^ Beitz, J .; Wester, D .; Уильямс, К. (1983). Взаимодействие состояния 5f с лигандами внутренней координационной сферы: Es3+ ионная флуоресценция в водной и органической фазах ». Журнал менее распространенных металлов. 93 (2): 331–338. Дои:10.1016/0022-5088(83)90178-9.
- ^ Это элементаль - Элемент Эйнштейний. Проверено 2 декабря 2007 года.
- ^ Ghiorso, A .; Харви, B .; Choppin, G .; Thompson, S .; Сиборг, Г. (1955). "Новый элемент Менделевий, атомный номер 101". Физический обзор. 98 (5): 1518–1519. Bibcode:1955ПхРв ... 98.1518Г. Дои:10.1103 / PhysRev.98.1518. ISBN 978-981-02-1440-1.
- ^ Schadel, M .; Bruchle, W .; Brugger, M .; Gaggeler, H .; Муди, К .; Schardt, D .; Summerer, K .; Hulet, E .; Дуган, А .; Dougan, R .; Landrum, J .; Lougheed, R .; Wild, J .; O'Kelley, G .; Хан Р. (1986). "Производство тяжелых изотопов реакциями многонуклонного переноса с 254Es ". Журнал менее распространенных металлов. 122: 411–417. Дои:10.1016/0022-5088(86)90435-2.
- ^ Lougheed, R.W .; Landrum, J. H .; Hulet, E.K .; Wild, J. F .; Dougan, R.J .; Dougan, A.D .; Gäggeler, H .; Schädel, M .; Муди, К. Дж .; Грегорич, К. Э. и Сиборг, Г. Т. (1985). "Поиск сверхтяжелых элементов с помощью 48Ca + 254Esграмм реакция ». Физический обзор C. 32 (5): 1760–1763. Bibcode:1985PhRvC..32.1760L. Дои:10.1103 / PhysRevC.32.1760. PMID 9953034.
- ^ Туркевич, А.Л .; Franzgrote, E.J .; Паттерсон, Дж. Х. (1967). «Химический анализ Луны на месте посадки Surveyor V». Наука. 158 (3801): 635–637. Bibcode:1967Научный ... 158..635Т. Дои:10.1126 / science.158.3801.635. PMID 17732956.
- ^ Международная комиссия по радиологической защите (1988 г.). Пределы поступления радионуклидов рабочими, Часть 4. 19. Elsevier Health Sciences. С. 18–19. ISBN 978-0-08-036886-3.
Библиография
- Greenwood, Norman N .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0080379418.
- Haire, Ричард Г. (2006). «Эйнштейний». In Morss, Lester R .; Эдельштейн, Норман М .; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (PDF). 3 (3-е изд.). Дордрехт, Нидерланды: Springer. С. 1577–1620. Дои:10.1007/1-4020-3598-5_12. ISBN 978-1-4020-3555-5. Архивировано из оригинал (PDF) 17 июля 2010 г.
- Холлеман, Арнольд Ф. и Виберг, Нильс (2007). Учебник неорганической химии (102-е изд.). Берлин: де Грюйтер. ISBN 978-3-11-017770-1.
- Сиборг, Г.Т., изд. (23 января 1978 г.). Материалы симпозиума, посвященного 25-летию элементов 99 и 100 (PDF). Отчет LBL-7701.
внешняя ссылка
- Эйнштейний в Периодическая таблица видео (Ноттингемский университет)
- Возрастные факторы в метаболизме и дозиметрии радионуклидов: Труды - содержит несколько исследований эйнштейния, связанных со здоровьем



![{displaystyle {ce {^ {238} _ {92} U -> [{ce {+6 (n, gamma)}}] [- 2 eta ^ {-}] {} _ {94} ^ {244} Pu }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/adc5607f4aa66702f7f8331613b838b19e5fbccc)
![{displaystyle {ce {^ {238} _ {92} U -> [{ce {+ 15n}}] [6 eta ^ -] ^ {253} _ {98} Cf -> [eta ^ -] ^ {253 } _ {99} Es}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/54c4fccdd01ebda8ab75c3aac855a348c6f5ea2c)
![{displaystyle {ce {^ {252} _ {98} Cf -> [{ce {(n, gamma)}}] ^ {253} _ {98} Cf -> [eta ^ -] [17.81 {ce {d }}] ^ {253} _ {99} Es -> [{ce {(n, gamma)}}] ^ {254} _ {99} Es -> [eta ^ -] ^ {254} _ {100} Fm}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/63f13874738d0dfe8637d3dd71bef4ba0cbc6b14)
![{displaystyle {ce {^ {253} _ {99} Es -> [alpha] [20 {ce {d}}] ^ {249} _ {97} Bk -> [eta ^ -] [314 {ce {d} }}] ^ {249} _ {98} Cf}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/864c693290ca15763e10e38145d86820f7ebe7d3)
![{displaystyle {ce {^ {249} _ {98} Cf + ^ {2} _ {1} D -> ^ {248} _ {99} Es + 3 ^ {1} _ {0} n}} четверть влево ({ce {^ {248} _ {99} Es -> [эпсилон] [27 {ce {min}}] ^ {248} _ {98} Cf}} ight)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b42bfcc37be3fe9bc6251a1bb1dd647e564b664b)
![{displaystyle {ce {^ {249} _ {97} Bk -> [+ alpha] ^ {249,250,251,252} _ {99} Es}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/46af865ac0b1463965f1790285f36a01d24eb318)
![{displaystyle {ce {^ {252} _ {98} Cf -> [{ce {(n, gamma)}}] ^ {253} _ {98} Cf -> [eta ^ -] [17.81 {ce {d }}] ^ {253} _ {99} Es}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/45d75d0f0badaf920ba511372718f8dc284b9587)
