Одинокая пара - Википедия - Lone pair

В химия, а одинокая пара относится к паре валентные электроны которые не используются другим атомом в Ковалентная связь[1] и иногда его называют неразделенная пара или же некрепляющая пара. Одинокие пары находятся в крайних электронная оболочка атомов. Их можно идентифицировать с помощью Структура Льюиса. Поэтому электронные пары считаются неподеленными, если два электрона спарены, но не используются в химическая связь. Таким образом, количество неподеленной пары электроны плюс количество связывающие электроны равно общему количеству валентность электроны вокруг атома.
Одинокая пара - это концепция, используемая в валентная оболочка теория отталкивания электронных пар (Теория VSEPR), которая объясняет формы молекул. Они также упоминаются в химии Кислоты и основания Льюиса. Однако не все несвязывающие пары электронов химики считают неподеленными. Примерами являются переходные металлы, в которых несвязывающие пары не влияют на геометрию молекул и считаются стереохимически неактивными. В теории молекулярных орбиталей (полностью делокализованные канонические орбитали или локализованные в какой-либо форме) концепция неподеленной пары менее четкая, поскольку соответствие между орбиталью и компонентами структуры Льюиса часто не является прямым. Тем не менее, оккупированные несвязывающие орбитали (или орбитали преимущественно несвязывающего характера) часто идентифицируются как неподеленные пары.
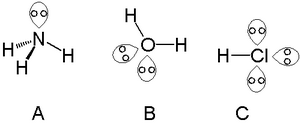
А Один неподеленную пару можно найти с атомами в группа азота такие как азот в аммиак, два неподеленные пары можно найти с атомами в халькоген группа, такая как кислород в воде и галогены могу нести три одинокие пары, такие как в хлористый водород.
В Теория VSEPR электронные пары на атоме кислорода в воде образуют вершины тетраэдра с неподеленными парами на двух из четырех вершин. H – O – H угол связи составляет 104,5 °, что меньше 109 °, прогнозируемых для четырехгранный угол, что можно объяснить отталкивающим взаимодействием неподеленных пар.[2][3][4]
Были предложены различные вычислительные критерии наличия неподеленных пар. А электронная плотность ρ (р) сам по себе, как правило, не дает полезного руководства в этом отношении, лапласианин электронной плотности, и одним из критериев расположения неподеленной пары является то, где L(р) = –∇2ρ (р) является локальным максимумом. Минимумы электростатического потенциала V(р) - еще один предлагаемый критерий. Еще один считает функция локализации электронов (ELF).[5]
Угловые изменения

Пары часто показывают отрицательный полярный характер с высокой плотностью заряда и расположены ближе к атомное ядро в среднем по сравнению со связывающей парой электронов. Наличие неподеленной пары уменьшает угол связи между связывающей парой электронов из-за их высокого электрического заряда, который вызывает сильное отталкивание между электронами. Они также используются при формировании дательная облигация. Например, создание гидроксоний (ЧАС3О+) ион возникает, когда кислоты растворяются в воде, и возникает из-за кислород атом жертвует одинокую пару водород ион.
Это можно увидеть более четко, если взглянуть на это еще двумя распространенными молекулы. Например, в углекислый газ (CO2) атомы кислорода находятся по разные стороны от углерода, тогда как в воды (ЧАС2O) существует угол между атомами водорода 104,5º. Из-за силы отталкивания неподеленных пар атома кислорода водород отталкивается еще дальше, до точки, где силы всех электронов на атоме водорода равны. равновесие. Это иллюстрация Теория VSEPR.
Дипольные моменты
Одинокие пары могут вносить вклад в дипольный момент. NH3 имеет дипольный момент 1,47 D. Поскольку электроотрицательность азота (3,04) больше, чем у водорода (2,2), в результате связи N-H полярны с суммарным отрицательным зарядом на атоме азота и меньшим суммарным положительным зарядом на атомах водорода. Существует также диполь, связанный с неподеленной парой, и это усиливает вклад, вносимый полярными ковалентными связями N-H в аммиак. дипольный момент. В отличие от NH3, NF3 имеет гораздо более низкий дипольный момент 0,24 D. Фтор больше электроотрицательный чем азот и полярность связей N-F противоположно связям N-H в аммиаке, так что диполь из-за неподеленной пары противостоит диполям связи N-F, что приводит к низкому молекулярному дипольному моменту.[6]
Стереогенные одиночные пары
 | ⇌ |  |
| Инверсия общей молекулы органического амина при азоте | ||
Неподеленная пара может способствовать существованию хиральности в молекуле, когда три другие группы, присоединенные к атому, все различаются. Эффект виден в некоторых амины, фосфины,[7] сульфоний и оксоний ионы, сульфоксиды, и даже карбанионы.
В разрешающая способность энантиомеров, стереогенный центр которых представляет собой амин, обычно исключается, поскольку энергетический барьер для азотная инверсия в стереоцентре низкий, что позволяет двум стереоизомерам быстро взаимопревращаться при комнатной температуре. В результате такие хиральные амины не могут быть разделены, если аминовые группы не ограничены циклической структурой (например, в База Трегера ).
Необычные одиночные пары
Стереохимически активная неподеленная пара также ожидается для двухвалентной вести и банка ионов из-за их формальной электронной конфигурации ns2. В твердом состоянии это приводит к искаженной координации металлов, наблюдаемой в глетевой структуре, принятой как PbO, так и SnO. Образование этих тяжелых металлов ns2 неподеленные пары, которые ранее приписывались внутриатомной гибридизации s- и p-состояний металла[8] недавно было показано, что он имеет сильную анионную зависимость.[9] Эта зависимость от электронных состояний аниона может объяснить, почему некоторые материалы из двухвалентного свинца и олова, такие как PbS и SnTe, не показывают стереохимических свидетельств неподеленной пары и принимают симметричную кристаллическую структуру каменной соли.[10][11]
В молекулярных системах неподеленная пара также может приводить к нарушению координации лигандов вокруг иона металла. Эффект неподеленной пары свинца может наблюдаться в супрамолекулярных комплексах нитрат свинца (II), а в 2007 году исследование связывало одинокую пару с отравление свинцом.[12] Ионы свинца могут заменять естественные ионы металлов в нескольких ключевых ферментах, таких как катионы цинка в ALAD фермент, который также известен как порфобилиногенсинтаза, и важен в синтезе гем, ключевой компонент молекулы, переносящей кислород гемоглобин. Это ингибирование синтеза гема, по-видимому, является молекулярной основой отравления свинцом (также называемого «сатурнизмом» или «плюмбизмом»).[13][14][15]
Вычислительные эксперименты показывают, что хотя координационный номер не изменяется при замене в кальций-связывающих белках, введение свинца искажает способ организации лигандов для размещения такой возникающей неподеленной пары: следовательно, эти белки нарушаются. Этот эффект одиночной пары становится драматичным для цинк-связывающих белков, таких как вышеупомянутая порфобилиногенсинтаза, поскольку природный субстрат больше не может связываться - в этих случаях белок подавленный.
В Группа 14 элементы ( группа углерода ), одиночные пары могут проявляться сокращением или удлинением одиночных (ордер на облигации 1) длины облигаций,[16] а также в эффективном порядке тройных связей.[17][18] Знакомый алкины имеют тройную углерод-углеродную связь (ордер на облигации 3) и линейная геометрия с валентными углами 180 ° (рисунок А в отношении [19]). Однако дальше в группе (кремний, германий, и банка ), формальные тройные связи имеют эффективный порядок связи 2 с одной неподеленной парой (рисунок B[19]) и транс -гнутая геометрия. В вести, эффективный порядок связи еще больше снижается до одинарной связи с двумя неподеленными парами для каждого атома свинца (рисунок C[19]). в германийорганическое соединение (Схема 1 в ссылке), эффективный порядок связи также равен 1, с комплексообразованием кислый изонитрил (или же изоцианид) C-N группы, основанные на взаимодействии с пустой 4p-орбиталью германия.[19][20]

Различные описания для нескольких одиночных пар
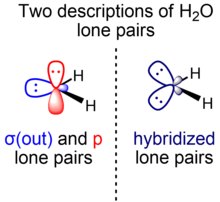
На курсах элементарной химии неподеленные пары воды описываются как «кроличьи уши»: две эквивалентные пары электронов приблизительно sp3 гибридизации, а валентный угол HOH составляет 104,5 °, что немного меньше идеального тетраэдрического угла arccos (–1/3) ≈ 109,47 °. Меньший угол связи объясняется Теория VSEPR приписывая большую потребность в пространстве для двух идентичных неподеленных пар по сравнению с двумя связующими парами. В более продвинутых курсах альтернативное объяснение этого явления рассматривает большую стабильность орбиталей с избыточным s-характером, используя теорию изовалентная гибридизация, в которых связи и неподеленные пары могут быть построены с помощью spИкс гибриды, у которых нецелочисленные значения Икс разрешены, пока сохраняется общее количество символов s и p (одна s и три p орбитали в случае элементов p-блока второй строки).
Чтобы определить гибридизацию кислородных орбиталей, используемых для образования пар связывания и неподеленных пар воды на этом рисунке, мы используем формулу 1 + Икс cos θ = 0, который связывает валентный угол θ с индексом гибридизации Икс. Согласно этой формуле, связи O – H считаются построенными из O-связывающих орбиталей ~ sp4.0 гибридизация (~ 80% символов p, ~ 20% s символов), которая оставляет за собой O неподеленные пары орбиталей ~ sp2.3 гибридизация (~ 70% символов p, ~ 30% s символов). Эти отклонения от идеализированных зр.3 гибридизация для тетраэдрической геометрии согласуется с Правило Бента: неподеленные пары локализуют большую электронную плотность ближе к центральному атому, чем связывающие пары; следовательно, использование орбиталей с избыточным s-характером для образования неподеленных пар (и, следовательно, с избыточным p-характером для образования пар связывания) является энергетически выгодным.
Однако теоретики часто предпочитают альтернативное описание воды, которое разделяет неподеленные пары воды в соответствии с симметрией относительно плоскости молекулы. В этой модели существуют две энергетически и геометрически различные неподеленные пары воды, обладающие разной симметрией: одна (σ) в плоскости и симметрична относительно плоскости молекулы, а другая (π) перпендикулярна и антисимметрична относительно молекулярной плоскости. самолет. Неподеленная пара σ-симметрии (σ (out)) образована из гибридной орбитали, которая смешивает символы 2s и 2p, в то время как неподеленная пара π-симметрии (p) имеет исключительное 2p-орбитальное происхождение. Символ s богатый O σ (out) орбиталь неподеленной пары (также обозначен пО(σ)) является ~ sp0.7 гибрид (~ 40% символов p, 60% s символов), в то время как пара p lone орбитальная (также обозначена пО(π)) состоит на 100% из символа p.
Обе модели представляют ценность и представляют одну и ту же полную электронную плотность, а орбитали связаны соотношением унитарное преобразование. В этом случае мы можем построить две эквивалентные гибридные орбитали неподеленных пар час и час'взяв линейные комбинации час = c1σ (выход) + c2р и час' = c1σ (выход) - c2p для подходящего выбора коэффициентов c1 и c2. Для химических и физических свойств воды, которые зависят от общий электронное распределение молекулы, использование час и час'так же верно, как и использование σ (out) и p. В некоторых случаях такое представление интуитивно полезно. Например, требование стереоэлектроники для аномерный эффект можно рационализировать, используя эквивалентные одиночные пары, поскольку это общий передача электронной плотности на разрыхляющую орбиталь, что имеет значение. Альтернативный подход с использованием одиночных пар, разделенных σ / π, также применим, но он требует соблюдения баланса между максимизацией пО(π)-σ * перекрытие (максимум при двугранном угле 90 °) и пО(σ)-σ * перекрытие (максимум при двугранном угле 0 °), компромисс, который приводит к заключению, что бестактный конформация (двугранный угол 60 °) является наиболее благоприятным, тот же вывод, который модель эквивалентных неподеленных пар рационализируется гораздо более прямолинейно.[21] Точно так же водородные связи воды образуются по направлениям неподеленных пар «кроличьих ушей», что является отражением повышенной доступности электронов в этих областях. Это представление поддерживается в вычислительном отношении.[5] Однако, поскольку только адаптированные к симметрии канонические орбитали обладают физически значимыми энергиями, явления, которые имеют отношение к энергиям индивидуальный орбитали, такие как фотохимическая реактивность или фотоэлектронная спектроскопия, легче всего объяснить с помощью неподеленных пар σ и π, которые соблюдают симметрию молекулы.[21][22]
Из-за популярности Теория VSEPR, рассмотрение одиночных пар воды как эквивалента преобладает на вводных курсах химии, и многие практикующие химики продолжают рассматривать это как полезную модель. Аналогичная ситуация возникает при описании двух неподеленных пар карбонильного кислорода кетона.[23] Однако вопрос о том, является ли концептуально полезным выводить эквивалентные орбитали из адаптированных к симметрии орбиталей с точки зрения теории связывания и педагогики, все еще остается спорным, поскольку в недавних (2014 и 2015 гг.) Статьях[24] и поддержка[25] практика.
Смотрите также
Рекомендации
- ^ ИЮПАК Золотая книга определение: одинокая (электронная) пара
- ^ Органическая химия Мэри Энн Фокс, Джеймс К. Уайтселл, 2-е издание, 2001 г.
- ^ Органическая химия Джон Макмерри, 5-е издание, 2000 г.
- ^ Краткая неорганическая химия Дж. Д. Ли, 4-е издание, 1991 г.
- ^ а б Кумар, Анмол; Gadre, Shridhar R .; Мохан, Нита; Суреш, Черумуттатху Х. (06.01.2014). «Одинокие пары: электростатическая точка зрения». Журнал физической химии A. 118 (2): 526–532. Bibcode:2014JPCA..118..526K. Дои:10.1021 / jp4117003. ISSN 1089-5639. PMID 24372481.
- ^ Housecroft, C.E .; Шарп, А. Г. (2004). Неорганическая химия (2-е изд.). Прентис Холл. п. 40. ISBN 978-0-13-039913-7.
- ^ Куин, Л. Д. (2000). Руководство по химии фосфорорганических соединений, РАСПОЛОЖЕНИЕ: John Wiley & Sons. ISBN 0471318248.
- ^ Стереохимия ионных твердых тел J.D.Dunitz, L.E.Orgel, Advan. Неорг. и Радиохим. 1960, 2, 1–60
- ^ Пейн, Д. Дж. (2006). «Электронное происхождение структурных искажений в оксидах металлов после переходного периода: экспериментальные и теоретические доказательства для пересмотра модели неподеленной пары». Письма с физическими проверками. 96 (15): 157403. Дои:10.1103 / PhysRevLett.96.157403. PMID 16712195.
- ^ Уолш, Арон (2005). «Происхождение стереохимически активной неподеленной пары Pb (II): расчеты методом DFT на PbO и PbS». Журнал химии твердого тела. 178 (5): 1422–1428. Bibcode:2005JSSCh.178.1422W. Дои:10.1016 / j.jssc.2005.01.030.
- ^ Уолш, Арон (2005). «Влияние аниона на образование неподеленной пары в монохалькогенидах Sn (II): исследование методом DFT». Журнал физической химии B. 109 (40): 18868–18875. Дои:10.1021 / jp051822r. PMID 16853428.
- ^ Гурлауэн, Кристоф; Паризель, Оливье (15 января 2007 г.). "Является ли электронный щит молекулярным источником отравления свинцом? Вычислительный эксперимент моделирования". Angewandte Chemie International Edition. 46 (4): 553–556. Дои:10.1002 / anie.200603037. PMID 17152108.
- ^ Jaffe, E.K .; Martins, J .; и другие. (13 октября 2000 г.). «Молекулярный механизм свинцового ингибирования человеческой порфобилиногенсинтазы». Журнал биологической химии. 276 (2): 1531–1537. Дои:10.1074 / jbc.M007663200. PMID 11032836.
- ^ Сциникариелло, Франко; Мюррей, Х. Эдвард; и другие. (15 сентября 2006 г.). «Свинец и полиморфизм дегидратазы δ-аминолевулиновой кислоты: к чему он ведет? Метаанализ». Перспективы гигиены окружающей среды. 115 (1): 35–41. Дои:10.1289 / ehp.9448. ЧВК 1797830. PMID 17366816.
- ^ Чхабра, Намрата (15 ноября 2015 г.). «Влияние отравления свинцом на путь биосинтеза гема». Клинические случаи: биохимия для врачей. Архивировано из оригинал 3 апреля 2016 г.. Получено 30 октября 2016.
- ^ Ричардс, Энн Ф .; Брында, Марчин; Власть, Филип П. (2004). «Влияние противоионов щелочного металла на длину двойной связи германий-германий в более тяжелой соли этенида 14-го элемента». Chem. Commun. (14): 1592–1593. Дои:10.1039 / B401507J. PMID 15263933.
- ^ Власть, Филип П. (декабрь 1999 г.). «π-соединение и эффект неподеленной пары в множественных связях между более тяжелыми элементами основной группы». Химические обзоры. 99 (12): 3463–3504. Дои:10.1021 / cr9408989. PMID 11849028.
- ^ Владимир Я. Ли; Акира Секигучи (22 июля 2011 г.). Металлоорганические соединения низкокоординатных Si, Ge, Sn и Pb: от фантомных форм к стабильным соединениям. Джон Вили и сыновья. п. 23. ISBN 978-1-119-95626-6.
- ^ а б c d Спайки, Джеффри Х .; Власть, Филип П. (2007). "Основание Льюиса индуцировало настройку порядка связей Ge – Ge в" дигермине"". Chem. Commun. (1): 85–87. Дои:10.1039 / b612202g. PMID 17279269.
- ^ Власть, Филип П. (2003). «Кремниевые, германиевые, оловянные и свинцовые аналоги ацетиленов». Химические коммуникации (17): 2091–101. Дои:10.1039 / B212224C. PMID 13678155.
- ^ а б А., Олбрайт, Томас (2013-04-08). Орбитальные взаимодействия в химии. Бёрдетт, Джереми К., 1947-, Вангбо, Мён-Хван (второе изд.). Хобокен, Нью-Джерси. ISBN 9780471080398. OCLC 823294395.
- ^ Пока пО(π) неподеленная пара эквивалентна канонической МО с меткой Малликена 1б1, то пО(σ) неподеленная пара не совсем эквивалент канонической МО метки Малликена 2а1, поскольку полностью делокализованная орбиталь включает смешивание с адаптированной синфазной симметрией линейной комбинацией водородных 1s-орбиталей, что делает ее слегка связывающей по характеру, а не строго несвязывающей.
- ^ Ansyln, E. V .; Догерти, Д. А. (2006). Современная физико-органическая химия. Саусалито, Калифорния: Университетские научные книги. стр.41. ISBN 978-1-891389-31-3.
- ^ Clauss, Allen D .; Нельсен, Стивен Ф .; Аюб, Мохамед; Мур, Джон В .; Лэндис, Кларк Р .; Вайнхольд, Франк (2014-10-08). «Гибриды кроличьих ушей, стерики VSEPR и другие орбитальные анахронизмы». Химическое образование, исследования и практика. 15 (4): 417–434. Дои:10.1039 / C4RP00057A. ISSN 1756-1108.
- ^ Hiberty, Philippe C .; Данович, Давид; Шайк, Сэсон (07.07.2015). "Комментарий к" Гибридам с кроличьими ушами, стерикам VSEPR и другим орбитальным анахронизмам ". Ответ на критику". Химическое образование, исследования и практика. 16 (3): 689–693. Дои:10.1039 / C4RP00245H. S2CID 143730926.
