Перилен - Википедия - Perylene
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Перилен | |||
| Другие имена пери-динафталин; Перилен; Дибенз [де,kl] антрацен | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.365 | ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C20ЧАС12 | |||
| Молярная масса | 252.316 г · моль−1 | ||
| Внешность | Коричневое твердое вещество | ||
| Температура плавления | От 276 до 279 ° C (от 529 до 534 ° F, от 549 до 552 K) | ||
| -166.8·10−6 см3/ моль | |||
| Опасности | |||
| S-фразы (устарело) | S22 S24 / 25 | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Перилен или же перилен это полициклический ароматический углеводород с химическая формула C20ЧАС12в виде коричневого твердого вещества. Он или его производные могут быть канцерогенный, и считается опасным загрязнитель. В клеточная мембрана цитохимия перилен используется как флуоресцентный липидный зонд. Это исходное соединение класса риленовые красители.
Реакции
Как и другие полициклические ароматические соединения, перилен восстанавливается щелочными металлами с образованием сильно окрашенного анион-радикала и дианиона. В диглим сольваты этих солей характеризуются Рентгеновская кристаллография.[2]
Эмиссия
Перилен отображается синим цветом флуоресценция. Он используется в качестве легирующего материала, излучающего синий цвет. Светодиоды, либо чистый, либо замещенный. Перилен можно также использовать в качестве органического фотопроводник. Он имеет максимум поглощения при 434 нм и, как и все полициклические ароматические соединения, низкую растворимость в воде (1,2 × 10−5 ммоль / л). Перилен имеет молярная поглощающая способность 38500 М−1см−1 при 435,7 нм.

Перилен растворен в дихлорметан подвергать Длинноволновое УФ-излучение

Растворенный в дихлорметане перилен под воздействием Коротковолновое УФ-излучение
Структура

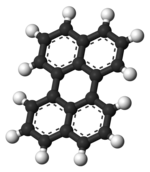
Перилен молекула состоит из двух нафталин молекулы соединены углерод-углеродной связью в положениях 1 и 8 обеих молекул. Все углерод атомы в перилене зр2 гибридизированный. Структура перилена широко изучена Рентгеновская кристаллография.[3]
Биология
Природный перилен хиноны были идентифицированы в лишайники Лаурера сангвинария Мальме и Graphis haematites Платеж. [4]
Рекомендации
- ^ Перилен в Сигма-Олдрич
- ^ Нэтер, Кристиан; Бок, Ганс; Гавлас, Зденек; Хаук, Тим (1998). "Совместно используемые и разделенные растворителем ионные множественные радикалы периленовых анионов и дианионов: пример сольватации катионов щелочных металлов". Металлоорганические соединения. 17 (21): 4707–4715. Дои:10.1021 / om970610g.
- ^ Donaldson, D.M .; Робертсон, Дж. М .; Уайт, Дж. Г. (1953). «Кристаллическая и молекулярная структура перилена». Труды Королевского общества А. 220 (1142): 311–321. Bibcode:1953RSPSA.220..311D. Дои:10.1098 / rspa.1953.0189. JSTOR 99329. S2CID 97262226.
- ^ Анник Мэти, Вим Ван Рой, Люк Ван Век, Герт Экхардт, Вольфганг Штеглих (1994). «Анализ in situ нового периленхинона в лишайниках с помощью лазерной микрозондовой масс-спектрометрии с преобразованием Фурье с внешним источником». Быстрые коммуникации в масс-спектрометрии. 8 (1): 46–52. Bibcode:1994RCMS .... 8 ... 46M. Дои:10.1002 / RCM.1290080109.CS1 maint: несколько имен: список авторов (связь)