Молекулярная симметрия - Molecular symmetry
Молекулярная симметрия в химия описывает симметрия присутствует в молекулы и классификация молекул по их симметрии. Молекулярная симметрия - это фундаментальное понятие в химии, так как ее можно использовать для предсказания или объяснения многих свойств молекулы. химические свойства, например, его дипольный момент и это разрешено спектроскопические переходы. Для этого необходимо классифицировать состояния молекулы с помощью неприводимые представления от таблица символов группы симметрии молекулы. Многие учебники университетского уровня по физическая химия, квантовая химия, спектроскопия и неорганическая химия посвятите главу симметрии.[1][2][3][4][5][6]
Рамки для изучения симметрии молекул обеспечиваются теория групп, и в частности неприводимое представление теория. Симметрия полезна при изучении молекулярные орбитали, с такими приложениями, как Метод Хюккеля, теория поля лигандов, а Правила Вудворда-Хоффмана. Еще одна основа в более широком масштабе - использование кристаллические системы описать кристаллографический симметрия в объемных материалах.
Существует множество методов практической оценки симметрии молекул, в том числе Рентгеновская кристаллография и различные формы спектроскопия. Спектроскопические обозначения основан на соображениях симметрии.
Концепции симметрии
Изучение симметрии в молекулах использует теория групп.
| Вращательный ось (Cп) | Неправильные элементы вращения (Sп) | ||
|---|---|---|---|
| Хиральный нет Sп | Ахирал зеркальная плоскость S1 = σ | Ахирал центр инверсии S2 = я | |
| C1 | 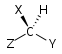 |  |  |
| C2 |  | 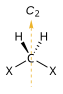 |  |
Элементы
Точечная групповая симметрия молекулы может быть описана 5 типами элемент симметрии.
- Ось симметрии: ось, вокруг которой вращение от в результате получается молекула, неотличимая от оригинала. Это также называется п-сложить ось вращения и сокращенно Cп. Примеры: C2 ось в воды и C3 ось в аммиак. Молекула может иметь более одной оси симметрии; тот, у кого самый высокий п называется главная ось, и по соглашению выровнен с осью z в Декартова система координат.
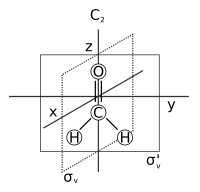
- Плоскость симметрии: плоскость отражения, в которой создается идентичная копия исходной молекулы. Это также называется зеркальная плоскость и сокращенно σ (сигма = греч. «s», от немецкого «Spiegel», что означает зеркало).[7] У воды их два: один в плоскости самой молекулы и один. перпендикуляр к нему. Плоскость симметрии параллельно с главной осью дублируется вертикальный (σv) и один перпендикулярно ему горизонтальный (σчас). Существует третий тип плоскости симметрии: если вертикальная плоскость симметрии дополнительно делит пополам угол между двумя осями 2-кратного вращения, перпендикулярными главной оси, плоскость дублируется двугранный (σd). Плоскость симметрии также можно определить по ее декартовой ориентации, например (xz) или (yz).
- Центр симметрии или центр инверсии, сокращенно я. У молекулы есть центр симметрии, когда для любого атома в молекуле существует идентичный атом, диаметрально противоположный этому центру, на равном расстоянии от него. Другими словами, молекула имеет центр симметрии, когда точки (x, y, z) и (−x, −y, −z) соответствуют идентичным объектам. Например, если в некоторой точке (x, y, z) находится атом кислорода, то в точке (−x, −y, −z) находится атом кислорода. В самом центре инверсии может быть или не быть атом. Примеры тетрафторид ксенона где центр инверсии находится на атоме Xe, а бензол (C6ЧАС6), где центр инверсии находится в центре кольца.
- Ось вращения-отражения: ось, вокруг которой вращается с последующим отражением в перпендикулярной к нему плоскости, молекула остается неизменной. Также называется п-сложить неправильная ось вращения, сокращенно Sп. Примеры представлены в тетраэдрических тетрафторид кремния, с тремя S4 топоры, а шахматное телосложение из этан с одним S6 ось. S1 ось соответствует зеркальной плоскости σ, а S2 ось - центр инверсии я. Молекула, не имеющая Sп ось для любого значения n является хиральный молекула.
- Идентичность, сокращенно E, от немецкого «Einheit», означающего единство.[8] Этот элемент симметрии просто не меняется: каждая молекула имеет этот элемент. Хотя этот элемент кажется физически тривиальным, его необходимо включить в список элементов симметрии, чтобы они образовывали математический группа, определение которого требует включения тождественного элемента. Это так называется, потому что аналогично умножению на единицу (единицу). Другими словами, E - это свойство, которым должен обладать любой объект, независимо от его свойств симметрии.[9]
Операции
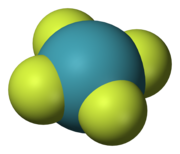
С пятью элементами симметрии связаны пять типов операция симметрии, которые оставляют молекулу в состоянии, неотличимом от исходного состояния. Иногда их отличает от элементов симметрии символ каретка или циркумфлекс. Таким образом, Ĉп - вращение молекулы вокруг оси, Ê - операция тождества. С элементом симметрии может быть связано более одной операции симметрии. Например, C4 ось квадрат тетрафторид ксенона (XeF4) молекула связана с двумя Ĉ4 вращения (90 °) в противоположных направлениях и Ĉ2 вращение (180 °). Поскольку Ĉ1 эквивалентно Ê, Ŝ1 к σ и Ŝ2 к я, все операции симметрии можно классифицировать как правильные или неправильные вращения.
Для линейных молекул вращение либо по часовой стрелке, либо против часовой стрелки вокруг оси молекулы на любой угол Φ является операцией симметрии.
Группы симметрии
Группы
Операции симметрии молекулы (или другого объекта) образуют группа. В математике группа - это набор с бинарная операция который удовлетворяет четырем свойствам, перечисленным ниже.
В группа симметрии, элементы группы являются операциями симметрии (не элементами симметрии), а бинарная комбинация состоит из применения сначала одной операции симметрии, а затем другой. Примером может служить последовательность C4 вращение вокруг оси z и отражение в плоскости xy, обозначенное σ (xy) C4. По соглашению порядок операций - справа налево.
Группа симметрии подчиняется определяющим свойствам любой группы.
(1) закрытие свойство:
Для каждой пары элементов Икс и у в г, то товар Икс*у также в г.
(в символах на каждые два элемента Икс, у∈г, Икс*у также в г ).
Это означает, что группа закрыто так что объединение двух элементов не дает новых элементов. Операции симметрии обладают этим свойством, потому что последовательность из двух операций создаст третье состояние, неотличимое от второго и, следовательно, от первого, так что результирующее воздействие на молекулу по-прежнему будет операцией симметрии.
(2) ассоциативный свойство:
Для каждого Икс и у и z в г, и то и другое (Икс*у)*z и Икс*(у*z) результат с тем же элементом в г.
(в символах, (Икс*у)*z = Икс*(у*z ) для каждого Икс, у, и z ∈ г)
(3) наличие личности свойство:
Должен быть элемент (скажем, е ) в г так что продукт любой элемент г с участием е не вносите изменений в элемент.
(в символах, Икс*е=е*Икс= Икс для каждого Икс∈ г )
(4) наличие обратного свойство:
Для каждого элемента ( Икс ) в г, должен быть элемент у в г такой, что продукт Икс и у является элементом идентичности е.
(в символах, для каждого Икс∈г Существует у ∈ г такой, что Икс*у=у*Икс= е для каждого Икс∈г )
В порядок группы - это количество элементов в группе. Для групп небольших заказов свойства группы можно легко проверить, рассмотрев ее таблицу состава, таблицу, строки и столбцы которой соответствуют элементам группы, а записи - их продуктам.
Точечные группы и группы перестановок-инверсий

Последовательное приложение (или сочинение) одной или нескольких операций симметрии молекулы имеет эффект, эквивалентный действию некоторой операции одной симметрии молекулы. Например, C2 вращение с последующим σv отражение рассматривается как σv'операция симметрии: σv* C2 = σv'. («Операция A, за которой следует B для формирования C» записывается как BA = C).[9] Более того, множество всех операций симметрии (включая эту операцию композиции) подчиняется всем свойствам группы, указанным выше. Так (S,*) - группа, где S - набор всех операций симметрии некоторой молекулы, а * обозначает композицию (повторное применение) операций симметрии.
Эта группа называется точечная группа этой молекулы, потому что набор операций симметрии оставляет по крайней мере одну точку фиксированной (хотя для некоторых симметрий вся ось или вся плоскость остается фиксированной). Другими словами, точечная группа - это группа, которая суммирует все операции симметрии, которые имеют все молекулы в этой категории.[9] Симметрия кристалла, напротив, описывается космическая группа операций симметрии, в том числе переводы в космосе.
Можно определить операции симметрии точечной группы для конкретной молекулы, учитывая геометрическую симметрию ее молекулярной модели. Однако когда ИСПОЛЬЗУЕТСЯ точечная группа для классификации молекулярных состояний, операции в ней нельзя интерпретировать одинаково. Вместо этого операции интерпретируются как вращение и / или отражение вибронных (вибро-электронных) координат.[10] и эти операции коммутируют с вибронным гамильтонианом. Это «операции симметрии» этого вибронного гамильтониана. Точечная группа используется для классификации вибронных собственных состояний по симметрии. Классификация по симметрии вращательных уровней, собственных состояний полного (вращательно-колебательно-электронного) гамильтониана, требует использования соответствующей группы перестановки-инверсии, введенной Лонге-Хиггинс.[11]
Примеры точечных групп
Присвоение каждой молекуле точечной группы классифицирует молекулы по категориям с аналогичными свойствами симметрии. Например, PCl3, POF3, XeO3, а NH3 у всех одинаковые операции симметрии.[12] Все они могут пройти операцию идентичности E, два разных C3 операции вращения, и три различных σv плоские отражения без изменения их идентичности, поэтому они помещаются в одну точечную группу C3в, с заказом 6.[13] Аналогично вода (H2O) и сероводорода (H2S) также имеют идентичные операции симметрии. Оба они проходят операцию идентичности E, один C2 вращения, а два σv отражения без изменения их идентичности, поэтому они оба помещаются в одну точечную группу, C2v, с заказом 4.[14] Эта система классификации помогает ученым более эффективно изучать молекулы, поскольку химически связанные молекулы в одной точечной группе, как правило, демонстрируют похожие схемы связывания, диаграммы молекулярных связей и спектроскопические свойства.[9]
Группы общих точек
В следующей таблице содержится список групп точек, помеченных с помощью Обозначение Шенфлиса, распространенное в химии и молекулярной спектроскопии. Описание структуры включает общие формы молекул, которые можно объяснить Модель VSEPR.
| Группа точек | Симметрийные операции[15] | Простое описание типовой геометрии | Пример 1 | Пример 2 | Пример 3 |
| C1 | E | нет симметрии, хиральный | 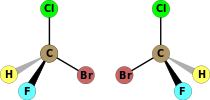 бромхлорфторметан (и то и другое энантиомеры показано) | 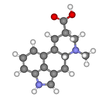 лизергиновая кислота | 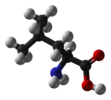 L-лейцин и большинство других α-аминокислоты Кроме глицин |
| Cs | E σчас | плоскость зеркала, другой симметрии нет | 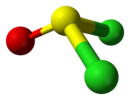 тионилхлорид |  хлорноватистая кислота | 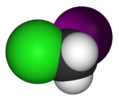 хлоройодметан |
| Cя | E я | центр инверсии | 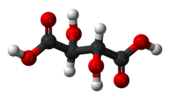 мезо-Винная кислота | 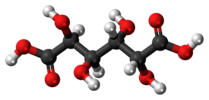 слизевая кислота (мезо-галактаровая кислота) | (S,р) 1,2-дибром-1,2-дихлорэтан (анти конформер) |
| C∞v | E 2C∞Φ ∞σv | линейный |  фтороводород (и все другие гетероядерные двухатомные молекулы ) |  оксид азота (окись азота) |  синильная кислота (цианистый водород) |
| D∞h | E 2C∞Φ ∞σя я 2S∞Φ ∞C2 | линейный с центром инверсии |  кислород (и все другие гомоядерные двухатомные молекулы ) | 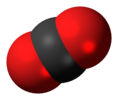 углекислый газ |  ацетилен (этин) |
| C2 | E C2 | "геометрия открытой книги", хиральная |  пероксид водорода |  гидразин | 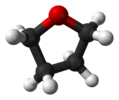 тетрагидрофуран (форма скручивания) |
| C3 | E C3 | пропеллер, хиральный |  трифенилфосфин |  триэтиламин |  фосфорная кислота |
| C2ч | E C2 я σчас | планарный с центром инверсии, без вертикальной плоскости |  транс -1,2-дихлорэтилен | 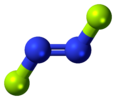 транс -дифторид диазота |  транс -азобензол |
| C3ч | E C3 C32 σчас S3 S35 | пропеллер |  борная кислота |  флороглюцин (1,3,5-тригидроксибензол) | |
| C2v | E C2 σv(xz) σv'(yz) | угловой (H2O) или качели (SF4) или Т-образной формы (ClF3) |  воды |  тетрафторид серы |  трифторид хлора |
| C3в | E 2C3 3σv | тригонально-пирамидальный |  не инвертирующий аммиак |  оксихлорид фосфора |  тетракарбонилгидрид кобальта, HCo (CO)4 |
| C4в | E 2C4 C2 2σv 2σd | квадратно-пирамидальный |  окситетрафторид ксенона | 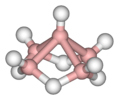 пентаборана (9), B5ЧАС9 | 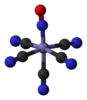 анион нитропруссида [Fe (CN)5(НЕТ)]2− |
| C5в | E 2C5 2C52 5σv | доильный табурет комплекс | 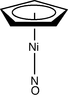 Ni (C5ЧАС5) (НЕТ) |  кораннулен | |
| D2 | E C2(х) С2(y) C2(z) | твист, хиральный | 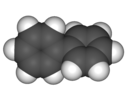 бифенил (перекос) |  Twistane (C10ЧАС16) | конформация циклогексанового твиста |
| D3 | E C3(z) 3C2 | тройная спираль, хиральная |  Катион трис (этилендиамин) кобальта (III) | 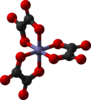 трис (оксалато) анион железа (III) | |
| D2ч | E C2(z) С2(у) С2(Икс) я σ (xy) σ (xz) σ (yz) | планарная с центром инверсии, вертикальная плоскость |  этилен | 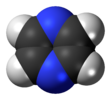 пиразин | 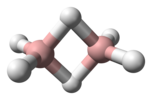 диборан |
| D3ч | E 2C3 3C2 σчас 2S3 3σv | тригональный плоский или тригональный бипирамидальный |  трифторид бора |  пентахлорид фосфора | 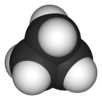 циклопропан |
| D4ч | E 2C4 C2 2C2'2C2" я 2S4 σчас 2σv 2σd | квадратный плоский |  тетрафторид ксенона |  октахлордимолибдат (II) анион | 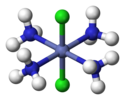 Транс- [CoIII(NH3)4Cl2]+ (за исключением атомов H) |
| D5ч | E 2C5 2C52 5C2 σчас 2S5 2S53 5σv | пятиугольник |  циклопентадиенил анион | 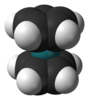 рутеноцен |  C70 |
| D6ч | E 2C6 2C3 C2 3C2'3C2‘’ я 2S3 2S6 σчас 3σd 3σv | шестиугольник | 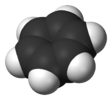 бензол |  бис (бензол) хром |  коронен (C24ЧАС12) |
| D7ч | E C7 S7 7C2 σчас 7σv | семиугольный |  тропилий (C7ЧАС7+) катион | ||
| D8ч | E C8 C4 C2 S8 я 8C2 σчас 4σv 4σd | восьмиугольный |  циклооктатетраенид (C8ЧАС82−) анион |  ураноцен | |
| D2d | E 2S4 C2 2C2'2σd | Поворот на 90 ° | 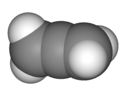 аллен |  тетранитрид тетрасеры |  диборан (4) (возбужденное состояние) |
| D3D | E 2C3 3C2 я 2S6 3σd | Поворот на 60 ° |  этан (в шахматном порядке ротамер ) | 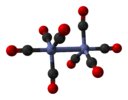 дикобальт октакарбонил (без моста изомер ) | 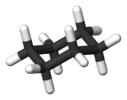 конформация кресла циклогексана |
| D4d | E 2S8 2C4 2S83 C2 4C2'4σd | Поворот на 45 ° |  сера (конформация короны S8) |  декарбонил диманганца (ротамер в шахматном порядке) | 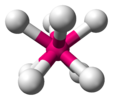 октафтороксенат-ион (идеализированная геометрия) |
| D5d | E 2C5 2C52 5C2 я 2S103 2S10 5σd | Поворот на 36 ° |  ферроцен (ротамер в шахматном порядке) | ||
| S4 | E 2S4 C2 |  тетрафенилборат анион | |||
| Тd | E 8C3 3C2 6S4 6σd | четырехгранный |  метан |  пятиокись фосфора | 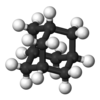 адамантан |
| Тчас | E 4C3 4C32 я 3C2 4S6 4S65 3σчас | пиритоэдр | |||
| Очас | E 8C3 6C2 6C4 3C2 я 6S4 8S6 3σчас 6σd | восьмигранный или кубический |  гексафторид серы | 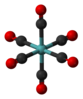 гексакарбонил молибдена |  кубан |
| ячас | E 12C5 12C52 20C3 15C2 я 12S10 12S103 20S6 15σ | икосаэдр или додекаэдр |  Бакминстерфуллерен |  додекаборат анион | 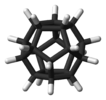 додекаэдран |
Представления
Операции симметрии могут быть представлен разными способами. Удобное представление матрицы. Для любого вектора, представляющего точку в декартовых координатах, умножение влево дает новое положение точки, преобразованное операцией симметрии. Состав операций соответствует умножению матриц. Внутри точечной группы умножение матриц двух операций симметрии приводит к матрице другой операции симметрии в той же точечной группе.[9] Например, в C2v пример это:
Хотя существует бесконечное количество таких представлений, неприводимые представления (или «непокрытые») группы обычно используются, поскольку все другие представления группы могут быть описаны как линейная комбинация неприводимых представлений.
Таблицы символов
Для каждой точечной группы таблица символов суммирует информацию о его операциях симметрии и о его неприводимых представлениях. Поскольку всегда существует равное количество неприводимых представлений и классов операций симметрии, таблицы имеют квадратную форму.
Сама таблица состоит из символы которые представляют, как конкретное неприводимое представление преобразуется при применении определенной операции симметрии. Любая операция симметрии в точечной группе молекулы, действующая на саму молекулу, оставит ее неизменной. Но для воздействия на общую сущность, такую как вектор или орбитальный, этого не должно быть. Вектор может менять знак или направление, а орбиталь может менять тип. Для простых точечных групп значения либо 1, либо -1: 1 означает, что знак или фаза (вектора или орбитали) не изменяется операцией симметрии (симметричный), а −1 означает смену знака (асимметричный).
Представления помечаются в соответствии с набором соглашений:
- A, когда вращение вокруг главной оси симметрично
- B, когда вращение вокруг главной оси несимметрично
- E и T - дважды и трехкратно вырожденные представления соответственно
- когда точечная группа имеет центр инверсии, индекс g (Немецкий: Gerade или даже) сигнализирует об отсутствии изменения знака, а нижний индекс u (отменить или неровный) изменение знака относительно инверсии.
- с точечными группами C∞v и D∞h символы заимствованы из угловой момент описание: Σ, Π, Δ.
В таблицах также содержится информация о том, как декартовы базисные векторы, вращения вокруг них и их квадратичные функции преобразуются с помощью операций симметрии группы, отмечая, какое неприводимое представление преобразуется таким же образом. Эти обозначения обычно находятся в правой части таблиц. Эта информация полезна, потому что химически важные орбитали (в частности, п и d орбитали) обладают той же симметрией, что и эти объекты.
Таблица символов для C2v точечная группа симметрии представлена ниже:
| C2v | E | C2 | σv(xz) | σv'(yz) | ||
|---|---|---|---|---|---|---|
| А1 | 1 | 1 | 1 | 1 | z | Икс2, у2, z2 |
| А2 | 1 | 1 | −1 | −1 | рz | ху |
| B1 | 1 | −1 | 1 | −1 | Икс, Ру | xz |
| B2 | 1 | −1 | −1 | 1 | у, РИкс | yz |
Рассмотрим на примере воды (H2O), который имеет C2v симметрия, описанная выше. 2пИкс орбитальный кислорода имеет B1 симметрия, как в четвертой строке таблицы символов выше, с x в шестом столбце). Он ориентирован перпендикулярно плоскости молекулы и меняет знак на C2 и σv'(yz), но остается неизменным с двумя другими операциями (очевидно, символ для операции идентичности всегда +1). Таким образом, набор символов этой орбиты равен {1, −1, 1, −1}, что соответствует B1 неприводимое представление. Точно так же 2пz орбиталь имеет симметрию A1 неприводимое представление (т.е..: ни одна из операций симметрии его не меняет), 2пу B2, а 3dху орбиталь А2. Эти и другие назначения отмечены в двух крайних правых столбцах таблицы.
Историческое прошлое
Ганс Бете использовал символы точечных групповых операций в своем исследовании теория поля лигандов в 1929 г. и Юджин Вигнер использовал теорию групп, чтобы объяснить правила отбора атомная спектроскопия.[16] Первые таблицы символов были составлены Ласло Тиса (1933), в связи с колебательными спектрами. Роберт Малликен был первым, кто опубликовал таблицы символов на английском языке (1933), и Э. Брайт Уилсон использовал их в 1934 году для предсказания симметрии колебательного нормальные режимы.[17] Полный набор из 32 точечных кристаллографических групп был опубликован в 1936 г. Розенталем и Мерфи.[18]
Молекулярная нежесткость
Как обсуждалось выше в разделе Точечные группы и группы перестановок-инверсий, точечные группы полезны для классификации вибронных состояний жесткий молекулы (иногда называемые полужесткие молекулы), которые совершают лишь небольшие колебания относительно одной равновесной геометрии. Лонге-Хиггинс ввел более общий тип группы симметрии, пригодный не только для классификации ровибронных состояний жестких молекул, но и для классификации состояний нежесткий (или текучий) молекулы, которые туннелируют между эквивалентными геометриями (называемые версии[19]), которые также могут учитывать искажающие эффекты вращения молекул.[11] Эти группы известны как перестановка-инверсия группы, потому что операции симметрии в них являются энергетически допустимыми перестановками идентичных ядер или инверсией относительно центра масс ( паритет операция) или их комбинацию.
Например, этан (C2ЧАС6) имеет три эквивалентных шахматные конформации. Туннелирование между конформациями происходит при обычных температурах за счет внутреннее вращение одной метильной группы относительно другого. Это не вращение всей молекулы вокруг C3 ось. Хотя каждая конформация имеет D3D симметрии, как и в таблице выше, описание внутреннего вращения и связанных квантовых состояний и уровней энергии требует более полной группы перестановки-инверсии G36.
Так же, аммиак (NH3) имеет две эквивалентные пирамидальные (C3в) конформации, которые взаимно превращаются в процессе, известном как азотная инверсия. Это не операция инверсии группы точек. я используется для центросимметричных жестких молекул (т. е. инверсия колебательных смещений и электронных координат в центре масс ядра), поскольку NH3 не имеет центра инверсии и не является центросимметричным. Скорее это инверсия ядерных и электронных координат в молекулярном центре масс (иногда называемая операцией четности), которая оказывается энергетически осуществимой для этой молекулы. Подходящей группой перестановки-инверсии, которая будет использоваться в этой ситуации, является D3ч(M), изоморфная точечной группе D3ч.
Кроме того, в качестве примеров метан (CH4) и H3+ молекулы имеют высокосимметричные равновесные структуры с Td и D3ч точечные групповые симметрии соответственно; им не хватает постоянных электрических дипольных моментов, но они имеют очень слабые спектры чистого вращения из-за вращательно-центробежного искажения.[20][21] Группы перестановки-обращения, необходимые для полного изучения CH4 и H3+ Тd(M) и D3ч(M) соответственно.
Второй и менее общий подход к симметрии нежестких молекул принадлежит Альтману.[22][23] В этом подходе группы симметрии известны как Супергруппы Шредингера и состоят из двух типов операций (и их комбинаций): (1) операции геометрической симметрии (вращения, отражения, инверсии) жестких молекул и (2) изодинамические операции, которые принимают нежесткую молекулу в энергетически эквивалентную форму с помощью физически разумного процесса, такого как вращение вокруг одинарной связи (как в этане) или молекулярная инверсия (как в аммиаке).[23]
Смотрите также
- Четность (физика) § Молекулы
- Неприводимое представление § Приложения в теоретической физике и химии
- Правила Вудворда-Хоффмана § Диаграммы корреляции
- Тактильность § Тактильность и подвижность
- Таблица символов
- Кристаллографическая точечная группа
- Группы точек в трех измерениях
- Симметрия двухатомных молекул
- Симметрия в квантовой механике
использованная литература
- ^ Квантовая химия, 3-е изд. Джон П. Лоу, Кирк Петерсон ISBN 0-12-457551-X
- ^ Физическая химия: молекулярный подход Дональд А. МакКуорри, Джон Д. Саймон ISBN 0-935702-99-7
- ^ Химическая связь2-е изд. J.N. Мюррелл, С.Ф.А. Чайник, Дж. М. Теддер ISBN 0-471-90760-X
- ^ Физическая химия, 8-е изд. П.В. Аткинс и Дж. Де Паула, W.H. Фримен, 2006 ISBN 0-7167-8759-8, глава 12
- ^ Г. Л. Мисслер, Д. А. Тарр Неорганическая химия2-е изд. Пирсон, Прентис-Холл, 1998 г. ISBN 0-13-841891-8, глава 4.
- ^ Молекулярная симметрия и спектроскопия2-е изд. Филип Р. Банкер и Пер Дженсен, NRC Research Press, Оттава (1998) [1] ISBN 9780660196282
- ^ «Операции симметрии и таблицы символов». Эксетерский университет. 2001. Получено 29 мая 2018.
- ^ LEO Ergebnisse für "einheit"
- ^ а б c d е Пфеннинг, Брайан (2015). Основы неорганической химии. Джон Вили и сыновья. ISBN 9781118859025.
- ^ П. Р. Банкер и П. Дженсен (2005),Основы Молекулярная симметрия (CRC Press)ISBN 0-7503-0941-5[2]
- ^ а б Лонге-Хиггинс, Х. (1963). «Группы симметрии нежестких молекул». Молекулярная физика. 6 (5): 445–460. Bibcode:1963молФ ... 6..445л. Дои:10.1080/00268976300100501.
- ^ Пфенниг, Брайан. Основы неорганической химии. Вайли. п. 191. ISBN 978-1-118-85910-0.
- ^ пфенниг, Брайан. Основы неорганической химии. Вайли. ISBN 978-1-118-85910-0.
- ^ Мисслер, Гэри (2004). Неорганическая химия. Пирсон. ISBN 9780321811059.
- ^ Мисслер, Гэри Л. (1999). Неорганическая химия (2-е изд.). Прентис-Холл. С. 621–630. ISBN 0-13-841891-8.
Таблицы символов (все, кроме D7h)
- ^ Теория групп и ее приложение к квантовой механике атомных спектров, Э. П. Вигнер, Academic Press Inc. (1959)
- ^ Исправление двух давних ошибок в таблицах символов симметрии групп точек Randall B. Рубашки J. Chem. Educ. 2007, 84, 1882. Абстрактные
- ^ Розенталь, Дженни Э .; Мерфи, Г. М. (1936). "Теория групп и колебания многоатомных молекул". Ред. Мод. Phys. 8: 317–346. Bibcode:1936РвМП .... 8..317Р. Дои:10.1103 / RevModPhys.8.317.
- ^ Bone, R.G.A .; и другие. (1991). «Переходные состояния из молекулярных групп симметрии: Анализ нежесткого тримерного ацетилена». Молекулярная физика. 72 (1): 33–73. Дои:10.1080/00268979100100021.
- ^ Уотсон, Дж. К. Г. (1971). «Запрещенные вращательные спектры многоатомных молекул». Журнал молекулярной спектроскопии. 40 (3): 546–544. Bibcode:1971JMoSp..40..536W. Дои:10.1016/0022-2852(71)90255-4.
- ^ Oldani, M .; и другие. (1985). «Чистые вращательные спектры метана и метана-d4 в основном колебательном состоянии, наблюдаемые с помощью микроволновой спектроскопии с преобразованием Фурье». Журнал молекулярной спектроскопии. 110 (1): 93–105. Bibcode:1985JMoSp.110 ... 93O. Дои:10.1016/0022-2852(85)90215-2.
- ^ Альтманн С.Л. (1977) Индуцированные представления в кристаллах и молекулах, Academic Press
- ^ а б Flurry, R.L. (1980) Группы симметрии, Прентис-Холл, ISBN 0-13-880013-8, стр.115-127
внешние ссылки
- Точечная групповая симметрия @ Ньюкаслский университет
- Молекулярная симметрия @ Имперский колледж Лондон
- Молекулярная симметрия онлайн @ Открытый университет Израиля
- Таблицы симметрии групп молекулярных точек
- Симметрия @ Otterbein
- Интернет-курс лекций по симметрии молекул @ Bergische Universitaet
- Таблицы символов для точечных групп по химии Ссылка на сайт


