Тетранитрид тетрасеры - Tetrasulfur tetranitride
 | |||
| |||
| Имена | |||
|---|---|---|---|
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| S 4N 4 | |||
| Молярная масса | 184,287 г моль−1 | ||
| Внешность | Яркие оранжевые непрозрачные кристаллы | ||
| Температура плавления | 187 ° С (369 ° F, 460 К) | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Тетранитрид тетрасеры является неорганическое соединение с формула S4N4. Это твердое вещество золотисто-макового цвета является наиболее важным двоичным нитрид серы, которые представляют собой соединения, содержащие только элементы сера и азот. Он является предшественником многих соединений S-N и вызвал широкий интерес благодаря своей необычной структуре и связям.[1][2]
Азот и сера имеют одинаковые электроотрицательность. Когда свойства атомов так похожи, они часто образуют обширные семьи ковалентно склеенные конструкции и компаунды. Действительно, известно большое количество соединений S-N и S-NH с S4N4 как их родитель.
Структура
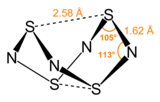
S4N4 принимает необычную конструкцию «экстремальной колыбели», при этом D2d точечная групповая симметрия. Его можно рассматривать как производное от гипотетического восьмичленного кольца чередующихся атомов серы и азота.[требуется разъяснение ] Пары атомов серы в кольце разделены на 2,586 Å, что приводит к образованию каркасной структуры, определенной с помощью дифракции рентгеновских лучей на монокристалле.[3] Природа "трансаннулярных" S – S-взаимодействий остается предметом исследования, поскольку она значительно короче суммы ван-дер-ваальских расстояний[4] но было объяснено в контексте теория молекулярных орбиталей.[1] Связь в S4N4 считается делокализованным, на что указывает тот факт, что расстояния связи между соседними атомами серы и азота почти одинаковы. S4N4 было показано совместно кристаллизоваться с бензол и C60 молекула.[5]
Характеристики
S4N4 устойчив к воздуха. Однако она нестабильна в термодинамический смысл с положительным энтальпия образования +460 кДж моль−1. Этот эндотермический энтальпия образования происходит из разницы в энергии S4N4 по сравнению с его высокостабильными продуктами разложения:
- 2 ю.ш.4N4 → 4 с.ш.2 + S8
Поскольку одним из продуктов его разложения является газ, S4N4 может использоваться как взрывчатое вещество.[1] Более чистые образцы имеют тенденцию быть более взрывоопасными. Небольшие образцы можно взорвать, ударив молотком. S4N4 является термохромный, меняющий цвет от бледно-желтого при температуре ниже -30 ° C до оранжевого при комнатной температуре до темно-красного при температуре выше 100 ° C.[1]
Синтез
S
4N
4 был впервые приготовлен в 1835 г. М. Грегори по реакции дихлорид дисеры с аммиак,[6] оптимизированный процесс:[7]
- 6 ю.ш.2Cl2 + 16 NH3 → S4N4 + S8 + 12 NH4Cl
Побочные продукты этой реакции включают: гептасульфур имид (S7NH) и элементарной серы. В родственном синтезе используется монохлорид серы и NH4Cl вместо:[1]
- 4 NH4Cl + 6 S2Cl2 → S4N4 + 16 HCl + S8
Альтернативный синтез предполагает использование [(Me3Si)2N]2S в качестве предшественника с предварительно сформированными связями S – N. [(Мне3Si)2N]2S получают по реакции бис (триметилсилил) амид лития и SCl2.
- 2 [(CH3)3Si]2NLi + SCl2 → [((CH3)3Si)2N]2S + 2 LiCl
[((CH3)3Si)2N]2S реагирует с комбинацией SCl2 и ТАК2Cl2 образовать S4N4, триметилсилилхлорид, и диоксид серы:[8]
- 2 [((CH3)3Si)2N]2S + 2SCl2 + 2SO2Cl2 → S4N4 + 8 (CH3)3SiCl + 2SO2
Кислотно-основные реакции

S4N4 служит База Льюиса путем связывания через азот с прочным Льюис кислый такие соединения, как SbCl5 и ТАК3. Клетка искажена в этих аддукты.[1]
- S4N4 + SbCl5 → S4N4· SbCl5
- S4N4 + ТАК3 → S4N4·ТАК3
Реакция [Pt2Cl4(PMe2Ph)2] с S4N4 Сообщается, что образует комплекс, в котором сера образует дативную связь с металлом. Это соединение при стоянии изомеризуется в комплекс, в котором атом азота образует дополнительную связь с металлическим центром.
Протонирован HBF4 сформировать тетрафторборат соль:
- S4N4 + HBF4 → [S4N4ЧАС+] [BF−
4]
Мягкая кислота Льюиса CuCl образует координационный полимер:[1]
- п S4N4 + п CuCl → (S4N4)п-μ - (- Cu-Cl-)п
Разбавить NaOH гидролизует S4N4 следующим образом, давая тиосульфат и тритионат:[1]
- 2 ю.ш.4N4 + 6 ОН− + 9 часов2O → S2О2−
3 + 2 S3О2−
6 + 8 NH3
Более концентрированный основание дает сульфит:
- S4N4 + 6 ОН− + 3 часа2O → S2О2−
3 + 2 СО2−
3 + 4 NH3
Металлические комплексы
S4N4 реагирует с комплексами металлов. В некоторых случаях клетка остается неповрежденной, но в других случаях она разрушена.[2][9] S4N4 реагирует с Васьковский комплекс ([Ir (Cl) (CO) (PPh3)2] в окислительная добавка реакция на формирование шести координат иридий комплекс, где S4N4 связывается через два атома серы и один атом азота.
S4N4 как предшественник других соединений S-N
Многие соединения S-N получают из S4N4.[10] Реакция с пиперидин генерирует [S4N5]−:
- 3 ю.ш.4N4 + 4 С5ЧАС10NH → (C5ЧАС10NH2)+[S4N5]− + (C5ЧАС10N)2S + ⅜ S8 + N2
Связанный катион также известно, т.е. [S4N5]+. Лечение с тетраметиламмоний азид образует гетероцикл [S3N3]−:
- S4N4 + NMe4N3 → NMe4[S3N3] + ⅛ S8 + 2 N2
Цикло- [S3N3]− имеет 10 пи-электронов: 2e−/ S плюс 1e−/ N плюс 1e− для отрицательного заряда.
В очевидно связанной реакции использование PPN+N3 дает соль, содержащую синий [NS4]− анион:[10]
- 2 ю.ш.4N4 + PPN (N3) → PPN [NS4] + ½ S8 + 5 N2
Анион NS4− имеет цепную структуру, описываемую с помощью резонанса [S = S = N – S – S]− ↔ [S – S – N = S = S]−.
S4N4 реагирует с электронным обеднением алкины.[11]
Хлорирование S4N4 дает тиазилхлорид.
Проходящий газообразный S4N4 над серебро металл дает низкую температуру сверхпроводник политиазил или полисульфурнитрид (температура перехода (0,26 ± 0,03) K[12]), часто называемый просто "(SN)Икс". При преобразовании серебро сначала становится сульфидированным, а образующийся Ag2S катализирует превращение S4N4 в четырехчленное кольцо S2N2, который легко полимеризуется.[1]
- S4N4 + 8 Ag → 4 Ag2S + 2 N2
- S4N4 → (SN)Икс
Se4N4
В селен соединение Se4N4 известен и был предметом некоторых исследований.[13][14] Кроме того, аддукты хлорид алюминия с Se2N2 были изолированы; это образовано из Se4N4.[15]
Безопасность
S4N4 чувствителен к ударам. Более чистые образцы более чувствительны к ударам, чем образцы, загрязненные элементарной серой.[7]
Рекомендации
- ^ а б c d е ж грамм час я Greenwood, N. N .; Эрншоу, А. (1997). Химические элементы (2-е изд.). Бостон, Массачусетс: Баттерворт-Хайнеманн. С. 721–725.
- ^ а б Чиверс, Т. (2004). Руководство по химии халькогена и азота. Сингапур: World Scientific Publishing. ISBN 981-256-095-5.
- ^ Sharma, B.D .; Донохью, Дж. (1963). «Кристаллическая и молекулярная структура нитрида серы, S4N4". Acta Crystallographica. 16 (9): 891–897. Дои:10.1107 / S0365110X63002401.
- ^ Рзепа, Х.С.; Вуллинз, Дж. Д. (1990). "Исследование структуры и связи в клеточных системах с помощью PM3 SCF-MO S4N4 и S4N4Х (Х = N+, N−, S, N2S, P+, C, Si, B− и Al−)". Многогранник. 9 (1): 107–111. Дои:10.1016 / S0277-5387 (00) 84253-9.
- ^ Конарев, Д. В .; Любовская, Р. Н .; Дричко, Н. В .; и другие. (2000). «Донорно-акцепторные комплексы фуллерена С»60 с органическими и металлоорганическими донорами ". Журнал химии материалов. 10 (4): 803–818. Дои:10,1039 / a907106g.
- ^ Jolly, W. L .; Липп, С. А. (1971). «Реакция тетранитрида тетрасеры с серной кислотой». Неорганическая химия. 10 (1): 33–38. Дои:10.1021 / ic50095a008.
- ^ а б Villena-Blanco, M .; Jolly, W. L .; и другие. (1967). С. Ю. Тайри-младший (ред.). "Тетрасера тетранитрид, S
4N
4". Неорганические синтезы. 9: 98–102. Дои:10.1002 / 9780470132401.ch26. - ^ Maaninen, A .; Shvari, J .; Laitinen, R. S .; Чиверс, Т. (2002). Coucouvanis, Дмитрий (ред.). «Компаунды общего интереса». Неорганические синтезы. 33: 196–199. Дои:10.1002 / 0471224502.ch4. ISBN 9780471208259.
- ^ Келли, П. Ф .; Славин, А. М. З .; Уильямс, Д. Дж .; Вуллинз, Дж. Д. (1992). «Взрывчатые вещества в клетках: нитриды халькогена, стабилизированные металлами». Обзоры химического общества. 21 (4): 245–252. Дои:10.1039 / CS9922100245.
- ^ а б Bojes, J .; Chivers, T .; Oakley, R.D .; и другие. (1989). Оллкок, Х. Р. (ред.). «Бинарные циклические анионы азота и серы». Неорганические синтезы. 25: 30–35. Дои:10.1002 / 9780470132562.ch7. ISBN 9780470132562.
- ^ Dunn, P.J .; Рзепа, Х.С. (1987). "Реакция между тетрасульфур тетранитридом (S4N4) и электронодефицитные алкины. Исследование молекулярной орбиты ». Журнал химического общества, Perkin Transactions 2. 1987 (11): 1669–1670. Дои:10.1039 / p29870001669.
- ^ Greene, R.L .; Улица, Г. Б .; Сутер, Л. Дж. (1975). «Сверхпроводимость в нитриде полисеры (СН)Икс". Письма с физическими проверками. 34 (10): 577–579. Bibcode:1975ПхРвЛ..34..577Г. Дои:10.1103 / PhysRevLett.34.577.
- ^ Келли, П. Ф .; Вуллинз, Дж. Д. (1993). "Реакционная способность Se4N4 в жидком аммиаке ». Многогранник. 12 (10): 1129–1133. Дои:10.1016 / S0277-5387 (00) 88201-7.
- ^ Келли, П. Ф .; Славин, А. М. З .; Сориано-Рама, А. (1997). "Использование Se4N4 и Se (НСО)2 в получении палладиевых аддуктов динитрида дизелена, Se2N2; Кристаллическая структура [PPh4]2[Pd2Br6(Se2N2)]". Dalton Transactions. 1997 (4): 559–562. Дои:10.1039 / a606311j.
- ^ Келли, П. Ф .; Славин, А. М. З. (1996). «Получение и кристаллическая структура [(AlBr3)2(Se2N2)], первый пример аддукта элемента основной группы динитрида дизелена ». Dalton Transactions. 1996 (21): 4029–4030. Дои:10.1039 / DT9960004029.
| NH3 N2ЧАС4 | Курицы2)11 | ||||||||||||||||
| Ли3N | Быть3N2 | BN | β-C3N4 g-C3N4 CИксNу | N2 | NИксОу | NF3 | Ne | ||||||||||
| Na3N | Mg3N2 | AlN | Si3N4 | PN п3N5 | SИксNу SN S4N4 | NCl3 | Ar | ||||||||||
| K | Ca3N2 | ScN | Банка | VN | CrN Cr2N | MnИксNу | FeИксNу | Против | Ni3N | CuN | Zn3N2 | GaN | Ge3N4 | В качестве | Se | NBr3 | Kr |
| Руб. | Sr3N2 | YN | ZrN | NbN | β-Mo2N | Tc | RU | Rh | PdN | Ag3N | CdN | Гостиница | Sn | Sb | Te | NI3 | Xe |
| CS | Ба3N2 | Hf3N4 | TaN | WN | Re | Операционные системы | Ir | Pt | Au | Hg3N2 | TlN | Pb | BiN | По | В | Rn | |
| Пт | Ра3N2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла | CeN | Pr | Nd | Вечера | См | Европа | GdN | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||
| Ac | Чт | Па | ООН | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||


