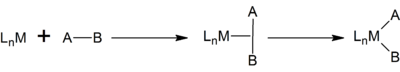Окислительное добавление - Oxidative addition
Окислительное добавление и восстановительное устранение два важных и связанных класса реакций в металлоорганическая химия.[1][2][3][4] Окислительное добавление - это процесс, который увеличивает степень окисления и координационный номер металлического центра. Окислительное добавление часто является этапом каталитические циклы, в сочетании с его обратной реакцией, восстановительным элиминированием.[5]
Роль в химии переходных металлов
Для переходных металлов окислительная реакция приводит к уменьшению dп в конфигурацию с меньшим количеством электронов, часто на 2e меньше. Окислительное добавление предпочтительно для металлов, которые (i) являются основными и / или (ii) легко окисляются. Металлы с относительно низким степень окисления часто удовлетворяют одному из этих требований, но даже металлы с высокой степенью окисления подвергаются окислительному присоединению, как показано окислением Pt (II) хлором:
- [PtCl4]2− + Cl2 → [PtCl6]2−
В классическом металлоорганическая химия формальная степень окисления металла и количество электронов в комплексе увеличиваются на два.[6] Одноэлектронные изменения также возможны, и на самом деле некоторые реакции окислительного присоединения протекают через серию 1e-изменений. Хотя окислительные добавки могут происходить при внедрении металла во многие различные субстраты, окислительные добавки чаще всего наблюдаются со связями H – H, H – X и C – X, поскольку эти субстраты наиболее актуальны для коммерческого применения.
Окислительное добавление требует, чтобы комплекс металла имел свободный координационный центр. По этой причине для четырех- и пятикоординированных комплексов характерны окислительные добавки.
Восстановительное удаление является обратным окислительному добавлению.[7] Восстановительное устранение благоприятно, когда вновь образованная связь X – Y прочная. Чтобы произошло восстановительное устранение, две группы (X и Y) должны быть взаимно соседними на поверхности металла. сфера координации. Восстановительное устранение является ключевым этапом высвобождения продукта в нескольких реакциях, которые образуют связи C – H и C – C.[5]
Механизмы окислительного присоединения
Окислительные добавки происходят по многим путям, которые зависят от металлического центра и субстратов.
Согласованный путь
Окислительные добавки неполярных субстратов, таких как водород и углеводороды, по-видимому, проходят через согласованный пути. Такие подложки не имеют π-связи, следовательно, трехцентровая σ комплекс вызывается с последующим разрывом внутримолекулярной лигандной связи лиганда (вероятно, путем передачи электронной пары на сигма * орбиталь межлигандной связи) с образованием окисленного комплекса. Полученные лиганды будут взаимно СНГ,[2] хотя может происходить последующая изомеризация.
Этот механизм применяется к добавлению гомоядерные двухатомные молекулы такие как H2. Многие реакции активации C – H также следуют согласованному механизму через образование M– (C – H) агостический комплекс.[2]
Характерный пример - реакция водород с участием Васьковский комплекс, транс-IrCl (CO) [P (C6ЧАС5)3]2. В этом превращении иридий меняет свой формальный степень окисления от +1 до +3. Продукт формально связан с тремя анионами: одним хлористый и два гидрид лиганды. Как показано ниже, исходный комплекс металла имеет 16 валентных электронов и координационное число четыре, тогда как продукт представляет собой шестикоординированный 18-электронный комплекс.
Формирование тригонально-бипирамидный дигидрогенизированный промежуточный продукт сопровождается разрывом связи H – H из-за обратного донорства электронов на H – H σ * -орбиталь. Эта система также находится в химическое равновесие, с обратной реакцией, протекающей путем отщепления газообразного водорода с одновременным восстановлением металлического центра.[8]
Обратное донорство электронов на H – H σ * -орбиталь для разрыва связи H – H заставляет богатые электронами металлы поддерживать эту реакцию.[8] Согласованный механизм производит СНГ дигидрид, в то время как стереохимия других путей окислительного присоединения обычно не дает СНГ аддукты.
SN2 типа
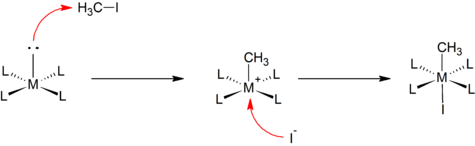
Некоторые окислительные добавки действуют аналогично хорошо известным бимолекулярное нуклеофильное замещение реакции в органическая химия. Нуклеофильная атака металлическим центром у менее электроотрицательного атома в субстрате приводит к разрыву связи R – X с образованием [M – R]+ виды. После этого шага следует быстрое согласование аниона с катионным металлическим центром. Например, реакция квадратного плоского комплекса с йодистый метил:
Этот механизм часто предполагается при добавлении полярных и электрофильных подложек, таких как алкилгалогениды и галогены.[2]
Ионный
Ионный механизм окислительного присоединения аналогичен SN2 типа, поскольку он включает поэтапное добавление двух различных фрагментов лиганда. Ключевое отличие состоит в том, что ионные механизмы включают в себя субстраты, которые диссоциируют в растворе до любых взаимодействий с металлическим центром. Примером ионного окислительного присоединения является добавление соляной кислоты.[2]
Радикальный
Помимо прохождения SN2-типа реакции, алкилгалогениды и аналогичные субстраты могут присоединяться к металлическому центру через радикальный механизм, хотя некоторые детали остаются спорными.[2] Однако известны реакции, которые обычно протекают по радикальному механизму. Один пример был предложен Леднором и сотрудниками.[9]
- Инициация
- [(CH3)2C (CN) N]2 → 2 (CH3)2(CN) C• + N2
- (CH3)2(CN) C• + PhBr → (CH3)2(CN) CBr + Ph•
- Распространение
- Ph• + [Pt (PPh3)2] → [Pt (PPh3)2Ph]•
- [Pt (PPh3)2Ph]• + PhBr → [Pt (PPh3)2PhBr] + Ph•
Приложения
Окислительное добавление и восстановительное отщепление используются во многих каталитических процессах как в гомогенный катализ (т.е. в растворе), например Монсанто процесс и алкен гидрирование с помощью Катализатор Уилкинсона. Часто предполагается, что реакции, подобные окислительному присоединению, также участвуют в механизмах гетерогенный катализ, например гидрирование, катализируемое металлической платиной. Однако металлы характеризуются ленточные конструкции, так степени окисления не имеют смысла. Окислительная добавка также необходима для нуклеофильное присоединение алкильной группы. Окислительная вставка также является важным этапом во многих реакциях кросс-сочетания, таких как Муфта Suzuki, Муфта Негиши, а Муфта Соногашира.
использованная литература
- ^ Джей А. Лабинджер "Учебное пособие по окислительному добавлению" Металлоорганические соединения, 2015, том 34, стр 4784–4795. Дои:10.1021 / acs.organomet.5b00565
- ^ а б c d е ж Крэбтри, Роберт (2005). Металлоорганическая химия переходных металлов.. Wiley-Interscience. С. 159–180. ISBN 0-471-66256-9.
- ^ Мисслер, Гэри Л .; Тарр, Дональд А. Неорганическая химия (3-е изд.).[ISBN отсутствует ]
- ^ Шрайвер, Д. Ф .; Аткинс, П.В. Неорганическая химия.[ISBN отсутствует ]
- ^ а б Хартвиг, Дж. Ф. (2010). Химия органических переходных металлов, от связывания до катализа. Нью-Йорк: Университетские научные книги. ISBN 978-1-891389-53-5.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "окислительная добавка ". Дои:10.1351 / goldbook.O04367
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "восстановительное устранение ". Дои:10.1351 / goldbook.R05223
- ^ а б Джонсон, Кертис; Айзенберг, Ричард (1985). «Стереоселективное окислительное присоединение водорода к комплексам иридия (I). Кинетический контроль на основе электронных эффектов лиганда». Журнал Американского химического общества. 107 (11): 3148–3160. Дои:10.1021 / ja00297a021.
- ^ Hall, Thomas L .; Лапперт, Майкл Ф .; Леднор, Питер В. (1980). «Механистические исследования некоторых реакций окислительного присоединения: свободнорадикальные пути в Pt0-RX, Pt0-PhBr и PtII-Р'СО2X-реакции (R = алкил, R '= арил, X = галогенид) и в родственных системах родия (I) или иридия (I) ». J. Chem. Soc., Dalton Trans. (8): 1448–1456. Дои:10.1039 / DT9800001448.
дальнейшее чтение
- Анаников, Валентин П .; Мусаев, Джамаладдин Г .; Морокума, Кейджи (2005). "Теоретическое понимание реакций связывания C − C виниловых, фенильных, этинильных и метиловых комплексов палладия и платины". Металлоорганические соединения. 24 (4): 715. Дои:10.1021 / om0490841.
внешние ссылки
- Тореки, Р. «Окислительная добавка». Металлоорганический гипертекст. Interactive Learning Paradigms Inc.
- Тореки, Р. «Редуктивное устранение». Металлоорганический гипертекст. Interactive Learning Paradigms Inc.