Муфта Негиши - Negishi coupling
| Муфта Негиши | |
|---|---|
| Названный в честь | Эй-ичи Негиси |
| Тип реакции | Реакция сцепления |
| Идентификаторы | |
| Портал органической химии | Негиши-сцепление |
| RSC ID онтологии | RXNO: 0000088 |
В Муфта Негиши широко используемый переходный металл катализированный реакция кросс-сочетания. Реакция пары органические галогениды или же трифлаты с цинкорганические соединения, формируя углерод-углеродные связи (c-c) в процессе. А палладий (0) разновидность обычно используется в качестве металла катализатор, хотя никель иногда используется:[1][2]
- Уходящая группа Икс обычно хлористый, бромид, или же йодид, но тройной и ацетилокси группы также возможны. Икс = Cl обычно приводит к медленным реакциям.
- Органический остаток р = алкенил, арил, аллил, алкинил или же пропаргил.
- Галогенид ИКС' в цинкорганическом соединении может быть хлористый, бром или же йод и органический остаток Р' является алкенил, арил, аллил, алкил, бензил, гомоаллил и гомопропаргил.
- Металл M в катализаторе никель или же палладий
- В лиганд L в катализаторе может быть трифенилфосфин, dppe, БИНАП или же хирафос
Палладиевые катализаторы в целом имеют более высокую химические выходы и выше функциональная группа толерантность.
Муфта Негиши находит широкое применение в области полный синтез как метод селективного образования с-с-связей между сложными синтетическими промежуточными продуктами. Реакция позволяет связывать sp3, sp2, и sp углерод (см. орбитальная гибридизация ), что делает его несколько необычным среди Катализируемые палладием реакции сочетания. Оцинканоорганические соединения - это влага и чувствительный к воздуху, поэтому соединение Негиши должно выполняться в кислород и среда, свободная от воды, что препятствовало его использованию по сравнению с другими реакциями кросс-сочетания, которые требуют менее жестких условий (например, реакция Сузуки). Однако цинкорганические соединения более реакционноспособны, чем органостаннаны и органобораты, что коррелирует с более быстрым временем реакции.
Реакция названа в честь Эй-ичи Негиси кто был сореципиентом 2010 Нобелевская премия по химии за открытие и развитие этой реакции.
Негиши и его коллеги первоначально исследовали перекрестное связывание алюминийорганический реагентов в 1976 г. Ni и Pd в качестве катализаторов переходных металлов, но было отмечено, что Ni приводит к распаду стереотипность тогда как Pd этого не сделал.[3] Переход от алюминийорганических соединений к цинкорганическим соединениям Негиши и его коллеги сообщили об использовании комплексов Pd в реакциях сочетания цинкорганических соединений и провели исследования методов, в конечном итоге разработав условия реакции до тех, которые обычно используются сегодня.[4] Наряду с Ричард Ф. Хек и Акира Сузуки Эль-ичи Негиши был со-лауреатом Нобелевской премии по химии в 2010 году за свою работу по «Катализируемым палладием кросс-сочетаниям в органическом синтезе».
Механизм реакции
Считается, что механизм реакции протекает через стандартный путь перекрестного связывания, катализируемый Pd, начиная с разновидностей Pd (0), которые окисляются до Pd (II) на стадии окислительного присоединения с участием разновидностей галогенидов.[5] На этом этапе используются арил, винил, алкинил и ацилгалогениды, ацетаты или трифлаты с субстратами, соответствующими стандарту. окислительная добавка относительные скорости (I> OTf> Br >> Cl).[6]
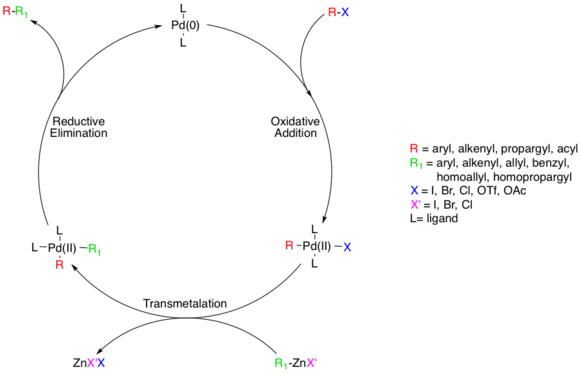
Фактический механизм окислительного добавления не выяснен, хотя есть два возможных пути. Считается, что один путь проходит через SN2 подобный механизм, приводящий к перевернутой стереохимии. Другой путь проходит через согласованное дополнение и сохраняет стереохимию.

Хотя добавки являются цис-комплексом Pd (II), он быстро изомеризуется в транс-комплекс.[7]

Далее трансметалляция Этап происходит, когда цинкорганический реагент обменивает свой органический заместитель на галогенид в комплексе Pd (II), образуя комплекс транс-Pd (II) и соль галогенида цинка. Цинкорганический субстрат может представлять собой арил, винил, аллил, бензил, гомоаллил или гомопропаргил.[5] Трансметалляция обычно ограничение скорости и полное механистическое понимание этого шага еще не достигнуто, хотя несколько исследований пролили свет на этот процесс. Недавно было определено, что частицы алкилцинка должны продолжать образовывать частицы цинката более высокого порядка перед трансметаллированием, тогда как частицы арилцинка этого не делают.[8] ZnXR и ZnR2 оба могут использоваться в качестве реактивных реагентов, и известно, что Zn предпочитает четыре координационных комплекса, что означает комплексы Zn, координированные растворителем, такие как ZnXR (растворитель)2 нельзя исключать априори.[9] Исследования показывают, что между цис- и транс-бис-алкилорганопалладиевыми комплексами существуют конкурирующие равновесия, но единственным продуктивным промежуточным продуктом является цис-комплекс.[10] [11]

Последним этапом каталитического пути сочетания Негиши является восстановительное устранение, который, как считается, осуществляется через трехкоординатную переходное состояние, давая связанный органический продукт и регенерируя катализатор Pd (0). Для того, чтобы эта стадия произошла, должен образоваться вышеупомянутый цис-алкилорганический палладиевый комплекс.[12]

В качестве исходных материалов могут использоваться как галогениды цинка, так и диорганоцинковые соединения. В одной модельной системе было обнаружено, что на стадии трансметаллирования первая дает цис-аддукт R-Pd-R ', приводя к быстрому восстановительному отщеплению до продукта, в то время как последняя дает транс-аддукт, который должен пройти медленную транс-цис-изомеризация первый.[10]
Обычный побочная реакция гомосвязь. В одной модельной системе Негиши было обнаружено, что образование гомосцепления является результатом второй реакции трансметаллирования между промежуточным диарилметаллом и галогенидом арилметалла:[13]
- Ar – Pd – Ar '+ Ar' – Zn – X → Ar' – Pd – Ar' + Ar – Zn – X
- Ar' – Pd – Ar '→ Ar' – Ar' + Pd (0) (гомосвязь)
- Ar – Zn – X + H2O → Ar – H + HO – Zn – X (реакция сопровождается дегалогенирование )
Объем
Для сочетания Негиши были применены следующие иллюстративные синтезы:
- несимметричный 2,2'-бипиридины из 2-бромпиридин с тетракис (трифенилфосфин) палладий (0),[14]
- бифенил из о-толилцинк хлорид и о-иодотолуол и тетракис (трифенилфосфин) палладий (0),[15]
- 5,7-гексадекадиен из 1-децина и (Z) -1-гексенилиодид.[16]

Сочетание Негиши было применено в синтезе гексаферроценилбензол:[17]
с гексаиодидобензолом, диферроценилцинком и трис (дибензилиденацетон) дипалладий (0) в тетрагидрофуран. Выход составляет всего 4%, что означает значительное скопление вокруг арильного ядра.
В новой модификации палладий сначала окисляется галокетон 2-хлор-2-фенилацетофенон 1 и полученный комплекс палладия OPdCl затем принимает оба цинкорганическое соединение 2 и оловоорганическое соединение 3 в двойном трансметалляция:[18]
Недавние условия для реакции Негиши продемонстрировали чрезвычайно широкий диапазон и толерантность к широкому диапазону функциональных групп и гетероароматических ядер и протекают при комнатной температуре или около нее.[19]
Промышленное применение
Муфта Negishi не так часто используется в промышленности, как ее собратья, Сузуки реакция и Чертовски реакция в основном из-за чувствительности к воде и воздуху необходимых арильных или алкилцинковых реагентов.[20][21] В 2003 г. Новартис использовал муфту Негиши при производстве PDE472, a фосфодиэстераза ингибитор типа 4D, который исследовался как ведущее лекарство для лечения астма.[22] Сочетание Негиши использовали в качестве альтернативы реакции Сузуки, обеспечивая улучшенный выход, 73% в масштабе 4,5 кг, желаемого промежуточного синтетического бензодиоксазола.[23]
Приложения в полном синтезе
В то время как соединение Негиши редко используется в промышленной химии из-за вышеупомянутой чувствительности к воде и кислороду, оно находит широкое применение в области натуральные продукты тотальный синтез. Повышенная реакционная способность по сравнению с другими реакциями кросс-сочетания делает сочетание Негиши идеальным для соединения сложных промежуточных продуктов в синтезе природных продуктов.[5] Кроме того, Zn более экологичен, чем другие металлы, такие как Sn используется в Муфта стилла. Хотя муфта Негиши исторически не использовалась так часто, как муфта Стилле или Сузуки, в последние годы муфта Негиши прочно закрепилась в области синтетическая химия настолько, что он стал предпочтительным методом перекрестной связи для избранных синтетических задач. Когда дело доходит до процессов связывания фрагментов, связывание Негиши особенно полезно, особенно по сравнению с вышеупомянутыми реакциями связывания Стилле и Сузуки.[24] Основным недостатком муфты Негиси, помимо чувствительности к воде и кислороду, является относительное отсутствие функциональная группа толерантность по сравнению с другими реакциями кросс-сочетания.[25]
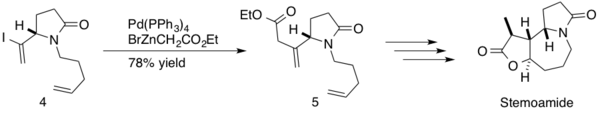
(-) - стемоамид - это натуральный продукт, содержащийся в экстрактах корня «Stemona tuberosa». Эти экстракты были использованы японскими и китайскими Народная медицина для лечения респираторных заболеваний; (-) - стемоамид также является противоглистным средством. Somfai и его коллеги использовали сочетание Негиши в своем синтезе (-) - стемоамида.[26] Реакция осуществлялась в середине синтеза, образуя пр.3-sp2 c-c связь между β, γ-ненасыщенным сложным эфиром и промежуточным диеном 4 с выходом продукта 78% 5. Somfai завершил стереоселективный общий синтез (-) - стемоамида в 12 этапов с общим выходом 20%.
Кибаяси и его коллеги использовали сочетание Негиси в полном синтезе Пумилиотоксин B. Пумилиотоксин B - один из основных токсичных алкалоиды изолирован от Dendrobates pumilio, панамской ядовитой лягушки. Эти токсичные алкалоиды обладают модулирующим действием на зависимые от напряжения натриевые каналы, что приводит к кардиотонической и миотонической активности.[27] Кибаяши использовал позднюю стадию связывания Негиси в синтезе пумилиотоксина B, связывая гомоаллильный sp.3 углерод на цинке алкилиден индолизидин 6 с (E) -винилиодидом 7 с доходностью 51%. Затем после снятия защиты получали натуральный продукт.[28]
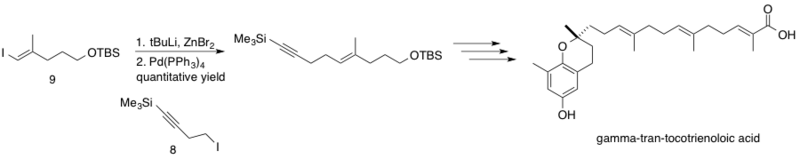
δ-транс-токотриеноловая кислота, выделенная из растения, Chrysochlamys ulei, представляет собой натуральный продукт, который, как было показано, ингибирует ДНК-полимераза β (pol β), который функционирует для восстановления ДНК путем вырезания оснований. Подавление pol B в сочетании с другими химиотерапия лекарства могут увеличить цитотоксичность этих химиотерапевтических средств, что приводит к снижению эффективных доз. Сочетание Негиши было реализовано в синтезе δ-транс-токотриеноловой кислоты путем связывания Хехта и Мэлони sp3 гомопропаргил-цинковый реагент 8 с зр2 винилйодид 9.[29] Реакция протекает с количественным выходом, связывая фрагменты в середине синтеза на пути к стереоселективно синтезированному природному продукту δ-транс-токотриеноловой кислоте.
Получение прекурсоров цинкорганического происхождения
Реагенты алкилцинка можно получить из соответствующих алкилбромидов с использованием йода в диметилацетамиде (DMAC).[30] Каталитический I2 служит для активации цинка в направлении нуклеофильного присоединения.
Арилцинки можно синтезировать в мягких условиях реакции через Гриньяр как промежуточный.[31]
Смотрите также
внешняя ссылка
- Связка Негиши на сайте www.organic-chemistry.org: Связь
Рекомендации
- ^ Король АО, Окукадо Н, Негиси Э (1977). «В высшей степени общий стерео-, регио- и хемоселективный синтез концевых и внутренних конъюгированных енинов с помощью Pd-катализируемой реакции алкинилцинковых реагентов с алкенилгалогенидами». Журнал химического общества, химические коммуникации (19): 683. Дои:10.1039 / C39770000683.
- ^ Курти Л., Чако Б. (2007). Стратегические применения названных реакций в органическом синтезе: предпосылки и подробные механизмы; 250 названных реакций. Амстердам: Elsevier Academic Press. ISBN 978-0-12-429785-2.
- ^ Баба С, Негиси Э (1976). «Новое стереоспецифическое перекрестное связывание алкенилалкенила путем катализируемой палладием или никелем реакции алкенилаланов с алкенилгалогенидами». Журнал Американского химического общества. 98 (21): 6729–6731. Дои:10.1021 / ja00437a067.
- ^ Негиси Э, Король АО, Окукадо Н. (1977). «Селективное образование углерод-углеродных связей посредством катализа переходных металлов. 3. Высокоселективный синтез несимметричных биарилов и диарилметанов путем катализируемой никелем или палладием реакции производных арил- и бензилцинка с арилгалогенидами». Журнал органической химии. 42 (10): 1821–1823. Дои:10.1021 / jo00430a041.
- ^ а б c Курти Л., Чако Б. (2005). Стратегические применения названных реакций в органическом синтезе. Нью-Йорк: Elsevier Academic Press.
- ^ Исследовательская группа Эндрю Дж. Майерса. «Химия 115 Раздаточный материал». Бостон, Массачусетс: Химический факультет Гарвардского университета.
- ^ Касадо А.Л., Эспине П. (1998). «О конфигурации, возникающей в результате окислительного добавления RX к Pd (PPh3) 4, и механизме цис-транс-изомеризации комплексов [PdRX (PPh3) 2] (R = арил, X = галогенид)». Металлоорганические соединения. 17 (5): 954–959. Дои:10.1021 / om9709502.
- ^ McCann LC, Хантер HN, Clyburne JA, Organ MG (июль 2012 г.). «Цинкаты высшего порядка как трансметалляторы в перекрестном связывании алкил-алкил негиши». Angewandte Chemie. 51 (28): 7024–7. Дои:10.1002 / anie.201203547. PMID 22685029.
- ^ Гарсия-Мельчор М., Брага А.А., Лледос А., Ухаке Г., Масерас Ф. (ноябрь 2013 г.). "Вычислительная перспектива катализируемых Pd механизмов реакции кросс-сочетания C-C". Отчеты о химических исследованиях. 46 (11): 2626–34. Дои:10.1021 / ar400080r. PMID 23848308.
- ^ а б Касарес Дж. А., Эспине П., Фуэнтес Б., Салас Г. (март 2007 г.). «Понимание механизма реакции Негиши: ZnRX против реагентов ZnR2». Журнал Американского химического общества. 129 (12): 3508–9. Дои:10.1021 / ja070235b. PMID 17328551.
- ^ Фуэнтес Б., Гарсия-Мельчор М., Лледос А., Мазерас Ф, Касарес Дж. А., Ухак Г., Эспине П. (август 2010 г.). «Палладий туда и обратно в соединении Негиши транс- [PdMeCl (PMePh2) 2] с ZnMeCl: экспериментальное и DFT исследование стадии трансметаллирования». Химия. 16 (29): 8596–9. Дои:10.1002 / chem.201001332. PMID 20623568.
- ^ Крэбтри Р. (2005). Металлоорганическая химия переходных металлов.. 4. Хобокен, Нью-Джерси: John Wiley and Sons Inc.
- ^ Лю Цюй, Лань И, Лю Дж, Ли Дж, Ву ЙД, Лэй А. (июль 2009 г.). «Выявление второго этапа трансметалляции в сочетании Негиши и его конкуренции с восстановительным устранением: улучшение интерпретации механизма биарилсинтеза». Журнал Американского химического общества. 131 (29): 10201–10. Дои:10.1021 / ja903277d. PMID 19572717.
- ^ Адам П. Смит, Скотт А. Сэвидж, Дж. Кристофер Лав и Кассандра Л. Фрейзер (2004). «Синтез 4-, 5- и 6-метил-2,2'-бипиридина с помощью стратегии перекрестного связывания Негиши: 5-метил-2,2'-бипиридин». Органический синтез.CS1 maint: несколько имен: список авторов (связь); Коллективный объем, 10, п. 517
- ^ Эй-ичи Негиси, Тамоцу Такахаши и Энтони О. Кинг (1993). "Синтез биарилов посредством катализируемого палладием кросс-сочетания: 2-метил-4'-нитробифенил". Органический синтез.CS1 maint: несколько имен: список авторов (связь); Коллективный объем, 8, п. 430
- ^ Эй-ичи Негиси, Тамоцу Такахаши и Сигеру Баба (1993). «Синтез сопряженных диенов, катализируемый палладием». Органический синтез.CS1 maint: несколько имен: список авторов (связь); Коллективный объем, 8, п. 295
- ^ Ю. Ю., Бонд А. Д., Леонард П. У., Лоренц У. Дж., Тимофеева Т. В., Фоллхардт К. П., Уайтнер Г. Д., Яковенко А. А. (июнь 2006 г.). «Гексаферроценилбензол». Химические коммуникации (24): 2572–4. Дои:10,1039 / b604844g. PMID 16779481.
- ^ Чжао И, Ван Х, Хоу Х, Ху И, Лэй А., Чжан Х, Чжу Л. (ноябрь 2006 г.). «Окислительное перекрестное сочетание посредством двойного трансметаллирования: неожиданно высокая селективность катализируемого палладием перекрестного сочетания алкилцинка и алкинилстаннанов». Журнал Американского химического общества. 128 (47): 15048–9. Дои:10.1021 / ja0647351. PMID 17117830.
- ^ Ян Y, Oldenhuis NJ, Buchwald SL (январь 2013 г.). «Мягкие и общие условия для кросс-сочетания негиши, обеспечиваемые использованием предкатализаторов палладацикла». Angewandte Chemie. 52 (2): 615–9. Дои:10.1002 / anie.201207750. ЧВК 3697109. PMID 23172689.
- ^ Johansson Seechurn CC, Китчинг, Миссури, Colacot TJ, Snieckus V (май 2012 г.). «Катализируемое палладием кросс-сочетание: историческая контекстуальная перспектива Нобелевской премии 2010 года». Angewandte Chemie. 51 (21): 5062–85. Дои:10.1002 / anie.201107017. PMID 22573393.
- ^ Сасе С., Ярич М., Мецгер А., Малахов В., Кнохель П. (сентябрь 2008 г.). «Реакции кросс-сочетания по Негиши в одном сосуде для цинковых реагентов in situ с арилхлоридами, бромидами и трифлатами». Журнал органической химии. 73 (18): 7380–2. Дои:10.1021 / jo801063c. PMID 18693766.
- ^ Мэнли П. У., Аджемоглу М., Мартерер В., Пачингер В. (2003). «Крупномасштабное связывание Негиши применительно к синтезу PDE472, ингибитора фосфодиэстеразы типа 4D». Исследования и разработки в области органических процессов. 7 (3): 436–445. Дои:10.1021 / op025615q.
- ^ Торборг С, Беллер М (2009). «Недавнее применение реакций связывания, катализируемых палладием, в фармацевтической, агрохимической и тонкой химической промышленности». Расширенный синтез и катализ. 351 (18): 3027–3043. Дои:10.1002 / adsc.200900587.
- ^ Николау К.С., Балджер П.Г., Сарлах Д. (июль 2005 г.). «Катализируемые палладием реакции кросс-сочетания в полном синтезе». Angewandte Chemie. 44 (29): 4442–89. Дои:10.1002 / anie.200500368. PMID 15991198.
- ^ Лессен Г (2004). «Успехи муфты Негиши». Aust. J. Chem. 57 (1): 107. Дои:10.1071 / ch03225.
- ^ Торсселл С., Ваннгрен Э., Сомфай П. (май 2007 г.). «Полный синтез (-) - стемоамида». Журнал органической химии. 72 (11): 4246–9. Дои:10.1021 / jo070498o. PMID 17451274.
- ^ Гусовский Ф., Пэджетт В.Л., Кревелинг С.Р., Дейли Дж.В. (декабрь 1992 г.). «Взаимодействие пумилиотоксина B с« алкалоид-связывающим доменом »на потенциал-зависимом натриевом канале». Молекулярная фармакология. 42 (6): 1104–8. PMID 1336116.
- ^ Аояги С., Хирасима С., Сайто К., Кибаяси С. (2002). «Конвергентный подход к алкалоидам пумилиотоксинов. Асимметричный полный синтез (+) - пумилиотоксинов A, B и 225F». Журнал органической химии. 67 (16): 5517–5526. Дои:10.1021 / jo0200466. PMID 12153249.
- ^ Мэлони DJ, Hecht SM (сентябрь 2005 г.). «Стереоконтролируемый синтез дельта-транс-токотриеноловой кислоты». Органические буквы. 7 (19): 4297–300. Дои:10.1021 / ol051849t. PMID 16146411.
- ^ Хо С (февраль 2003 г.). «Высокоэффективный общий метод получения алкилцинковых реагентов из неактивированных алкилбромидов и хлоридов». Органические буквы. 5 (4): 423–5. Дои:10.1021 / ol0272693. PMID 12583734.
- ^ Джованнини Р., Кнохель П. (1998). «Ni (II) -катализируемая перекрестная связь между полифункциональными производными арилцинка и первичными алкилйодидами». Журнал Американского химического общества. 120 (43): 11186–11187. Дои:10.1021 / ja982520o.

![{displaystyle {egin {matrix} {} {color {Red} {ce {R}}} {-} {color {Blue} {ce {X}}} + {color {Green} {ce {R}} ' } {-} {ce {Zn}} {color {Magenta} {ce {X}} '} {ce {-> [{ce {PdL}} _ {n} {ext {or}} {ce {NiL} } _ {n}]}} {color {Red} {ce {R}}} {-} {color {Green} {ce {R}} '} end {matrix}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/17a2635d55fb246a74645c9525486eafe68ec3e3)





![Приготовление арилцинкового реагента {displaystyle {egin {matrix} {} {ce {Ar-I -> [{egin {matrix} {ce {iPrMgCl}} {ext {THF}} end {matrix}}] [{ce {ZnBr2}}} ] Ar-ZnBr}} конец {матрица}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/207cdded6086749bdb7e5dd64cf22c29306ff367)